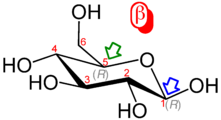
글루코스
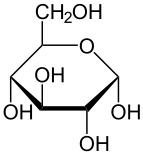
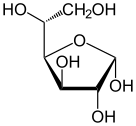
 D-글루코스의 피셔 투영식
| |
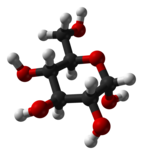
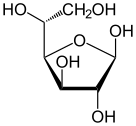
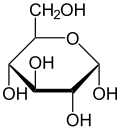 α-D-글루코피라노스의 하워스 투영식
| |
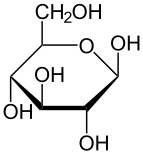
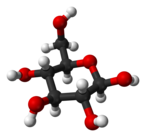
 D-글루코스의 골격 구조식
| |
| 이름 | |
|---|---|
| 발음 | /ˈɡluːkoʊz/, /ɡluːkoʊs/ |
| IUPAC 이름
allowed trivial names:[1]
| |
| 우선명 (PIN)
천연물의 경우 PIN이 식별되지 않는다. | |
체계명
| |
| 별칭
blood sugars,
dextrose, corn sugar, D-glucose, grape sugar | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| 3DMet | |
| 약어 | Glc |
| 1281604 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| EC 번호 |
|
| 83256 | |
| KEGG | |
| MeSH | Glucose |
PubChem CID
|
|
| RTECS 번호 |
|
| UNII |
|
| |
| |
| 성질 | |
| C6H12O6 | |
| 몰 질량 | 180.156 g/mol |
| 겉보기 | 흰색 분말 |
| 밀도 | 1.54 g/cm3 |
| 녹는점 | α-d-Glucose: 146 °C (295 °F; 419 K) β-d-Glucose: 150 °C (302 °F; 423 K) |
| 909 g/L (25 °C (77 °F)) | |
자화율 (χ)
|
−101.5×10−6 cm3/mol |
| 8.6827 | |
| 열화학 | |
열용량 (C)
|
218.6 J/(K·mol)[2] |
표준 몰 엔트로피 (S
|
209.2 J/(K·mol)[2] |
표준 생성 엔탈피 (ΔfH⦵298)
|
−1271 kJ/mol[3] |
연소열, 고위발열량 (HHV)
|
2,805 kJ/mol (670 kcal/mol) |
| 약리학 | |
| B05CX01 (WHO) V04CA02, V06DC01 | |
| 위험 | |
| 물질 안전 보건 자료 | ICSC 08655 |
| NFPA 704 (파이어 다이아몬드) | |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
글루코스(영어: glucose) 또는 포도당(葡萄糖, 영어: grape sugar)은 분자식이 C6H12O6인 단당류이다. 덱스트로스(영어: dextrose)라고도 한다. 포도당은 탄수화물의 하위 범주로, 가장 풍부한 단당류이다.[4] 포도당은 주로 식물과 대부분의 조류에 의해 태양의 빛에너지를 사용하여 물과 이산화 탄소로부터 광합성을 하는 동안 만들어지며 자연에서 가장 풍부한 탄수화물인 식물 세포벽의 셀룰로스를 만드는 데 사용된다.[5][6][7]
에너지 대사에서 포도당은 모든 생명체에서 가장 중요한 에너지원이다. 대사를 위한 포도당은 중합체로 저장되며, 식물에서는 주로 녹말(아밀로펙틴 및 아밀로스)로, 동물에서는 글리코젠으로 저장된다. 포도당은 동물의 혈액에서 혈당으로 순환한다.[5][7] 자연적으로 생성되는 포도당의 형태는 D-포도당이며, L-포도당은 비교적 적은 양으로 합성되며 생물학적 활성이 낮다.[8] 포도당은 6개의 탄소 원자와 카보닐기(알데하이드)를 포함하는 단당류로, 알도헥소스이다. 포도당은 선형 또는 고리형으로 존재할 수 있다. 포도당은 자연적으로 생성되며 열매 및 식물의 다른 부위에서 유리된 상태로 발견된다. 동물에서 포도당은 글리코젠 분해로 알려진 과정을 통해 글리코젠으로부터 방출된다.
정맥 내 당 용액으로서의 포도당은 세계보건기구(WHO)의 필수 의약품 목록에 포함되어 있다.[9] 또한 포도당은 염화 나트륨과 함께 필수 의약품 목록에 있다.[9]
포도당이라는 이름은 "포도주(wine)", "필수(must)"라는 의미의 그리스어 γλεῦκος (gleûkos)와 "달콤한, 단(sweet)"이라는 의미의 그리스어 γλυκύς (glykýs)로부터 유래되었다.[10][11] 접미사 "-ose"는 당을 나타내는 화학적 접미사이다.
역사[편집]
포도당은 1747년에 독일의 화학자 안드레아스 지기스문트 마르크그라프에 의해 건포도로부터 처음으로 분리되었다.[12][13] 포도당은 1792년에 또 다른 독일의 화학자인 요한 토비아스 로비츠가 포도에서 발견했으며, 사탕수수(수크로스)와 다른 것으로 구별되었다. 포도당은 1838년에 장바티스트 뒤마가 만든 용어로 화학 문헌에서 널리 사용되었다. 아우구스트 케쿨레는 덱스트로스("오른쪽"을 의미하는 라틴어 "dexter"에서 유래)라는 용어를 제안했는데, 이는 포도당 수용액에서 선형 편광된 빛의 평면이 오른쪽으로 향하기 때문이다. 대조적으로 L-과당(케토헥소스)과 L-포도당은 선형으로 편광된 빛을 왼쪽으로 돌린다. 선형 편광면의 회전에 따른 이전 표기법(D- 및 L-표기법)은 나중에 카보닐기로부터 가장 멀리 떨어져 있는 비대칭 중심의 절대배치를 나타내고 D- 또는 L-글리세르알데하이드의 입체배치와 일치하는 D- 및 L-표기법을 선호하여 폐기되었다.[14][15]
포도당은 많은 생물체들이 기본적으로 필요로 하기 때문에 그 화학적 구성과 구조에 대한 올바른 이해는 유기화학의 발전에 크게 기여했다. 이러한 이해는 1902년에 노벨 화학상을 수상한 독일의 화학자 에밀 피셔의 연구 결과로 크게 증진되었다.[16] 포도당의 합성은 유기 화합물의 구조를 확립하는 데 기여했고, 결과적으로 야코뷔스 헨리퀴스 반트호프의 화학 반응속도론과 탄소 함유 분자의 화학 결합의 배열에 대한 최초의 결정적인 검증을 가능하게 했다.[17] 1891년에서 1894년 사이에 피셔는 알려진 모든 당들의 입체화학적 입체배치를 규명하고 반트호프의 비대칭 탄소 원자 이론을 적용하여 가능한 이성질체들을 정확하게 예측했다. 이들 이름은 처음에 천연 물질들을 지칭했다. 이들의 거울상 이성질체는 절대 입체화학을 고려하여 계통적 명명법(예: 피셔 명명법, D/L 명명법)을 도입하여 동일한 이름을 부여했다.
포도당 대사의 발견으로 오토 마이어호프는 1922년에 노벨 생리학·의학상을 수상했다.[18] 한스 폰 오일러켈핀은 "당의 발효와 이 과정에서 효소의 역할에 대한 연구"로 1929년에 아서 하든과 공동으로 노벨 화학상을 수상했다.[19][20] 1947년에 베르나르도 우사이(포도당과 파생된 탄수화물의 대사에서 뇌하수체의 역할을 발견한 공로)와 칼 퍼디낸드 코리 및 거티 코리(포도당으로부터 글리코젠으로의 전환 과정을 발견한 공로)는 공동으로 노벨 생리학·의학상을 수상했다.[21][22][23] 1970년에 루이스 페데리코 를루아르는 탄수화물의 생합성에서 포도당 유래 당뉴클레오타이드를 발견한 공로로 노벨 화학상을 수상했다.[24]
화학적 특성 및 물리적 특성[편집]
포도당은 물과 아세트산에 잘 녹지만 메탄올과 에탄올에는 잘 녹지 않는 흰색 또는 무색의 고체이다. 포도당은 146 °C (295 °F) (α) 및 150 °C (302 °F) (β)에서 녹고 다양한 휘발성 생성물을 방출하면서 188 °C (370 °F)부터 분해되기 시작하여 궁극적으로 탄소 잔류물을 남긴다.[25] 포도당은 25 °C (77 °F)의 물에서 pKa 값이 12.16이다.[26]
 |
포도당은 6개의 탄소 원자를 가지고 있으며 단당류의 하위 범위인 육탄당으로 분류된다. D-포도당은 16가지의 알도헥소스 입체 이성질체들 중 하나이다. 덱스트로스라고도 알려진 D-이성질체인 D-포도당은 자연에서 널리 발견되지만 L-이성질체인 L-포도당은 그렇지 않다. 포도당은 젖당, 설탕(수크로스), 엿당, 셀룰로스, 글리코젠 등과 같은 탄수화물의 가수분해에 의해 얻을 수 있다. 포도당은 일반적으로 미국과 일본에서는 옥수수 녹말, 유럽에서는 감자 녹말과 밀 녹말, 열대 지역에서는 타피오카 녹말로 상업적으로 제조된다.[27] 제조 공정은 제트에서 제어된 pH에서 가압 스팀을 통한 가수분해에 이어 추가적인 효소 해중합을 사용한다.[28] 결합되지 않은 포도당은 꿀의 주요 성분 중 하나이다.[29][30][31][32][33]
"덱스트로스(dextrose)"라는 용어는 임상적(환자의 건강 상태와 관련됨) 또는 영양학적 맥락(식품 라벨 또는 식이 지침과 같은 식이 섭취와 관련된)에서 자주 사용되는 반면, "글루코스(glucose)"라는 용어는 생물학적 또는 생리학적 맥락(화학적 과정 및 분자 상호작용)에서 사용되며,[34][35][36][37] 이때는 모두 동일한 분자, 특히 D-글루코스를 나타낸다.[36][38]
덱스트로스 일수화물(dextrose monohydrate)은 D-포도당의 수화된 형태로, 이는 추가적인 물 분자가 부착된 포도당 분자임을 의미한다.[39] 덱스트로스 일수화물의 화학식은 C
6H
12O
6·H
2O이다.[39][40] 덱스트로스 일수화물은 수화된 D-포도당(hydrated D-glucose)이라고도 하며, 일반적으로 옥수수 녹말이나 감자 녹말과 같은 식물성 녹말로부터 제조된다.[39][41] 덱스트로스 일수화물은 음료 혼합물과 같은 식품 응용 분야에서 주요 유형의 포도당으로 활용된다. 이는 식품 생산에서 영양 보충제로 널리 사용되는 일반적인 형태의 포도당이다. 덱스트로스 일수화물은 주로 북미에서 옥수수 시럽 또는 고과당 옥수수 시럽으로 소비된다.[36]
반면, 무수 덱스트로스(anhydrous dextrose)는 물 분자가 결합되어 있지 않은 포도당이다.[41][42] 무수 화합물은 일반적으로 수화물을 가열하거나 건조하는 등의 방법을 통해 수분을 제거하여 생산한다.[43][44][45] 덱스트로스 일수화물은 산업적 환경에서 무수 덱스트로스로 탈수될 수 있다.[46][47] 덱스트로스 일수화물은 질량 기준으로 약 9.5%의 물로 구성된다. 탈수 과정을 통해 이와 같은 수분 함량이 제거되어 무수(건조) 포도당이 생성된다.[41]
무수 덱스트로스는 포도당과 동일하게 물 분자가 부착되지 않은 화학식 C
6H
12O
6을 갖는다.[39] 야외에서 무수 덱스트로스는 수분을 흡수하여 일수화물로 전환되는 경향이 있으며, 무수 덱스트로스의 생산 비용이 더 비싸다.[41] 무수 덱스트로스(무수 D-포도당)은 안정성이 증가되었고 유통 기한이 증가되었으며,[44] 경구 포도당 부하 검사(OGTT)와 같은 의학적 용도로 사용된다.[48]
D-포도당 일수화물의 분자량은 198.17 g/mol인 반면,[49][50] 무수 D-포도당의 분자량은 180.16 g/mol이다.[51][52][53] 이 두 가지 형태의 포도당의 밀도도 또한 다르다.
화학 구조상 포도당은 6개의 탄소 원자와 카보닐기(알데하이드)를 가지고 있는 단당류이기 때문에 알도헥소스이다. 포도당은 열린 사슬 형태(비고리 형태) 및 고리 형태로 존재할 수 있다. 이는 하이드록실기(알코올) 또는 카보닐기(알데하이드 또는 케톤)의 존재로 인해 곧은 사슬을 갖는 형태는 탄수화물에서 흔히 발견되는 의자 모양의 헤미아세탈 고리 구조로 쉽게 전환될 수 있다.[54]
구조 및 명명법[편집]
포도당은 일반적으로 닫힌 피란 고리가 있는 일수화물(포도당 수화물)로 고체 형태로 존재한다. 반면에 수용액에서는 소량이 열린 사슬 형태로 존재하며 상호변환되는 α-피라노스 또는 β-피라노스로 주로 존재한다. 수용액에서 세 가지 알려진 형태인 α-글루코피라노스, β-글루코피라노스 및 α-글루코피라노스 수화물을 결정화할 수 있다.[55] 포도당은 젖당과 설탕(사탕수수 또는 사탕무의 당)과 같은 이당류, 라피노스와 같은 올리고당류, 녹말(아밀로스 및 아밀로펙틴), 글리코젠, 셀룰로스와 같은 다당류의 구성 요소이다. 포도당의 유리 전이 온도는 31 °C (88 °F)이고 고든-테일러 상수(두 물질의 혼합물의 서로 다른 질량 분율에 대한 유리 전이 온도 예측을 위해 실험적으로 결정된 상수)는[56] 4.5이다.[57]
| D-글루코스의 형태와 투영식의 비교 | ||
|---|---|---|
| 나타 투영식 | 하워스 투영식 | |

|
 α-D-글루코푸라노스 α-D-글루코푸라노스
|
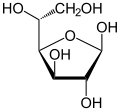 β-D-글루코푸라노스 β-D-글루코푸라노스
|
 α-D-글루코피라노스 α-D-글루코피라노스
|
 β-D-글루코피라노스 β-D-글루코피라노스
| |
| α-D-글루코피라노스의 (1) 톨렌스/피셔 (2) 하워스 투영식 (3) 의자형 입체구조 (4) 밀스 투영식 | ||

| ||
열린 사슬형[편집]

열린 사슬 형태의 포도당은 수용액에서 전체 포도당의 0.02% 미만을 차지한다.[58] 나머지는 두 가지 고리형 헤미아세탈 형태 중 하나이다. 열린 사슬형에서 포도당은 6개의 탄소 원자로 구성된 열린 사슬형(고리형과 반대)의 가지가 없는 골격을 가지고 있으며, 여기서 1번 탄소(C1)는 카보닐기(알데하이드, H(C=O)−)의 탄소이다. 따라서 포도당은 알도스 또는 알도헥소스로 분류된다. 카보닐기(알데하이드)는 포도당을 환원당으로 만들어 펠링 반응에서 양성 반응을 보이게 한다.
고리형[편집]
용액에서 포도당의 열린 사슬형(D- 또는 L-)은 각각 하나의 산소 원자에 의해 닫힌 탄소 고리를 포함하는 여러 고리형 이성질체들과 평형 상태로 존재한다. 그러나 수용액에서는 포도당의 99% 이상이 피라노스 형태로 존재한다. 열린 사슬 형태는 약 0.25%로 제한되며 푸라노스 형태는 무시할 수 있는 양으로 존재한다. "포도당" 및 "D-포도당"이라는 용어는 일반적으로 이러한 고리 형태에서도 사용된다. 고리는 카보닐기(알데하이드, C1)과 C4 또는 C5의 하이드록실기 사이의 분자 내 친핵성 첨가 반응에 의해 열린 사슬 형태로부터 헤미아세탈 결합(−C(OH)H−O−)을 형성함으로써 만들어진다.
C1과 C5 사이의 반응은 유도된 피란 골격을 포함하는 단당류인 피라노스라고 하는 6원자 헤테로고리를 생성한다. C1과 C4 사이의 훨씬 더 드문 반응은 사이클릭 에터인 푸란의 이름을 따서 명명된 5원자 푸라노스 고리를 생성한다. 두 경우 모두 고리의 각 탄소에는(마지막 탄소인 C4 또는 C5는 제외) 1개의 수소 원자와 1개의 하이드록실기가 부착되어 있다. 마지막 탄소인 C4 또는 C5를 제외하고 하이드록실기가 열린 분자의 나머지 부분(각각 −(C(CH
2OH)HOH)−H 또는 −(CHOH)−H) 으로 대체된다.
고리 닫힘 반응은 "α-" 및 "β-"로 표시된 두 가지 생성물을 생성할 수 있다. 글루코피라노스 분자를 하워스 투영식으로 그릴 때 "α-"는 C1의 하이드록실기와 C5의 −CH
2OH기가 고리 평면의 반대쪽에 있음을 의미하고(트랜스 배열), "β-"는 C1의 하이드록실기와 C5의 −CH
2OH가 고리 평면의 같은 쪽에 있다는 것을 의미(시스 배열)한다. 따라서 열린 사슬 이성질체인 D-포도당은 α-D-글루코피라노스, β-D-글루코피라노스, α-D-글루코푸라노스, β-D-글루코푸라노스의 4가지 별개의 고리형 이성질체를 생성한다. 이들 5가지 구조는 평형 상태로 존재하며 상호전환되며, 이러한 상호전환은 산 촉매의 작용 하에서 보다 더 빠르게 일어난다.
 |
다른 열린 사슬 이성질체인 L-포도당은 마찬가지로 L-포도당의 4가지 고리 형태를 생성하며 각각은 해당하는 D-포도당의 거울상 이성질체이다.
글루코피라노스 고리(α 또는 β)는 사이클로헥세인의 "의자형" 및 "보트형" 입체구조와 유사한 여러 비평면 모양을 가정할 수 있다. 유사하게 글루코푸라노스 고리는 사이클로펜테인의 "봉투형" 입체구조와 유사한 여러 모양을 가정할 수 있다.
고체 상태에서는 글루코피라노스 형태만 관찰된다.
1,2-O-아이소프로필리덴-D-글루코푸라노스와 같은 글루코푸라노스의 일부 유도체는 안정적이며 순수한 결정질 고체로 얻을 수 있다.[59][60] 예를 들어 α-D-글루코스와 파라-톨릴보론산(H
3C−(C
6H
4)−B(OH)
2)의 반응은 정상적인 피라노스 고리를 재형성하여 4-폴드 에스터 α-D-글루코푸라노스 1,2:3,5-비스(p-톨릴보론산염)을 생성한다.[61]
변광회전[편집]
 |
변광회전은 고리 형성 반응의 일시적인 역전으로 구성되며, 열린 사슬 형태로 전환된 다음 고리가 다시 형성된다. 고리 닫힘 단계는 열린 단계에서 재형성된 것과 다른 하이드록실기를 사용(따라서 피라노스와 푸라노스 형태 사이의 전환)하거나 C1에서 생성된 새로운 헤미아세탈은 원래의 작용기와 동일하거나 반대 방향(따라서 α 형태와 β 형태 사이의 전환)일 수 있다. 따라서 열린 사슬 형태는 용액에서 거의 탐지할 수 없지만 평형의 필수 구성 요소이다.
열린 사슬 형태는 열역학적으로 불안정하며 자발적으로 고리 형태로 이성질화된다. 고리 닫힘 반응은 이론적으로 4원자 또는 3원자 고리를 형성할 수 있지만, 이러한 고리는 긴장도가 매우 높기 때문에 실제로 관찰되지는 않는다. 실온의 용액에서 4가지 고리형 이성질체는 변광회전이라고 불리는 과정에서 시간 단위로 상호전환된다.[62] 어떤 비율에서 시작하더라도 혼합물은 α:β가 36:64의 안정적인 비율로 수렴한다. 아노머 효과의 영향이 없다면 α:β의 비율은 11:89가 된다.[63] 변광회전은 0 °C (32 °F)에 가까운 온도에서 상당히 느려진다.
광학 활성[편집]
물에 있든 고체 형태로 존재하는 D-(+)-포도당은 우선성이다. 즉, 광원을 바라볼 때 편광의 방향을 시계 방향으로 회전시킨다. 이 효과는 분자의 카이랄성 때문이며 실제로 거울상 이성질체인 L-(−)-포도당은 같은 양만큼 좌선성(편광을 시계 반대 방향으로 회전시킴)이다. 효과의 강도는 5가지 호변 이성질체 각각에 대해 다르다.
D-접두사는 화합물의 광학 특성을 직접적으로 나타내지 않음에 유의해야 한다. 이것은 C5 카이랄 중심이 D-글리세르알데하이드(우선성이기 때문에 이렇게 표시됨)와 동일한 선성을 가짐을 나타낸다. D-포도당이 우선성이라는 사실은 C5 뿐만 아니라 4개의 카이랄 중심에 결합된 효과이다. 실제로 다른 D-알도헥소스 중 일부는 좌선성이다.
순수한 α-D-포도당은 +112.2° mL/(dm·g)의 특정 회전각을 갖고 순수한 β-D-포도당은 +17.5° mL/(dm·g)의 특정 회전각을 갖고 있기 때문에 두 아노머 사이의 전환은 편광계에서 관찰할 수 있다.[64] 변광회전으로 인해 일정 시간이 지난 후 평형에 도달하면 회전각은 +52.7° mL/(dm·g)가 된다.[64] 산이나 염기를 추가하면 이러한 전환은 보다 더 가속화된다. 평형은 열린 사슬 알데하이드 형태를 통해 일어난다.
이성질화[편집]
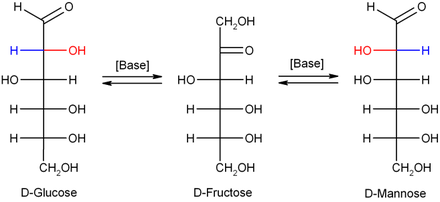
묽은 수산화 나트륨 또는 기타 묽은 염기에서 단당류인 만노스, 포도당, 과당은 서로 전환되어(로브리 드 브로인-반 에켄슈타인 전환을 통해) 이러한 이성질체들 사이의 균형이 형성된다. 이 반응은 엔다이올을 통해 진행된다.
 |
생화학적 특성[편집]
| 해당과정, 포도당신생합성, 글리코젠 합성, 글리코젠 분해를 포함하는 일반적인 단당류의 대사 과정 |
|---|
 |
포도당은 가장 풍부한 단당류이다. 포도당은 또한 대부분의 살아 있는 생물에서 가장 널리 사용되는 알도헥소스이다. 이에 대한 한 가지 가능한 설명은 포도당이 다른 알도헥소스보다 단백질의 아미노기와 비특이적으로 반응하는 경향이 낮다는 것이다.[65] 이 반응(당화)은 많은 단백질(예: 당화 헤모글로빈)의 기능을 손상시키거나 파괴한다.[65] 포도당의 낮은 당화율은 다른 알도헥소스에 비해 더 안정적인 고리 형태를 가지고 있기 때문일 수 있다. 즉, 반응성 열린 사슬 형태보다 더 적은 시간을 소비한다.[65] 포도당이 모든 알도헥소스 중에서 가장 안정적인 고리형을 갖는 이유는 하이드록실기(D-포도당의 아노머 탄소에 있는 하이드록실기는 제외)가 적도 위치에 있기 때문이다. 아마도 포도당은 다른 단당류보다 단백질에 덜 당화되기 때문에 가장 풍부한 천연 단당류이다.[65][66] 또 다른 가설은 β-D-포도당의 형태로 적도 위치에 5개의 하이드록실 치환기를 모두 갖는 유일한 D-알도헥소스인 포도당이 에스터화[67] 또는 아세탈 형성[68]과 같은 화학 반응[69]에 더 쉽게 접근할 수 있다는 것이다. 이러한 이유로 D-포도당은 천연 다당류(글리칸)에서 매우 선호되는 구성 요소이기도 하다. 포도당만으로 구성된 다당류를 글루칸이라고 한다.
포도당은 식물이 햇빛, 물, 이산화 탄소를 이용한 광합성을 통해 생산되며[70][71] 모든 생명체가 에너지원 및 탄소원으로 사용할 수 있다. 그러나 대부분의 포도당은 유리된 형태로 존재하지 않고 에너지 저장 물질인 젖당, 설탕, 녹말 및 식물 세포벽의 구성 요소인 셀룰로스, 균류의 세포벽 및 절지동물의 외골격의 구성 요소인 키틴의 형태로 존재한다. 동물, 균류 및 세균에 의해 섭취될 때 이러한 중합체는 효소를 사용하여 포도당으로 분해된다. 모든 동물은 또한 필요에 따라 특정 전구체로부터 포도당을 스스로 생성할 수 있다. 뉴런, 콩팥 속질 세포, 적혈구는 에너지 생성을 위해 포도당에 의존한다.[71] 성인의 경우 약 18 g (0.63 oz)의 포도당이 있으며,[72] 그 중 약 4 g (0.14 oz)은 혈액에 존재한다.[73] 약 180–220 g (6.3–7.8 oz)의 포도당이 성인의 간에서 24시간 동안 생성된다.[72]
당뇨병의 많은 장기적인 합병증(예: 실명, 신부전 및 말초 신경병증)은 아마도 단백질 또는 지질의 당화로 인한 것이다.[74] 비효소적 과정인 당화와는 대조적으로 단백질에 대한 효소적 조절에 의한 당의 첨가는 글리코실화라고 하며, 이는 많은 단백질들의 기능에 필수적이다.[75]
흡수[편집]
섭취된 포도당은 처음에 사람의 혀에 있는 단맛 수용체에 결합한다. 단백질 TAS1R2 및 TAS1R3의 복합체는 포도당 함유 식품 공급원을 식별할 수 있게 한다.[76][77] 포도당은 주로 음식물로부터 공급되며 하루에 약 300 g (11 oz)이 음식물의 전환에 의해 생성되지만[77] 신체 세포의 다른 대사 산물로부터도 합성된다. 사람의 경우 포도당 함유 다당류의 분해는 부분적으로 이미 씹는 동안 타액에 포함된 아밀레이스에 의해 일어나며, 뿐만 아니라 소장의 솔가장자리에 있는 말테이스, 락테이스, 수크레이스에 의해 분해된다. 포도당은 많은 탄수화물들의 구성 요소이며 특정 효소를 사용하여 분리할 수 있다. 글리코시데이스의 하위 부류인 글루코시데이스는 먼저 포도당을 함유한 긴 사슬의 다당류의 가수분해를 촉매하여 말단 포도당을 절단한다. 차례로 이당류는 대부분 특정 글리코시데이스에 의해 포도당으로 분해된다. 분해 효소의 이름은 보통 특정 다당류 및 이당류의 이름으로부터 파생된다. 특히 다당류를 분해하는 효소에는 아밀레이스(녹말의 성분인 아밀로스에서 이름을 따서 명명됨), 셀룰레이스(셀룰로스에서 이름을 따서 명명됨), 키티네이스(키틴에서 이름을 따서 명명됨) 등이 있다. 또한, 이당류를 분해하는 효소에는 말테이스, 락테이스, 수크레이스, 트레할레이스 등이 있다. 사람에서 글리코시데이스를 암호화하는 약 70가지의 유전자가 알려져 있다. 이들은 글리코젠, 스핑고지질, 뮤코다당류 및 폴리(ADP-리보스)의 소화 및 분해 기능을 가지고 있다. 사람은 셀룰레이스, 키티네이스, 트레할레이스를 생성할 수 없지만 사람의 장내 미생물군에 있는 세균은 생성할 수 있다.
세포의 세포막과 세포 구획의 막으로 들어오거나 나가기 위해 포도당은 주요 촉진자 슈퍼패밀리의 특별한 수송 단백질을 필요로 한다. 소장(보다 정확하게는 공장)에서[78] 포도당은 나트륨/포도당 공동수송체 1(SGLT1)을 통해 나트륨 이온-포도당 동반 수송이라고 하는 2차 능동수송 메커니즘을 통해[79] 포도당 수송체의 도움으로 장 상피로 흡수된다.[80] 추가적인 이동은 포도당 수송체인 GLUT2를 통해 장 상피세포의 기저 측면에서 일어나며,[79] 간세포, 콩팥 세포, 랑게르한스섬 세포, 뉴런, 별아교세포, 띠뇌실막세포로 흡수된다.[81] 포도당은 간문맥을 통해 간으로 들어가 글리코젠으로 저장된다.[82] 간세포에서는 포도당의 6번 위치에서 글루코키네이스에 의해 인산화되어 세포 밖으로 나갈 수 없는 포도당 6-인산이 생성된다. 포도당 6-인산가수분해효소는 간에서만 포도당 6-인산을 다시 포도당으로 전환시키기 때문에 신체가 충분한 혈당 농도를 유지할 수 있게 한다. 다른 세포에서 포도당의 흡수는 14가지의 GLUT 단백질 중 하나를 통한 수동 수송에 의해 일어난다.[79] 다른 유형의 세포에서 인산화는 헥소키네이스를 통해 일어나며 이때 포도당은 더 이상 세포 밖으로 확산될 수 없다.
포도당 수송체인 GLUT1은 대부분 세포에서 생성되며, 신경 세포 및 이자의 β 세포에 특히 중요하다.[79] GLUT3는 신경 세포에서 고도로 발현된다.[79] 혈류의 포도당은 근육 세포(골격근[83]과 심장근의 근육 세포)와 지방 세포에서 GLUT4에 의해 흡수된다.[84] GLUT14는 고환에서만 발현된다.[85] 과도한 포도당은 분해되어 지방산으로 전환된 다음 트라이글리세라이드로 저장된다. 콩팥에서 소변의 포도당은 정단 세포막의 SGLT1 및 SGLT2를 통해 흡수되고 기저외측 세포막의 GLUT2를 통해 전달된다.[86] 콩팥의 포도당 재흡수의 약 90%는 SGLT2를 통해 이루어지며 약 3%는 SGLT1을 통해 이루어진다.[87]
생합성[편집]
식물과 일부 원핵생물에서 포도당은 광합성의 산물이다.[88] 포도당은 또한 글리코젠(동물 및 버섯의 경우) 또는 녹말(식물의 경우)과 같은 포도당의 중합체가 분해되어 생성된다. 글리코젠이 분해되는 것을 글리코젠 분해라고 하며 녹말이 분해되는 것을 녹말 분해라고 한다.[89]
2~4개의 탄소 원자(C)를 포함하는 분자로 시작하여 6개의 탄소 원자를 포함하는 포도당 분자에서 끝나는 대사 경로를 포도당신생합성이라고 하며, 살아 있는 모든 생물에서 일어난다. 더 작은 시작 물질은 다른 대사 경로의 결과물이다. 궁극적으로 거의 모든 생체분자는 식물과 미생물에 의한 광합성 동안 이산화 탄소의 동화로부터 생성된다.[67] α-D-포도당 형성의 자유 에너지는 몰당 917.2 kJ이다.[67] 사람의 경우 포도당신생합성은 간과 콩팥에서 일어나지만[90] 다른 유형의 세포에서도 일어난다. 간에는 약 150 g (5.3 oz)의 글리코젠이 저장되고 골격근에는 약 250 g (8.8 oz)의 글리코젠이 저장된다.[91] 그러나 글리코젠이 분해되어 근육세포에서 방출된 포도당은 헥소키네이스에 의해 포도당이 인산화되고 인산기를 제거하는 포도당 6-인산가수분해효소가 발현되지 않아 순환계로 전달되지 못한다. 포도당과는 달리 포도당 6-인산에 대한 수송 단백질은 존재하지 않는다. 포도당신생합성은 생물이 에너지를 소비하면서 젖산이나 특정 아미노산을 포함한 다른 대사 산물로부터 포도당을 축적할 수 있게 한다. 신세뇨관 세포도 또한 포도당을 생성할 수 있다.
포도당은 또한 주변 환경에서 살아 있는 생물체의 외부에서 찾을 수 있다. 대기 중의 포도당 농도는 항공기에 의한 샘플 수집을 통해 감지되며 위치에 따라 다른 것으로 알려져 있다. 예를 들어, 중국 내륙의 대기 중 포도당 농도는 0.8~20.1 pg/L인 반면, 중국 동해안의 포도당 농도는10.3~142 pg/L이다.[92]
포도당 분해[편집]
사람에서 포도당은 해당과정[93]과 오탄당 인산 경로[94]에 의해 대사된다. 해당과정은 약간의 차이가 있지만 모든 살아 있는 생물에 의해 사용되며,[69][95] 모든 생물은 단당류의 분해로부터 에너지를 생성한다.[95] 물질대사의 추가적인 과정에서 산화적 탈카복실화, 시트르산 회로 및 전자전달계를 통해 물과 이산화 탄소로 완전히 분해될 수 있다. 이를 위한 산소가 충분하지 않으면 동물의 포도당 분해는 젖산 발효를 통해 혐기적으로 젖산을 생성하고 산소 호흡에 비해 훨씬 더 적은 에너지를 방출한다. 포유류에서 근육의 젖산은 혈류를 통해 포도당신생합성이 일어나는 간으로 들어간다(코리 회로). 포도당의 공급량이 많으면 시트르산 회로의 대사 산물인 아세틸-CoA도 지방산 합성에 사용될 수 있다.[96] 포도당은 간과 골격근에서 글리코젠의 저장량을 보충하는 데에도 사용된다. 이러한 과정은 호르몬으로 조절된다.
다른 살아 있는 생물에서는 다른 형태의 발효가 일어날 수 있다. 세균인 대장균은 포도당이 유일한 탄소원인 영양 배지에서 자랄 수 있다.[67] 일부 세균과 고세균에서 포도당은 엔트너-듀도로프 경로를 통해 분해된다.[97]
세포에서 포도당은 호기성 호흡, 혐기성 호흡 또는 발효에 의해 에너지원으로 사용된다.[98] 해당과정의 첫 번째 단계는 헥소키네이스에 의한 포도당의 인산화로 포도당 6-인산을 생성하는 것이다. 포도당이 즉시 인산화되는 주된 이유는 하전된 인산기가 포도당 6-인산이 세포막을 쉽게 통과하는 것을 방지하기 때문에 세포 밖으로 확산되는 것을 막기 위함이다.[99] 또한 고에너지 인산기의 첨가는 포도당을 활성화시키고 이는 해당과정의 나중 단계에서 후속적인 분해를 하기 위함이다.[100] 생리학적 조건에서 이 초기 반응은 비가역적이다.
혐기성 호흡에서 1분자의 포도당은 2분자의 ATP를 순생성한다. 해당과정 동안 4분자의 ATP가 기질수준 인산화에 의해 생성되지만 2분자의 ATP는 해당과정의 에너지 투자기에서 소모된다.[101] 1분자의 포도당이 호기성 호흡에 사용되면 해당과정에서 기질수준 인산화로 2분자의 ATP, 시트르산 회로에서 기질수준 인산화로 2분자의 ATP, 산화적 인산화에서 최대 28분자의 ATP가 생성되므로 최대 총 32분자의 ATP가 생성된다는 점에서 혐기성 호흡보다 훨씬 더 효율적이다.[102]
종양 세포는 비교적 빠르게 생장하고 산소가 있는 경우에도 포유동물에서 발효의 최종 생성물인 젖산을 생성하는 해당과정에 의해 평균 이상의 양의 포도당을 소비한다.[103] 이를 바르부르크 효과라고 한다. 종양에서 증가되는 포도당의 흡수를 위해 다양한 SGLT 및 GLUT가 과도하게 생성된다.[104][105]
효모에서 에탄올은 산소가 있는 경우에도 포도당의 농도가 높을 경우에 발효될 수 있다(일반적으로 발효보다는 산소 호흡으로 이어짐). 이를 크랩트리 효과라고 한다.
포도당은 또한 비생물적 수단을 통해 분해되어 이산화 탄소를 생성할 수 있다. 이는 22 °C 및 pH 2.5에서 산화 및 가수분해를 통해 실험적으로 일어나는 것으로 입증되었다.[106]
에너지원[편집]

포도당은 생물학에서 생물의 보편적인 에너지원이다. 포도당은 호기성 호흡, 혐기성 호흡 또는 발효를 통해 세균에서 사람에 이르기까지 생물체의 에너지원으로 사용된다. 포도당은 호기성 호흡을 통해 그램 당 약 3.75 kcal (16 kJ)의 에너지를 제공하는 인체의 주요 에너지원이다.[107] 탄수화물(예: 녹말)을 분해하면 단당류와 이당류가 생성되며, 이들 분해 산물의 대부분은 포도당이다. 해당과정과 이후에 일어나는 시트르산 회로 및 산화적 인산화를 통해 포도당은 산화되어 결국 이산화 탄소와 물을 생성하고 ATP와 열에너지의 형태로 에너지를 생성한다. 인슐린 및 기타 메커니즘은 혈액 내 포도당의 농도를 조절한다. 포도당의 생리학적 열량은 공급원에 따라 다르지만 16.2 kJ/g[108] 또는 15.7 kJ/g (3.74 kcal/g)이다.[109] 식물의 바이오매스에서 탄수화물의 높은 이용 가능성은 진화하는 동안 특히 미생물에서 에너지 및 탄소 저장을 위한 포도당을 활용하기 위해 다양한 방법으로 이어졌다. 이들은 최종 산물을 더 이상 에너지 생성에 사용할 수 없다는 점에서 차이가 있다. 개별 유전자의 존재와 이들 유전자의 산물인 효소가 어떤 반응이 가능한 지를 결정한다. 거의 모든 생물체가 해당과정을 사용한다. 해당과정 사용의 본질적인 차이점은 그렇지 않으면 간접적으로 생성되어야 하는 동화작용에 대한 환원제로서 NADPH의 회복이다.[110]
포도당과 산소는 뇌에 거의 모든 에너지를 공급하기 때문에[111] 그 이용 가능성은 심리적 과정에 영향을 미친다. 포도당 농도가 낮으면 정신적 노력이 필요한 심리적 과정(예: 자기 조절, 노력이 필요한 의사 결정)이 손상된다.[112][113][114][115] 주요 에너지원으로 포도당을 사용하는 뇌에서 포도당의 농도는 보통 4~6 mM (5 mM은 90 mg/dL과 같음)이지만[72] 단식시에는 2~3 mM로 감소한다.[116] 혼란은 1mM 미만에서 일어나고 혼수 상태는 낮은 수준에서 일어난다.[116]
혈액 속에 있는 포도당을 혈당이라고 한다. 혈당량은 시상하부의 포도당 결합 신경 세포에 의해 조절된다.[117] 또한 뇌의 포도당은 측좌핵에 있는 보상 시스템의 포도당 수용체에 결합한다.[117] 혀의 단맛 수용체에 포도당이 결합하면 포도당 또는 다른 당을 통해 다양한 에너지 대사 호르몬의 방출을 유도하여 세포 흡수를 증가시키고 혈당량을 낮춘다.[118] 인공 감미료는 혈당량을 낮추지 않는다.[118]
단기간 단식 상태에 있는 건강한 사람의 혈당 함량, 예를 들어 하룻밤 금식 후는 약 70~100 mg/dL (4~5.5 mM)이다. 혈장에서 측정된 값은 약 10~15% 더 높다. 또한 모세혈관을 통과하는 동안 포도당이 조직으로 흡수되기 때문에 동맥혈의 혈당 농도가 정맥혈의 혈당 농도보다 높다. 또한 혈당을 결정하는 데 자주 사용되는 모세혈에서 때때로 값이 정맥혈보다 더 높다. 혈액의 포도당 함량은 인슐린, 인크레틴, 글루카곤과 같은 호르몬에 의해 조절된다.[117][119] 인슐린은 포도당 수치를 낮추고 글루카곤은 이를 증가시킨다.[72] 또한, 에피네프린, 티록신, 당질 코르티코이드, 소마토트로핀 및 부신겉질 자극호르몬과 같은 호르몬은 포도당 수치를 증가시킨다.[72] 포도당 자동조절이라고 하는 호르몬의 독립적인 조절도 있다.[120] 음식을 섭취하면 혈당 농도가 증가한다. 정맥 전혈에서 180 mg/dL 이상의 값은 고혈당증이라고 하며, 40 mg/dL 미만의 값은 저혈당증이라고 한다.[121] 포도당은 필요할 때 간과 콩팥의 글리코젠에서 유래한 포도당 6-인산으로부터 포도당 6-인산가수분해효소에 의해 혈류로 방출되어 혈당 농도의 항상성을 조절한다.[90][71] 반추동물에서는 탄수화물의 장내 미생물에 의해 짧은 사슬 지방산으로 더 많이 전환되기 때문에 혈당의 농도가 더 낮다(소의 경우 60 mg/dL, 양의 경우 40 mg/dL).[122]
일부 포도당은 성상세포에 의해 젖산으로 전환된 다음 뇌세포에서 에너지원으로 활용된다. 일부 포도당은 장세포와 적혈구에서 사용되고 나머지는 간, 지방 조직 및 근육 세포에 도달하여 흡수되어 글리코젠으로 저장된다(인슐린의 영향 하에서). 간세포의 글리코젠은 포도당으로 전환될 수 있으며, 인슐린이 낮거나 없을 때 포도당은 혈액으로 되돌아간다. 근육 세포의 글리코젠은 효소 부족으로 인해 분해되어 혈액으로 되돌아가지 않는다. 지방 세포에서 포도당은 일부 유형의 지방을 합성하고 다른 목적을 갖는 반응을 일으키는 데 사용된다. 신체는 포도당을 글리코젠의 형태로 저장한다. 이는 글리코젠이 훨씬 더 "공간 효율적"이고 포도당보다 반응성이 낮기 때문이다.
인체의 건강에서 포도당의 중요성 때문에 포도당은 일반적인 혈액 검사인 포도당 검사의 분석물이다.[123] 혈액 샘플을 채취하기 전에 먹거나 금식하면 혈액 내 포도당 분석에 영향을 미칠 수 있다. 높은 공복 혈당 수치는 당뇨병 전단계 또는 당뇨병의 징후일 수 있다.[124]
혈당 지수는 섭취한 탄수화물의 재흡수 및 혈당량으로의 전환 속도를 나타내는 지표이며, 포도당(포도당은 100으로 정의됨)과 비교하여 소비 후 혈당 곡선의 아래에서 측정된다.[125] 지방 함량이 높은 식품(예: 아이스크림)은 탄수화물의 재흡수를 늦추고 혈당 지수를 낮추기 때문에[126] 혈당 지수의 임상적 중요성은 논란의 여지가 있다.[125][126] 대체 지표는 탄수화물 소비가 혈중 인슐린 수치에 미치는 영향으로 측정되는 인슐린 지수이다.[127] 혈당 부하는 혈당 지수와 섭취한 음식을 양을 기준으로 소비 후 혈당량에 추가된 포도당의 양을 나타내는 지표이다.
전구체[편집]
생물체는 몇 가지 중요한 물질을 합성하기 위한 전구체로 포도당을 사용한다. 녹말, 셀룰로스, 글리코젠은 포도당의 일반적인 중합체(다당류)이다. 이러한 중합체 중 일부(녹말 또는 글리코젠)는 에너지 저장의 역할을 하는 반면, 다른 중합체(셀룰로스 및 포도당의 유도체로부터 만들어지는 키틴)은 구조적인 역할을 한다. 다른 당과 결합된 포도당의 화합물은 에너지 저장에 중요한 역할을 한다. 여기에는 포도당과 갈락토스로 구성된 이당류로 우유의 주요 당인 젖당 및 포도당과 과당으로 구성된 또 다른 이당류인 설탕(수크로스)이 포함된다. 포도당은 또한 글리코실화라고 불리는 과정에서 특정 단백질과 지질에 첨가된다. 이것은 종종 기능에 있어서 중요하다. 포도당을 다른 분자에 결합시키는 효소는 일반적으로 인산화된 포도당을 사용하여 포도당-인 결합의 파괴와 짝지어져 새로운 결합의 형성을 강화한다.
포도당은 단량체로 직접 사용되는 것 외에도 다양한 다른 생체분자를 합성하기 위해 분해될 수 있다. 이것은 포도당이 에너지의 주요 저장원이자 유기 탄소의 공급원으로 역할을 하기 때문에 중요하다. 포도당은 분해되어 지질로 전환될 수 있다. 또한 포도당은 비타민 C(아스코르브산)와 같은 다른 중요한 분자의 합성을 위한 전구체이기도 하다. 살아 있는 생물에서 포도당은 다양한 대사 경로의 출발 물질인 몇 가지 다른 화합물로 전환된다. 그 중에서 과당(폴리올 경로를 통해),[79] 만노스(2번 탄소에서 포도당의 에피머), 갈락토스(4번 탄소에서 포도당의 에피머), 푸코스, 다양한 우론산 및 아미노당과 같은 다른 모든 단당류[128]는 포도당으로부터 생성된다.[82] 해당과정의 일부인 포도당 6-인산으로의 인산화 외에도, 포도당은 글루코노-1,5-락톤으로 분해되는 동안 산화될 수 있다. 포도당은 일부 세균에서 트레할로스 또는 덱스트란 생합성의 빌딩 블록으로 사용되며 동물에서는 글리코젠의 빌딩 블록으로 사용된다. 포도당은 또한 세균의 자일로스 이성질화효소에 의해 과당으로 전환될 수 있다. 또한 포도당의 대사 산물은 모든 비필수 아미노산, 만니톨 및 소르비톨과 같은 당알코올, 지방산, 콜레스테롤, 핵산을 생성한다.[128] 마지막으로 포도당은 단백질을 당단백질, 당지질, 펩티도글리칸, 글리코사이드 및 기타 물질(글리코실기전이효소에 의해 촉매됨)로 글리코실화시키는 구성 요소로 사용되며 글리코시데이스에 의해 분해될 수 있다.
병리학[편집]
당뇨병[편집]
당뇨병은 체내 인슐린이 부족하거나 체내 세포가 인슐린에 적절하게 반응하지 못하기 때문에 신체가 혈중 포도당 수치를 조절할 수 없는 대사 장애이다. 이러한 각각의 상황은 이자 소진 및 인슐린 저항성을 통해 지속적으로 혈당량의 높은 상승으로 인해 일어날 수 있다. 이자는 호르몬인 인슐린과 글루카곤의 분비를 담당하는 기관이다.[129] 인슐린은 포도당의 수준을 조절하는 호르몬으로, 신체의 세포가 포도당을 흡수하고 사용할 수 있도록 한다. 인슐린이 없이는 포도당이 세포로 들어갈 수 없기 때문에 신체 기능을 위한 에너지원으로 포도당을 사용할 수 없다.[130] 이자가 지속적으로 높은 혈당량에 노출되면 이자의 인슐린 생성 세포가 손상되어 체내 인슐린의 부족을 유발할 수 있다. 인슐린 저항성은 이자가 지속적으로 상승된 혈당량에 반응하여 점점 더 많은 인슐린을 생성하려고 할 때 일어난다. 결국 신체의 나머지 부분은 이자가 생산하는 인슐린에 저항성을 갖게 되어 동일한 혈당 강하 효과를 달성하기 위해 더 많은 인슐린을 필요로 하게 되고 이자는 저항에 맞서서 더 많은 인슐린을 생산하게 된다. 이러한 연쇄 고리는 이자의 피로 및 당뇨병의 발병 진행에 기여한다.
혈당 강하 요법에 대한 신체 반응을 모니터링하기 위해 포도당 수치를 측정할 수 있다. 혈당 모니터링은 8시간 금식 후 혈중 포도당의 수준을 측정하는 공복 혈당 검사와 같은 여러 방법에 의해 수행될 수 있다. 또 다른 검사는 2시간 내당능 검사(GTT)이다. 이 검사에서는 공복 혈당 검사를 받은 후 75 g의 포도당 음료를 마시고 다시 검사를 받는다. 이 검사는 사람의 신체가 포도당을 처리하는 능력을 측정한다. 시간이 지남에 따라 인슐린이 세포에 흡수되어 혈류를 빠져나가기 때문에 혈당량은 감소해야 한다.
저혈당증 관리[편집]

저혈당증을 초래하는 당뇨병 또는 기타 상태가 있는 사람은 보통 다양한 형태의 소량의 당을 지니고 있다. 일반적으로 사용되는 당은 보통 포도당 정제(때때로 한 가지 이상의 다른 성분을 바인더로 사용하여 정제 모양으로 압축한 포도당), 하드 캔디 또는 설탕 패킷 형태의 포도당이다.
공급원[편집]

대부분의 식이 탄수화물은 포도당이 유일한 구성 성분(녹말, 글리코젠과 같은 다당류)이거나 다른 단당류를 포함(설탕, 젖당과 같은 이당류)이다.[131] 결합되지 않은 포도당은 꿀의 주요 구성 성분 중 하나이다. 포도당은 매우 풍부하게 존재하며 로마의 침염수 울레미아 노빌리스(Wollemia nobilis)의 숫나무의 콘,[132] 중국의 일렉스 아스프렐라(Ilex asprella) 식물의 뿌리,[133] 캘리포니아의 벼에서 나온 짚[134]을 포함하여 전 세계의 다양한 천연 공급원에서 분리되었다.
| 식품 | 탄수화물, 전체[a] 식이 섬유 포함 |
총 당류 |
유리 과당 |
유리 포도당 |
설탕 (수크로스) |
과당/ 포도당의 비율 |
총 당류 (%)의 비율로서의 설탕(수크로스) |
|---|---|---|---|---|---|---|---|
| 과일 | |||||||
| 사과 | 13.8 | 10.4 | 5.9 | 2.4 | 2.1 | 2.0 | 19.9 |
| 살구 | 11.1 | 9.2 | 0.9 | 2.4 | 5.9 | 0.7 | 63.5 |
| 바나나 | 22.8 | 12.2 | 4.9 | 5.0 | 2.4 | 1.0 | 20.0 |
| 무화과, 건조 | 63.9 | 47.9 | 22.9 | 24.8 | 0.9 | 0.93 | 0.15 |
| 포도 | 18.1 | 15.5 | 8.1 | 7.2 | 0.2 | 1.1 | 1 |
| 네이블 오렌지 | 12.5 | 8.5 | 2.25 | 2.0 | 4.3 | 1.1 | 50.4 |
| 복숭아 | 9.5 | 8.4 | 1.5 | 2.0 | 4.8 | 0.9 | 56.7 |
| 배 | 15.5 | 9.8 | 6.2 | 2.8 | 0.8 | 2.1 | 8.0 |
| 파인애플 | 13.1 | 9.9 | 2.1 | 1.7 | 6.0 | 1.1 | 60.8 |
| 자두 | 11.4 | 9.9 | 3.1 | 5.1 | 1.6 | 0.66 | 16.2 |
| 채소 | |||||||
| 비트, 붉은색 | 9.6 | 6.8 | 0.1 | 0.1 | 6.5 | 1.0 | 96.2 |
| 당근 | 9.6 | 4.7 | 0.6 | 0.6 | 3.6 | 1.0 | 77 |
| 고추 | 6.0 | 4.2 | 2.3 | 1.9 | 0.0 | 1.2 | 0.0 |
| 양파 | 7.6 | 5.0 | 2.0 | 2.3 | 0.7 | 0.9 | 14.3 |
| 고구마 | 20.1 | 4.2 | 0.7 | 1.0 | 2.5 | 0.9 | 60.3 |
| 마 | 27.9 | 0.5 | Traces | Traces | Traces | 빈칸 | Traces |
| 사탕수수 | 13–18 | 0.2–1.0 | 0.2–1.0 | 11–16 | 1.0 | high | |
| 사탕무 | 17–18 | 0.1–0.5 | 0.1–0.5 | 16–17 | 1.0 | high | |
| 곡물 | |||||||
| 옥수수 | 19.0 | 6.2 | 1.9 | 3.4 | 0.9 | 0.61 | 15.0 |
- ↑ 탄수화물 값은 미국 농무부(USDA) 데이터베이스에서 계산되며 당류, 녹말 및 "식이 섬유"의 합과 항상 일치하지는 않는다.
상업적 생산[편집]
포도당은 포도당 아밀레이스를 사용하는 효소적 가수분해 또는 산을 사용하여 녹말로부터 산업적으로 생산된다. 효소적 가수분해는 주로 산 촉매 가수분해 반응을 대체했다.[136] 그 결과 포도당 시럽(효소적으로 건조 물질에 포도당이 90% 이상 포함됨)이 탄생했으며[136] 전 세계 연간 생산량은 2천만 톤(2011년 기준)이다.[137] 이것이 포도당의 이전의 통칭인 "녹말당(starch sugar)"인 이유이다. 아밀레이스는 대부분 바실루스 리케니포르미스(Bacillus licheniformis)[138] 또는 고초균(Bacillus subtilis) (MN-385 균주)[138]에서 유래하며 원래 사용된 효소보다 열에 더 안정적이다.[138][139] 1982년부터 아스페르길루스 니게르(Aspergillus niger)의 풀루라네이스가 포도당 시럽 생산에 사용되어 아밀로펙틴을 아밀로스로 전환하여 포도당 생산 수율을 높였다.[140] 반응은 pH 4.6~5.2 및 55~60 °C의 온도에서 수행된다.[12] 옥수수 시럽은 건조 물질에서 20~95%의 포도당을 함유하고 있다.[141][142] 포도당 시럽의 한국식 형태인 물엿은 고구마 녹말 또는 쌀 녹말로 만든다.[143] 말토덱스트린은 약 20%의 포도당을 함유하고 있다.
많은 작물들이 녹말을 공급원으로 사용될 수 있다. 옥수수,[136] 쌀,[136] 밀,[136] 카사바,[136] 감자,[136] 보리,[136] 고구마,[144] 옥수수 껍질 및 사고는 모두 세계 곳곳에서 사용된다. 미국에서는 옥수수 녹말이 거의 독점적으로 사용된다. 일부 상업용 포도당은 설탕으로부터 생산되는 포도당과 과당의 대략 1:1 혼합물인 전화당의 성분으로 생성된다. 이론적으로 셀룰로스는 포도당으로 가수분해될 수 있지만, 이 과정은 아직 상업적으로 실용적이지 못하다.[55]
과당으로의 전환[편집]
미국에서는 거의 전적으로 옥수수(더 정확하게는 옥수수 시럽)가 포도당과 과당의 혼합물인 아이소글루코스 생산을 위한 포도당 공급원으로 사용된다. 과당은 100 g당 374 kcal의 동일한 생리학적 열량을 갖고 있으며 더 높은 감미력을 지니고 있다. 아이소글루코스의 연간 전 세계 생산량은 800만톤(2011년 기준)이다.[137] 옥수수 시럽으로 만들 때 최종 산물은 고과당 옥수수 시럽(HFCS)이다.
상업적 사용[편집]

포도당은 주로 과당 및 포도당 함유 식품의 생산에 사용된다. 식품에서는 감미료, 습윤제로 사용되며 부피를 증가시키고 더 부드러운 식감을 만든다.[136] 포도 주스(포도주용) 또는 맥아(맥주용)와 같은 다양한 포도당 공급원은 알코올 음료 생산을 위한 에탄올 발효에 사용된다. 미국에서 대부분의 청량 음료는 HFCS-55(건조 중량에서 과당 함량이 55%)를 사용하는 반면 미국에서 대부분의 다른 고과당 옥수수 시럽(HFCS) 가당 식품은 HFCS-42(건조 중량에서 과당 함량이 42%)를 사용한다.[146] 반면에 맥시코에서는 청량 음료에 사탕수수 당을 넣어 단맛을 내는데, 이것은 감미력이 더 높다.[147] 또한 포도당 시럽은 특히 사탕, 토피, 퐁당과 같은 과자 생산에 사용된다.[148] 물이 없는 조건에서 포도당의 전형적인 화학 반응은 캐러맬화이며, 아미노산이 있는 경우 마이야르 반응이다.
또한 예를 들어, 무렐라 테르모아세티카(Moorella thermoacetica)로 발효하여 아세트산을 생성하고, 페니실리움 크리소게눔(Penicillium chrysogenum)으로 발효하여 아라보아스코르브산을 생성하고 리조푸스 델레마르(Rhizopus delemar)로 발효하여 푸마르산을 생성하고, 아스페르길루스 니게르(Aspergillus niger)로 발효하여 글루콘산을 생성하고, 칸디다 브룸프티이(Candida brumptii)로 발효하여 아이소시트르산을 생성하고, 아스페르길루스 테레우스(Aspergillus terreus)로 발효하여 이타콘산을 생성하고, 슈도모나스 플루오레스센스(Pseudomonas fluorescens)로 발효하여 2-케토글루콘산을 생성하고, 글루코노박터 서브옥시단스(Gluconobacter suboxydans)로 발효하여 5-케토글루콘산을 생성하고, 누룩곰팡이(Aspergillus oryzae)로 발효하여 코지산을 생성하고, 락토바실루스 델브루엑키이(Lactobacillus delbrueckii)로 발효하여 젖산을 생성하고, 레비락토바실루스 브레비스(Levilactobacillus brevis)로 발효하여 말산을 생성하고, 프로피오니박테리움 프레우덴레이치이(Propionibacterium freudenreichii)로 발효하여 프로피온산을 생성하고, 녹농균(Pseudomonas aeruginosa)로 발효하여 피루브산을 생성하고, 글루코노박터 서브옥시단스(Gluconobacter suboxydans)로 발효하여 타르타르산을 생성하는 것과 같이 다양한 유기산을 포도당으로부터 생명공학적으로 생성할 수 있다.[149] 일반 전사인자 TFIIH의 XPB 소단위체의 억제를 통해 포유동물의 전사를 억제하는 트립톨라이드와 같은 강력한 생체활성 천연 생성물이 최근 포도당 수송체 발현이 증가된 저산소증 암세포를 표적으로 하는 포도당 접합체로 보고되었다.[150] 최근에 포도당은 다양한 암과 감염을 퇴치하기 위해 저혈당증과 고젖산혈증을 유도하기 위한 젖산과 인슐린을 포함하는 "키트"의 핵심적인 구성 성분으로 상업적으로 사용되고 있다.[151]
분석[편집]
더 큰 분자의 특정 위치에서 포도당 분자를 검출하려면 포도당 또는 만노스에만 결합하는 콘카나발린 A 리포터 효소 접합체를 사용하여 핵자기 공명 분광법, X선 결정학 분석 또는 렉틴 면역염색을 수행해야 한다.
고전적인 정성적 검출 반응[편집]
이들 반응은 역사적 중요성만 가지고 있다.
펠링 시험[편집]
펠링 시험은 알도스를 검출하기 위한 고전적인 방법이다.[152] 변광회전으로 인해 포도당은 항상 열린 사슬 알데하이드로 소량 존재한다. 펠링 시약(펠링 (I) 용액 및 펠링 (II) 용액)을 첨가하면 알데하이드 부분이 카복실산으로 산화되는 반면 Cu2+ 주석산염 복합체는 Cu+로 환원되어 적갈색 침전물(Cu2O)을 생성한다.
톨렌스 시험[편집]
톨렌스 시험에서 샘플 용액에 암모니아성 질산 은(AgNO3)을 첨가한 후 포도당은 Ag+를 원소 은으로 환원시킨다.[153]
바포드 시험[편집]
바포드 시험[154]에서 용해된 아세트산 구리, 아세트산 나트륨 및 아세트산 용액을 테스트할 당 용액에 첨가한 다음 수조에서 몇 분 동안 가열한다. 포도당 및 기타 단당류는 빠르게 붉은색과 적갈색의 산화 구리(I) (Cu2O)을 생성한다.
닐란더 검당법[편집]
환원당으로서 포도당은 닐란더 검당법에서 반응한다.[155]
기타 시험[편집]
묽은 수산화 칼륨 용액과 포도당을 100 °C로 가열하면 강한 적갈변과 캐러멜 같은 냄새가 난다.[156] 농축 황산은 상온에서 흑화되지 않고 건조 포도당을 용해하여 당 황산을 생성한다.[156] 효모 용액에서 알코올 발효는 2.0454 분자의 포도당과 1분자의 이산화 탄소의 비율로 이산화 탄소를 생성한다.[156] 포도당은 염화 주석(II)과 함께 검은 덩어리를 형성한다.[156] 암모니아성 은 용액에서 포도당(젖당 및 덱스트린 포함)은 은의 침착을 유도한다. 암모니아성 아세트산 납 용액에서 흰색 납 글리코사이드는 포도당이 있는 상태에서 형성되며 요리시 덜 용해되고 갈색으로 변한다.[156] 암모니아성 구리 용액에서 실온에서 포도당과 함께 황색 산화 구리 수화물이 형성되는 반면, 끓는 동안 적색 산화 구리가 형성(암모니아성 아세트산 구리 용액을 제외하고 덱스트린과 동일)된다.[156] 하거 시약을 사용하면 포도당이 끓는 동안 산화 수은이 형성된다.[156] 알칼리성 비스무트 용액은 포도당과 함께 흑갈색 비스무트를 침전시키는 데 사용된다.[156] 몰리브데넘산 암모늄 용액에 끓인 포도당을 첨가하면 용액을 파란색으로 변화시킨다. 인디고 카민과 탄산 나트륨이 포함된 용액은 포도당과 함께 끓일 때 탈색된다.[156]
기기 정량화[편집]
굴절계 및 편광계[편집]
다른 탄수화물의 비율이 낮은 포도당 농축 용액에서 그 농도는 편광계로 측정할 수 있다. 설탕 혼합물의 경우 농도는 예를 들어 포도주의 생산 과정에서 웩슬러 측정에서 굴절계로 측정할 수 있다.
용액의 광도 측정 효소 방법[편집]
포도당 산화효소(GOx)는 산소를 소비하면서 포도당을 글루콘산과 과산화 수소로 전환시킨다. 또 다른 효소인 과산화효소는 페놀과 4-아미노안티피린을 보라색 염료로[157] 발색 반응(트린더 반응)[158]을 촉매한다.
광측정 테스트 스트립 방법[편집]
테스트 스트립 방법은 위에서 언급한 과산화 수소를 형성하기 위해 포도당을 글루콘산으로 전환시키는 효소를 사용한다. 시약은 다소 강렬한 색상을 나타내는 소위 테스트 스트립이라고 하는 폴리머 매트릭스에 고정된다. 이는 LED 기반 휴대용 광도계를 사용하여 510 nm에서 반사율로 측정할 수 있다. 이를 통해 비과학자도 일상적인 혈당 측정이 가능하게 되었다. 페놀과 4-아미노안티피린의 반응 외에도 더 높은 파장(550 nm, 750 nm)에서 광측정을 할 수 있게 하는 새로운 발색 반응이 개발되었다.[157][159]
전류 측정 포도당 센서[편집]
포도당의 전기 분석도 위에서 언급한 효소 반응을 기반으로 한다. 생성된 과산화 수소는 600 mV에서 양극 산화에 의해 전류 측정법으로 정량화할 수 있다.[160] 포도당 산화효소(GOx)는 전극의 표면 또는 전극에 가까운 막에 고정된다. 백금이나 금과 같은 귀금속은 탄소 나노튜브 전극(예: 붕소도 도핑된) 뿐만 아니라 전극에도 사용된다.[161] Cu–CuO 나노와이어는 효소가 없는 전류 측정 전극으로도 사용되며 검출 한계는 50 μmol/L이다.[162] 특히 유망한 방법은 산화 중에 흐르는 전자가 분자 와이어를 통해 효소에서 전극으로 직접적으로 전달되는 소위 "효소 배선(enzyme wiring)"이다.[163]
기타 감작 방법[편집]
포도당을 측정하기 위한 다양한 화학 센서들이 있다.[164][165] 생명과학에서 포도당 분석의 중요성을 감안할 때 붕산의 사용을 기반으로 한 당류에 대한 수많은 광학 탐침도 개발되었으며,[166] 이는 다른 광학적 방법이 사용될 수 없거나 조건부로만 사용할 수 있는 세포 내 감작 활용 분야에 특히 유용하다. 보통 당의 1,2-다이올 그룹에 매우 특이적으로 결합하는 유기 붕산 유도체 외에도 선택적 포도당 결합 단백질(예: 콘카나발린 A)을 수용체로 사용하는 기능적 메커니즘으로 분류되는 다른 탐침 개념도 있다. 또한 대산 산물의 농도를 통해 포도당이 농도를 간접적으로 감지하는 방법(예: 형광 광학 센서를 사용하여 산소를 소비함으로써)이 개발되었다.[167] 마지막으로 형광 표지된 효소의 고유 흡광도 또는 형광을 리포터로 사용하는 효소 기반 개념이 있다.[164]
구리 아이오딘 적정법[편집]
포도당은 구리 아이오딘 적정법으로 정량화할 수 있다.[168]
크로마토그래피법[편집]
특히 포도당을 포함하는 복잡한 혼합물의 분석을 위해 예를 들면 꿀에서는 고성능 액체 크로마토그래피 및 기체 크로마토그래피와 같은 크로마토그래피법이[168] 질량 분석법과 함께 사용된다.[169][170] 동위 원소 비율을 고려하면 이러한 방법으로 첨가된 당에 의한 꿀의 불순물을 안정적으로 감지할 수도 있다.[171] 실릴화 시약을 사용한 유도체화가 일반적으로 사용된다.[172] 또한 이당류와 삼당류의 비율을 정량화할 수 있다.
생체 내 분석[편집]
세포의 포도당 흡수는 2-디옥시-D-글루코스 또는 플루오로디옥시글루코스 (18F)로 측정된다.[116] 플루오로디옥시글루코스 (18F)는 종양학 및 신경학에서 양전자 방출 단층촬영에서 추적자로 사용되며,[173] 가장 일반적으로 사용되는 진단제이다.[174]
같이 보기[편집]
각주[편집]
- ↑ Nomenclature of Carbohydrates (Recommendations 1996) | 2-Carb-2. iupac.qmul.ac.uk.
- ↑ 가 나 Boerio-Goates, Juliana (1991), “Heat-capacity measurements and thermodynamic functions of crystalline α-D-glucose at temperatures from 10K to 340K”, 《J. Chem. Thermodyn.》 23 (5): 403–09, doi:10.1016/S0021-9614(05)80128-4
- ↑ Ponomarev, V. V.; Migarskaya, L. B. (1960), “Heats of combustion of some amino-acids”, 《Russ. J. Phys. Chem. (Engl. Transl.)》 34: 1182–83
- ↑ Domb, Abraham J.; Kost, Joseph; Wiseman, David (1998년 2월 4일). 《Handbook of Biodegradable Polymers》. CRC Press. 275쪽. ISBN 978-1-4200-4936-7.
- ↑ 가 나 “NCATS Inxight Drugs — DEXTROSE, UNSPECIFIED FORM”. 2023년 12월 11일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Kamide, Kenji (2005). 《Cellulose products and Cellulose Derivatives: Molecular Characterization and its Applications》 1판. Amsterdam: Elsevier. 1쪽. ISBN 978-0-08-045444-3. 2021년 5월 13일에 확인함.
- ↑ 가 나 “L-glucose”. 《Biology Articles, Tutorials & Dictionary Online》 (미국 영어). 2019년 10월 7일. 2022년 5월 25일에 원본 문서에서 보존된 문서. 2022년 5월 6일에 확인함.
- ↑ “L-glucose”. 《Biology Articles, Tutorials & Dictionary Online》 (미국 영어). 2019년 10월 7일. 2022년 5월 6일에 확인함.
- ↑ 가 나 World Health Organization (2019). 《World Health Organization model list of essential medicines: 21st list 2019》. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ “Online Etymology Dictionary”. 《Etymonline.com》. 2016년 11월 26일에 원본 문서에서 보존된 문서. 2016년 11월 25일에 확인함.
- ↑ Thénard, Gay-Lussac, Biot, and Dumas (1838) "Rapport sur un mémoire de M. Péligiot, intitulé: Recherches sur la nature et les propriétés chimiques des sucres". 보관됨 2015-12-06 - 웨이백 머신 (Report on a memoir of Mr. Péligiot, titled: Investigations on the nature and chemical properties of sugars), Comptes rendus, 7 : 106–113. From page 109. 보관됨 2015-12-06 - 웨이백 머신: "Il résulte des comparaisons faites par M. Péligot, que le sucre de raisin, celui d'amidon, celui de diabètes et celui de miel ont parfaitement la même composition et les mêmes propriétés, et constituent un seul corps que nous proposons d'appeler Glucose (1). ... (1) γλευχος, moût, vin doux." It follows from the comparisons made by Mr. Péligot, that the sugar from grapes, that from starch, that from diabetes and that from honey have exactly the same composition and the same properties, and constitute a single substance that we propose to call glucose (1) ... (1) γλευχος, must, sweet wine.
- ↑ 가 나 《Encyclopedia of Food and Health》 (영어). Academic Press. 2015. 239쪽. ISBN 9780123849533. 2018년 2월 23일에 원본 문서에서 보존된 문서.
- ↑ Marggraf (1747) "Experiences chimiques faites dans le dessein de tirer un veritable sucre de diverses plantes, qui croissent dans nos contrées" 보관됨 2016-06-24 - 웨이백 머신 [Chemical experiments made with the intention of extracting real sugar from diverse plants that grow in our lands], Histoire de l'académie royale des sciences et belles-lettres de Berlin, pp. 79–90. From page 90: 보관됨 2014-10-27 - 웨이백 머신 "Les raisins secs, etant humectés d'une petite quantité d'eau, de maniere qu'ils mollissent, peuvent alors etre pilés, & le suc qu'on en exprime, etant depuré & épaissi, fournira une espece de Sucre." (Raisins, being moistened with a small quantity of water, in a way that they soften, can be then pressed, and the juice that is squeezed out, [after] being purified and thickened, will provide a sort of sugar.)
- ↑ John F. Robyt: Essentials of Carbohydrate Chemistry. Springer Science & Business Media, 2012, ISBN 978-1-461-21622-3. p. 7.
- ↑ Rosanoff, M. A. (1906). “On Fischer's Classification of Stereo-Isomers.1”. 《Journal of the American Chemical Society》 28: 114–121. doi:10.1021/ja01967a014.
- ↑ 《Emil Fischer》, Nobel Foundation, 2009년 9월 3일에 원본 문서에서 보존된 문서, 2009년 9월 2일에 확인함
- ↑ Fraser-Reid, Bert, “van't Hoff's Glucose”, 《Chem. Eng. News》 77 (39): 8
- ↑ "Otto Meyerhof - Facts - NobelPrize.org" 보관됨 2018-07-15 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Hans von Euler-Chelpin - Facts - NobelPrize.org" 보관됨 2018-09-03 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Arthur Harden - Facts - NobelPrize.org" 보관됨 2018-09-03 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Bernardo Houssay - Facts - NobelPrize.org" 보관됨 2018-07-15 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Carl Cori - Facts - NobelPrize.org" 보관됨 2018-07-15 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Gerty Cori - Facts - NobelPrize.org" 보관됨 2018-07-15 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ "Luis Leloir - Facts - NobelPrize.org" 보관됨 2018-07-15 - 웨이백 머신. NobelPrize.org. Retrieved on 5 September 2018.
- ↑ Wenyue Kang and Zhijun Zhang (2020): "Selective Production of Acetic Acid via Catalytic Fast Pyrolysis of Hexoses over Potassium Salts", Catalysts, volume 10, pages 502–515. doi 10.3390/catal10050502
- ↑ Bosch, L.I.; Fyles, T.M.; James, T.D. (2004). “Binary and ternary phenylboronic acid complexes with saccharides and Lewis bases”. 《Tetrahedron》 60 (49): 11175–11190. doi:10.1016/j.tet.2004.08.046. ISSN 0040-4020.
- ↑ Yebra-Biurrun, M.C. (2005), 〈Sweeteners〉, 《Encyclopedia of Analytical Science》 (영어), Elsevier, 562–572쪽, doi:10.1016/b0-12-369397-7/00610-5, ISBN 978-0-12-369397-6
- ↑ "glucose." The Columbia Encyclopedia, 6th ed.. 2015. Encyclopedia.com. 17 Nov. 2015 http://www.encyclopedia.com 보관됨 2009-04-26 - 웨이백 머신.
- ↑ Aga MB, Sharma V, Dar AH, Dash KK, Singh A, Shams R, Khan SA (2023). “Comprehensive review on functional and nutraceutical properties of honey”. 《Efood》 4 (2). doi:10.1002/efd2.71.
- ↑ Bobiş O, Dezmirean DS, Moise AR (2018). “Honey and Diabetes: The Importance of Natural Simple Sugars in Diet for Preventing and Treating Different Type of Diabetes”. 《Oxidative Medicine and Cellular Longevity》 2018: 1–12. doi:10.1155/2018/4757893. PMC 5817209. PMID 29507651.
- ↑ Wani HA, Majid S, Khan MS, Bhat AA, Wani RA, Bhat SA, Ali S, Rehman MU (2020). 〈Scope of Honey in Diabetes and Metabolic Disorders〉. 《Therapeutic Applications of Honey and its Phytochemicals》. Springer. 195–217쪽. doi:10.1007/978-981-15-7305-7_9. ISBN 978-981-15-7304-0. 2021년 4월 14일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Alvarez-Suarez JM, Tulipani S, Romandini S, Bertoli E, Battino M (2010). “Contribution of honey in nutrition and human health: A review”. 《Mediterranean Journal of Nutrition and Metabolism》 3: 15–23. doi:10.1007/s12349-009-0051-6. 2024년 2월 12일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Ischayek JI, Kern M (2006). “US Honeys Varying in Glucose and Fructose Content Elicit Similar Glycemic Indexes - Journal of the American Dietetic Association”. 《Journal of the American Dietetic Association》 106 (8): 1260–1262. doi:10.1016/j.jada.2006.05.003. PMID 16863724.
- ↑ “Potentially Important Contribution of Dextrose Used as Diluent to Hyperglycemia in Hospitalized Patients | Diabetes Care | American Diabetes Association”. 2022년 5월 29일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Dextrose: Why is it in food and medicine?”. 2018년 6월 24일. 2024년 2월 13일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 가 나 다 “What is Dextrose, How is It Used, and is It Healthy? - the Nutrition Insider”. 2023년 10월 27일. 2024년 2월 14일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Dextrose vs. Glucose: Are These Sugars Equal?”. 2023년 9월 29일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Baron, D. N.; McIntyre, N. (1976). “Letter: Glucose is dextrose is glucose”. 《British Medical Journal》 2 (6026): 41–42. doi:10.1136/bmj.2.6026.41-c. PMC 1687736. PMID 938892.
- ↑ 가 나 다 라 “Prakash Chemicals International”. 2023년 6월 6일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “API | glucose monohydrate”. 2023년 3월 24일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 가 나 다 라 “The difference between dextrose anhydrous and dextrose monohydrate”. 2022년 12월 28일. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Dextrose anhydrous”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Khvorova LS, Andreev NR, Lukin ND (2020). “Study of Conditions for Applying Surfactants in Crystalline Glucose Production”. 《Russian Agricultural Sciences》 46 (1): 90–93. Bibcode:2020RuAgS..46...90K. doi:10.3103/S1068367420010048. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 가 나 “What is the difference between anhydrous glucose and glucose”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Anhydrous vs. Monohydrate - What's the Difference?”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Trasi NS, Boerrigter SX, Byrn SR, Carvajal TM (2011년 3월 15일). “Investigating the effect of dehydration conditions on the compactability of glucose - ScienceDirect”. 《International Journal of Pharmaceutics》 406 (1): 55–61. doi:10.1016/j.ijpharm.2010.12.042. PMID 21232587. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Mitra B, Wolfe C, Wu S (2018). “Dextrose monohydrate as a non-animal sourced alternative diluent in high shear wet granulation tablet formulations”. 《Drug Development and Industrial Pharmacy》 44 (5): 817–828. doi:10.1080/03639045.2017.1414231. PMID 29300107. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Diabetes & Prediabetes Tests - NIDDK”. 2023년 12월 16일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Dextrose Monohydrate”. 2023년 12월 2일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Archived copy”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “D-Glucose”. 2023년 12월 15일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Archived copy”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Archived copy”. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ “Glucose (Dextrose)”. 2013년 10월 2일. 2023년 12월 21일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 가 나 Schenck, Fred W. (2006). 〈Glucose and Glucose-Containing Syrups〉. 《Ullmann's Encyclopedia of Industrial Chemistry》. doi:10.1002/14356007.a12_457.pub2. ISBN 978-3527306732.
- ↑ Patrick F. Fox: Advanced Dairy Chemistry Volume 3: Lactose, water, salts and vitamins, Springer, 1992. Volume 3, ISBN 9780412630200. p. 316.
- ↑ Benjamin Caballero, Paul Finglas, Fidel Toldrá: Encyclopedia of Food and Health. Academic Press (2016). ISBN 9780123849533, Volume 1, p. 76.
- ↑ “16.4: Cyclic Structures of Monosaccharides”. 《Chemistry LibreTexts》 (영어). 2014년 7월 18일. 2023년 4월 17일에 확인함.
- ↑ Takagi, S.; Jeffrey, G. A. (1979). “1,2-O-isopropylidene-D-glucofuranose”. 《Acta Crystallographica Section B》 B35 (6): 1522–1525. doi:10.1107/S0567740879006968.
- ↑ Bielecki, Mia; Eggert, Hanne; Christian Norrild, Jens (1999). “A fluorescent glucose sensor binding covalently to all five hydroxy groups of α-D-glucofuranose. A reinvestigation”. 《Journal of the Chemical Society, Perkin Transactions》 2 (3): 449–456. doi:10.1039/A808896I.
- ↑ Chandran, Sreekanth K.; Nangia, Ashwini (2006). “Modulated crystal structure (Z′ = 2) of α-d-glucofuranose-1,2:3,5-bis(p-tolyl)boronate”. 《CrystEngComm》 8 (8): 581–585. doi:10.1039/B608029D.
- ↑ 틀:McMurry2nd.
- ↑ Juaristi, Eusebio; Cuevas, Gabriel (1995), 《The Anomeric Effect》, CRC Press, 9–10쪽, ISBN 978-0-8493-8941-2
- ↑ 가 나 Manfred Hesse, Herbert Meier, Bernd Zeeh, Stefan Bienz, Laurent Bigler, Thomas Fox: Spektroskopische Methoden in der organischen Chemie. 8th revised Edition. Georg Thieme, 2011, ISBN 978-3-13-160038-7, p. 34 (in German).
- ↑ 가 나 다 라 Bunn, H. F.; Higgins, P. J. (1981). “Reaction of monosaccharides with proteins: possible evolutionary significance”. 《Science》 213 (4504): 222–24. Bibcode:1981Sci...213..222B. doi:10.1126/science.12192669. PMID 12192669.
- ↑ Jeremy M. Berg: Stryer Biochemie. Springer-Verlag, 2017, ISBN 978-3-662-54620-8, p. 531. (german)
- ↑ 가 나 다 라 Voet, Donald; Voet, Judith G. (2011). 《Biochemistry》 4판. Hoboken, NJ: John Wiley & Sons. ISBN 978-0470-57095-1.
- ↑ Albert L. Lehninger, Biochemistry, 6th printing, Worth Publishers Inc. 1972, ISBN 0-87901-009-6 p. 228.
- ↑ 가 나 Garrett, Reginald H. (2013). 《Biochemistry》 5판. Belmont, CA: Brooks/Cole, Cengage Learning. ISBN 978-1-133-10629-6.
- ↑ “Chemistry for Biologists: Photosynthesis”. 《www.rsc.org》. 2016년 8월 4일에 원본 문서에서 보존된 문서. 2018년 2월 5일에 확인함.
- ↑ 가 나 다 Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 195. (german)
- ↑ 가 나 다 라 마 U. Satyanarayana: Biochemistry. Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7. p. 674.
- ↑ Wasserman, D. H. (2009). “Four grams of glucose”. 《American Journal of Physiology. Endocrinology and Metabolism》 296 (1): E11–21. doi:10.1152/ajpendo.90563.2008. PMC 2636990. PMID 18840763.
- ↑ “High Blood Glucose and Diabetes Complications: The buildup of molecules known as AGEs may be the key link”, 《Diabetes Forecast》 (American Diabetes Association), 2010, ISSN 0095-8301, 2013년 10월 14일에 원본 문서에서 보존된 문서, 2010년 5월 20일에 확인함
- ↑ Varki, A.; Cummings, R. D.; Esko, J. D.; Freeze, H. H.; Stanley, P.; Bertozzi, C. R.; Hart, G. W.; Etzler, M. E. (2009). Varki, Ajit, 편집. 《Essentials of Glycobiology》 2판. Cold Spring Harbor Laboratories Press. ISBN 978-0-87969-770-9. PMID 20301239. 2016년 12월 6일에 원본 문서에서 보존된 문서.
- ↑ “Showing Compound D-Glucose (FDB012530) - FooDB”. 2022년 12월 6일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 가 나 Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 404.
- ↑ Harold A. Harper: Medizinische Biochemie. Springer-Verlag, 2013, ISBN 978-3-662-22150-1, p. 641. (독일어)
- ↑ 가 나 다 라 마 바 Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 199, 200. (독일어)
- ↑ Navale, A. M.; Paranjape, A. N. (2016). “Glucose transporters: Physiological and pathological roles”. 《Biophysical Reviews》 8 (1): 5–9. doi:10.1007/s12551-015-0186-2. PMC 5425736. PMID 28510148.
- ↑ Thorens, B. (2015). “GLUT2, glucose sensing and glucose homeostasis”. 《Diabetologia》 58 (2): 221–32. doi:10.1007/s00125-014-3451-1. PMID 25421524.
- ↑ 가 나 Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 214. (독일어)
- ↑ Huang, S.; Czech, M. P. (2007). “The GLUT4 glucose transporter”. 《Cell Metabolism》 5 (4): 237–52. doi:10.1016/j.cmet.2007.03.006. PMID 17403369.
- ↑ Govers, R. (2014). 《Cellular regulation of glucose uptake by glucose transporter GLUT4》. 《Advances in Clinical Chemistry》 66. 173–240쪽. doi:10.1016/B978-0-12-801401-1.00006-2. ISBN 9780128014011. PMID 25344989.
- ↑ Wu, Xiaohua; Freeze, Hudson H. (December 2002). “GLUT14, a Duplicon of GLUT3, is Specifically Expressed in Testis as Alternative Splice Forms”. 《Genomics》 80 (6): 553–7. doi:10.1006/geno.2002.7010. PMID 12504846.
- ↑ Ghezzi, C.; Loo DDF; Wright, E. M. (2018). “Physiology of renal glucose handling via SGLT1, SGLT2, and GLUT2”. 《Diabetologia》 61 (10): 2087–2097. doi:10.1007/s00125-018-4656-5. PMC 6133168. PMID 30132032.
- ↑ Poulsen, S. B.; Fenton, R. A.; Rieg, T. (2015). “Sodium-glucose cotransport”. 《Current Opinion in Nephrology and Hypertension》 24 (5): 463–9. doi:10.1097/MNH.0000000000000152. PMC 5364028. PMID 26125647.
- ↑ “Chemistry for Biologists: Photosynthesis”. 《www.rsc.org》. 2016년 8월 4일에 원본 문서에서 보존된 문서. 2018년 2월 5일에 확인함.
- ↑ Smith, Alison M.; Zeeman, Samuel C.; Smith, Steven M. (2005). “Starch Degradation”. 《Annu. Rev. Plant Biol.》 56: 73–98. doi:10.1146/annurev.arplant.56.032604.144257. PMID 15862090.
- ↑ 가 나 Leszek Szablewski: Glucose Homeostasis and Insulin Resistance. Bentham Science Publishers, 2011, ISBN 978-1-608-05189-2, p. 46.
- ↑ Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 389. (독일어)
- ↑ Wang, Gehui; Kawamura, Kimitaka; Hatakeyama, Shiro; Takami, Akinori; Li, Hong; Wang, Wei (2007년 4월 4일). “Aircraft Measurement of Organic Aerosols over China”. 《Environmental Science & Technology》 41 (9): 3115–3120. Bibcode:2007EnST...41.3115W. doi:10.1021/es062601h. ISSN 0013-936X. PMID 17539513.
- ↑ Adeva-Andany, M. M.; Pérez-Felpete, N.; Fernández-Fernández, C.; Donapetry-García, C.; Pazos-García, C. (2016). “Liver glucose metabolism in humans”. 《Bioscience Reports》 36 (6): e00416. doi:10.1042/BSR20160385. PMC 5293555. PMID 27707936.
- ↑ H. Robert Horton, Laurence A. Moran, K. Gray Scrimgeour, Marc D. Perry, J. David Rawn: Biochemie. Pearson Studium; 4. aktualisierte Auflage 2008; ISBN 978-3-8273-7312-0; p. 490–496. (german)
- ↑ 가 나 Brian K. Hall: Strickberger's Evolution. Jones & Bartlett Publishers, 2013, ISBN 978-1-449-61484-3, p. 164.
- ↑ Jones, J. G. (2016). “Hepatic glucose and lipid metabolism”. 《Diabetologia》 59 (6): 1098–103. doi:10.1007/s00125-016-3940-5. PMID 27048250.
- ↑ Entner, N.; Doudoroff, M. (1952). “Glucose and gluconic acid oxidation of Pseudomonas saccharophila”. 《J Biol Chem》 196 (2): 853–862. doi:10.1016/S0021-9258(19)52415-2. PMID 12981024.
- ↑ Bonadonna, Riccardo C; Bonora, Enzo; Del Prato, Stefano; Saccomani, Maria; Cobelli, Claudio; Natali, Andrea; Frascerra, Silvia; Pecori, Neda; Ferrannini, Eleuterio; Bier, Dennis; DeFronzo, Ralph A; Gulli, Giovanni (July 1996). “Roles of glucose transport and glucose phosphorylation in muscle insulin resistance of NIDDM” (PDF). 《Diabetes》 45 (7): 915–25. doi:10.2337/diab.45.7.915. PMID 8666143. S2CID 219249555. 2017년 3월 6일에 원본 문서 (PDF)에서 보존된 문서. 2017년 3월 5일에 확인함.
- ↑ Bonadonna, Riccardo C; Bonora, Enzo; Del Prato, Stefano; Saccomani, Maria; Cobelli, Claudio; Natali, Andrea; Frascerra, Silvia; Pecori, Neda; Ferrannini, Eleuterio; Bier, Dennis; DeFronzo, Ralph A; Gulli, Giovanni (July 1996). “Roles of glucose transport and glucose phosphorylation in muscle insulin resistance of NIDDM” (PDF). 《Diabetes》 45 (7): 915–25. doi:10.2337/diab.45.7.915. PMID 8666143. S2CID 219249555. 2017년 3월 6일에 원본 문서 (PDF)에서 보존된 문서. 2017년 3월 5일에 확인함.
- ↑ “Glucose”. 2023년 12월 5일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ 《Medical Biochemistry at a Glance @Google books》, Blackwell Publishing, 2006, 52쪽, ISBN 978-1-4051-1322-9, 2018년 2월 23일에 원본 문서에서 보존된 문서
- ↑ 《Medical Biochemistry at a Glance @Google books》, Blackwell Publishing, 2006, 50쪽, ISBN 978-1-4051-1322-9, 2018년 2월 23일에 원본 문서에서 보존된 문서
- ↑ Annibaldi, A.; Widmann, C. (2010). “Glucose metabolism in cancer cells”. 《Current Opinion in Clinical Nutrition and Metabolic Care》 13 (4): 466–70. doi:10.1097/MCO.0b013e32833a5577. PMID 20473153. S2CID 205782021.
- ↑ Szablewski, L. (2013). “Expression of glucose transporters in cancers”. 《Biochimica et Biophysica Acta (BBA) - Reviews on Cancer》 1835 (2): 164–9. doi:10.1016/j.bbcan.2012.12.004. PMID 23266512.
- ↑ Adekola, K.; Rosen, S. T.; Shanmugam, M. (2012). “Glucose transporters in cancer metabolism”. 《Current Opinion in Oncology》 24 (6): 650–4. doi:10.1097/CCO.0b013e328356da72. PMC 6392426. PMID 22913968.
- ↑ Schümann, U.; Gründler, P. (1998). “Electrochemical degradation of organic substances at PbO2 anodes: Monitoring by continuous CO2 measurements”. 《Water Research》 32 (9): 2835–2842. doi:10.1016/s0043-1354(98)00046-3. ISSN 0043-1354.
- ↑ 〈Chapter 3: Calculation of the Energy Content of Foods – Energy Conversion Factors〉, 《Food energy – methods of analysis and conversion factors》, FAO Food and Nutrition Paper 77, Rome: Food and Agriculture Organization, 2003, ISBN 978-92-5-105014-9, 2010년 5월 24일에 원본 문서에서 보존된 문서
- ↑ Georg Schwedt: Zuckersüße Chemie. John Wiley & Sons, 2012, ISBN 978-3-527-66001-8, p. 100 (독일어).
- ↑ Schmidt, Lang: Physiologie des Menschen, 30. Auflage. Springer Verlag, 2007, p. 907 (독일어).
- ↑ Dandekar, T.; Schuster, S.; Snel, B.; Huynen, M.; Bork, P. (1999). “Pathway alignment: Application to the comparative analysis of glycolytic enzymes”. 《The Biochemical Journal》 343 (1): 115–124. doi:10.1042/bj3430115. PMC 1220531. PMID 10493919.
- ↑ Dash, Pramod. “Blood Brain Barrier and Cerebral Metabolism (Section 4, Chapter 11)”. 《Neuroscience Online: An Electronic Textbook for the Neurosciences》. Department of Neurobiology and Anatomy – The University of Texas Medical School at Houston. 2016년 11월 17일에 원본 문서에서 보존된 문서.
- ↑ Fairclough, Stephen H.; Houston, Kim (2004), “A metabolic measure of mental effort”, 《Biol. Psychol.》 66 (2): 177–190, doi:10.1016/j.biopsycho.2003.10.001, PMID 15041139, S2CID 44500072
- ↑ Gailliot, Matthew T.; Baumeister, Roy F.; DeWall, C. Nathan; Plant, E. Ashby; Brewer, Lauren E.; Schmeichel, Brandon J.; Tice, Dianne M.; Maner, Jon K. (2007), “Self-Control Relies on Glucose as a Limited Energy Source: Willpower is More than a Metaphor” (PDF), 《J. Pers. Soc. Psychol.》 92 (2): 325–336, CiteSeerX 10.1.1.337.3766, doi:10.1037/0022-3514.92.2.325, PMID 17279852, S2CID 7496171, 2017년 8월 18일에 원본 문서 (PDF)에서 보존된 문서
- ↑ Gailliot, Matthew T.; Baumeister, Roy F. (2007), “The Physiology of Willpower: Linking Blood Glucose to Self-Control”, 《Personal. Soc. Psychol. Rev.》 11 (4): 303–327, CiteSeerX 10.1.1.475.9484, doi:10.1177/1088868307303030, PMID 18453466, S2CID 14380313
- ↑ Masicampo, E. J.; Baumeister, Roy F. (2008), “Toward a Physiology of Dual-Process Reasoning and Judgment: Lemonade, Willpower, and Expensive Rule-Based Analysis”, 《Psychol. Sci.》 19 (3): 255–60, doi:10.1111/j.1467-9280.2008.02077.x, PMID 18315798, S2CID 38596025
- ↑ 가 나 다 Donard Dwyer: Glucose Metabolism in the Brain. Academic Press, 2002, ISBN 978-0-123-66852-3, p. XIII.
- ↑ 가 나 다 Koekkoek, L. L.; Mul, J. D.; La Fleur, S. E. (2017). “Glucose-Sensing in the Reward System”. 《Frontiers in Neuroscience》 11: 716. doi:10.3389/fnins.2017.00716. PMC 5742113. PMID 29311793.
- ↑ 가 나 Tucker, R. M.; Tan, S. Y. (2017). “Do non-nutritive sweeteners influence acute glucose homeostasis in humans? A systematic review”. 《Physiology & Behavior》 182: 17–26. doi:10.1016/j.physbeh.2017.09.016. PMID 28939430. S2CID 38764657.
- ↑ La Fleur, S. E.; Fliers, E.; Kalsbeek, A. (2014). 〈Neuroscience of glucose homeostasis〉. 《Diabetes and the Nervous System》. Handbook of Clinical Neurology 126. 341–351쪽. doi:10.1016/B978-0-444-53480-4.00026-6. ISBN 9780444534804. PMID 25410233..
- ↑ Bisschop, P. H.; Fliers, E.; Kalsbeek, A. (2015). “Autonomic regulation of hepatic glucose production”. 《Comprehensive Physiology》 5 (1): 147–165. doi:10.1002/cphy.c140009. PMID 25589267.
- ↑ W. A. Scherbaum, B. M. Lobnig, In: Hans-Peter Wolff, Thomas R. Weihrauch: Internistische Therapie 2006, 2007. 16th Edition. Elsevier, 2006, ISBN 3-437-23182-0, p. 927, 985 (독일어).
- ↑ Harold A. Harper: Medizinische Biochemie. Springer-Verlag, 2013, ISBN 978-3-662-22150-1, p. 294.
- ↑ Clarke, S. F.; Foster, J. R. (2012). “A history of blood glucose meters and their role in self-monitoring of diabetes mellitus”. 《British Journal of Biomedical Science》 69 (2): 83–93. CiteSeerX 10.1.1.468.2196. doi:10.1080/09674845.2012.12002443. PMID 22872934. S2CID 34263228.
- ↑ “Diagnosing Diabetes and Learning About Prediabetes”. 《American Diabetes Association》 (영어). 2017년 7월 28일에 원본 문서에서 보존된 문서. 2018년 2월 20일에 확인함.
- ↑ 가 나 Richard A. Harvey, Denise R. Ferrier: Biochemistry. 5th Edition, Lippincott Williams & Wilkins, 2011, ISBN 978-1-608-31412-6, p. 366.
- ↑ 가 나 U Satyanarayana: Biochemistry. Elsevier Health Sciences, 2014, ISBN 978-8-131-23713-7, p. 508.
- ↑ Holt, S. H.; Miller, J. C.; Petocz, P. (1997). “An insulin index of foods: The insulin demand generated by 1000-kJ portions of common foods”. 《The American Journal of Clinical Nutrition》 66 (5): 1264–1276. doi:10.1093/ajcn/66.5.1264. PMID 9356547.
- ↑ 가 나 Peter C. Heinrich: Löffler/Petrides Biochemie und Pathobiochemie. Springer-Verlag, 2014, ISBN 978-3-642-17972-3, p. 27. (독일어)
- ↑ Röder PV, Wu B, Liu Y, Han W (2016). “Pancreatic Regulation of Glucose Homeostasis”. 《Exp. Mol. Med.》 48 (3, March): e219–. doi:10.1038/emm.2016.6. PMC 4892884. PMID 26964835.
- ↑ Estela, Carlos (2011) "Blood Glucose Levels," Undergraduate Journal of Mathematical Modeling: One + Two: Vol. 3: Iss. 2, Article 12.
- ↑ “Carbohydrates and Blood Sugar”. 《The Nutrition Source》 (미국 영어). 2013년 8월 5일. 2017년 1월 30일에 원본 문서에서 보존된 문서. 2017년 1월 30일에 확인함 – Harvard T.H. Chan School of Public Health 경유.
- ↑ Venditti, Alessandro; Frezza, Claudio; Vincenti, Flaminia; Brodella, Antonia; Sciubba, Fabio; Montesano, Camilla; Franceschin, Marco; Sergi, Manuel; Foddai, Sebastiano; Di Cocco, Maria Enrica; Curini, Roberta (2019). “A syn-ent-labdadiene derivative with a rare spiro-β-lactone function from the male cones of Wollemia nobilis”. 《Phytochemistry》 158: 91–95. doi:10.1016/j.phytochem.2018.11.012. ISSN 0031-9422. PMID 30481664. S2CID 53757166.
- ↑ Lei, Yu; Shi, She-Po; Song, Yue-Lin; Bi, Dan; Tu, Peng-Fei (2014). “Triterpene Saponins from the Roots of Ilex asprella”. 《Chemistry & Biodiversity》 11 (5): 767–775. doi:10.1002/cbdv.201300155. ISSN 1612-1872. PMID 24827686. S2CID 40353516.
- ↑ Balan, Venkatesh; Bals, Bryan; Chundawat, Shishir P. S.; Marshall, Derek; Dale, Bruce E. (2009), 〈Lignocellulosic Biomass Pretreatment Using AFEX〉, 《Biofuels》, Methods in Molecular Biology 581, Totowa, NJ: Humana Press, 61–77쪽, Bibcode:2009biof.book...61B, doi:10.1007/978-1-60761-214-8_5, ISBN 978-1-60761-213-1, PMID 19768616, 2021년 11월 11일에 확인함
- ↑ “FoodData Central”. 《fdc.nal.usda.gov》.
- ↑ 가 나 다 라 마 바 사 아 자 P. J. Fellows: Food Processing Technology. Woodhead Publishing, 2016, ISBN 978-0-081-00523-1, p. 197.
- ↑ 가 나 Thomas Becker, Dietmar Breithaupt, Horst Werner Doelle, Armin Fiechter, Günther Schlegel, Sakayu Shimizu, Hideaki Yamada: Biotechnology, in: Ullmann's Encyclopedia of Industrial Chemistry, 7th Edition, Wiley-VCH, 2011. ISBN 978-3-527-32943-4. Volume 6, p. 48.
- ↑ 가 나 다 The Amylase Research Society of Japan: Handbook of Amylases and Related Enzymes. Elsevier, 2014, ISBN 978-1-483-29939-6, p. 195.
- ↑ Madsen, G. B.; Norman, B. E.; Slott, S. (1973). “A New, Heat Stable Bacterial Amylase and its Use in High Temperature Liquefaction”. 《Starch – Stärke》 25 (9): 304–308. doi:10.1002/star.19730250906.
- ↑ Norman, B. E. (1982). “A Novel Debranching Enzyme for Application in the Glucose Syrup Industry”. 《Starch – Stärke》 34 (10): 340–346. doi:10.1002/star.19820341005.
- ↑ James N. BeMiller, Roy L. Whistler (2009). 《Starch: Chemistry and Technology》. Food Science and Technology 3판. New York: Academic Press. ISBN 978-0080926551.
- ↑ BeMiller, James N.; Whistler, Roy L., 편집. (2009). 《Starch: Chemistry and Technology》. Food Science and Technology 3판. New York: Academic Press. ISBN 978-0080926551. 2016년 11월 25일에 확인함.
- ↑ Alan Davidson: Oxford Companion to Food (1999). "Mizuame", p. 510 ISBN 0-19-211579-0.
- ↑ Alan Davidson: The Oxford Companion to Food. OUP Oxford, 2014, ISBN 978-0-191-04072-6, p. 527.
- ↑ “Sugar”. Learning, Food Resources. 《food.oregonstate.edu》. Oregon State University, Corvallis, OR. 2012년 5월 23일. 2011년 7월 18일에 원본 문서에서 보존된 문서. 2018년 6월 28일에 확인함.
- ↑ “High Fructose Corn Syrup: Questions and Answers”. US Food and Drug Administration. 2014년 11월 5일. 2018년 1월 25일에 원본 문서에서 보존된 문서. 2017년 12월 18일에 확인함.
- ↑ Kevin Pang: Mexican Coke a hit in U.S. In: Seattle Times, October 29, 2004.
- ↑ Steve T. Beckett: Beckett's Industrial Chocolate Manufacture and Use. John Wiley & Sons, 2017, ISBN 978-1-118-78014-5, p. 82.
- ↑ James A. Kent: Riegel's Handbook of Industrial Chemistry. Springer Science & Business Media, 2013, ISBN 978-1-475-76431-4, p. 938.
- ↑ Datan E, Minn I, Peng X, He QL, Ahn H, Yu B, Pomper MG, Liu JO (2020). “A Glucose-Triptolide Conjugate Selectively Targets Cancer Cells under Hypoxia”. 《iScience》 23 (9): 101536. Bibcode:2020iSci...23j1536D. doi:10.1016/j.isci.2020.101536. PMC 7509213. PMID 33083765.
- ↑ Goodwin, Matthew L.; Gladden, L. Bruce; Nijsten, Maarten W. N. (2020년 9월 3일). “Lactate-Protected Hypoglycemia (LPH)”. 《Frontiers in Neuroscience》 14: 920. doi:10.3389/fnins.2020.00920. ISSN 1662-453X. PMC 7497796. PMID 33013305.
- ↑ H. Fehling: Quantitative Bestimmung des Zuckers im Harn. In: Archiv für physiologische Heilkunde (1848), volume 7, p. 64–73 (in German).
- ↑ B. Tollens: Über ammon-alkalische Silberlösung als Reagens auf Aldehyd. In Berichte der Deutschen Chemischen Gesellschaft (1882), volume 15, p. 1635–1639 (in German).
- ↑ Barfoed, C. (1873). “Ueber die Nachweisung des Traubenzuckers neben Dextrin und verwandten Körpern”. 《Zeitschrift für Analytische Chemie》 (독일어) 12: 27–32. doi:10.1007/BF01462957. S2CID 95749674.
- ↑ Emil Nylander: Über alkalische Wismuthlösung als Reagens auf Traubenzucker im Harne, Zeitschrift für physiologische Chemie. Volume 8, Issue 3, 1884, p. 175–185 Abstract. 보관됨 2015-09-23 - 웨이백 머신 (in German).
- ↑ 가 나 다 라 마 바 사 아 자 Georg Schwedt: Zuckersüße Chemie. John Wiley & Sons, 2012, ISBN 978-3-527-66001-8, p. 102 (in German).
- ↑ 가 나 Zhang Q, Zhao G, Yang N, Zhang L (2019). 〈Fasting blood glucose levels in patients with different types of diseases〉. 《Glycans and Glycosaminoglycans as Clinical Biomarkers and Therapeutics - Part A》. Progress in Molecular Biology and Translational Science 162. 277–292쪽. doi:10.1016/bs.pmbts.2019.01.004. ISBN 978-0-12-817738-9. PMID 30905457. 2024년 3월 18일에 원본 문서에서 보존된 문서. 2024년 3월 18일에 확인함.
- ↑ Trinder, P. (1969). “Determination of Glucose in Blood Using Glucose Oxidase with an Alternative Oxygen Acceptor”. 《Annals of Clinical Biochemistry》 6: 24–27. doi:10.1177/000456326900600108. S2CID 58131350.
- ↑ Mizoguchi, Makoto; Ishiyama, Munetaka; Shiga, Masanobu (1998). “Water-soluble chromogenic reagent for colorimetric detection of hydrogen peroxide—an alternative to 4-aminoantipyrine working at a long wavelength”. 《Analytical Communications》 35 (2): 71–74. doi:10.1039/A709038B.
- ↑ Wang, J. (2008). “Electrochemical glucose biosensors”. 《Chemical Reviews》 108 (2): 814–825. doi:10.1021/cr068123a. PMID 18154363..
- ↑ Chen, X.; Chen, J.; Deng, C.; Xiao, C.; Yang, Y.; Nie, Z.; Yao, S. (2008). “Amperometric glucose biosensor based on boron-doped carbon nanotubes modified electrode”. 《Talanta》 76 (4): 763–767. doi:10.1016/j.talanta.2008.04.023. PMID 18656655.
- ↑ Wang, Guangfeng; Wei, Yan; Zhang, Wei; Zhang, Xiaojun; Fang, Bin; Wang, Lun (2010). “Enzyme-free amperometric sensing of glucose using Cu-CuO nanowire composites”. 《Microchimica Acta》 168 (1–2): 87–92. doi:10.1007/s00604-009-0260-1. S2CID 98567636.
- ↑ Ohara, T. J.; Rajagopalan, R.; Heller, A. (1994). “"Wired" enzyme electrodes for amperometric determination of glucose or lactate in the presence of interfering substances”. 《Analytical Chemistry》 66 (15): 2451–2457. doi:10.1021/ac00087a008. PMID 8092486.
- ↑ 가 나 Borisov, S. M.; Wolfbeis, O. S. (2008). “Optical biosensors”. 《Chemical Reviews》 108 (2): 423–461. doi:10.1021/cr068105t. PMID 18229952.
- ↑ Ferri, S.; Kojima, K.; Sode, K. (2011). “Review of glucose oxidases and glucose dehydrogenases: A bird's eye view of glucose sensing enzymes”. 《Journal of Diabetes Science and Technology》 5 (5): 1068–76. doi:10.1177/193229681100500507. PMC 3208862. PMID 22027299.
- ↑ Mader, Heike S.; Wolfbeis, Otto S. (2008). “Boronic acid based probes for microdetermination of saccharides and glycosylated biomolecules”. 《Microchimica Acta》 162 (1–2): 1–34. doi:10.1007/s00604-008-0947-8. S2CID 96768832.
- ↑ Wolfbeis, Otto S.; Oehme, Ines; Papkovskaya, Natalya; Klimant, Ingo (2000). “Sol–gel based glucose biosensors employing optical oxygen transducers, and a method for compensating for variable oxygen background”. 《Biosensors and Bioelectronics》 15 (1–2): 69–76. doi:10.1016/S0956-5663(99)00073-1. PMID 10826645.
- ↑ 가 나 Galant, A. L.; Kaufman, R. C.; Wilson, J. D. (2015). “Glucose: Detection and analysis”. 《Food Chemistry》 188: 149–160. doi:10.1016/j.foodchem.2015.04.071. PMID 26041177.
- ↑ Sanz, M. L.; Sanz, J.; Martínez-Castro, I. (2004). “Gas chromatographic-mass spectrometric method for the qualitative and quantitative determination of disaccharides and trisaccharides in honey.”. 《Journal of Chromatography A》 1059 (1–2): 143–148. doi:10.1016/j.chroma.2004.09.095. PMID 15628134.
- ↑ Max Planck Institute of Molecular Plant Physiology in Golm Database (2007년 7월 19일). “Glucose mass spectrum”. 《Golm Metabolome Database》. 2018년 9월 9일에 원본 문서에서 보존된 문서. 2018년 6월 4일에 확인함.
- ↑ Cabañero, A. I.; Recio, J. L.; Rupérez, M. (2006). “Liquid chromatography coupled to isotope ratio mass spectrometry: a new perspective on honey adulteration detection.”. 《J Agric Food Chem》 54 (26): 9719–9727. doi:10.1021/jf062067x. PMID 17177492.
- ↑ Becker, M.; Liebner, F.; Rosenau, T.; Potthast, A. (2013). “Ethoximation-silylation approach for mono- and disaccharide analysis and characterization of their identification parameters by GC/MS”. 《Talanta》 115: 642–51. doi:10.1016/j.talanta.2013.05.052. PMID 24054643.
- ↑ Gesellschaft Deutscher Chemiker: wayback=20100331071121 Anlagen zum Positionspapier der Fachgruppe Nuklearchemie 보관됨 2010-03-31 - 웨이백 머신, February 2000.
- ↑ Maschauer, S.; Prante, O. (2014). “Sweetening pharmaceutical radiochemistry by (18)f-fluoroglycosylation: A short review”. 《BioMed Research International》 2014: 1–16. doi:10.1155/2014/214748. PMC 4058687. PMID 24991541.