리보스

| |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
(2R,3R,4S,5R)-5-(hydroxymethyl)oxolane-2,3,4-triol
| |||
| 별칭
d-Ribose
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
| ||
| ChEMBL | |||
| ChemSpider |
| ||
| DrugBank | |||
| EC 번호 |
| ||
PubChem CID
|
|||
| UNII | |||
| |||
| |||
| 성질[1][2] | |||
| C5H10O5 | |||
| 몰 질량 | 150.13 | ||
| 겉보기 | 흰색 고체 | ||
| 녹는점 | 95 °C (203 °F; 368 K) | ||
| 100 g/L (25 °C, 77 °F) | |||
손지기 회전 ([α]D)
|
−21.5° (H2O) | ||
| 관련 화합물 | |||
관련 알도펜토스
|
아라비노스, 자일로스, 릭소스 | ||
관련 화합물
|
디옥시리보스 | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
리보스(영어: ribose)는 5개의 탄소 원자가 포함된 단당류이고, 알데하이드기를 가지고 있는 알도스이며, 화학식은 C5H10O5이다. 피셔 투영식에서 모든 하이드록시기가 같은 쪽에 위치하고 있다.
D-리보스와 L-리보스는 서로 거울상 이성질체이다. D-리보스는 자연계에서 흔히 생성되는 반면 L-리보스는 자연계에서 발견되지 않는다.
D-리보스는 1891년에 헤르만 에밀 피셔에 의해 처음 보고되었다. D-리보스와 D-아라비노스(아라비아 고무에서 그 이름이 유래됨)는 2번 탄소(C-2)에서 입체화학적 성질이 다른 에피머이고, 'arabinose' 단어 문자를 부분적으로 재배열하여 'ribose'로 명명되었다.[3]
리보스 중 β-D-리보푸라노스는 RNA 골격의 일부를 형성한다. 이것은 DNA에서 발견되는 디옥시리보스와도 관련이 있다. ATP와 NADH와 같은 리보스의 인산화된 유도체는 물질대사에서 중심적인 역할을 수행한다. ATP 및 GTP로부터 형성된 cAMP와 cGMP는 일부 신호 전달 경로에서 2차 전달자로 작용한다.
RNA는 DNA의 정보를 전사하고 운반하며, 단백질을 합성하는 유전자 발현 과정에 참여한다.[4]
구조[편집]
리보스는 5개의 탄소 원자가 포함된 단당류이며, 사슬형일 때 사슬 끝부분에 알데하이드기를 가지고 있는 알도스이다. 단당류에 대한 종래의 번호 매김 체계대로 알데하이드기의 탄소를 1번(C1)으로 하여 5번(C5)까지 번호를 매기되, 뉴클레오타이드나 뉴클레오사이드의 경우 질소 염기에 붙이는 번호와 구별하기 위하여 오탄당의 탄소 번호에 프라임 부호(')를 붙여서 표시한다. DNA에서 발견되는 리보스의 유도체인 디옥시리보스는 C2'에서 하이드록시기 대신에 수소 원자를 가지는 점이 리보스와 다르다. 리보스의 C2' 하이드록시기는 RNA 스플라이싱에서 그 기능을 수행한다.
많은 단당류와 마찬가지로 리보스는 다섯 가지 형태의 평형 상태로 존재한다. 각각은 H−(C=O)−(CHOH)4–H 인 사슬형, 5원자 고리형인 α-리보푸라노스, β-리보푸라노스, 6원자 고리형인 α-리보피라노스, β-리보피라노스이다. 수용액에서 우세한 형태는 β-리보피라노스이다.[5]
D-리보스에서 "D-"는 알데하이드기로부터 가장 멀리 떨어져 있는 키랄 탄소의 입체화학적 배치를 의미한다. 모든 D-당류와 마찬가지로 D-리보스에서 이 키랄 탄소의 입체화학적 배치는 D-글리세르알데하이드의 배치와 동일하다.
| D-리보스의 구조 | ||
|---|---|---|
| 골격 구조식 | 하워드 투영식 | |

|
 α-D-리보푸라노스 |
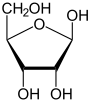 β-D-리보푸라노스 |
 α-D-리보피라노스 |
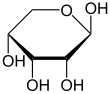 β-D-리보피라노스 | |
수용액에서 리보스 각 형태의 상대적 비율은 β-D-리보피라노스 (59%), α-D-리보피라노스 (20%), β-D-리보푸라노스 (13%), α-D-리보푸라노스 (7%), 사슬형 (0.1%)이다.[6]
인산화[편집]
생물학에서 D-리보스는 세포에 의해 인산화되어야 사용될 수 있다. 리보키네이스는 리보스를 리보스 5-인산으로 전환하는 반응을 촉매한다. 일단 전환되면 리보스 5-인산은 트립토판 및 히스티딘 아미노산 생성에 이용 가능하고, 펜토스 인산 경로에서 이용될 수 있다. D-리보스의 흡수는 소장에서 88~100% (최대 200 mg/kg/h)이다.[7]
같이 보기[편집]
각주[편집]
- ↑ 《The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals》 11판, Merck, 1989, ISBN 091191028X, 8205
- ↑ Weast, Robert C., 편집. (1981). 《CRC Handbook of Chemistry and Physics》 62판. Boca Raton, FL: CRC Press. C-506쪽. ISBN 0-8493-0462-8.
- ↑ Nechamkin, Howard (December 1958). “Some interesting etymological derivations of chemical terminology”. 《Science Education》 42 (5): 463–474. doi:10.1002/sce.3730420523.
- ↑ Pulves 외, 이광웅 외 역, 생명 생물의 과학, 2006, 교보문고, ISBN 89-7085-516-5, 224-225쪽
- ↑ Angyal, S. J. (March 1969). “The Composition and Conformation of Sugars in Solution”. 《Angewandte Chemie》 8 (3): 157–166. doi:10.1002/anie.196901571. 2012년 6월 5일에 확인함.
- ↑ Drew, Kenneth N.; Zajicek, Jaroslav; Bondo, Gail; Bose, Bidisha; Serianni, Anthony S. (February 1998). “13C-labeled aldopentoses: detection and quantitation of cyclic and acyclic forms by heteronuclear 1D and 2D NMR spectroscopy”. 《Carbohydrate Research》 307 (3-4): 199–209. doi:10.1016/S0008-6215(98)00040-8. 2014년 12월 11일에 확인함.
- ↑ “Herbal Remedies, Supplements A-Z Index”. PDRHealth. 2008년 10월 11일에 원본 문서에서 보존된 문서.

