비타민 C
| |

| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
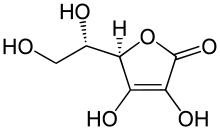
| l-threo-Hex-2-enono-1,4-lactone or (R)-3,4-Dihydroxy-5-((S)- 1,2-dihydroxyethyl)furan-2(5H)-one | |
| 식별 정보 | |
| CAS 등록번호 | 50-81-7 |
| ATC 코드 | A11GA01 A11GB01 G01AD03 S01XA15 |
| PubChem | 54670067 |
| 드러그뱅크 | DB00126 |
| ChemSpider | 10189562 |
| 화학적 성질 | |
| 화학식 | C6H8O6 |
| 분자량 | ? |
| 유의어 | 아스코르브산 |
| 물리적 성질 | |
| 밀도 | 1.694 g/cm³ |
| 녹는점 | 190–192 °C (374–378 °F) (some decomposition)[1] |
| 끓는점 | 552.7 °C (1027 °F) [2] |
| 약동학 정보 | |
| 생체적합성 | 빠르게 완전히 흡수됨 |
| 단백질 결합 | 미미함 |
| 동등생물의약품 | ? |
| 약물 대사 | ? |
| 생물학적 반감기 | 혈장 농도에 따라 달라짐 |
| 배출 | 콩팥 |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | ? |
| 법적 상태 | |
| 투여 방법 | 경구 투여, 근육 주사 (IM), 정맥 주사 (IV), 피하 주사 |
비타민 C(영어: Vitamin C) 또는 L-아스코베이트(영어: L-ascorbate)는 수용성 비타민의 한 종류이다. 귤과 같은 과일이나 여러 채소에 풍부하게 들어있고 정제하여 건강보조식품으로 판매되기도 한다.[8] 괴혈병의 예방 및 치료제로 쓰인다.[9]
강한 환원제로서 콜라겐의 합성 효소 활성화등 인체에 있어 필수적인 성분중 하나이다.[10] 음식이나 약제를 통해 콜라겐을 섭취하더라도 소화 과정에서 대부분 아미노산을 통해 분해되며 인체는 필요한 콜라겐을 스스로 합성한다.[11] 비타민 C는 인체의 콜라겐 합성에 꼭 필요한 요소이다.
비타민 C는 일부 동물의 경우 채내에서 스스로 합성하지만 사람은 그렇지 못하기 때문에 음식을 통해 섭취하여야만 한다.[12]
역사[편집]
비타민 C의 부족과 그에 따른 괴혈병은 이미 선사시대의 시체서도 발견된다.[13]:42 - 43 아마도 빙하기를 견디며 식물성 음식을 구하기 어려웠기 때문일 것이다. 인류가 겨울철에도 비타민 C를 충분히 공급받기 시작한 것은 농업 혁명이 있던 신석기 시대 이후이다.[14] 그러나 괴혈병의 예방과 치료법은 역사 시대 동안 간헐적으로 발견되었어도 다시 잊혀졌다. 비타민의 발견과 과학적 탐구는 근세 이후의 일이다. 대항해 시대 동안 선원들은 알려지지 않은 질병으로 고통받았다. 오랫 동안 항해를 하다 보면 피부가 탄력을 잃고 입에서 피가 나며 무기력증에 시달리다 심할 경우 사망에 이르렀다. 사람들은 원인을 알 수 없는 이 병을 괴혈병이라 불렀다. 바스쿠 다가마가 희망봉을 돌 무렵 선원 160 명 가운데 100 여명이 괴혈병으로 사망할 정도로 오랜 항해에 괴혈병은 심각한 장애였다. 18세기 후반 영국 해군 소속 군의관 제임스 린드는 실험을 통해 감귤류 등의 과일을 제공하면 괴혈병을 예방하고 치료할 수 있다는 사실을 발견했다. 이후 제임스 쿡의 시기에 이르면 세계를 일주하는 동안 단 한 명의 선원도 괴혈병에 걸리지 않을 만큼 영국 해군은 과일 지급을 통해 괴혈병을 억제하는 데 성공하였다. 20세기에 들어 헝가리 출신의 생화학자 알베르트 센트죄르지가 비타민 C 결정을 추출하는 데 성공하여 1932년 《네이쳐》에 발표하였고 1937년 이 공로로 노벨 생리학상을 수상하였다. 1933년 영국의 월터 노먼 하워스가 포도당을 재료로 비타민 C를 합성하여 인공적인 생산의 길을 열었다.[13]:42 - 52
비타민[편집]
비타민으로 불리는 영양소들은 많은 양이 필요하지는 않지만 부족할 경우 건강에 문제가 생긴다. 영양과 신진 대사에 대한 지식이 부족한 시기 비타민 C의 부족으로 인한 괴혈병과 비타민 B의 부족으로 인한 각기병은 근세 여러 문화에서 새롭게 부각된 질병이었다.[15] 여러 경로를 통해 이들 질병의 원인과 치료법이 점차 발견되었고 1912년 폴란드의 카지미르 풍크가 이들을 묶어 비타민이라는 이름을 붙였다. 풍크는 이 물질들이 모두 아민을 포함하고 있다고 여겨 라틴어로 생명을 뜻하는 Vita- 와 아민(Amine)을 조합하여 Vitamine 이라고 이름을 붙였지만 훗날 모든 비타민이 아민을 포함하고 있지는 않다는 것이 밝혀지며 맨 뒤의 e 를 뺀 Vitamin 이 학술명으로 채택되었다.[16] 비타민을 알파벳 순으로 정리한 사람은 미국의 생화학자 엘머 매콜럼으로 비타민 A를 발견한 사람이기도 하다. 그는 1913년 기름에 녹는 지용성 비타민을 비타민 A로 물에 녹는 비타민을 비타민 B로 구분하였다. 그러나 1920년 영국의 잭 드러먼드가 비타민 B와 비타민 C가 서로 다른 수용성 비타민임을 밝혀 둘을 구분하였다.[17] 오늘날 비타민은 A에서 K까지 구분된다.
효능과 부작용[편집]
비타민 C는 사람을 포함한 동물들의 결합조직의 형성을 위한 효소의 작용을 매개하는 보조 인자로 혈관, 피부, 인대 등의 생장과 상처 치료에 반드시 필요하다. 임신과 출산 이후 수유 과정에서 비타민 C의 손실이 크게 발생하고 이외에도 각종 감염이나 상처, 수술 후에도 비타민 C의 손실이 있다. 비타민 C가 부족해지면 쉽게 피로감을 느끼고 피부의 탄력이 떨어지며 심하면 잇몸에서 피가 나는 괴혈병에 걸린다.[9]
비타민 C의 복용은 비타민 부족에 의한 질병을 예방하는 효과가 있지만 일정 이상의 복용은 오히려 해가 된다. 성인 기준 500 mg이 하루 섭취 최대 최적치로 이를 초과하면 백혈구의 DNA가 손상될 수 있다.[18]
문화[편집]
세계 대부분의 지역에서 사람들은 과일과 채소등 식물성 음식을 통해 자연스럽게 비타민 C를 섭취한다. 그러나 극지방에 사는 이누이트와 같이 식물성 음식을 구하기 어려운 사람들은 사냥한 동물의 부신을 먹어 비타민 C를 보충한다. 사람과 달리 동물들은 자체적으로 비타민 C를 합성할 수 있으며 부신에 저장하기 때문이다. 이 때문에 이누이트는 평생 고기만 먹어도 괴혈병에 걸리지 않는다.[12]
같이 보기[편집]
각주[편집]
- ↑ Merck Index, 14th ed.
- ↑ “Vitamin C”. 《ChemSpider》. Royal Society of Chemistry. 2020년 7월 25일에 확인함.
- ↑ “Ascorbic Acid Injection 500mg/5ml - Summary of Product Characteristics (SmPC)”. 《(emc)》. 2015년 7월 15일. 2020년 10월 12일에 확인함.
- ↑ “Ascorbic Acid 100mg Tablets - Summary of Product Characteristics (SmPC)”. 《(emc)》. 2018년 10월 29일. 2020년 9월 21일에 원본 문서에서 보존된 문서. 2020년 10월 12일에 확인함.
- ↑ “Ascor- ascorbic acid injection”. 《DailyMed》. 2020년 10월 2일. 2020년 10월 12일에 확인함.
- ↑ “Ascorbic Acid liquid”. 《DailyMed》. 2018년 11월 13일. 2020년 10월 12일에 확인함.
- ↑ “Leonas Vitamin C- ascorbic acid tablet, chewable”. 《DailyMed》. 2018년 9월 14일. 2020년 10월 12일에 확인함.
- ↑ “Ascorbic Acid”. The American Society of Health-System Pharmacists. 2016년 12월 30일에 원본 문서에서 보존된 문서. 2016년 12월 8일에 확인함.
- ↑ 가 나 비타민C 결핍, MSD 메뉴얼
- ↑ ‘콜라겐’ 양보다 궁합…비타민C 없으면 무용지물, 매경헬스, 2022년 3월 3일
- ↑ "먹는 콜라겐 효과, 광고처럼 좋을까?"...의사들이 답했다, 하이닥, 2021년 5월 13일
- ↑ 가 나 괴혈병과 에스키모인…’비타민C의 비밀’, 사이언스타임스, 2010년 1월 26일
- ↑ 가 나 사토 겐타로 저, 서수지 역, 《세계사를 바꾼 10가지 약》, 사람과나무사이, ISBN 9791188635108
- ↑ 만일 재배식물이 없었다면? 모든 것이 곡물에 달렸다, 프레시안, 2018년 1월 6일
- ↑ 구석구석 과학사 (40) 각기병을 연구하다 비타민을 찾아내다, 경향신문, 2018년 9월 17일 - 근세 이후 쌀의 겉면을 크게 깍아내는 도정법의 개량으로 백미를 먹게 되면서 기존의 현미와 함께 자연스럽게 섭쉬하던 비타민 B가 부족해 진 것이 각기병의 원인이다.
- ↑ 최진호 양계 영양 강좌, 월간양계, 1992년 1월호
- ↑ 재미있는 생명이야기 - 비타민 발견의 역사에 담긴 이야기들, 기술과 혁신, 2022년 11월/12월호
- ↑ 비타민 C의 과다복용은 당신의 건강을 해치는가?, 서울아산병원
외부 링크[편집]
- (영어) Vitamin C Fact Sheet from the U.S. National Institutes of Health
- (영어) Vitamin C bound to proteins in the PDB
- (영어) National Nutrient Database Archived 2014년 8월 10일 - 웨이백 머신 at USDA Website
