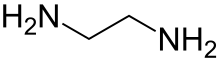
에틸렌다이아민
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Ethane-1,2-diamine | |||
| 체계명
Ethane-1,2-diamine[2] | |||
| 별칭
Edamine[1] 1,2-Diaminoethane, 'en' when a ligand
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 약어 | en | ||
| 605263 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.154 | ||
| EC 번호 |
| ||
| 1098 | |||
| KEGG | |||
| MeSH | ethylenediamine | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1604 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C2H8N2 | |||
| 몰 질량 | 60.100 g·mol−1 | ||
| 겉보기 | 무색 액체[3] | ||
| 냄새 | Ammoniacal[3] | ||
| 밀도 | 0.90 g/cm3[3] | ||
| 녹는점 | 8 °C (46 °F; 281 K)[3] | ||
| 끓는점 | 116 °C (241 °F; 389 K)[3] | ||
| miscible | |||
| log P | −2.057 | ||
| 증기 압력 | 1.3 kPa (at 20 °C) | ||
헨리 상수 (kH)
|
5.8 mol Pa−1 kg−1 | ||
자화율 (χ)
|
| ||
굴절률 (nD)
|
1.4565 | ||
| 열화학 | |||
열용량 (C)
|
172.59 J K−1 mol−1 | ||
표준 몰 엔트로피 (S
|
202.42 J K−1 mol−1 | ||
표준 생성 엔탈피 (ΔfH⦵298)
|
−63.55–−62.47 kJ mol−1 | ||
표준 연소 엔탈피 (ΔcH⦵298)
|
−1.8678–−1.8668 MJ mol−1 | ||
| 위험 | |||
| GHS 그림문자 |    
| ||
| 신호어 | 위험 | ||
| H226, H302, H312, H314, H317, H334 | |||
| P261, P280, P305+351+338, P310 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 34 °C (93 °F; 307 K)[3] | ||
| 385 °C (725 °F; 658 K)[3] | |||
| 폭발 한계 | 2.7–16% | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose)
|
500 mg/kg (구강, 생쥐) 470 mg/kg (구강, 기니피그) 1160 mg/kg (구강, 생쥐)[5] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용)
|
TWA 10 ppm (25 mg/m3)[4] | ||
REL (권장)
|
TWA 10 ppm (25 mg/m3)[4] | ||
IDLH (직접적 위험)
|
1000 ppm[4] | ||
| 관련 화합물 | |||
관련 alkanamines
|
1,2-프로필렌다이아민, 1,3-프로필렌다이아민 | ||
관련 화합물
|
에틸아민, 에틸렌디니트로아민 | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
에틸렌다이아민(영어: ethylenediamine), 에틸렌디아민 또는 1,2-다이아미노에테인(영어: 1,2-diaminoethane)은 유기 화합물의 일종이다. 킬레이트제로 작용할 수 있으며 리간드일 경우 en으로 축약시켜 표기하기도 한다. 화학식은 C2H4(NH2)2이다. 무색 액체 상태로 존재하며 분자량은 60.1, 밀도는 0.899g/cm3, 녹는점은 8.5℃, 끓는점은 116.5℃이다. 강염기성이며, 암모니아 냄새가 난다.
제법[편집]
에틸렌다이아민은 암모니아와 1,2-다이클로로에테인의 반응으로 얻어진다. 반응식은 다음과 같다.
- ClCH2CH2Cl + 4 NH3 → H2NCH2CH2NH2 + 2 NH4Cl
용도[편집]
에틸렌다이아민은 여러 가지 용도로 사용된다. 대표적인 것으로는 다음과 같은 것들이 있다.
합성의 재료[편집]
에틸렌다이아민은 유기 합성의 원료로 사용된다. 에틸렌다이아민으로부터 생성되는 물질은 대표적으로 다음과 같은 것들이 있다.
- 에틸렌다이아민테트라아세트산(ethylenediaminetetraacetic acid, EDTA)는 에틸렌다이아민과 폼알데하이드, 물, 그리고 사이안화 나트륨이 반응하여 생성된다.
- 테트라아세틸에틸렌다이아민(tetraacetylethylenediamine, TAED)는 표백제에 사용되는 물질이다. TAED는 에틸렌다이아민과 아세트산이 반응한 후 무수아세트산이 반응한 결과 생성된다.
- 의약품인 아미노필린의 성분으로 사용된다. 아미노필린은 에틸렌다이아민과 테오필린을 1 : 2의 비율로 섞은 것이다.
이 외에도 각종 착화합물, 섬유처리제, 합성수지 등의 원료로도 사용된다.
킬레이트제[편집]
에틸렌다이아민은 두 자리 리간드로 작용할 수 있어서, 금속 이온과 배위하여 착물을 형성한다. 따라서 특정한 금속 이온을 농축, 분리, 제거, 이동하는 데 사용될 수 있다.
이러한 성질을 활용한 대표적인 예로 에틸렌다이아민 착염을 이용한 금속 이온의 분석시약을 들 수 있다. [Cuen2](NO3)2, [Coen3]Cl3와 같은 에틸렌다이아민의 금속 착염은 특정 금속 이온과 반응하여 난용성의 염을 침전시키는데, 이 성질을 이용하여 용액 내의 금속 이온의 양을 측정할 수 있다.
위험성[편집]
에틸렌다이아민은 체내에 흡수되었을 때 알레르기 반응을 일으킬 수 있다. 피부에 염증을 일으킬 수 있으며 점액질 막을 파괴시킬 수 있다.
섭취[편집]
부식성이 있어 삼킬 경우 해롭다. 목의 통증, 복통, 구토, 설사가 있을 수 있다.
흡입[편집]
코와 목, 호흡계에 자극을 줄 수 있다. 기침, 목의 통증, 호흡곤란이 있을 수 있다. 심할 경우 치명적일 수도 있다. 일부에게 알레르기 반응이 있을 수 있다.
피부[편집]
부식성이 있으며, 독성이 있다. 심한 자극과 함께 발적, 통증이 있을 수 있고 화상을 입을 수도 있다. 피부를 통해 흡수될 수 있으며 일부에게 알레르기 반응이 있을 수 있다.
눈[편집]
부식성이 있다. 증기는 자극성이며, 액체는 화상을 입힐 수 있다.
참고 문헌[편집]
- http://msds.chem.ox.ac.uk/ET/ethylenediamine.html Archived 2008년 5월 27일 - 웨이백 머신
- https://web.archive.org/web/20080416220406/http://www.dow.com/amines/apps/
- https://web.archive.org/web/20080527092306/http://www.jtbaker.com/msds/englishhtml/e4500.htm
각주[편집]
- ↑ “32007R0129”. European Union. 2007년 2월 12일. Annex II. 2012년 5월 3일에 확인함.
- ↑ “ethylenediamine - Compound Summary”. 《PubChem Compound》. USA: National Center for Biotechnology Information. 2004년 9월 16일. Identification and Related Records. 2012년 5월 3일에 확인함.
- ↑ 가 나 다 라 마 바 사 Record in the GESTIS Substance Database of the Institute for Occupational Safety and Health
- ↑ 가 나 다 NIOSH Pocket Guide to Chemical Hazards. “#0269”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ “에틸렌디아민”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).



