세포 호흡

세포 호흡(細胞呼吸, 영어: cellular respiration)은 생화학적 에너지를 영양소로부터 아데노신 삼인산(ATP)으로 전환하고, 부산물을 방출하는 생명체의 세포에서 일어나는 일련의 대사 반응과 과정들이다.[1] 세포 호흡과 관련된 반응들은 소위 "고에너지"의 약한 결합이 생성물에서 더 강한 결합으로 대체되기 때문에 큰 분자를 더 작은 분자로 분해하는 과정에서 에너지를 방출하는 이화작용이다. 세포 호흡은 세포가 세포 활동을 촉진하기 위해 화학 에너지를 방출하는 핵심적인 방법들 중 하나이다. 세포 호흡은 열에너지를 방출하는 발열 반응이며, 산화환원 반응으로 간주된다. 전체적인 반응은 일련의 생화학적 단계에서 일어나는데, 대부분은 산화환원 반응이다. 세포 호흡은 기술적으로 연소 반응이지만, 일련의 반응들로부터 에너지가 느리게 방출되기 때문에 살아있는 세포에서 일어나는 세포 호흡은 연소 반응과 완전하게 동일하지는 않다. 산소를 사용하는 산소 호흡(또는 유기 호흡)과 산소를 사용하지 않는 무산소 호흡(또는 무기 호흡)으로 나눌 수 있다.
동물 세포 및 식물 세포가 세포 호흡에 일반적으로 사용하는 영양소로는 탄수화물, 아미노산, 지방산이 있으며, 가장 일반적인 산화제(전자수용체)는 산소 분자(O2)이다. ATP에 저장된 화학 에너지는 세포막을 가로지르는 분자의 생합성, 이동이나 수송을 포함하여 에너지를 필요로 하는 과정을 추진하는 데 사용될 수 있다. ATP의 세 번째 인산기는 쉽게 가수분해되어 세포가 사용하는 에너지를 전달할 수 있다.
산소 호흡
[편집]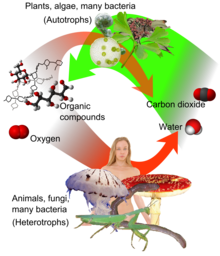
산소 호흡은 ATP를 생성하기 위해 산소(O2)를 필요로 한다. 탄수화물, 지방, 단백질은 반응물로 섭취되며, 해당 과정에서 호흡 기질은 주로 피루브산으로 분해되며, 피루브산이 시트르산 회로에서 완전히 산화되기 위해서는 미토콘드리아 기질로 들어가야 한다. 호흡 기질이 완전히 분해되면 이산화탄소와 물이 생성되며, 이 과정에서 방출되는 에너지의 일부는 기질 수준 인산화나 산화적 인산화 과정을 통해 ATP를 생성하는 데 사용된다.
| 단순화한 반응식: | C6H12O6 (고체) + 6 O2 (기체) + 6 H2O (액체) → 6 CO2 (기체) + 12 H2O (액체) + 32 ATP + 열 |
| ΔG = −2880 kJ (C6H12O6 1몰당) |
음(−)의 ΔG 값은 반응이 자발적으로 일어날 수 있음을 나타낸다.
NADH와 FADH2가 가지고 있는 화학적 위치 에너지는 산소(O2)를 최종 전자수용체로 하는 전자전달계를 통해 더 많은 ATP로 전환된다. 산소 호흡에 의해 생성된 대부분의 ATP는 산화적 인산화에 의해 만들어진다. 이것은 호흡 기질이 분해될 때 방출되는 에너지에 의해 작용하여 막을 가로질러 H+(양성자)를 능동수송함으로써 전기화학적 기울기를 형성하는 데 사용된다. 이러한 전기화학적 기울기에 의해 형성된 위치 에너지는 ATP 생성 효소를 작동시키는 데 사용되며, ADP와 Pi(무기 인산)으로부터 ATP를 생성하는 데 사용된다. 생물학 교과서에서는 보통 세포 호흡에서 포도당 1분자당 32 ATP가 만들어질 수 있다고 기술되어 있다(NADH당 2.5 ATP, FADH2당 1.5 ATP가 만들어진다고 할 경우에 해당 과정에서 2 ATP, 시트르산 회로에서 2 ATP, 산화적 인산화에서 28 ATP).[2] 그러나 ATP의 이론적인 최대 생산량은 막의 누수 및 피루브산과 ADP를 미토콘드리아 기질로 운반하는 비용으로 인해 절대로 달성될 수 없으며, 현재 추정치는 포도당 1 분자당 약 29 ~ 30 ATP이다.[2]
산소 호흡은 무산소 호흡(포도당 1 분자당 2 ATP를 생성함)보다 15배 이상 효율적이다. 그러나 메테인 세균과 같은 일부 혐기성 생물들은 혐기성 호흡을 계속 할 수 있으며, 전자전달계에서 최종 전자수용체로 O2가 아닌 다른 무기 분자들을 사용하여 더 많은 ATP를 생성한다. 이들 혐기성 대사 경로들은 해당 과정의 초기 경로를 공유하지만, 호기성 대사 경로는 시트르산 회로와 산화적 인산화로 이어진다. 해당 과정 이후의 과정들은 진핵세포에서는 미토콘드리아에서 일어나고, 원핵세포에서는 세포질에서 일어난다.
해당 과정
[편집]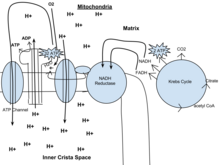
해당 과정은 모든 생명체의 세포의 세포질에서 일어나는 대사 경로이다. 해당 과정은 산소(O2)의 존재 여부와 상관 없이 일어날 수 있다. 사람의 경우, 호기성 조건에서는 피루브산을 생성하고, 혐기성 조건에서는 젖산을 생성한다. 호기성 조건에서 해당 과정은 1 분자의 포도당을 2분자의 피루브산으로 전환시키고, 이 과정에서 방출되는 에너지로 2 분자의 ATP를 순생산한다. 포도당 1 분자당 4 ATP가 생성되지만, 에너지 투자기에 2 ATP를 소비하므로 2 ATP를 순생산하는 것이 된다. 해당 과정의 에너지 투자기에서 포도당의 인산화는 6탄당을 알돌레이스에 의해 2 분자의 피루브산으로 분해하기 위해 반응성을 증가(안정성을 감소)시키는 데에 필요하다. 해당 과정의 에너지 회수기에서 기질 수준 인산화에 의해 4 ATP가 생성되고, 2 NADH가 생성된다. 해당 과정의 전체 반응식은 다음과 같다.
- 포도당 + 2 NAD+ + 2 Pi + 2 ADP → 2 피루브산 + 2 NADH + 2 ATP + 2 H+ + 2 H2O + 열
해당 과정의 초기에 포도당은 ATP로부터 인산기를 전달받아 포도당 6-인산으로 전환된다. 글리코젠은 글리코젠 가인산분해효소에 의해 포도당 6-인산으로 전환될 수 있다. 해당 과정에서 포도당 6-인산은 과당 6-인산으로 전환된다. 과당 6-인산은 포스포프럭토키네이스-1에 의해 과당 1,6-이중인산으로 인산화되며, 이 과정에서 ATP가 소모된다. 과당 1,6-이중인산은 2 분자의 삼탄당 인산으로 분해된 후에 여러 단계를 거쳐서 피루브산으로 전환된다.
"해당 과정(glycolysis)"은 문자 그대로 당을 분해하는 과정이라는 의미로 포도당(글루코스, glucose)의 옛 이름인 "글리코스(glycose)"와 분해를 의미하는 "-lysis"의 합성어이다.[3]
피루브산의 산화적 탈카복실화 및 TCA 회로(=시트르산 회로)
[편집]피루브산은 피루브산 탈수소효소 복합체에 의해 아세틸-CoA와 CO2로 산화된다. 피루브산 탈수소 효소 복합체는 3 가지 효소의 여러 소단위체들을 포함하고 있으며, 진핵세포의 미토콘드리아와 원핵세포의 세포질에 위치한다. 피루브산이 아세틸-CoA로 전환되는 과정에서 1 분자의 NADH와 1 분자의 CO2가 생성된다.
TCA 회로는 트라이카복실산 회로(tricarboxylic acid cycle, TCA 회로) 또는 크렙스 회로(Krebs cycle)라고도 한다. 산소가 있으면, 해당 과정으로부터 생성된 피루브산으로부터 아세틸-CoA가 생성된다. 아세틸-CoA가 생성되면, 산소 호흡이 일어날 수 있다.[4] 산소가 있으면, 미토콘드리아는 시트르산 회로를 거쳐 산소 호흡을 진행한다. 그러나 산소가 없으면, 발효가 일어난다. 산소가 있으면, 생성된 아세틸-CoA는 미토콘드리아 기질에 있는 TCA 회로로 들어가서 CO2로 산화되고, 이 과정에서 방출되는 에너지로 NAD+를 NADH로 환원시킨다. NADH는 산화적 인산화에 의한 ATP 합성에 사용되기 위해 전자전달계에서 사용될 수 있다. 포도당 1 분자를 완전히 산화시키기 위해서는 2 분자의 아세틸-CoA가 시트르산 회로에 의해 대사되어야 한다. TCA 회로에서 H2O와 CO2가 부산물로 생성된다.
TCA 회로는 여러 효소와 조효소들이 관여하는 8 단계 과정이다.[4] TCA 회로에서 아세틸-CoA(2 탄소, CoA의 탄소는 제외)는 옥살아세트산(4 탄소)과 반응하여 시트르산(6 탄소)을 생성하며, 다음 단계에서 아이소시트르산(6 탄소)이라고 하는 더 반응성이 큰 형태로 재배열된다. 아이소시트르산은 α-케토글루타르산(5 탄소), 석시닐-CoA(4 탄소, CoA의 탄소는 제외), 석신산(4 탄소), 푸마르산(4 탄소), 말산(4 탄소), 옥살아세트산(4 탄소)으로 순차적으로 전환된다.
TCA 회로가 1 번 돌아갈 때 고에너지 화합물의 순생성량은 3NADH, 1 FADH2, 1 GTP이며, GTP는 이후에 ATP를 생성하는 데 사용될 수 있다. 따라서 포도당 1 분자(피루브산 2 분자)로부터의 총 생성량은 6 NADH, 2 FADH2, 2 ATP이다.
산화적 인산화
[편집]진핵생물에서 산화적 인산화는 미토콘드리아 내막에서 일어난다. 산화적 인산화는 해당 과정과 시트르산 회로에서 생성된 NADH를 산화시켜 미토콘드리아 내막을 경계로 H+(양성자)의 농도 기울기(전기화학적 기울기)를 형성시키는 전자전달계를 포함한다. 미토콘드리아 내막을 경계로 형성된 H+(양성자)의 농도 기울기에 의해 H+이 ATP 생성 효소를 통해 막 사이 공간에서 미토콘드리아 기질로 확산될 때(화학 삼투) ATP가 합성된다. 전자는 최종적으로 외부로부터 공급된 산소(O2)로 전달되고, 두 개의 H+(양성자)가 첨가됨으로써 물이 형성된다.
ATP 생성의 효율
[편집]아래 표는 포도당 1 분자가 이산화탄소(CO2)로 완전히 산화될 때의 반응을 설명한다. 환원된 조효소들은 전자전달계에 의해 산화되어 산화적 인산화에서 모두 사용된다고 가정한다.
| 단계 | 조효소의 생성량 | ATP의
생성량 |
ATP의 생성 방식 |
|---|---|---|---|
| 해당 과정의 에너지 투자기 | −2 | 세포질에서 포도당 및 과당 6-인산의 인산화 과정에서 2 ATP가 소모된다. | |
| 해당 과정의 에너지 회수기 | 4 | 기질 수준 인산화 | |
| 2 NADH | 3 또는 5 | 산화적 인산화: 각각의 NADH는 미토콘드리아 막을 통한 NADH의 수송(ATP를 소모함)으로 인해 1.5 ATP(일반적으로는 2.5 ATP)를 순생산한다. | |
| 피루브산의 산화적 탈카복실화 | 2 NADH | 5 | 산화적 인산화 |
| TCA 회로 | 2 | 기질 수준 인산화 | |
| 6 NADH | 15 | 산화적 인산화 | |
| 2 FADH2 | 3 | 산화적 인산화 | |
| 총 생성량 | 30 또는 32 ATP | 포도당이 이산화탄소로 완전 산화되는 과정, 모든 환원된 조효소의 산화 | |
세포 호흡에서 이론적으로는 포도당 1 분자당 38 ATP를 생성할 수 있지만, 실제로는 피루브산(해당 과정에서 생성됨), 인산과 ADP(ATP 합성의 기질)를 미토콘드리아 기질로 이동시키는 데 드는 비용과 같은 손실 때문에 일반적으로 이론치만큼 ATP를 생성하지 못 한다. 이들은 모두 H+(양성자)의 전기화학적 기울기에 의해 저장된 에너지를 이용하는 운반체를 사용하여 능동수송된다.
- 피루브산은 Km이 낮은 특이적인 운반체에 의해 미토콘드리아 기질로 운반되며, 피루브산 탈수소 효소 복합체의 기질로 사용된다.
- 인산 운반체는 인산(H2PO4−, Pi)과 OH−의 역수송을 매개하거나, 미토콘드리아 내막을 가로질러 H+(양성자)와 인산의 동반 수송을 매개한다. 인산을 미토콘드리아로 운반시키는 추진력은 양성자 구동력이다.
- ADP/ATP 트랜스로케이스(아데닌 뉴클레오타이드 트랜스로케이스라고도 함)는 미토콘드리아 내막을 가로질러 ADP와 ATP를 교환하는 역수송체이다. 교환시키는 힘은 ADP(−3)보다 더 음전하를 가진 ATP(−4)에 기인하며, 따라서 H+(양성자)의 전기화학적 기울기의 일부 전기적인 요인들을 상쇄한다.
H+(양성자)의 전기화학적 기울기를 이용한 이러한 운반 과정의 결과는 1ATP를 만들기 위해 3 H+ 이상이 필요하다는 것이다. 분명히 이것은 전체 과정의 이론적인 효율성을 감소시키고, 가능한 최대값은 28 ~ 30 ATP에 더 가깝다.[2] 실제로 미토콘드리아 내막을 통해 H+(양성자)가 약간 새어나가기 때문에 효율성은 더 낮을 수 있다.[5] 다른 요인들도 미토콘드리아에서 양성자를 누출시킬 수 있기 때문에 H+(양성자)의 농도 기울기를 상쇄할 수 있다. 단백질인 터모제닌은 일부 세포 유형에서 발현되며, 양성자를 운반할 수 있는 통로이다. 터모제닌이 미토콘드리아 내막에서 활성화하면 전자전달계와 ATP 합성 사이의, 짝지어져 있는 연결을 풀리게 한다. 이때 H+(양성자)의 농도 기울기에 의해 형성된 위치 에너지는 ATP를 만드는 데 사용되지 않고, 열 에너지를 발생시킨다. 터모제닌은 신생아와 동면하는 포유동물의 갈색 지방에서 열 생성에 특히 중요하다.
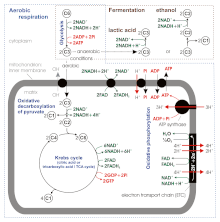
일부 새로운 출처에 따르면 산소 호흡에서 포도당 1 분자당 ATP의 생성량은 36 ~ 38 ATP가 아니라 약 30 ~ 32 ATP인데,[6] 그 이유는 다음과 같다. (교육 과정이 바뀜)
- 1 분자의 NADH의 산화에 의해 약 3 ATP가 아니라 약 2.5 ATP가, 1 분자의 FADH2 산화에 의해 약 2 ATP가 아니라 약 1.5 ATP가 생성되는 것으로 나타났다. 기질 수준 인산화와는 달리, 산화적 인산화의 화학 양론은 계산하기가 어렵다.
- ATP 생성 효소는 3 H+당 1 ATP를 생성한다. 그러나 ADP/ATP 트랜스로케이스와 인산 운반체에 의해 매개되는 세포질의 ADP, Pi와 미토콘드리아 기질의 ATP 사이의 교환(OH−와 역수송 또는 H+와 동반 수송)은 교환 과정 동안 막전위의 변화의 결과로 1 ATP당 1H+를 소비한다. 따라서 ATP 합성의 순비율은 4H+당 1 ATP를 생성한다.
- 미토콘드리아 내막에 있는 전자전달계의 양성자 펌프는 미토콘드리아 기질에서 막 사이 공간으로 1 NADH당 10 H+(복합체 I이 4 H+, 복합체 III가 4 H+, 복합체 IV가 2 H+를 능동 수송함)을 능동수송하며, 1 FADH2당 6 H+(복합체 III가 4 H+, 복합체 IV가 2 H+를 능동수송함)을 능동수송한다.
- 따라서 최종적인 ATP 생성량은 다음과 같다.
- 1 NADH+H+ : 10 H+ : 10/4 ATP = 1 NADH+H+ : 2.5 ATP
- 1 FADH2 : 6 H+ : 6/4 ATP = 1 FADH2 : 1.5 ATP
- 세포질에서 일어나는 해당 과정을 통해 생성된 NADH는 산화적 인산화를 통해 다음과 같이 ATP를 생성한다.
- FADH2와 마찬가지로 세포질의 NADH로부터 수소 원자(2 H++2e−)가 미토콘드리아 내막에 위치한 글리세롤 3-인산 왕복 통로에 의해 미토콘드리아의 FAD로 전달되는 경우에 1 NADH는 1.5 ATP를 생성한다.
- 세포질의 NADH로부터 수소 원자가 말산-아스파르트산 왕복 통로에 의해 미토콘드리아의 NAD+로 전달되는 경우에는 1 NADH는 2.5 ATP를 생성한다.
따라서 포도당 1 분자당 생성할 수 있는 ATP의 양은 다음과 같다.
- 기질 수준 인산화: 해당 과정에서 2 ATP + 시트르산 회로에서 2 ATP (GTP)
- 산화적 인산화
- 해당 과정에서 2 NADH : 2 × 1.5 ATP = 3 ATP(글리세롤 3-인산 왕복 통로를 사용할 경우) 또는 2 × 2.5 ATP = 5 ATP(말산-아스파르트산 왕복 통로를 사용할 경우)
- 피루브산의 산화적 탈카복실화에서 2 NADH : 2 × 2.5 ATP = 5 ATP
- 시트르산 회로에서 6 NADH : 6 × 2.5 ATP = 15 ATP
- 시트르산 회로에서 2 FADH2 : 2 × 1.5 ATP = 3 ATP
따라서 포도당 1 분자당 생성할 수 있는 ATP의 양은 2 + 2 + 3(또는 5) + 5 + 15 + 3 = 30(또는 32) ATP이다.
이러한 수치는 새로운 구조적인 세부 정보를 사용할 수 있게 되면 추가적인 조정을 필요로 할 수 있다. ATP 생성 효소에 대한 3 H+당 1 ATP의 값은 ATP 생성 효소가 9 H+를 이동시키고, 1 회전당 3 ATP를 생성한다고 본 것이다. H+(양성자)의 수는 Fo c-고리의 c 소단위체의 수에 따라 다르며, 현재 효모에서는 10 H+,[7] 척추동물에서는 8 H+이라고 알려져 있다.[8] 운반 과정에서 소모되는 1 H+를 포함하면 ATP의 합성을 위해 효모에서는 1 H+ + 10 H+ / 3 = 4.33 H+, 척추동물에서는 1 H+ + 8 H+ / 3 = 3.67 H+가 필요하다는 것을 의미한다. 이는 인간의 미토콘드리아에서 1 NADH를 산화시켜 얻은 10 H+가 2.72 ATP(2.5 ATP가 아닌), 1 FADH2를 산화시켜 얻은 6 H+가 1.64 ATP (1.5 ATP가 아닌)를 생성한다는 것을 의미한다. 이는 최근 보고서에서 설명된 오차 범위 내의 실험 결과와 일치한다.[9]
알코올 발효나 젖산 발효에서 총 ATP 생성량은 해당 과정에서 생성되는 2 ATP에 지나지 않는다. 왜냐하면 피루브산은 미토콘드리아로 운반되지 않아서 이산화탄소(CO2)로 완전 산화되지 않으며 세포질에서 에탄올 또는 젖산으로 환원되기 때문이다.[6]
무산소 호흡
[편집]무산소 호흡은 산소를 사용하지 않는 호흡 방식을 통칭한다. 또한 발효는 해당 과정을 사용하고, 산소를 사용하는 시트르산 회로와 산화적 인산화 과정을 거치지 않기 때문에 발효도 무산소 호흡으로 분류한다.
세포 호흡은 생물학적 연료를 무기전자수용체(예: 산소 등)가 있는 상태에서 산화시켜 다량의 에너지를 생산하고, ATP의 대량 생산을 추진하는 과정이다. 산소(산소 호흡)와 피루브산 유도체들(발효)이 최종 전자수용체가 아닌 무산소 호흡은 일부 미생물에 의해 사용된다. 오히려 황산염 또는 질산염과 같은 무기 수용체가 사용된다. 이러한 생명체는 보통 수중 동굴이나 해저의 열수 분출공 근처와 같은 이례적인 장소에서 발견된다.
발효
[편집]산소가 없으면, 피루브산은 세포 호흡에 의해 대사되지 않고, 세포질에서 발효 과정을 거친다. 이때 피루브산은 미토콘드리아로 운반되지 않고, 세포질에 남아서 세포에서 제거될 수 있는 분해 산물로 변환된다. 이것은 전자 운반체를 산화시켜서 다시 해당 과정을 수행할 수 있도록 하고, 과량의 피루브산을 제거할 목적으로 사용된다. 발효는 NADH를 NAD+로 산화시켜서 해당 과정에서 NAD+를 재사용할 수 있도록 한다. 산소가 없으면, 발효는 세포질에서 NADH가 축적되는 것을 막고, 해당 과정에서 NAD+를 제공한다. 발효의 분해 산물은 생명체에 따라 다르다. 골격근에서 분해 산물은 젖산이다. 이러한 종류의 발효를 젖산 발효라고 한다. 격렬한 운동 과정에서 에너지 요구량이 에너지 공급량을 초과하면 전자전달계는 NADH에 결합한 전자를 모두 처리할 수 없다. 혐기적인 해당 과정에서 수소 쌍이 피루브산과 결합하여 젖산을 형성하면 NAD+가 재생된다. 젖산은 젖산 탈수소 효소에 의해 촉매되는 가역 반응에서 생성된다. 젖산은 또한 간에서 글리코젠 합성의 간접적인 전구 물질로 사용될 수 있다. 회복 과정에서 산소를 다시 이용할 수 있게 되면 근육 세포에 축적된 젖산은 혈액을 통해 간으로 운반된 후 피루브산으로 전환되어 산소 호흡에 이용되거나 포도당으로 전환된다. 효모에서 분해 산물은 에탄올과 이산화탄소이다. 이러한 종류의 발효를 알코올 발효 또는 에탄올 발효라고 한다. 알코올 발효에서 생성된 ATP는 산소를 필요로 하지 않는 해당 과정의 기질 수준 인산화에 의해 만들어진다.
발효는 산소 호흡에 비해 포도당으로부터 ATP를 생성하는 것이 효율적이지 못 하다. 포도당 1 분자당 산소 호흡에 의해서는 명목상 38 ATP가 생성되지만, 발효 과정에서는 단지 2 ATP만 생성된다. 이것은 발효에 의해 생성된 분해 산물이 산화 과정을 통해 방출할 수 있는 화학 에너지를 여전히 포함하고 있기 때문이다. 예를 들어, 에탄올은 휘발유처럼 내연 기관에서 연소될 수 있다. 그러나, 해당 과정에서 생성되는 ATP는 보다 빠르게 만들어진다. 원핵생물이 호기성 환경에서 혐기성 환경으로 옮겨질 때 빠른 성장을 계속 유지하려면, 해당 과정의 비율을 증가시켜야 한다. 다세포 생물의 경우, 짧은 격렬한 활동 동안 근육 세포는 ATP 생성 속도가 느린 산소 호흡으로부터 ATP 생산을 보충하기 위해 발효를 사용한다.
같이 보기
[편집]각주
[편집]- ↑ Bailey, Regina. “Cellular Respiration”. 2012년 5월 5일에 원본 문서에서 보존된 문서.
- ↑ 가 나 다 Rich, P. R. (2003). “The molecular machinery of Keilin's respiratory chain”. 《Biochemical Society Transactions》 31 (Pt 6): 1095–1105. doi:10.1042/BST0311095. PMID 14641005.
- ↑ Reece1 Urry2 Cain3 Wasserman4 Minorsky5 Jackson6, Jane1 Lisa2 Michael3 Steven4 Peter5 Robert6 (2010). 《Campbell Biology Ninth Edition》. Pearson Education, Inc. 168쪽.
- ↑ 가 나 “Cellular Respiration” (PDF). 2017년 5월 10일에 원본 문서 (PDF)에서 보존된 문서.
- ↑ Porter, R.; Brand, M. (1995년 9월 1일). “Mitochondrial proton conductance and H+/O ratio are independent of electron transport rate in isolated hepatocytes”. 《The Biochemical Journal》 (Free full text) 310 (Pt 2): 379–382. doi:10.1042/bj3100379. ISSN 0264-6021. PMC 1135905. PMID 7654171.
- ↑ 가 나 다 Stryer, Lubert (1995). 《Biochemistry》 four판. New York – Basingstoke: W. H. Freeman and Company. ISBN 978-0716720096.
- ↑ Stock D, Leslie AG, Walker JE (1999). “Molecular architecture of the rotary motor in ATP synthase”. 《Science》 286: 1700–5. PMID 10576729.
- ↑ Watt, I.N., Montgomery, M.G., Runswick, M.J., Leslie, A.G.W., Walker, J.E. (2010). “Bioenergetic Cost of Making an Adenosine Triphosphate Molecule in Animal Mitochondria”. 《Proc.Natl.Acad.Sci.USA》 107: 16823. PMID 20847295.
- ↑ P.Hinkle (2005). “P/O ratios of mitochondrial oxidative phosphorylation”. 《Biochimica et Biophysica Acta》 1706: 1 – 11. PMID 15620362.
