염증
염증(炎症, 영어: inflammation) 또는 염(炎)은 유해한 자극에 대한 생체반응 중 하나로 면역세포, 혈관, 염증 매개체들이 관여하는 보호반응이다. 염증의 목적은 세포의 손상을 초기 단계에서 억제하고, 상처부분의 파괴된 조직 및 괴사된 세포를 제거하며, 동시에 조직을 재생하는 것이다. 염증 반응을 일으키는 물질로는 병원체, 손상된 세포, 자극물질, 위험신호 등이 있다.[2] 염증 자체는 질병이 아니며, 오히려 생명체에 필요한 방어 체계에 해당한다.[3]
염증은 선천 면역에 의해 매개되는 비특이적 반응으로, 병원체에 의해 일어나는 경우 병원체의 종류나 이전 감염(infection) 여부에 관계없이 일어난다.[4][5] 선천 면역 뿐만 아니라 일부 국소적 적응면역 역시 염증에 관여한다.[6] 염증은 감염을 치유하거나 조직의 재생을 증진시키는 보호 기능을 가지지만, 동시에 염증의 결과로 조직의 손상이나 질병이 일어날 수 있다.[7][8] 프롤로테라피 등과 같이 의도적으로 염증 반응을 유도하여 조직의 재생을 꾀하는 방법도 있다.[9]
진단학에서 염증의 임상적 징후로 꼽는 것은 발적, 열감, 붓기, 통증, 기능저하의 다섯 가지이다.[10] 염증 반응이 전혀 일어나지 못하거나 지나치게 약한 경우 세포 및 조직의 손상을 가져올 수 있으며, 생명에 영향을 줄 수 있다.[11] 반대로 지나친 염증은 패혈증, DIC 등을 일으킬 수 있다. 만성염증 역시 동맥경화, 퇴행성 관절염, 치주염 등 다양한 질병의 위험인자로 작용한다. 염증과 감염은 흔히 혼동되지만 서로 다른데, 감염이 미생물의 개체 내 침입과 이로 인한 반응을 일컫는 반면, 염증은 그 원인에 상관없이 선천 면역에 의해 매개되는 비특이적 반응 전체를 지칭한다.[12] 일부 기생충이 면역조절을 통하여 염증 반응을 피해가는 경우처럼 미생물의 침입이 염증을 일으키지 않는 경우도 있으며,[13] 허혈 등의 저산소상태나 자가면역질환 등의 과민반응, 물리적인 손상 등은 감염 없이도 염증을 일으킨다.[14][15][16] 이러한 현상은 위험 이론을 통해 설명할 수 있다.[17]
인간 뿐만 아니라 다양한 동물에서 염증 반응이 일어나며, 이들 중 일부는 인간과 유사한 기전을 가져 임상시험에 사용되기도 한다.[18][19] 일반적으로 척추동물과 무척추동물, 식물은 서로 다른 형태의 면역 체계를 가지고 있고, 특히 무척추동물과 식물에게는 적응성 면역이 존재하지 않는다.[20][21] 무척추동물의 염증반응은 인간 및 대부분의 척추동물과 다른 기전을 가지며 참여하는 세포도 다르다.[22] 무척추동물은 대부분 단순한 혈관계를 가지고 있어 척추동물처럼 혈관이 관여하는 염증반응이 일어날 수 없고, 이 때문에 염증 대신 '손상반응' 또는 '복구반응'이라는 용어가 적합하다고 제안되었다.[23] 식물의 경우, 활성산소와 Ca2+, 살리실산, RNA 등의 작용에 의해 선천 면역이 이루어지기 때문에 염증반응이 일어나지 않는다.[24][25]
증상[편집]
염증으로 인한 질병의 경우 그 질병의 발생 부위와 진행양상 등에 따라 다른 증상이 나타나게 된다.
급성 염증의 경우 다음의 특징적인 5가지 국소 증상이 알려져 있다.[10] 영미권의 경우 이 다섯 가지 증상을 축약하여 "PRISH"라고 일컫는다.[26]
로마의 출판 편집자 켈수스는 1세기에 출판한 《의학에 대하여》(De Medicina)에서 기능 저하를 제외한 나머지 증상들(통증, 발적, 부종, 열감)을 염증의 4요소라 칭한 바 있다.[27] 후대의 갈레노스,[28] 시든햄,[29] 피르호[27] 등이 염증 발생 후 기능 저하에 대한 언급을 하였다.
국소 증상은 염증 부위의 혈관이 이완되고, 모세혈관들의 투과성이 증가하며, 혈류가 증가하는 과정에서 생기게 된다.[30] 발적과 열감은 혈액의 흐름이 염증 부위 쪽으로 증가되기 때문에 생기며, 혈관 투과성이 증가하여 조직에 체액이 축적되고 부종이 생긴다. 신경 말단을 자극하는 히스타민과 브래디키닌이 방출되어 고통을 느끼게 된다. 이러한 복합적인 요인이 모여 염증 부위의 기능 상실을 일으킬 수 있다.[31] 염증이 발생한 부위에 따라 다양한 기능 상실이 나타날 수 있다. 예를 들어 감기의 경우 냄새를 맡지 못하고, 급성 요로 감염의 경우 소변이 참기 어렵거나, 배뇨 통증, 잔뇨감 등이 있을 수 있다.
급성 염증이 조직에 국한되지 않고 광범위하게 일어나는 경우 전신 증상이 생긴다.[1] 대표적인 증상으로 피곤함, 열, 근육통, 기분 저하 및 우울감 등이 있다.[32][33] 패혈증이나 사이토카인 폭풍과 같이 염증의 정도가 심한 경우 고열, 심박수와 호흡수 증가, 의식 저하와 함께 혈류 장애로 인해 소변이 나오지 않는 등의 증상이 발생할 수 있다.[34]
만성 염증의 경우 다양한 증상을 보이며, 증상이 없는 경우도 있다.[35] 특히 다른 질병과 구별하기 힘든 비특이적인 증상(피곤함, 열, 복통, 흉통 등)을 가지고, 급성 염증에 비해 상대적으로 경미한 증상을 보인다.[36]
분류[편집]
염증의 종류를 분류하는 대표적인 기준에는 염증의 지속 기간, 염증의 원인, 염증이 생긴 부위, 병리학적 양상 등이 있다.[37] 염증의 원인은 크게 물리적 요인, 화학적 요인, 생물학적 요인, 심리적 요인 등이 있으며, 생물학적 요인은 감염 또는 비감염으로 나눌 수 있다.[3][37] 또한 염증은 국소적인 염증과 전신의 염증으로 나눌 수 있다.[38] 병리학적 양상에 따라 염증을 분류할 수 있으며, 대표적으로 장액성, 섬유소성, 화농성 염증 등을 꼽을 수 있다.[39]
많은 경우 염증은 급성과 만성으로 구분된다.[40][41] 조금 더 세분화해서 나누자면 급성, 아급성, 만성의 단계로 나눌 수 있다. 시간적으로 급성 염증은 수 분에서 수 일, 아급성은 수 주(보통 2주에서 6주 사이의 염증), 만성은 수 개월에서 수 년에 걸친 반응을 의미한다.[40][42][43] 급성염증은 유해한 자극원에 의해 초기에 일어나는 반응을 말한다. 염증매개물질의 분비와 함께 혈관투과성이 증가하고 백혈구와 혈장 단백질의 이동이 증가된다.[44] 이와 반대로 만성염증은 반응이 일어난 장소에서 염증 세포(예를 들어, 단핵세포)가 점진적으로 영향을 주게 되며, 염증 조직에서 부분적인 회복과 재손상이 지속적으로 일어난다는 특징을 갖는다.[45] 만성염증은 때때로 조직 손상에 이어서 일어나는 회복 반응 없이 장기간 지속되기 때문에 영구적인 손상을 일으킬 수 있다.[46]
급성염증과 만성염증의 비교[편집]

| 종류 및 원인 | 급성염증 | 만성염증 |
|---|---|---|
| 발병 | 즉시 | 천천히 |
| 기간 | 며칠 | 몇 개월 또는 1년 이상 |
| 원인 물질 | 미생물, 손상된 조직 | 지속적인 급성 염증 (원인: 분해·제거되지 않는 미생물, 바이러스 감염, 이물질 또는 지속적인 자가면역반응) |
| 관련된 세포 | 호중구(염증반응의 주 세포, 초기 반응 수행)[48] 호염구(히스타민 분비, 알레르기)[49] 호산구(기생충에 대한 방어, 알레르기) 단핵세포(단핵구, 대식세포) |
단핵세포(단핵구, 대식세포, 림프구, 형질세포) 섬유아세포 |
| 염증매개물질 | 혈관활성아민(혈관작용아민) 아이코사노이드 전염증성 사이토카인(IL-1β, IL-8, TNF-α, IL-6, IL-12 등)[50] |
체액성 면역 유도 사이토카인(IL-3, IL-4, IL-5, IL-7, IL-9, IL-10, IL-13, IL-14 등)[51] 세포성 면역 유도 사이토카인(IL-2, IL-12, IL-15, IFN-γ 등)[51] 생장인자 활성산소종 가수분해효소 |
| 결과 | 증상 완화 농양 형성 염증의 만성화 |
조직손상 섬유화 괴사 |


생리작용[편집]
급성 염증반응의 경우 혈관 및 혈장 단백질, 사이토카인 등의 변화가 일어난 후, 면역세포들의 작용이 일어난다. 염증에 관여하는 화학물질들에는 대표적으로 히스타민과 프로스타글란딘, 키닌류가 있다. 히스타민은 혈관작용아민(혈관활성아민) 종류로 분류할 수 있으며,[52] 손상된 부위에 혈액과 림프액이 더 많이 오도록 작용한다. 키닌류는 근육의 수축을 완화하여 모세혈관을 확장시켜 혈액 운반을 원활하게 하고 통증이 느껴지도록 한다. 대표적으로 브라디키닌이 있다. 백혈구가 세포내로 유입되면 프로스타글란딘이 합성되어 통증과 발열을 일으킨다.
급성 염증의 과정[편집]

급성 염증반응은 흔히 조직의 손상에 대한 1차 방어 작용으로 여겨진다.[5] 급성 염증반응이 일어나려면 일정한 자극원이 필요하다. 대부분의 염증전달물질은 조직에서 빠르게 분해되기 때문에, 자극원이 없어지면 급성 염증반응은 멈추게 된다.[53]
급성 염증의 진행은 주로 대식세포, 수지상 세포, 조직구, 쿠퍼세포, 비만세포 등의 면역세포가 먼저 자극을 인식하면, 면역 시스템이 활성화되고, 대기하던 면역세포가 반응을 일으키게 된다. 자극을 인식하는 세포들은 표면에 병원체연관분자유형(PAMPs), 손상연관분자유형(DAMPs)를 감지하는 수용체를 가지고 있다. PAMPs는 숙주에서 유래한 물질과는 명확히 구분되는 병원체(주로 미생물) 유래 물질이며, DAMPs는 숙주의 세포손상으로 인해 생성된 물질이다. 염증의 원인(감염, 물리적·화학적 손상 등)이 생기면 수용체를 가진 면역세포들(대식세포, 수지상 세포, 단핵구, 호중구, 상피세포 등[54])이 PAMPs, DAMPs 분자를 인식하고, NF-κB 등의 전사인자를 통한 신호전달경로가 시작되며 활성화된다.[55] 그 결과 TNF-α, IL-6, IL-1, IL-8 등의 전염증성 사이토카인이 분비되고, 염증 증상을 유발하는 염증전달물질들이 분비된다.[56] 혈관의 확장과 혈류의 증가는 열과 발적으로 이어진다. 투과성이 증가된 혈관을 통해 혈장단백질과 혈장이 조직으로 들어가 부종을 일으킨다. 브래디키닌과 같은 염증매개물질들은 감각신경을 자극하여 고통에 더욱 민감하게 만든다.[57] 통증이나 부종 등으로 인한 조직의 기능상실이 일어날 수 있다. 염증매개물질에 의해 호중구, 대식세포와 같은 염증세포들이 조직으로 유출된다. 호중구가 손상된 조직의 세포들에게서 생성되는 물질에 이끌려 이동하는 과정을 화학주성이라고 한다.[53]
세포 유래 염증전달물질 이외에 세포가 관여하지 않는 생화학적 경로가 염증반응에 기여한다. 몇몇 혈장단백질은 염증을 일으키는 역할을 하고 이를 전파하기도 한다. 미생물에 의해 작동한 보체계, 세포의 괴사로 시작된 혈액응고반응과 섬유소용해계의 활성화가 그 대표적인 예시이다.[53]
전신의 염증반응[편집]
국소적인 염증반응이 전신성 염증으로 진행될 수 있다. 이 과정은 국소 조직에 갇혀있던 염증반응의 산물들과 염증매개물질이 전신으로 퍼지고, 호르몬과 혈관이 관여하면서 일어날 수 있다.[58][59] 예를 들어 알라민과 같은 염증유발물질이 순환계로 스필오버되는 경우 국소염증반응이 전신염증반응으로 진행된다.[60] 혈관을 통해 전신을 순환하는 사이토카인들이 염증의 전파에 영향을 줄 수 있다.[61] 반면 항염증 사이토카인, 예를 들어 TNF 수용체, IL-1RA, IL-10 등의 항염증매개물질은 전신 염증을 미리 차단할 수 있다.[62]
순환계나 림프계를 통하여 감염원(병원체 등)이 국소 조직에서 전신으로 퍼질 수 있다. 감염원이 급성염증의 작용에 의해 적절히 통제되지 못하면 림프관을 통해 빠져나가 림프계로 들어갈 수 있다. 림프절과 림프관이 감염되면 각각 임파선염과 림프관염이 발생한다. 림프절의 면역세포들이 병원체를 제거하는데 실패한 경우 감염원은 전신으로 퍼져나갈 수 있다. 이 경우 병원체는 림프액 이동 경로를 따라 순환계로 흘러가게 된다.
전신에서 염증반응이 연속적으로 진행되어 과도한 상태가 될 경우 전신성염증반응증후군이 나타난다. 전신성염증반응증후군의 대표적 원인에는 감염, 화상, 출혈, 비감염성 염증 등이 있다.[63] 감염이 원인인 전신성염증반응증후군을 패혈증으로 진단할 수 있다[64][65](정확한 패혈증의 정의는 qSOFA 점수체계로 평가되어 결정된다[66]). 박테리아가 원인인 경우 균혈증, 바이러스 감염이 원인일 경우 바이러스혈증 등으로 원인을 구분한다. 패혈증의 진행과 함께 전신의 혈관확장으로 인한 저혈압, 장기 기능의 부전 등을 나타내는 패혈성 쇼크가 발생할 수 있고, 사망에 이를 수 있다.
혈관의 변화[편집]
염증반응이 일어나는 동안 혈관이 조절되면서 혈류와 투과성이 변한다. 혈관의 확장은 세동맥에서 처음 발생한 후 모세혈관에서 뒤따라 일어난다. 염증 초기에 혈관이 잠깐 수축한 후, 이완된 상태가 지속된다.[67] 이는 혈류를 증가시키고, 혈액량이 늘어나 발적과 열감이 유발된다. 세정맥에서 내피세포 사이에 틈이 생기게 되는데, 이는 혈관 내피세포들의 구조적인 수축 때문이다. 일부 혈관 내피세포들은 직접적인 손상이나 세포외배출, 백혈구 이동에 따른 손상을 받기도 하며, 이러한 기전들을 통하여 혈관 투과성이 증가하게 된다.[68][69] 다양한 염증매개물질이 이 과정에 관여한다.
병원체연관분자유형을 감지한 조직의 대식세포와 비만세포는 염증과 관련된 물질들을 분비한다. 히스타민, 세로토닌과 같은 혈관작용아민들, 프로스타글란딘 E2, 류코트리엔 B4와 같은 아라키돈산 대사물질, 일산화질소 등이 대표적이다. 이러한 물질들은 염증 부위의 혈관에 영향을 미쳐 혈관의 투과성과 굵기를 조절한다. 히스타민은 혈관(세동맥)의 확장과 모세혈관의 투과성 증가 등의 작용을 한다.[70][71] 세로토닌은 다양한 면역세포에 영향을 미치며 면역조절기능을 가지지만, 혈관을 수축 또는 이완시킬 수 있다.[72][73] 혈관마다 분포하는 세로토닌 수용체의 차이로 서로 다른 작용이 일어날 수 있으며, 세로토닌은 모세혈관에서 혈관 이완과 투과성 증가를 일으킨다.[71][74]

혈장 성분의 역할[편집]
혈관의 투과성이 증가하면 조직으로 혈장이 누출되고, 혈액의 혈구 농도가 진해지면서 혈류 정체가 일어난다. 혈관 투과성의 변화로 세포액이 조직으로 이동하면서 부종이 형성된다. 혈장에서 유래한 조직액에 포함된 보체, 라이소자임, 항체 등의 항균물질들은 미생물에 의한 공격에 직접 대응하는데 쓰이거나, 외부 병원체를 옵소닌화시켜서 면역세포의 인식작용을 돕는다. 예를 들어 열상(찢어진 상처)의 경우, 혈장에서 유래한 혈소판, 응고인자, 플라스민, 키닌류들이 상처 부위에 혈전을 형성하고 응고반응을 일으킨다. 응고 매개물질들은 염증 부위에서 피브린을 응집시켜 그물 형태로 만들고, 식작용을 통한 염증 원인 및 조직세포의 제거와 상처의 재생을 유도한다. 조직액의 일부는 림프계로 흘러들어가 림프절에서 미생물의 침입을 알리고, 적응 면역 시스템을 작동시킨다.
혈장의 연쇄반응과 염증[편집]
- 혈액의 응고반응은 상처 부위의 보호를 위해 단백질 그물을 형성하며, 이는 흔히 딱지라고 불린다.
- 섬유소 용해반응은 응고반응과 반대로 작용하여 균형을 맞추며, 염증매개물질을 생성한다. 특히 PAI-1, uPA 등의 몇몇 물질은 염증반응에 관여한다.[75]
- 키닌계 및 칼리크레인-키닌 체계는 혈관 확장 상태의 유지와 염증 효과를 일으키는 단백질들의 생성에 관여한다.
- 보체계는 막공격복합체를 형성하며, 옵소닌작용, 응집반응, 주화성을 일으키는 연쇄반응에 관여한다.
혈장 유래 염증매개물질[편집]
아래는 염증매개물질 및 사이토카인 중 혈장에서 유래한 물질들의 예시이다.[47][76]
| 이름 | 분류 | 역할 |
|---|---|---|
| 브라디키닌 | 키닌계 | 혈관에 작용하여 혈관의 이완, 투과성 증가, 평활근 수축을 유도하며, 고통을 유발한다. |
| C3 | 보체계 | C3은 C3 전환효소의 도움을 받거나 스스로 분해되어 C3a 와 C3b로 나뉜다. C3a는 비만세포에서 히스타민 분비를 유도하여 혈관 확장을 일으킨다. C3b는 세포 혹은 병원체의 표면에 결합한다. 박테리아의 세포벽에 부착된 C3b는 옵소닌 작용을 하여 식작용을 도와주고, 바이러스의 경우 중화한다.[77] 또한 다른 보체 단백질과 결합해 C3 전환효소, C5 전환효소로 작용한다. |
| C5a | 보체계 | C3a와 함께 비만세포의 탈과립을 유도하여 히스타민을 분비하도록 자극하고, 최종적으로 혈관 확장을 일으킨다.[78] 또한 주화인자로 작용하여 염증부위에서 주화성을 일으킨다. |
| XII 응고인자 | 혈액응고계 | 평상시에는 비활성형으로 혈액에 존재하며, 콜라겐, 혈소판에 의해 활성화된다. XII 인자는 다양한 물질(음전하를 띈 특정 물질, 일부 단백질, 콜라겐, 핵산 등)이나 기저막 등에 노출될 경우 접촉경로를 통하여 활성화된다.[79] 활성화된 XII인자는 키닌계, 섬유소용해계, 혈액응고계를 활성화시켜 염증반응에 기여한다. |
| 막공격복합체(MAC) | 보체계 | 보체계 단백질인 C5b, C6, C7, C8, C9 분자로 구성된다. 이들은 병원체에 결합하여 파괴하는 작용을 한다. 이들이 박테리아의 세포막에 원통형의 구멍을 뚫게 되면 삼투압에 의해 세균이 분해된다. |
| 플라스민 | 섬유소용해계 | 피브린으로 구성된 피떡을 분해할 수 있고, 보체 단백질인 C3을 자르며, XII인자를 활성화 시킨다. |
| 트롬빈 | 혈액응고계 | 혈장에 포함된 피브리노겐을 분해하여 활성상태의 피브린을 형성하는데 도움을 준다. 피브린은 물리적으로 결합하여 겔 상태의 불용성 피떡을 형성한다. 또한 트롬빈은 PAR1 수용체를 통해 세포에 결합하여 일산화질소나 케모카인 형성에 관여한다. |
면역세포계의 역할[편집]
면역체계를 유지하기 위해 다양한 세포들이 각자의 역할을 담당하고 있으며, 염증 반응에도 이러한 면역세포들이 참여하게 된다.[80][81][82]
이들에는 혈액에 존재하는 백혈구들도 포함된다. 혈류의 정체에 따라서 혈관 내의 백혈구가 혈관내피를 따라 이동할 수 있고, 투과성이 증가한 혈관을 빠져나가 조직으로 이동하게 된다. 백혈구 중 일부는 식세포로 기능하여 식작용으로 세균, 바이러스, 세포 찌꺼기 등을 섭식한다. 일부 백혈구는 다양한 효소가 포함된 과립을 분비하여 숙주조직을 정리하거나 외부 항원인 세균 등을 죽인다.[83] 다른 일부는 염증반응을 매개하고 조절하는 염증전달물질을 분비한다.
급성염증의 경우 일반적으로 과립구에 의해 조절된다. 반면, 만성염증의 경우 단핵구, 림프구 등의 단핵세포 참여가 두드러진다. 특히 염증 반응의 초기 단계에서는 항균 작용이 강한 호중구가 주로 반응하며, 이후 반응이 진행하면서 단핵구, 대식세포가 참여하게 된다.[84]
백혈구의 혈관외유출[편집]
다양한 백혈구, 특히 호중구는 염증 반응의 시작과 유지에 있어서 중요한 역할을 한다. 백혈구는 일반적으로 혈액에서 손상이 된 조직으로 이동을 하는 과정을 거친다. 백혈구가 혈관을 빠져나와 혈액에서 손상된 조직으로 이동하는 것을 혈관외유출이라 하며, 이러한 일련의 과정은 몇 가지 단계로 나뉘어 진행된다. 이 과정은 크게 화학쏠림, 구르기 및 부착, 내피세포 통과 이동의 3단계로 구성된다.[85]
- 주화성(chemotaxis): 조직의 대식세포나 혈액의 단핵구, 기타 다른 면역세포들이 조직에 침투한 병원체를 인식하면 다양한 사이토카인들이 분비된다.[56] 화학주성을 일으킬 수 있는 사이토카인들을 케모카인이라고 부른다.[86] IL-1, IL-8, TNF-α, C5a 등은 염증 부위 근처의 혈관내피세포가 셀렉틴 등의 세포부착분자를 발현하도록 한다. 혈관을 타고 순환하던 백혈구는 케모카인의 신호를 받고 손상 또는 감염이 생긴 부위로 동원된다.
- 접착(adhesion): 혈관에서 떠다니던 백혈구가 염증신호를 인식하면 염증 조직으로 빠져나가기 위해 혈관벽의 혈관내피세포에 붙어야 한다. 전통적으로 이 과정은 구름부착, 활성화, 정지부착의 3단계로 구성된다고 생각되었으나,[87] 최근에는 포획, 느린 구르기, 접착 강화, 혈관 내강을 타고 기어가기(crawling) 등의 과정으로 세분화되었다.[85] 혈관 중앙에서 흘러가던 백혈구는 케모카인을 인식한 후 혈관의 벽 방향으로 이동한다.[88] 포획은 혈구누출의 백혈구와 혈관의 내피세포 표면의 접촉을 의미한다.[89] 조직의 염증신호를 인식하여 활성화된 대식세포는 IL-1, TNF-α 등을 분비하고, 이들이 내피세포의 GPCR에 결합한다. 그 결과로 모세혈관 및 모세혈관이후세정맥의 내피세포에서는 셀렉틴이 발현된다. 셀렉틴은 호중구, 호산구, 단핵구, T세포 등의 수용체로 작용할 수 있으며, 내피세포에서는 P-셀렉틴과 E-셀렉틴이 발현되는데 P-셀렉틴은 내피세포의 자극 이후 E-셀렉틴보다 먼저 발현된다.[90] 포획된 백혈구는 PSGL-1과 같은 표면의 당단백질 리간드를 통하여 P-셀렉틴, E-셀렉틴과 결합되었다가 떨어졌다를 반복하면서 혈관 내피의 표면을 따라 구르게 된다. IL-8(CXCL8), SLC(CCL21), ELC(CCL19), SDF-1(CXCL12) 등의 케모카인이 분비되어 인테그린의 구조변화를 일으킨다.[91] LFA1, VLA4와 같은 백혈구 표면의 인테그린은 내피세포의 인테그린 수용체와 더 강한 결합을 형성하여 혈류 흐름으로부터 백혈구를 고정시킨다. 사이토카인들은 내피세포의 ICAM-1 및 VCAM-1과 같은 인테그린 리간드의 발현을 유도하여 접착을 매개하고 백혈구를 더욱 느리게 한다. 이후 내피세포 표면의 백혈구가 혈관벽을 따라 이동(crawling)하다가 적당한 위치에 이르게 되면 내피세포 사이나 내피세포를 건너서 통과해 혈관 속을 빠져나간다.[89]
- 내피세포 통과 이동(transmigration): 혈구누출 과정을 통하여 백혈구가 혈관 밖으로 빠져나가게 된다. 케모카인의 농도차이를 인식한 백혈구는 혈관 벽을 따라 이동하며 인접한 내피세포들의 틈으로 이동한다. 내피세포는 움츠러들면서 백혈구가 기저막을 통과할 수 있게 하고, 백혈구는 ICAM-1과 같은 부착분자를 이용하여 주위 조직으로 이동한다.[88]
면역세포의 식작용[편집]
염증이 일어난 조직에 도착한 백혈구(호중구)들은 병원체와 맞닥뜨리게 된다. 식작용을 할 수 있는 식세포들은 세포 표면에 유형인식수용체(PRR)를 통해 병원체연관분자유형 등의 위험신호를 인식한다.[92] 병원체연관분자유형은 병원체가 지니고 있는 특정한 분자로, 면역숙주에서는 발견되지 않으며, 대표적으로 지질다당류, 펩티도글리칸, 베타글루칸 등이 있다. 유형인식수용체는 식작용을 직접적으로 매개하는 기능(세포내 이입성 PRR)과 함께 옵소닌 작용에 도움을 주고(분비성 PRR) 염증성 신호 전달을 매개할 수 있다(신호전달 PRR).[93][94] 만노스 수용체, CD14, CD36, 덱틴-1(CLEC7A) 등의 세포내 이입성 유형인식수용체가 PAMPs를 인식하여 식작용을 유도한다.[95] 병원체 등의 외래 입자들은 식세포에 의해 인식될 수 있도록 옵소닌화 되는 경우가 많다. IgG 항체와 C3b 보체 등이 옵소닌으로 작용하여 미생물 항원에 결합하여 코팅한다. 백혈구 표면의 Fcγ 수용체와 1형 보체 수용체 등이 옵소닌을 감지할 수 있다.[96]
외부 물질이 수용체에 결합하면 세포막과 액틴 세포골격이 변화하면서 물질을 감싸게 된다.[96] 식작용으로 식세포로 들어온 외부 물질은 식포를 형성한다. 포스파티딜이노시톨 등이 관여하는 복잡한 경로를 통하여 식포의 성숙작용이 일어나고, 성숙된 식포는 리소좀과 결합하여 포식용해소체를 형성한다.[96] 소체 내의 활성산소종, 과산화물 및 염소이온 등은 소체 내의 물질을 분해한다.
세포 유래 염증매개물질[편집]
아래는 염증매개물질 및 사이토카인 중 면역세포에서 유래한 물질들의 예시이다.[47][76]
| 이름 | 분류 | 기원 | 역할 |
|---|---|---|---|
| 과립 | 효소 | 과립구 | 과립구의 과립에는 다양한 기능을 하는 수많은 종류의 효소가 포함되어 있다. 과립은 내용물에 따라서 특이과립과 아주르 친화성 과립으로 나뉠 수 있다. 여러 종류의 물질을 분해할 수 있으며, 이들 중 일부는 혈장유래 단백질효소로서 염증전달물질로 작용한다. |
| 히스타민 | 모노아민 | 비만세포, 호염구 | 과립에 저장되었다가 자극이 오면 히스타민이 분비된다. 소동맥의 확장과 정맥의 투과성을 증가시킨다. 다양한 장기에서 수용체에 따라서 특이적인 효과를 낸다. |
| IFN-γ | 사이토카인 | T세포, NK세포 | 이전에는 대식세포 활성인자로도 불렸다. 만성 염증의 유지에 중요한 역할을 한다. 항바이러스성, 항암성 역할을 하며, 면역조절기능이 있다.[97] 대식세포와 NK세포를 활성화시킬 수 있다. |
| IL-8 | 케모카인 | 주로 대식세포 | 호중구의 화학주성을 유도하는 물질로 작용하고, 식작용을 유도한다. |
| 류코트리엔 B4 | 아이코사노이드 | 백혈구, 암세포 | 백혈구의 부착과 활성과정에 참여하며, 백혈구가 혈관내피세포에 부착하거나 통과하여 이동할 수 있도록 한다. 호중구에 작용하여 화학주성을 일으킨다. 활성산소종 형성과 리소좀에 포함된 효소들의 분비에 관여한다. |
| 일산화질소 | 용해가스 | 대식세포, 내피세포, 일부 뉴런들 | 혈관을 이완시키고, 평활근을 이완시키며, 혈소판의 응집을 감소시킨다. 백혈구의 동원을 유도하고 고농도에서는 직접적으로 항균제로 작용한다. |
| 프로스타글란딘 | 아이코사노이드 | 비만세포 | 지질의 일종으로, 혈관 확장과 발열, 통증을 일으킬 수 있다. |
| TNF-α, IL-1 | 사이토카인 | 주로 대식세포 | 여러 종류의 세포에 염증반응을 유도한다. 열, 사이토카인의 생성, 내피세포의 유전자 조절, 백혈구의 주화성 유도, 백혈구의 부착, 섬유아세포의 활성 등에 관여한다. 염증의 전신적인 영향에도 관여하는데, 식욕감퇴나 심박 수의 증가 등에 영향을 미친다.
TNF-α는 염증에 관여하는 면역세포들을 활성화시키고,[98] 대식세포 활성에 관여하며, 내피세포에 작용하여 혈관신생과 혈관 투과성을 증가시키고, 간세포에 작용하여 CRP의 합성을 늘리며, 활막세포에 작용하여 관절 연골의 파괴를 촉진하고, 조골세포의 분화를 억제한다.[99] IL-1 가계 사이토카인에는 총 11개의 사이토카인이 속해있고, 이들의 수용체는 10가지 종류가 존재한다.[100] IL-1β는 다양한 장기에서 과분비되어 질병의 원인으로 작용할 수 있다.[101] IL-18은 NK세포와 T세포에 작용하여 IFN-γ 합성을 유도하고, 단핵구에 작용하여 GM-CSF, TNF-α, IL-1β 발현을 유도하며, 호중구의 활성화와 사이토카인 분비 과정에 관여한다.[7] |
염증 관해와 만성염증[편집]
염증 관해[편집]

염증반응은 필요한 역할을 다하였을 시 반드시 중단되어야 하며, 그렇지 못하고 계속 진행될 경우 조직에 손상을 줄 수 있다.[53] 염증반응이 적절히 중단되지 못한 경우 만성염증이 진행된다. 만성염증의 과정에서 세포사멸이 일어나 조직의 파괴가 일어날 수 있다.[102][103] 염증의 관해 과정은 조직에 따라 서로 다른 방식으로 진행된다. 다음은 염증반응이 종결되는 일부 메커니즘이다.[53][104]
- 염증매개물질들의 짧은 반감기 (in vivo에서)
- 대식세포에서 TGF-β의 생성과 분비[105][106]
- IL-10의 생성과 분비[107]
- 전염증성물질들의 발현 감소 (예: 류코트리엔 등)
- 항염증성물질들의 발현 증가 (예: TNF 수용체, IL-1RA 등)
- 항염증성 기능을 담당하는 염증해소촉진전달자의 생성 (예: 라이폭신, 레졸빈, 마레신, 프로텍틴 등)[108][109]
- 전염증성 세포들의 세포자살[110]
- 수용체들의 탈감작, 리간드로 인한 활성 감소
- 세포외기질과의 상호작용으로 인한 염증 조직의 세포 생존의 증가[111]
- 금속함유 단백분해효소에 의한 케모카인의 분해 (간접적으로 항염증성물질의 생성 증가를 유도)[112]
- 당질코르티코이드와 같은 호르몬의 분비[113]
염증 해소 과정에서 호중구들의 세포자살과 대식세포의 극성 전환이 중요한 과정을 담당한다.[114] 염증 기간에서 회복 기간으로 넘어가면서 조직의 세포 구성이 달라진다.[115][116] 이러한 과정에서 M2 대식세포, 세포자살한 호중구, 조직의 실질세포가 내뿜는 물질들이 염증 해소와 회복을 시작하는 신호로 작용할 수 있다.[114] 대식세포는 상황에 따라서 지질다당류, IFN-γ에 의해 주로 활성화되는 M1 대식세포와, TGF-β, IL-4, IL-10 IL-13 등에 의해 주로 활성화되는 M2 대식세포로 극화한다.[117][118] 이 두 형태는 서로 가역적으로 왔다갔다 할 수 있으며,[105] 상처 회복기의 조직에는 M2 대식세포가 더 많은 비율을 차지하고 있다.[114]
만성염증[편집]
이전에는 급성염증과 만성염증이 다른 이유로 발생하는 별개의 현상으로 생각되었지만, 최근에는 생명체의 항상성을 유지하기 위한 하나의 과정으로 묶여 이해되고 있다.[119] 이는 염증의 정의가 과거의 고전적 정의에서 "염증성물질의 상승 또는 발견"으로 변화하게 된 것과 관계가 깊다.[120] 수 분~수 일까지 지속되는 급성염증은 체액과 혈장단백질의 삼출로 인한 부종, 호중구로 대표되는 백혈구의 동원을 특징으로 한다. 반면 만성염증은 이보다 긴 기간에 걸쳐서 일어나며 림프구와 대식세포의 관여, 혈관 증식, 조직의 괴사 및 섬유화가 특징이다.[121] 만성염증이 발생하기 전 눈에 띄는 급성염증이 일어날 수도 있지만, 정상적인 자극에 대한 생리학적인 반응의 결과로 DAMPs가 쌓여 만성염증으로 발전할 수 있다.[119][121] 염증 관해가 실패하는 경우 만성염증으로 이어져 조직의 손상과 기능 상실로 이어질 수 있다.[117] 급성염증 상태에서 획득면역의 관여는 만성염증으로의 진행을 유도할 수 있다.[122]
만성염증에 관여하는 인자를 삼출성 요소와 세포성 요소의 2가지로 나눠볼 수 있다.[123] 삼출성 요소들은 혈관 투과성을 조절하여 에 조직의 부종을 유도한다. 혈관내피세포성장인자는 만성염증에서 혈관 투과성을 조절하는 대표적인 물질이다.[124] 단핵구/대식세포, 호중구, 수지상세포, 섬유세포, T세포, 비만세포 등 다양한 면역관련 세포들이 만성염증에 관여한다.[123]
만성염증의 지속상태는 거의 대부분의 장기에서 발생할 수 있으며[3] 매우 다양한 형태의 질병에 직접적으로 관여한다.[46][125][126]
저강도의 만성염증[편집]
저강도의 만성염증은 다양한 질병의 위험인자로 주목받고 있다. 저강도의 만성염증의 정의가 통일되진 않았지만, 흔히 염증의 5대 증상이 없이 염증반응이 지속되는 상태를 의미한다.[127] 저강도의 만성염증은 임상적으로 혈액 속의 hs-CRP 농도로 정의되는 경우가 많다.[128] 이 경우 AHA/CDC의 권고치[129]인 3mg/L를 기준으로 삼아 그보다 상승한 경우를 위험군으로 판단하는 경우가 많다.[128][130][131] 미국인의 약 30%,[131] 한국인의 약 10% 내외[132][133]가 저강도의 만성염증을 가지고 있다.
저강도의 만성염증은 다양한 원인으로 인해 생기며, 생활습관, 사회적 관계 및 식습관과도 밀접하게 연관되어 있다.[128][134][135] 건강하지 못한 식사, 적은 수면, 흡연 및 간접흡연, 신체활동 감소, 악력의 감소, 고지대에 거주, 미혼, 노화, 사회적 고립 등의 사회적 요인이 저강도의 만성염증을 유발할 수 있다.[128] 또한 고혈압 및 전고혈압, 저산소증, 폐쇄성 수면 무호흡, 비만, 허리디스크, 낮은 출생 체중, 다낭성 난소 증후군 등의 의료적 상황이 저강도의 만성염증을 유발할 수 있다.[128]
저강도의 만성염증은 많은 질병의 원인으로 작용하거나, 위험인자로 꼽힌다. 저강도의 만성염증이 지속되면 만성적으로 피로한 상태를 만들게 된다.[136] 저강도의 만성염증은 암, 관절염, 대사증후군, 당뇨병, 심혈관질환, 신경계질환 등의 원인 및 위험인자로 작용할 수 있다.[137][138]
제2형 당뇨병, 죽상경화증, 인슐린 저항성 등이 저강도의 만성염증과 연관되어 있지만, 이러한 경로를 조절하는 항염증제를 통해 질병을 완화하려는 시도는 부분적인 성공만을 거두었다.[139]
원인[편집]
염증은 미생물에 의한 감염, 외상으로 인한 상처, 수술, 화상 및 동상, 전기자극, 화학물질 등 다양한 원인에 의하여 발생한다.
원인은 크게 4가지로 나뉜다.
| 물리적 원인 | 화상, 동상, 외상, 이물질, 이온화 방사선 |
| 생물학적 원인 | 병원체에 의한 감염, 과민증으로 인한 면역반응, 스트레스, 손상된 세포 |
| 화학적 원인 | 화학자극, 독성, 알코올, 당분, 지방, 미세먼지 |
| 심리적 원인 | 쑥스러움, 흥분 |
결과[편집]

염증 반응의 결과는 손상을 입은 조직의 종류와 상태, 염증을 일으킨 원인에 의하여 결정된다. 염증으로 인해서 나타날 수 있는 결과들로 크게 4가지를 꼽을 수 있다.[53]
- 염증의 관해: 손상을 입은 조직이 염증 이전의 상태로 완전하게 재생되는 경우가 있다. 제한적인 염증반응이나 자극이 작고 짧은 기간동안 일어난 반응이 이런 결과를 낼 수 있다. 염증 반응으로 생긴 혈관의 확장, 염증과 관련된 화학물질의 생성, 백혈구의 조직 침투, 손상을 입은 조직의 실질세포 등이 원상태로 회복된다.
- 섬유화: 많은 양의 조직이 손상을 입거나 물리적으로 파괴된 경우, 이전과 같은 세포로 완벽하게 재생될 수 없다. 이러한 손상을 입은 부위는 흉터 조직으로 채워진다. 흉터는 주로 콜라겐으로 이루어져 있으며 기능적으로는 조직의 실질세포가 아니기 때문에 조직의 제 기능을 하지 못한다. 비후성 반흔이나 흉터로 인한 조직의 수축, 켈로이드 등이 형성될 수 있다.[140]
- 농양(종기) 형성: 염증이 다른 곳으로 퍼져나가지 못하게 하는 과정에서 고름이 모여서 화농할 수 있다. 고름에는 박테리아들과 죽은 백혈구, 파괴된 세포들의 잔해가 함유되어 있으며, 흔히 불투명한 색의 액체로 보인다. 농양에는 흔히 격벽이 형성되어 정상 조직이 농양 안의 박테리아로부터 감염되는 것을 막아준다. 농양을 치료하기 위해 항생제 투여와 함께 절개 및 배농 과정을 거쳐 고름을 제거하는 단계가 필요하며, 내시경이나 수술적인 방법이 필요할 수 있다.[141][142]
- 염증의 만성화: 급성 염증의 원인이 지속되는 경우 만성염증으로 발전할 수 있다. 염증의 만성화는 원인물질이 없어지지 않고 계속 남아있을 때 일어난다. 이러한 과정은 염증이 몇 개월 혹은 수 년간 지속되면서 발생하며, 손상된 조직에서 만성창상을 형성한다. 만성창상은 일반적으로 4주 이상 치유되지 않는 상처를 말한다.[143] 만성화된 염증은 조직에서 대식세포가 계속적으로 존재하는 특징을 지닌다. 대식세포는 강력한 면역세포이지만 이들이 내뿜는 세포독성물질들(활성산소 등)은 조직에 지속적으로 손상을 입힐 수 있다. 만성염증은 결과적으로 정상 조직의 파괴를 야기한다.
병리학적 특징[편집]


급성 및 만성 염증에서 특정한 병리학적 패턴이 관찰될 수 있으며, 대표적으로 상피세포에서 염증이 일어났을 때나, 감염에 의해 고름이 형성된 경우를 예로 들 수 있다.[145]
- 육아종성 염증: 병리 소견상 육아종으로 특징지어지며 일부 질병에서 특징적인 소견으로 나타난다. 대표적으로 결핵, 나병, 사르코이드증, 매독 등을 들 수 있다.
- 섬유소성 염증: 혈관 투과성 증가로 인해서 조직의 삼출액 내에 피브린 등의 섬유성 물질이 침착될 수 있다. 암[53]이나 류마티스 열,[146] 폐렴 등에서 같은 경우가 그 예인데, 적절한 전응고촉진 자극원이 존재한다면 섬유소의 유출이 누적된다. 장막 사이의 공간에 이러한 현상이 흔히 일어날 수 있으며, 섬유소를 포함한 삼출물이 흉터를 형성하는 원인이 되어 장막의 정상 기능을 방해할 수 있다. 이러한 삼출물의 축적은 가성막을 형성할 수 있으며 C. difficile 감염으로 인한 거짓막 결장염 등에서 관찰된다.
- 화농성 염증: 많은 양의 호중구, 죽은 세포들과 고농도의 단백질[147]을 함유하고 있는 고름을 만들어내며, 포도상구균과 같은 화농균에 감염되었을 때 특징적으로 나타난다. 고름이 배출되지 못하고 차서 주변 조직에 둘러쌓인 상태가 되면 농양이라 부른다.
- 장액성 염증: 수분이 많고 단백질이 적으며 점성이 적은 장액이 특징적으로 발생하는 염증이다. 이러한 장액은 장막의 중피세포에서 주로 형성되며, 혈장 유래 액체인 경우도 있다. 피부에 생기는 물집이 대표적이다.
- 궤양성 염증: 상피의 근처에서 일어나는 염증은 조직의 괴사에 의하여 아래의 층이 드러나는 경우가 있다. 상피가 손상되어 구멍이 생기는 것을 궤양이라고 한다.
진단적 특징[편집]
염증으로 인한 질환을 발견하기 위하여 임상 증상, 염증조직의 조직검사(병리소견), 혈액검사, 조직액 검사(활막액검사, 흉수검사 등), 내시경 소견, 영상의학 검사 등 다양한 진단적 특징을 종합적으로 고려해야 한다.[148][149]
임상적으로 염증을 발견하기 위해서 다양한 염증 표지자에 대한 검사를 할 수 있다. 혈구, 응고반응 검사, 화학 검사 등의 혈액 검사가 대표적인 예시이다.[150] 세포 표면에서 셀렉틴, 인테그린 등의 발현을 보거나, 염증매개물질과 사이토카인, 케모카인, 보체, 급성기 단백질 등을 분석할 수 있다.[150]
급성기 단백질[편집]
염증 반응의 결과로 급성기 단백질의 발현이 유도된다. 급성기 단백질은 간에서 주로 생성된다.[150] 대표적인 급성기 단백질로는 CRP, 혈청 아밀로이드 A, 혈청 아밀로이드 P, 알파-1 항트립신, D-이합체, 세룰로플라스민, 합토글로빈 등이 있다.[151] 염증 반응이 일어나면 농도가 증가하는 급성기 단백질이 있는 반면, 감소하는 단백질이 있고, 이러한 변화가 정상치를 넘어서는지를 검사하여 염증 여부를 판단할 수 있다.[152] 반면 알부민, AFP, 아포지단백 A1, 아포지단백 A2 등의 혈장 단백질은 감소하게 된다.[153]
급성기 단백질은 체액성 선천면역에 도움을 주고, 응고반응을 유발하며, 조직의 손상을 막고 복구에 도움을 준다.[153] 급성 염증에서는 이러한 단백질이 이롭다고 알려져 있으나, 만성염증에서는 아밀로이드증 발병에 영향을 줄 수 있다.[53] 이들은 열, 피로, 혈압 증가, 식욕 감퇴, 땀의 감소, 졸음 등의 전신 증상을 일으킬 수 있다.[53]
대표적인 급성기 단백질인 CRP의 경우, IL-6 등이 분비되면 간에서 발현 정도가 증가하게 된다. C1q 보체의 활성화를 유도하고 옵소닌화 반응을 촉진한다. 또한 단핵구와 마크로파지의 기능을 조절하고 IL-8 등의 사이토카인 분비를 조절할 수 있다.[154]
혈구[편집]
염증은 경우에 따라 신체 내의 백혈구 수에 영향을 줄 수 있다. 백혈구증가증은 말초혈액의 백혈구 수가 정상 범위에 비하여 증가하는 것으로 정의된다. 흔히 감염에 의해 일어나는 염증에서 미성숙한 백혈구가 혈액에 증가하면서 이러한 소견을 볼 수 있다. 백혈구의 수는 흔히 15,000–20,000개/μL까지 증가하는데, 극도로 증가된 경우에는 100,000개/μL까지 보이는 경우도 있다.[53] 박테리아에 의한 감염은 호중구를 증가시키며, 기생충에 의한 감염이나 천식, 알레르기 비염 등의 질병은 호산구의 증가가 일어난다. 반면 백혈구감소증은 바이러스 감염, 리케차 감염, 원생동물 감염, 결핵 및 암 등과 같은 특정 상황에서 관찰된다.[53]
ESR은 EDTA 튜브에 혈액을 채취한 후 1시간 동안 수직으로 세워 두었을 때 적혈구가 침강된 길이를 뜻하며, 염증 및 감염이 있을 경우 증가할 수 있다.[155]
염증 질환[편집]
비정상적인 염증은 수많은 인간의 질병에 관여하고 있다. 면역계의 이상은 알레르기성 질환과 몇몇 염증성 근병증에 영향을 끼칠 수 있다. 면역계의 이상이 직접적으로 동반되지 않더라도 염증은 암, 죽상경화증, 관상동맥질환의 발병에 기여할 수 있다.[53]
장기별 분류[편집]
- 심장: 관상동맥질환, 협심증, 심근경색, 심장막염, 심근염 등
- 혈관: 죽상경화증, 혈관염, DIC, ITP, TTP, 일부 빈혈 등
- 상기도: 급성 비인두염, 알레르기비염, 부비동염, 인두염, 편도염, 후두염 등
- 하기도 및 폐: 기관지염, 기관지확장증, 천식, COPD, 폐렴, 간질성 폐질환, 결핵 등
- 상부 위장관: 위염, 식도염 등
- 하부 위장관: 소장염, 궤양성 대장염, 크론병, 셀리악병, 게실염, 과민성대장증후군, 맹장염, 치루 등
- 간, 담도 및 췌장: 간염, 지방간, 담관염, 담낭염, 췌장염, 제1형 당뇨병 등
- 신장(상부요로): 신우신염, 사구체신염, 요로감염증 등
- 하부요로: 요로감염증, 요관염, 요도염, 방광염, 전립선염/만성골반통증후군 등
- 갑상선 및 부갑상선: 갑상선염, 부갑상선염 등
- 부신: 부신염 등
- 생식기관: 골반내 염증성 질환, 난소염, 고환염, 부고환염 등
- 뼈 및 관절: 골관절염, 류마티스 관절염, 골수염, 활막염 등
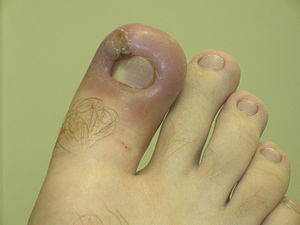
- 피부: 연조직염, 단독, 어루러기/무좀, 여드름 등
- 근육: 근염 등
- 뇌: 뇌염, 주요우울장애 등
- 신경: 눈/귀를 포함한 다양한 부위의 신경염, 복합부위 통증 증후군, 길랑-바레 증후군 등
- 눈: 다래끼, 포도막염, 결막염 등
- 귀: 중이염, 유양돌기염 등
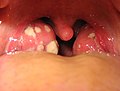
- 구강: 구내염, 치주염, 치은염 등
- 전신 질환: 다양한 자가면역질환, 대사증후군 관련 질환 등
- 다양한 장기에서 발생 가능한 질환: 암 등
- 기타: 복막염, 재관류 손상, 이식거부반응, 과민반응 등
원인에 따른 분류[편집]
비만과 염증 반응[편집]
비만은 전신의 만성염증 상태를 일으킨다.[156][157][158] 인터루킨의 발견과 함께 전신성 염증에 대한 관심이 커지게 되었다. 이러한 염증의 특징은 전체적인 진행 과정이 국소 조직의 염증과 동일하지만, 전신의 다른 장기와 내피에 영향을 미친다는 점이 다르다. 저강도의 만성염증은 TNF-α, IL-6, CRP의 농도가 일반인의 2–3배 증가해 있는 상태가 특징적이다.[159] 이러한 전신염증은 인슐린 저항성과 죽상경화증의 발생에도 연관이 있다.
허리둘레와 전신의 염증반응의 정도가 양의 상관관계를 보였다.[160] 중심성 비만, 특히 내장지방을 이루는 지방세포들은 렙틴, 레지스틴, IL-6, TNF-α와 같은 아디포카인들을 분비하고, 이들이 혈관의 염증과 죽상경화에 많은 역할들을 한다.[161] 비만한 사람은 지방조직이 더 많고, 그 결과 지방세포에서 직접 분비되는 IL-6과 같은 염증관련물질의 농도가 더 높다.[162] 정상 범위를 벗어난 과도한 지방조직은 대식세포의 활성을 증가시켜 IL-6, TNF-α와 같은 염증관련물질의 생산을 늘릴 수 있다.[163][164] 지방 조직, 그 중에서도 특히 백색지방 조직의 감소는 염증 마커의 감소를 일으켰다.[165]
비만인 사람에서 염증 마커가 일반적으로 상승할 수 있으며, IL-6, IL-8, IL-18, TNF-α, CRP, 인슐린, 혈당, 렙틴 등이 대표적이다.[158][166] CRP의 증가는 심혈관계질환의 발생 확률을 높이며, 비만인 사람은 CRP의 농도가 일반인에 비해 높다.[167]
노화와 염증 반응[편집]

노화는 분자, 세포 및 조직 수준에서 축적된 손상이 이들의 기능적인 감소와 오작동으로 연결되는 현상을 의미한다.[168] 나이가 들면서 이러한 노화과정은 자연스럽게 진행되지만, 이 과정에서 일어나는 손상에 염증반응이 중요한 역할을 차지하기 때문에 이를 조절하려는 노력 역시 활발히 진행 중이다.[169] 고전적으로 노화 과정과 염증은 자유라디칼과 활성산소, 산화적 손상을 지지하는 노화가설에 의해 연결되었다.[169][170]
건강한 사람도 정상적인 노화과정을 통해 저강도의 만성염증이 시작될 수 있다.[171] 많은 경우 질병이 없는 건강한 노인들에게서도 다양한 염증성 사이토카인의 농도가 상승해있는 것이 발견되지만,[172] 이를 반박하는 일부 증거도 있다.[173] 대사의 부산물로 생긴 단백질 퇴적물 및 세포 잔해를 제대로 처리하지 못하거나, 세포 자체의 노화, 선천면역의 기능 저하 등이 이러한 현상의 대표적인 원인으로 꼽힌다.[174] 알츠하이머, 파킨슨병 등 노화수반병을 가진 환자들에게서 만성염증은 병태생리에 중요한 기여를 한다.[121]
항염증제를 이용해 노인의 염증반응을 줄일 수 있지만, 위장관이나 심혈관계에 부작용을 일으킬 수 있다.[171] 운동과 칼로리 섭취 제한 등의 생활습관 변화가 면역노화와 염증노화를 방지할 수 있다.[175]
염증질환 각론[편집]
죽상경화증[편집]
죽상경화증은 대표적인 염증질환으로, 이전에는 단순히 혈관벽에 지방이 쌓이는 질병으로 생각되었다. 최근의 연구결과들은 죽상경화증의 모든 단계, 즉 콜레스테롤의 침착과 죽종의 형성, 혈관벽의 손상 및 죽상경화반의 형성, 혈전의 발생까지 모든 단계에 염증이 관여한다는 것을 입증하였다.[176][177] 이러한 새로운 발견은 죽종의 형성에 위험인자로 작용할 수 있는 요소들을 설명할 수 있다. 임상 연구에서 죽상경화증과 염증의 관련성이 환자의 다른 질병 발생 및 예후에 직접적인 영향을 끼칠 수 있음이 증명되었다.[178] CRP로 측정되는 저강도의 만성염증은 죽상경화증으로 인한 다양한 질병, 예를 들어 심혈관질환을 예측하는 주요한 인자로 쓰인다.[179] 관상동맥질환의 위험을 줄이는 치료들은 부가적으로 염증을 줄이는데 기여한다. 스타틴을 사용하여 혈중 지질 농도를 줄이는 경우, LDL의 감소와 관련없이 항염증효과를 얻을 수 있었다.[180] 죽상경화증의 염증에 대한 이러한 새로운 접근법은 세계적으로 점점 중요해지고 있는 이 질병에 대한 우리의 이해를 도울 뿐만 아니라 위험군 선별과 치료 목표 설정 등의 임상적 목표에 큰 도움을 주고 있다.[177]
암[편집]
염증이 있다고 해서 암이 무조건 발생하는 것은 아니지만, 암이 발생할 확률이 어느 정도 증가할 수 있다.[181] 염증은 암의 주변을 둘러싼 미세환경을 조절하여 종양의 증식, 암세포의 생존과 전이에 기여한다.[182][183] 암과 관련된 염증은 암세포의 유전자 돌연변이를 촉진할 수 있다.[184] 대략 15–25%의 암에서 만성염증이 관여한다.[3][185] 암세포는 조직으로의 침윤과 다른 곳으로의 이동, 전이를 위해 셀렉틴과 다양한 케모카인들을 이용한다.[186] 종양면역학에서 주목하는 다양한 면역계의 세포들은 암의 발생을 저해한다.[187] 세포 발달에 중요한 영향을 미치는 스테로이드 호르몬 수용체와 염증에 중요한 역할을 하는 NF-κB와 같은 전사인자의 상호작용은 암세포에 대한 염증 자극에 대단히 중요한 영향을 줄 수 있다.[188] 이러한 경로의 차단을 통하여 암의 진행을 막음과 동시에 암과 관련 없는 조직의 부작용을 최소로 하는 치료법에 기여할 수 있다.[189][190][191]
알레르기[편집]
제 1형 과민반응, 즉 알러지 반응은 면역관용이 필요한 물질들에 대해 부적절한 면역반응이 일어나 혈관확장과 염증반응 등이 일어나는 현상이다.[7] 사전에 감작된 비만세포는 자극에 활성화되어 탈과립을 일으킨다. 이러한 작용이 일어나면 비만세포에서 히스타민, 단백분해효소, 프로테오글리칸, TNF-α 등 다양한 물질이 염증매개물질을 생성, 분비된다.[192] 이렇게 분비된 히스타민은 염증에 관여하여 혈관확장, 전염증성물질과 사이토카인 분비, 백혈구의 혈관외유출을 일으킨다.[53] 대표적인 예로, 비만세포가 알레르겐에 의해 과민반응을 일으켜 알레르기 비염, 천식 등이 생길 수 있다.[192] 심각한 염증은 전신적인 반응이 오는 아나필락시스로 이어져 생명을 위협할 수 있다.[192] 제 2형, 제 3형 과민반응은 항체에 의한 반응과 백혈구에 의해 염증이 유도된다.[53][193]
우울증[편집]
우울증과 염증은 밀접한 관련을 가진다.[194] 예를 들어, 바이러스, 세균, 기생충 등의 감염원이 일으키는 염증반응이 우울증을 일으킬 가능성이 있다.[195] 이러한 기전은 우울증의 원인을 설명하는 한가지 가설인 '병원체 숙주 방어 가설'(PATHOS-D)에서도 잘 드러난다.[196] 염증성 사이토카인의 분비가 증가는 뇌가 우리 몸을 질병상태로 판단하도록 유도하고, 그 결과 우울한 감정 및 우울증이 발생할 수 있다.[197] 몸이 아프면 생길 수 있는 병적인 증상들, 예를 들어 감기에 걸렸을 때 피곤하고 무기력하며 아픈 기분이 드는 것처럼 우울증도 똑같은 증상이 나타날 수 있다.[198] 양극성장애를 겪는 환자에서 우울 삽화가 진행되면 염증성 사이토카인이 증가하고, 삽화가 종료됨에 따라 다시 감소하게 된다.[199] 주요우울장애 환자에게 항우울제 투여와 함께 소염제나 항염증치료를 같이 진행한 경우 우울 증상을 유의하게 개선되었고, 항우울제에 대한 치료반응 역시 더 좋게 나타났다.[200][201]
HIV/AIDS[편집]
HIV에 감염된 사람들에게 단순한 면역기능의 저하뿐만 아니라 지속적인 염증과 비정상적인 면역기능 활성화가 관찰된다.[202][203] 만성염증은 HIV 감염자에게 면역기능의 이상과 면역노화를 유도하여 노인성질병과 면역결핍의 조기발생을 일으킨다.[204][205] 심지어 오랜 기간동안 항레트로바이러스요법을 통하여 잘 관리되고 있는 HIV 감염자의 경우에도 지속적인 저강도의 만성염증이 나타난다.[206] 많은 학자들은 HIV 감염이 면역결핍과 함께 만성염증을 일으키는데 주목하고 있다.[207][208] HIV 감염자의 만성염증은 AIDS 이외의 원인으로 HIV 감염자가 사망하는데 중요한 영향을 미친다.[209]
근질환[편집]
염증성 근병증은 면역계가 불필요하게 근육을 공격하여, 근육의 염증이 일어나는 질환이다. 이러한 염증은 다양한 자가면역질환의 한 특징이기도 한데, 전신경화증, 다발성근염, 피부근염, 봉입체근염 등이 대표적이다.[53][210]
백혈구 이상[편집]
백혈구는 염증의 진행과 전파에서 중요한 역할을 담당한다. 따라서 백혈구의 기능 손상은 염증의 방어 기능에 악영향을 미치며, 인체를 감염에 취약하도록 만든다.[53] 기능이 손상된 백혈구는 부착수용체에 문제가 생겨 혈관벽을 빠져나갈 수 없거나(백혈구부착결핍증), 식작용에 문제가 생기거나(세디아크-히가시 증후군), 미생물 제거기능이 손상(만성 육아종병)되는 등의 유전질환에서 발견될 수 있다. 골수를 침범하는 다양한 질환들도 혈중 백혈구의 감소나 미성숙 백혈구 형성에 영향을 미친다.
일상활동과 염증[편집]
식습관과 염증[편집]
열량이 높고 포화 지방산을 많이 포함한 식단은 염증성 반응의 증가와 연관된다.[211][212] 과식과 체내 지방축적은 전신의 염증반응과 대사 증후군의 가능성을 높일 수 있다.[157][213] 염증과 식습관의 관련성은 음식에 함유된 영양소 단위에서부터 각각의 식품, 식사 패턴까지 다양하게 연구되고 있다.[214] 복합 탄수화물, 식이섬유, 다가불포화지방산, 비타민 C, 비타민 E 등이 염증을 감소시킬 수 있다는 보고가 있다.[214] 낮은 포화지방과 높은 식이섬유를 특징으로 하는 지중해식 식단[215][216]은 다양한 연구를 통하여 염증을 줄여주고 심혈관질환의 발생 가능성을 낮출 수 있다는 결과를 보였다.[217][218][219] 지중해식 식단과 유사한 노르딕 다이어트 식사법 역시 항염증 효과가 있을 가능성이 제기되었다.[220]
염증과 식습관 및 식사 패턴을 정량적으로 연결하려는 시도도 있다. 이러한 관점의 지표로는 식사염증지표와 건강식이지표(식생활평가지수) 등이 있다. 건강식이지표(HEI)는 미국 농무부에 의해 개발된 식사의 질 평가 도구로, 미국인을 위한 식사지침을 기준으로 식사 패턴을 평가한다.[221] 이와 유사한 방식으로 한국인에 맞추어 식생활평가지수가 개발되었다.[222] 식사염증지표는 항염증효과와 염증촉진효과를 동시에 평가하여 식단의 정량화된 염증 가능성을 추정하는 수단으로 쓰인다.[223]
운동과 염증[편집]
운동과 염증 완화[편집]
규칙적인 운동이 염증 반응의 감소에 도움이 될 수 있다.[224][225] 이러한 염증의 개선은 운동의 강도와 지속 기간에 따라 달라질 수 있으며, 어떤 경우 운동과 염증 정도의 개선이 관련이 없다는 보고도 있다.[171] 또한 건강한 일반인과 이미 만성질환 또는 대사성 질환을 앓고 있는 환자군의 운동에 대한 효과가 다를 수 있다.[226] 연구 대상의 조건(나이, 성별, 기저질환), 체중 조절 여부, 운동의 정도 및 기간에 따라 상반되는 다양한 결과가 존재한다.[227] 그럼에도 불구하고 생물학적, 의학적 기전에 따라 활동량의 증가와 운동이 염증 반응의 감소에 긍정적 영향을 끼친다는 의견이 지배적이다.[228][229][230][231]
유산소운동을 한 결과 염증을 나타내는 표지자들의 농도가 감소함을 보여준 메타분석 결과가 있다.[232] 만성 염증성 질환을 가진 사람들을 대상으로, 운동을 일회성으로 하고난 후에는 체내 염증을 나타내는 염증 수치들이 나빠졌지만, 장기간(8–12주)의 운동을 지속하는 경우 염증 수치들이 개선되는 것을 확인하였다.[226] 가벼운 운동을 한 경우에는 염증 관련 수치가 감소하였으나, 중등도 이상의 운동을 하였을 때는 이러한 효과가 적게 나타났다. 특히 강도가 아주 높은 운동은 인체를 감염에 취약한 상태로 만들고, 급성 염증을 유발할 수도 있다.[233] 예를 들어, 마라톤은 전염증성 사이토카인으로 분류되는 IL-6의 수치를 단기간에 상승시킬 수 있다.[234] 그러나 중등도 이상의 운동이 더 효과가 있다는 연구 결과도 존재한다.[235] 일반인과 운동선수의 기본적인 면역 기능에는 큰 차이가 없는 것으로 보인다.[236][237]
운동을 통해서 지방세포를 줄이고, 면역세포(단핵구)를 늘릴 수 있으며, 활성산소에 대한 항산화작용과 항염증 사이토카인의 분비를 늘릴 수 있다.[231] 또한 그렐린을 감소시키고 아디포넥틴을 증가시켜서 식욕을 조절하고, 뼈의 강도를 높여주며, 인슐린 저항성과 대사증후군에 긍정적인 영향을 미칠 수 있다.[231]
식사 등으로 섭취하는 열량의 감소나 꾸준한 신체활동의 증가처럼 장기적인 행동의 변화가 염증을 반영하는 마커들의 수치를 개선할 수 있다. 현재까지 진행된 여러 연구에서도 입증되었듯이, 적절한 운동은 만성염증 상태의 개선에 도움이 되며, 비활동적인 생활은 염증질환의 발생과 악화에 영향을 미친다. 지나치게 과도한 운동의 경우 염증반응을 악화시킬 수 있지만, 운동을 시행하는 대부분의 일반인에게는 거의 도달할 수 없는 수준이다.
근육의 성장 및 재생과 염증[편집]
염증반응과 근육 성장은 관계가 있는 것으로 알려져 있다.[238] 운동 및 근수축으로 인한 근육의 손상과 뒤따르는 국소적 염증반응은 근육의 성장에 필요하다.[239] 근수축에 반응하여 근육에 급성 염증반응이 일어나 손상을 입은 근육조직이 제거, 분해된다.[240]
신장성 운동[241]과 단축성 운동, 등척성 운동[242]을 시행한 후 근육의 염증이 일어날 수 있다. 특히 근육의 길이가 늘어나는 신장성 운동을 하고 난 이후 근육 조직에 염증이 주로 일어난다. 신장성 운동에 의한 운동유발성 근육 손상이 일어나고 복구되는 과정동안 염증 반응이 중요한 역할을 차지한다.
신장성 운동을 마친 후 24–48시간에 거쳐 근육통이 유발된다. 이러한 근육통을 지연성 근육통이라 부르며, 근육의 근섬유와 Z선에 대한 구조적인 손상이 그 원인으로 꼽힌다. Z선은 액틴과 마이오신 필라멘트가 붙어있는 부위로, 근섬유가 수축할 때 구조적인 지지대 역할을 한다. 그러나 근섬유에 과도한 부하가 걸리는 경우 Z선이 지지대 역할을 제대로 하지 못하고 움직이며 무너지는 현상이 발생한다.[243] 이에 따라 평행하게 배열되어 있던 액틴과 마이오신 필라멘트의 배열이 흐트러지게 된다. 이러한 근섬유의 분열은 백혈구를 자극하여 근육통을 유발하고, 염증반응을 일으키게 한다. 혈액의 크레아틴 키나아제와 미오글로빈 농도가 상승하고,[244] 근섬유의 손상으로 인해 정상 근육과는 다른 구조가 관찰된다. 손상 후 2일이 지난 후부터 서서히 근섬유가 재생되기 시작한다.[243] 염증 반응의 결과로 생긴 물질들(히스타민, K+, 키닌류 등)은 근육의 자유신경말단을 자극한다.[245]
운동유발성 근육 손상이 일어난 후 근육 조직에 백혈구가 동원되고, 다양한 사이토카인 및 마이오카인이 분비된다.[242] IL-1β, IL-8, TNF-α, IL-6 등의 전염증성 사이토카인이 분비된다. 이러한 사이토카인들은 흔히 손상 후 5–7일 정도까지 분비될 수 있다.[244][240] 염증이 생긴 근육에는 위성세포에 의해 근육의 성장과 손상 복구가 일어난다. 위성세포는 운동 등으로 인해 근육이 손상되면 활성화되고, 근육이 부하에 적응을 하거나 회복을 거쳐 더 강해지는데 중요한 역할을 하게 된다. 위성세포는 손상된 근섬유를 보수하기 위해 스스로 분열하고 다시 늘어나는 특성을 가진다.[246] 구체적으로, 위성세포는 근핵을 새로 만들고 손상된 근섬유를 보수하며 단백질을 합성하는 과정을 통해 근육을 재생시키고 근비대를 유도한다.[247] IL-6의 증가와 IL-6 수용체의 발현이 이 과정에 기여한다.[248] 엘리트 파워리프팅 선수의 경우 일반인에 비해 근육의 위성세포 수가 2배까지 늘어날 수 있다고 한다.[249]
근육에 대한 부하 운동 이후에는 근육의 성장과 분화를 억제하는 신호물질인 마이오스타틴이 감소하게 된다.[250] 동시에 근육세포에서 근육의 수축에 반응하여 마이오카인의 분비량이 증가한다.[251]
만성염증과 근육손실[편집]
과도한 염증상태나 만성염증은 근육 성장에 필요한 동화작용을 방해한다. 만성염증은 노화에 따른 근육량의 감소에 일정 부분 기여하는 것으로 알려져 있다.[252][253] 만성염증 상태에서 TNF-α가 증가하면서 IGF1-Akt/PKB 신호전달경로[254]나 mTOR 신호전달경로[255]가 억제되고, 그 결과 근육의 이화작용, 즉 근육량의 감소가 발생할 수 있다.[256] 다양한 사이토카인이 IGF1이 작용하는 것을 방해하여 동화작용 및 근육 합성을 방해할 수 있다. 패혈증과 같이 전신의 심각한 염증상태가 지속되는 경우, 류신의 근육 합성 작용과 근원섬유, 근육세포질 합성이 일어나지 않는 것이 관찰되었다.[256][257]
"신호 대 잡음비" 이론[편집]
국소부위의 급성염증은 근육의 성장에 필요한 반면, 저강도의 만성염증은 근육의 동화작용을 방해한다. 염증의 정도에 따라서 근육의 성장이 달라질 수 있다는 사실은 염증과 근육 성장이 신호 대 잡음비 모델을 따른다는 것을 시사한다. 영양학자 브래드 필론은 이러한 이론을 제안하면서[258] 만성염증으로 인한 "잡음"을 최소로 유지하고, 국소부위의 급성염증을 적절한 상태로 조절한다면 근육 성장에 도움을 줄 수 있다고 설명하였다.
염증 조절[편집]
염증조절복합체[편집]
염증복합체는 선천성 면역계의 일부로, 염증반응의 활성화에 관여하는 다단백질 올리고머이다.[259] 이들은 미생물의 감염이나 조직 손상 등의 염증유발 환경에서 발현, 조립된다.[260] 이러한 자극에 노출되어 형성된 염증조절복합체는 캐스페이즈-1의 활성화 과정에 관여한다.[261] 그 결과 전염증성 사이토카인인 IL-1β, IL-18의 분비와 가스더민 D의 분해 활성이 일어난다.[259] 또한 가스더민 D의 분해를 통해 세포막 천공을 일으키는 파이롭토시스와 같은 세포사멸 기전에도 연관되어 있다.[262] 염증복합체의 조절 기전이 비정상적일 경우, 제 1형 당뇨병, 류마티스 관절염, 다발경화증 등과 같은 자가면역질환[263]이나, 암, 대사성 질환, 신경퇴행성 질환 등이 발병할 수 있다.[259]
염증과 약물[편집]
항염증제는 염증을 억제할 수 있는 약물들이다. 코르티코스테로이드는 가장 강력한 항염증제 중 하나로, 다양한 염증성 질환에서 널리 사용된다.[264] 이들은 유전자 전사 과정과 세포의 신호전달경로, 예를 들어 AP-1, NF-κB의 활성을 조절하여 염증을 조절한다.[265][266] 흔히 NSAID로 불리는 비스테로이드 항염증제는 염증유발물질인 프로스타글란딘을 합성하는 COX 효소를 차단하여 항염증 작용을 한다. 이들은 COX-1, COX-2를 동시에 억제하는 비선택적 항염증제와 COX-2만을 선택적으로 억제하는 COX-2 선택적 항염증제로 분류할 수 있다.[267] 특정한 면역세포나 염증성 사이토카인을 타겟으로 하는 생물학적 제제들도 개발되고 있다.[268] 리툭시맙, 인플릭시맙 등은 류마티스 관절염에서 유용하게 사용된다.[269] 스타틴 역시 항염증작용을 보인다.[270]
특정한 약물이나 화학물질은 염증에 영향을 미칠 수 있다. 비타민의 적절한 섭취가 염증을 조절할 수 있다.[271] 비타민 A 결핍은 염증반응을 증가시킨다.[272] 비타민 C는 항산화작용을 통하여 염증마커의 감소를 유도한다.[271][273] 마약류 중 코카인과 엑스터시 등의 약물은 NF-κB와 같이 염증과 관련된 신호전달경로를 활성화시켜 영향을 미칠 수 있다.[274][275]
면역조절[편집]
면역계의 조절을 통하여 비정상적인 염증을 조절할 수 있다. 면역조절은 다양한 질병에서 치료방법으로 사용되고 있으며, 면역계의 활성을 증가시키거나 감소시켜 질병을 조절할 수 있다.[276] 면역요법이 사용되는 대표적인 질병은 암이며,[277] 이 과정에서 염증이 암의 치료에 기여할 수 있다.[278] 예를 들어 항 PD-1 단일클론항체와 같은 면역항암제들의 경우 T세포의 면역반응을 유도하여 암세포를 사멸시키는 기전을 가지는데, 종양의 미세환경에서 염증반응을 증가시켜 이러한 치료를 도울 수 있다.[279] 많은 만성질환에서 염증의 조절을 통해 질병의 조절 및 치료를 시도한다.[280] 자가면역질환,[281] 천식,[282] 감염질환[283] 등의 질병에서 염증 조절을 위한 면역요법이 사용된다.
일부 건강기능식품은 면역기능을 조절하여 염증을 완화시킬 수 있는 가능성이 있으며, 고려인삼, 홍삼, 알로에 겔, 클로렐라, 상어간유 등이 식약처의 고시형 원료로 인정받았다.[284] 나노입자를 통하여 면역조절 및 염증 완화를 유도할 수 있다.[285]
다른 생물의 염증[편집]
진화적으로 염증은 잘 보존되어 있는 현상이며, 척추동물과 무척추동물 모두에서 면역체계의 일차적인 방어기전으로 보인다.[286] 다세포생물의 경우 조직의 손상과 감염에 대항하기 위한 반응이 필요하다.[287] 무척추동물에게는 식세포의 식작용과 항균펩타이드 등의 선천성 면역이 존재하며, 적응 면역의 경우 진화적으로 나중에 나타나 척추동물 중 유악류에게서만 발견된다.[288] 따라서 무척추동물의 면역반응, 염증반응은 척추동물의 염증반응과 다른 형태로 발현된다.[289]
무척추동물[편집]

무척추동물은 개방순환계를 가지고 있으며 모세혈관이 없다.[290] 또한 혈액과 조직액이 서로 분리되지 않아 순환계를 도는 혈액을 체액으로 통칭한다. 따라서 척추동물과 동일한 형태의 염증반응이 일어날 수 없고, 외부 병원체에 대해 선천성 면역으로 대항한다. 체액 내에 다양한 체액세포(hemocyte)가 존재하여 무척추동물이 외부 병원체를 무력화시킬 수 있다.[291] 대표적으로 세포성 면역기전으로 식작용, 결절 형성, 캡슐화를 꼽을 수 있고, 체액성 면역기전으로 항균펩타이드와 페놀옥시데이즈 시스템을 꼽을 수 있다.[292] 히드라속 등의 무척추동물에서는 손상된 조직에서 발생하는 손상연관분자유형를 인식하여 선천성 면역 반응이 일어날 수 있다.[293] 또한 응고반응의 형태로 면역작용을 하는 투구게와 같은 경우도 있다.[287][294]
인간에게 염증성 질환으로 알려진 질병들이 무척추동물에게도 발생할 수 있다. 예를 들어 무척추동물에게도 암이 발생할 수 있다. 초파리속에 속한 파리들의 경우, JAK-STAT 신호전달경로의 과도한 활성이 세포증식을 유도하고, 양성종양이나 특정한 종류의 암을 형성한다.[295] 연체동물, 특히 조개류의 경우 체액(인간의 혈액에 대응됨)에서 비정상적인 체액세포(인간의 혈구에 대응됨)가 관찰되는, 인간의 백혈병과 대응되는 질병이 관찰되었고, p53 단백질 유전자의 돌연변이가 관찰되었다.[296] 그러나 무척추동물에게 암은 매우 희귀하게 발견되며, 이는 척추동물에 비해 무척추동물이 구조적으로 단순하기 때문이라고 추정된다.[297]
무척추동물은 때로 인간의 염증성 질환에 대한 연구 모델로 쓰이기도 한다. 예쁜꼬마선충은 감염에 대한 선천성 면역작용을 분석하기 위해 쓰인다.[298] 노화, 암, 노인성 심장질환, 혈관신생, 저산소증 등 다양한 염증 관련 인간 질병들의 실험 대상으로 초파리, 예쁜꼬마선충, 이매패류 등이 사용된다.[298]
척추동물[편집]
척추동물 간에도 염증반응의 차이가 존재한다. 다른 척추동물에서도 인간과 겹치는 염증마커들이 발견되었다.[299] 그러나 응고반응에 관여하는 응고인자가 척추동물 사이에서 조금씩 다르다.[300] 상처에 대한 조직의 복구 과정도 동물별로 조금씩 다르다.[301] 그럼에도 불구하고 쥐, 기니피그, 토끼, 개, 고양이, 영장류 등이 인간의 염증성 질환의 모델로 사용된다.[302]
반려동물의 수명이 길어지면서 이들에게도 염증성 질환이 대두되고 있다.[303][304]
염증과 역사[편집]
인간이 출현한 이후 염증은 인류와 함께 공존해왔다. 현대의 고고학자들과 생물학자들은 6000년에 살았던 인간의 뼈에서 관절염의 흔적을 발견하기도 한다.[305] 기원전 2000년의 이집트 파피루스에도 염증으로 인한 고름이 묘사되어 있을 만큼 염증의 역사는 길고 오래되었다.[306]
고대 그리스와 로마의 사람들은 염증에 관한 기록을 역사에 남겼다. 염증을 뜻하는 영어의 inflammation은 "불에 타다"를 뜻하는 라틴어인 inflammare에서 기원하였다.[307] 기원전 5세기의 히포크라테스는 염증을 조직이 손상된 후 조기 치유 과정의 하나라고 설명하였다.[308] 1세기의 켈수스는 "염증"이라는 단어를 처음 사용하고, 염증의 4요소를 묘사하였다.[309] 갈레노스는 조직의 기능 상실과 함께 사체액설을 이용하여 염증을 설명하였다.[308]
19세기 중반에 들어서 과학의 발달과 함께 감염에 대한 패러다임 전환이 일어나면서 염증에 대한 본격적인 연구가 시작되었다.[310] 다양한 학자들이 염증 반응에 대해 연구하여 각기 다른 발견을 할 수 있었다. 이 시기 생물학자들인 피르호와 콘하임, 메치니코프는 염증의 원인을 놓고 대립하였는데, 피르호는 조직세포의 과도한 대사작용 및 퇴행을, 콘하임은 혈관을, 메치니코프는 식세포 작용을 주 원인으로 주장하였다.[308][311] 셋 모두 염증이라는 현상을 단편적으로 바라본 결과 통합적인 설명을 해내지 못하게 되었다.[310]
20세기에 접어들며 면역학의 눈부신 발전과 함께 염증 과정이 통합적, 전체적으로 연구되기 시작하였다. 헨리 H. 데일은 자가약리학(Autopharmacology, 自家藥理學) 개념을 제안하며 염증을 설명하려 시도하였다.[310] 1926년 칼 아쇼프에 의해 망상내피계가 제안되며 식세포 작용의 실체가 밝혀졌다. 같은 해 가스통 라몽은 디프테리아 백신을 연구하던 중 염증반응을 이용한 면역 보조제를 처음으로 개발하였다.[312] 1900년대를 전후하여 리차드 파이퍼, 아돌프 빈다우스, 헨리 H. 데일, 윌리엄 S. 틸렛, 울프 폰 오일러 등 다양한 과학자들이 염증과 직·간접적으로 관련된 물질들을 발견하였다.[312] 1970년대 중반 스탠리 코헨에 의해 사이토카인이란 용어가 사용된 이후 다양한 염증매개물질이 규명되었다. 분자생물학과 면역학적 기법을 이용하여 염증의 비밀이 계속해서 밝혀지고 있다.[308]
염증질환 예시[편집]
관련 서적[편집]
- Cavaillon, Jean-Marc; Singer, Mervyn, 편집. (2017년 10월). 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》. Wiley. ISBN 9783527338993.
- Roy, Sashwati; Bagchi, Debasis; Raychaudhuri, Siba P., 편집. (2013). 《Chronic Inflammation: Molecular Pathophysiology, Nutritional and Therapeutic Interventions》 1판. Taylor & Francis Group, LLC. ISBN 978-1-4398-7215-4.
- 池谷, 敏郎 (2019년 4월). 오시연, 편집. 《아프다면 만성염증 때문입니다》 [体內の「炎症」を抑えると、病気にならない!]. 보누스. ISBN 9788964943724.
- Eula, Biss (2016년 11월). 김명남, 편집. 《면역에 관하여》 [On Immunity: An Inoculation]. 열린책들. ISBN 9788932918105.
같이 보기[편집]
참고 문헌[편집]
- ↑ 가 나 InformedHealth.org [Internet] (2018년 2월 22일), “What is an inflammation?”, Institute for Quality and Efficiency in Health Care (IQWiG), 2019년 10월 8일에 확인함
- ↑ Ferrero-Miliani L, Nielsen OH, Andersen PS, Girardin SE (2006년 11월 27일), “Chronic inflammation: importance of NOD2 and NALP3 in interleukin-1beta generation”, 《Clinical and Experimental Immunology》 147 (2): 227-235, doi:10.1111/j.1365-2249.2006.03261.x, PMC 1810472, PMID 17223962
- ↑ 가 나 다 라 Chen L, 외. (2018), “Inflammatory responses and inflammation-associated diseases in organs”, 《Oncotarget》 9: 7204-7218, doi:10.18632/oncotarget.23208, PMC 5805548, PMID 29467962, 2019년 10월 11일에 확인함
- ↑ Baron S, 외. (1996), 〈Chapter 49: Nonspecific Defences〉, 《Medical Microbiology》 4판, Galveston (TX): University of Texas Medical Branch at Galveston, ISBN 9780963117212, 2019년 10월 8일에 확인함
- ↑ 가 나 강희정, 구향모, 권주희, 김희수, 백승용, 이상인, 이재경, 황동준 (2018), 〈1차 방어 작용(비특이적 면역)〉, 《고등셀파: 생명과학1》, 천재교육, 2019년 10월 5일에 원본 문서에서 보존된 문서, 2019년 10월 8일에 확인함
- ↑ Vincenzo B, 외. (2015), “Adaptive Immunity and Inflammation”, 《International Journal of Inflammation》 2015: 575406, doi:10.1155/2015/575406, PMC 4352488, PMID 25793142, 2019년 10월 10일에 확인함
- ↑ 가 나 다 Abbas AK, 외. (2013), 세포분자면역학 교재연구회, 편집., 《Cellular and Molecular Immunology》 [세포분자면역학] 7판, 범문에듀케이션, ISBN 9788997140541
- ↑ Moilanen E (2014년 1월), “Two Faces of Inflammation: An Immunopharmacological View”, 《Basic & Clinical Pharmacology & Toxicology》 114 (1): 2–6, doi:10.1111/bcpt.12180, PMID 24286361
- ↑ 문상호, 이송, 배대경 (2018), “프롤로치료” (PDF), 《Journal of the Korean Orthopaedic Association》 (대한정형외과학회) 53: 393–399, doi:10.4055/jkoa.2018.53.5.393, 2019년 5월 2일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 14일에 확인함
- ↑ 가 나 Tracy RP (2006), “The Five Cardinal Signs of Inflammation: Calor, Dolor, Rubor, Tumor … and Penuria (Apologies to Aulus Cornelius Celsus, De medicina, c. A.D. 25)”, 《The Journals of Gerontology: Series A》 61 (10): 1051–1052, doi:10.1093/gerona/61.10.1051, PMID 17077197
- ↑ Oh SY, 외. (2015), “Sepsis in Patients Receiving Immunosuppressive Drugs in Korea: Analysis of the National Insurance Database from 2009 to 2013”, 《Korean Journal of Critical Care Medicine (대한중환자의학회지)》 30 (4): 249–257, doi:10.4266/kjccm.2015.30.4.249, 2019년 10월 8일에 확인함
- ↑ Signore A, “About inflammation and infection”, 《EJNMMI Research》 3: 8, doi:10.1186/2191-219X-3-8, PMC 3564704, PMID 23374699, 2019년 10월 8일에 확인함
- ↑ Zaccone P, 외. (2006), “Parasitic worms and inflammatory diseases”, 《Parasite Immunology》 28: 515–523, doi:10.1111/j.1365-3024.2006.00879.x
- ↑ Eltzschig HK, Carmeliet P (2011), “Hypoxia and Inflammation”, 《N Engl J Med》 364 (7): 656–665, doi:10.1056/NEJMra0910283, PMC 3930928, PMID 21323543, 2019년 10월 8일에 확인함
- ↑ Janeway, Charles A Jr; 외. (2001), 〈Hypersensitivity diseases〉, 《Immunobiology: The Immune System in Health and Disease》 (영어), Garland Science, ISBN 978-0-8153-3642-6
- ↑ Billiar TR, Vodovotz Y (2017), “Time for trauma immunology”, 《PLOS Medicine》 14 (7): e1002342, doi:10.1371/journal.pmed.1002342, PMC 5507395, PMID 28700602, 2019년 10월 8일에 확인함
- ↑ Matzinger, Polly (2002년 4월), “The Danger Model: A Renewed Sense of Self”, 《Science》 296 (5566): 301–305, doi:10.1126/science.1071059, PMID 11951032
- ↑ Seemann S, 외. (2017), “Comprehensive comparison of three different animal models for systemic inflammation”, 《Journal of Biomedical Science》 24 (1): 60, doi:10.1186/s12929-017-0370-8, PMC 5569462, PMID 28836970, 2019년 10월 8일에 확인함
- ↑ Webb DR (2014), “Animal models of human disease: Inflammation”, 《Biochemical Pharmacology》 87 (1): 121-130, doi:10.1016/j.bcp.2013.06.014, PMID 23811309
- ↑ Nyholm SV, Graf J (2012), “Knowing your friends: invertebrate innate immunity fosters beneficial bacterial symbioses”, 《Nature Reviews Microbiology》 10 (12): 815–827, doi:10.1038/nrmicro2894, PMC 3870473, PMID 23147708, 2019년 10월 10일에 확인함
- ↑ Janeway, Charles A Jr; Medzhitov, Ruslan (2002), “Innate Immune Recognition”, 《Annual Review of Immunology》 20: 197-216, doi:10.1146/annurev.immunol.20.083001.084359, PMID 11861602
- ↑ Rowley AF (1996년 2월), “The Evolution of Inflammatory Mediators”, 《Mediators of Inflammation》 5 (1): 3–13, doi:10.1155/S0962935196000014, PMC 2365766, PMID 18475690, 2019년 10월 10일에 확인함
- ↑ Scharrer B, Lochhead MS (1950년 7월), “Tumors in the Invertebrates: A Review”, 《Mediators of Inflammation》 10 (7): 403–419, PMID 15427079, 2019년 10월 10일에 확인함
- ↑ Stael S, 외. (2015년 1월), “Plant innate immunity – sunny side up?”, 《Trends in Plant Science》 (Cell Press) 20 (1): 3-11, doi:10.1016/j.tplants.2014.10.002, PMC 4817832, PMID 25457110, 2019년 10월 10일에 확인함
- ↑ Muthamilarasan M, Prasad M (2013년 6월), “Plant innate immunity: An updated insight into defense mechanism”, 《Journal of Biosciences》 (Indian Academy of Sciences) 38 (2): 433-449, doi:10.1007/s12038-013-9302-2, PMID 23660678
- ↑ Bullon P (2014), Ekuni D, Battino M, Tomofuji T, Putnins EE, 편집., 《Studies on Periodontal Disease》, Springer, 229쪽, doi:10.1007/978-1-4614-9557-4, ISBN 978-1-4614-9556-7
- ↑ 가 나 Garg N, Amit G (2007), 《Textbook of Endodontics》 1판, JP Medical Ltd, 70쪽, ISBN 9789352705351, 2019년 10월 11일에 확인함
- ↑ Rather LJ (1971년 3월), “Disturbance of function (functio laesa): the legendary fifth cardinal sign of inflammation, added by Galen to the four cardinal signs of Celsus”, 《Bulletin of the New York Academy of Medicine》 47 (3): 303-322, PMC 1749862, PMID 5276838, 2019년 10월 11일에 확인함
- ↑ Rush B, 외. (1809), 《The works of Thomas Sydenham, M. D., on acute and chronic diseases: with their histories and modes of cure》, Philadelphia: Benjamin & Thomas Kite, 448쪽, 2019년 10월 11일에 확인함
- ↑ Freire MO, Van Dyke TE (2013), “Natural resolution of inflammation”, 《Periodontology 2000》 63 (1): 149–164, doi:10.1111/prd.12034, PMC 4022040, PMID 23931059, 2019년 10월 11일에 확인함
- ↑ Chandrasoma P, Taylor CR (1997), 〈Chapter 3. The Acute Inflammatory Response〉, 《Concise Pathology》 3판, McGraw-Hill, ISBN 978-0-8385-1499-3, OCLC 150148447, 2019년 10월 11일에 확인함
- ↑ Light AR (2010), 〈Chapter 11. Myalgia and Fatigue〉, Kruger L, Light AR, 《Translational Pain Research: From Mouse to Man》, CRC Press/Taylor & Francis, ISBN 978-1-4398-1209-9, 2019년 10월 11일에 확인함
- ↑ Wright CE, 외. (2005년 7월), “Acute inflammation and negative mood: Mediation by cytokine activation”, 《Brain, Behavior, and Immunity》 19 (4): 345-350, doi:10.1016/j.bbi.2004.10.003, PMID 15944074
- ↑ Delinger RP, 외. (2013년 2월), “Surviving sepsis campaign: international guidelines for management of severe sepsis and septic shock: 2012” (PDF), 《Critical Care Medicine》 41 (2): 580–637, doi:10.1097/CCM.0b013e31827e83af, PMID 23353941, 2019년 10월 11일에 확인함
- ↑ Szalay, Jessie (2018년 10월 19일). “What Is Inflammation?”. 《Live Science》. 2019년 10월 7일에 원본 문서에서 보존된 문서. 2019년 10월 11일에 확인함.
- ↑ Santos-Longhurst, Adrienne (2018년 7월 27일). “Understanding and Managing Chronic Inflammation”. 《Healthline》. 2019년 7월 1일에 원본 문서에서 보존된 문서. 2019년 10월 11일에 확인함.
- ↑ 가 나 Damjanov I (2016), 〈2. Inflammation〉, 《Pathology for the Health Professions》 5판, Saunders, ISBN 978-0323357210
- ↑ Grigg JB, Sonnenberg GF (2017), “Host-Microbiota Interactions Shape Local and Systemic Inflammatory Diseases”, 《The Journal of Immunology》 198 (2): 564–571, doi:10.4049/jimmunol.1601621, PMC 5228396, PMID 28069751, 2019년 10월 14일에 확인함
- ↑ Kumar V, Abbas AK, Aster JC (2015), 〈8. Infectious Diseases〉, 《Robbins and Cotran Pathologic Basis of Disease Professional Edition》 9판, Saunders, ISBN 978-0-323-26616-1
- ↑ 가 나 Pahwa R, Jialal I (2019년 6월 4일), 〈Chronic Inflammation〉, 《StatPearls [Internet]》, StatPearls Publishing, 2019년 10월 14일에 확인함
- ↑ “III. What are the types of inflammation?”. 《Pathology Demystified》. NUS Centre for Instructional Technology. 2019년 10월 13일에 원본 문서에서 보존된 문서. 2019년 10월 14일에 확인함.
- ↑ Elmer, Jamie (2018년 12월 19일). “Inflammation: What You Need to Know”. 《Healthline》. 2019년 10월 14일에 확인함.
- ↑ Kemp WL, 외. (2008), 〈Chapter 2. Inflammation and Repair〉, 《Pathology: The Big Picture》, McGraw-Hill, ISBN 978-0-07-147748-2, 2019년 10월 14일에 확인함
- ↑ Ward PA, Lentsch AB (1999년 6월), “The Acute Inflammatory Response and Its Regulation”, 《Archives of Surgery》 134 (6): 666-669, doi:10.1001/archsurg.134.6.666, PMID 10367878
- ↑ Barnig C, 외. (2019), “Activation of Resolution Pathways to Prevent and Fight Chronic Inflammation: Lessons From Asthma and Inflammatory Bowel Disease”, 《Frontiers in Immunology》 10: 1699, doi:10.3389/fimmu.2019.01699, PMID 31396220
- ↑ 가 나 Schett G, Neurath MF (2018), “Resolution of chronic inflammatory disease: universal and tissue-specific concepts”, 《Nature Communications》 9: 3261, doi:10.1038/s41467-018-05800-6, PMC 6093916, PMID 30111884, 2019년 10월 14일에 확인함
- ↑ 가 나 다 Halim I (2008), 《Essential Revision Notes in Surgery for Medical Students》 1판, Cheshire, UK: PasTest, 15–16쪽, ISBN 978-1905635399
- ↑ Wright HL, 외. (2010), “Neutrophil function in inflammation and inflammatory diseases”, 《Rheumatology》 49 (9): 1618–1631, doi:10.1093/rheumatology/keq045, PMID 20338884
- ↑ Akin C (2007), “What does a basophil do?”, 《Blood》 110 (3): 790-791, doi:10.1182/blood-2007-04-085233
- ↑ Abdulkhaleq LA, 외. (2018), “The crucial roles of inflammatory mediators in inflammation: A review”, 《Veterinary World》 11 (5): 627–635, doi:10.14202/vetworld.2018.627-635, PMC 5993766, PMID 29915501, 2019년 10월 14일에 확인함
- ↑ 가 나 Feghali CA, Wright TM (1997), “Cytokines in Acute and Chronic Inflammation” (PDF), 《Frontiers in Bioscience》 2: d12–26, doi:10.2741/a171, PMID 9159205, 2019년 10월 15일에 확인함
- ↑ Branco AC, 외. (2018), “Role of Histamine in Modulating the Immune Response and Inflammation”, 《Mediators of Inflammation》 2018: 9524075, doi:10.1155/2018/9524075, PMC 6129797, PMID 30224900, 2019년 10월 16일에 확인함
- ↑ 가 나 다 라 마 바 사 아 자 차 카 타 파 하 거 너 Cotran RS, Colins T, Kumar V, 편집. (1998), 《Robbins Pathologic Basis of Disease》 6판, Philadelphia: Saunders, ISBN 978-0721673356
- ↑ Schroder K, Tschopp J (2010), “The Inflammasomes”, 《Cell》 140 (6): 821-832, doi:10.1016/j.cell.2010.01.040, PMID 20303873
- ↑ Bonizzi G, Karin M (2004), “The two NF-κB activation pathways and their role in innate and adaptive immunity”, 《Trends in Immunology》 25 (6): 280-288, doi:10.1016/j.it.2004.03.008, PMID 15145317
- ↑ 가 나 Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 9. Monocytes and Macrophages〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ Dray A (1995), “Inflammatory mediators of pain”, 《British Journal of Anaesthesia》 75 (2): 125-131, doi:10.1093/bja/75.2.125, PMID 7577246
- ↑ Brøchner AC, Toft P (2009년 9월 15일), “Pathophysiology of the systemic inflammatory response after major accidental trauma”, 《Scandinavian Journal of Trauma, Resuscitation and Emergency Medicine》 17: 43, doi:10.1186/1757-7241-17-43, PMC 2757019, PMID 19754938, 2019년 10월 27일에 확인함
- ↑ Goris R (1999년 10월 8일), “Local versus systemic inflammatory response in shock, trauma and sepsis” (PDF), 《Symposium Wondinfectie en brandwonden》: 37-44, 2019년 10월 27일에 확인함
- ↑ Adib-Conquy M, Cavaillon JM (2007년 7월), “Stress molecules in sepsis and systemic inflammatory response syndrome”, 《FEBS Letters》 581 (19): 3723–3733, doi:10.1016/j.febslet.2007.03.074, PMID 17428476
- ↑ Dinarello CA, Gelfand JA, Wolff SM (1993년 4월 14일), “Anticytokine Strategies in the Treatment of the Systemic Inflammatory Response Syndrome”, 《JAMA》 269 (14): 1829–1835, doi:10.1001/jama.1993.03500140081040, PMID 8459516
- ↑ Munford RS, Pugin J (2000년 2월), “Normal Responses to Injury Prevent Systemic Inflammation and Can Be Immunosuppressive”, 《American Journal of Respiratory and Critical Care Medicine》 163 (24): 316–321, doi:10.1164/ajrccm.163.2.2007102, PMID 11179099
- ↑ Cai B, Deitch EA, Ulloa L (2010), “Novel Insights for Systemic Inflammation in Sepsis and Hemorrhage”, 《Mediators of Inflammation》 2010: 642462, doi:10.1155/2010/642462, PMC 2902015, PMID 20628562, 2019년 10월 27일에 확인함
- ↑ “American College of Chest Physicians/Society of Critical Care Medicine Consensus Conference: definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis”, 《Critical Care Medicine》 20 (6): 864–874, 1992년 6월, doi:10.1097/00003246-199206000-00025, PMID 1597042
- ↑ Balk RA (2013), “Systemic inflammatory response syndrome (SIRS): Where did it come from and is it still relevant today?”, 《Virulence》 5 (1): 20–26, doi:10.4161/viru.27135, PMC 3916374, PMID 24280933, 2019년 10월 27일에 확인함
- ↑ Singer M, 외. (2016년 1월 12일), “The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3)”, 《JAMA》 315 (8): 801–810, doi:10.1001/jama.2016.0287, PMC 4968574, PMID 26903338, 2019년 10월 26일에 확인함
- ↑ Kokkas B (2010), “Tissue injury and inflammation”, 《Annals of General Psychiatry》, 9(Suppl 1): S1, doi:10.1186/1744-859X-9-S1-S1, PMC 2991780, PMID 25410142, 2019년 10월 17일에 확인함
- ↑ Claesson-Welsh L (2015년 8월), “Physiology of the endothelium”, 《Upsala Journal of Medical Sciences》 120 (3): 135–143, doi:10.3109/03009734.2015.1064501, PMC 4526869, PMID 26220421, 2019년 10월 17일에 확인함
- ↑ Galley HF, Webster NR (2004), “Physiology of the endothelium”, 《British Journal of Anaesthesia》 93 (1): 105-113, doi:10.1093/bja/aeh163, PMID 15121728
- ↑ Benly P (2015), “Role of Histamine in Acute Inflammation” (PDF), 《Journal of Pharmaceutical Sciences and Research》 (PharmaInfo Publications (India)) 7 (6): 373-376, 2019년 10월 17일에 확인함
- ↑ 가 나 Edwards SH, “Chemical Mediators of Inflammation”, 《MSD Manual Veterinary Manual》, 2019년 10월 17일에 확인함
- ↑ Wu H, 외. (2019년 2월), “Beyond a neurotransmitter: The role of serotonin in inflammation and immunity”, 《Pharmacological Research》 140: 100-114, doi:10.1016/j.phrs.2018.06.015, PMID 29953943
- ↑ Herr N, Bode C, Duerschmied D (2017), “The Effects of Serotonin in Immune Cells”, 《Frontiers in Cardiovascular Medicine》 4: 48, doi:10.3389/fcvm.2017.00048, PMC 5517399, PMID 28775986, 2019년 10월 17일에 확인함
- ↑ 송후림, 우영섭, 박원명 (2012), “중추신경계 외부의 세로토닌”, 《대한정신약물학회지》 23: 45-50
- ↑ Medcalf RL (2007년 7월), “Fibrinolysis, inflammation, and regulation of the plasminogen activating system”, 《Journal of Thrombosis and Haemostasis》 5 (Supplement 1): 132–142, doi:10.1111/j.1538-7836.2007.02464.x, PMID 17635719
- ↑ 가 나 Ganju K, Ganju E (2018), 《Pharma Triumph: An Encyclopedia For GPAT And All Pharmacy Recruitment And Entrance Exam》 1판, Bilaspur, India: Evincepub Publishing, 265–266쪽, ISBN 978-9388277150
- ↑ 황응수, 박정규, 차장용 (2004), “바이러스 감염에 대한 면역반응” (PDF), 《Immune Network》 (대한면역학회) 4 (2): 73–80, 2018년 7월 25일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 19일에 확인함
- ↑ Tizard IR (2017), 〈Chapter 7. Innate Immunity: The Complement System〉, 《Veterinary Immunology》 10판, Saunders, ISBN 9780323523493
- ↑ Naudin C, 외. (2017), “Factor XII Contact Activation”, 《Seminars in Thrombosis and Hemostasis》 43 (8): 814-826, doi:10.1055/s-0036-1598003, PMID 28346966
- ↑ Delves PJ, “Cellular Components of the Immune System”, 《MSD Manual Professional Version》, 2019년 10월 20일에 확인함
- ↑ Fang P, 외. (2018년 7월), “Immune cell subset differentiation and tissue inflammation”, 《Journal of Hematology & Oncology》 11 (1): 97, doi:10.1186/s13045-018-0637-x, PMC 6069866, PMID 30064449, 2019년 10월 20일에 확인함
- ↑ “Cellular Components of Inflammation”. 《Medictests》. 2019년 10월 20일에 확인함.
- ↑ Woo SY (2012), “Neutrophils in Immunity” (PDF), 《Journal of Bacteriology and Virology》 (대한미생물학회) 42 (2): 97, doi:10.4167/jbv.2012.42.2.172, 2018년 7월 26일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 20일에 확인함
- ↑ Kumar KP, Nicholls AJ, Wong CH (2018), “Partners in crime: neutrophils and monocytes/macrophages in inflammation and disease”, 《Cell and Tissue Research》 371 (3): 551–565, doi:10.1007/s00441-017-2753-2, PMC 5820413, PMID 29387942, 2019년 10월 20일에 확인함
- ↑ 가 나 Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 10. Neutrophils〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ Matovani A (1999년 6월), “The chemokine system: redundancy for robust outputs”, 《Immunology Today》 20 (6): 254-257, doi:10.1016/S0167-5699(99)01469-3, PMID 10354549
- ↑ Ray K (1996), “Molecular mechanisms of leukocyte recruitment in the inflammatory process”, 《Cardiovascular Research》 32 (4): 733-742, PMID 8915191
- ↑ 가 나 Herrington CS (2014), 《Muir's textbook of pathology》 15판, CRC Press, 59쪽, ISBN 9781444184976
- ↑ 가 나 송재우 (2017), “백혈구, 내피세포 혈소판의 상호작용에 의한 출혈과 지혈” (PDF), 《Clinical & Experimental Thrombosis and Hemostasis》 (한국혈전지혈학회) 3 (1): 12-15, doi:10.14345/ceth.17004, 2021년 8월 28일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 20일에 확인함
- ↑ 정혜리 (1996), “알레르기 질환에서의 adhesion molecule의 역할” (PDF), 《Korean Journal of Pediatrics》 (대한소아청소년과학회) 39 (10): 1344-1350, 2019년 10월 20일에 확인함[깨진 링크(과거 내용 찾기)]
- ↑ Lay K (2003), “Arrest Chemokines” (PDF), 《Microcirculation》 10: 289–295, doi:10.1038/sj.mn.7800194, PMID 12851646, 2019년 10월 21일에 확인함
- ↑ Mogensen TH (2009년 4월), “Pathogen Recognition and Inflammatory Signaling in Innate Immune Defenses”, 《Clinical Microbiology Reviews》 22 (2): 240–273, doi:10.1128/CMR.00046-08, PMC 2668232, PMID 19366914, 2019년 10월 22일에 확인함
- ↑ Medzhitov, Ruslan; Janeway, Charles, Jr (2000년 8월 3일), “Innate Immunity”, 《N Engl J Med》 343 (5): 338-344, doi:10.1056/NEJM200008033430506, PMID 10922424
- ↑ Moretti J, Blander JM (2014), “Insights into phagocytosis-coupled activation of Pattern Recognition Receptors and Inflammasomes”, 《Current Opinion in Immunology》 26: 100-110, doi:10.1016/j.coi.2013.11.003, PMC 3932007, PMID 24556406, 2019년 10월 22일에 확인함
- ↑ PrabhuDas MR, 외. (2017년 5월 15일), “A Consensus Definitive Classification of Scavenger Receptors and Their Roles in Health and Disease”, 《The Journal of Immunology》 198 (10): 3775–3789, doi:10.4049/jimmunol.1700373, PMC 5671342, PMID 28483986, 2019년 10월 22일에 확인함
- ↑ 가 나 다 Rosales C, Uribe-Querol E (2017), “Phagocytosis: A Fundamental Process in Immunity”, 《BioMed Research International》 2017: 9042851, doi:10.1155/2017/9042851, PMC 5485277, PMID 28691037, 2019년 10월 22일에 확인함
- ↑ Schroder K, Paul J H, Ravasi T, Hume DA (2004년 2월), “Interferon‐γ: an overview of signals, mechanisms and functions”, 《Journal of Leukocyte Biology》 75 (2): 163–189, doi:10.1189/jlb.0603252, PMID 14525967
- ↑ Parameswaran N, Patial S (2010), “Tumor Necrosis Factor-α Signaling in Macrophages”, 《Critical Reviews in Eukaryotic Gene Expression》 20 (2): 87–103, doi:10.1189/jlb.0603252, PMC 3066460, PMID 21133840, 2019년 10월 22일에 확인함
- ↑ Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 21. TNF Superfamily〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 20. IL-1 Superfamily and Inflammasome〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ Ren K, Torres R (2009), “Role of interleukin-1β during pain and inflammation”, 《Brain Research Reviews》 60 (1): 57–64, doi:10.1016/j.brainresrev.2008.12.020, PMC 3076185, PMID 19166877, 2019년 10월 22일에 확인함
- ↑ Rock KL, Kono H (2008), “The inflammatory response to cell death”, 《Annual Review of Pathology: Mechanisms of Disease》 3: 99-126, doi:10.1146/annurev.pathmechdis.3.121806.151456, PMC 3094097, PMID 18039143, 2019년 10월 29일에 확인함
- ↑ Suthahar N, 외. (2017년 8월), “From Inflammation to Fibrosis—Molecular and Cellular Mechanisms of Myocardial Tissue Remodelling and Perspectives on Differential Treatment Opportunities”, 《Current Heart Failure Reports》 14 (4): 235–250, doi:10.1007/s11897-017-0343-y, PMC 5527069, PMID 28707261, 2019년 10월 29일에 확인함
- ↑ Eming SA, Krieg T, Davidson JM (2007년 3월), “Inflammation in Wound Repair: Molecular and Cellular Mechanisms”, 《Journal of Investigative Dermatology》 127 (3): 514–525, doi:10.1038/sj.jid.5700701, PMID 17299434
- ↑ 가 나 Porcheray F, 외. (2005년 12월), “Macrophage activation switching: an asset for the resolution of inflammation”, 《Clinical & Experimental Immunology》 142 (3): 481-489, doi:10.1111/j.1365-2249.2005.02934.x, PMC 1809537, PMID 16297160, 2019년 11월 3일에 확인함
- ↑ Al-Mulla F, 외. (2011), “Impaired TGF-β signaling and a defect in resolution of inflammation contribute to delayed wound healing in a female rat model of type 2 diabetes”, 《Molecular BioSystems》 7: 3006-3020, doi:10.1039/C0MB00317D, PMID 21850315
- ↑ Sato Y, 외. (1999년 11월 11일), “Regulatory Role of Endogenous Interleukin-10 in Cutaneous Inflammatory Response of Murine Wound Healing”, 《Biochemical and Biophysical Research Communications》 265 (1): 194-199, doi:10.1006/bbrc.1999.1455, PMID 10548513
- ↑ Serhan CN (2014년 6월 5일), “Pro-resolving lipid mediators are leads for resolution physiology”, 《Nature》 510 (7503): 92–101, doi:10.1038/nature13479, PMC 4263681, PMID 24899309, 2019년 10월 29일에 확인함
- ↑ Basil MC, Levy BD (2016년 1월), “Specialized pro-resolving mediators: endogenous regulators of infection and inflammation”, 《Nature Reviews Immunology》 16 (1): 51–67, doi:10.1038/nri.2015.4, PMC 5242505, PMID 26688348, 2019년 10월 29일에 확인함
- ↑ Greenhalgh DG (1998년 9월), “The role of apoptosis in wound healing”, 《The International Journal of Biochemistry & Cell Biology》 30 (9): 1019-1030, doi:10.1016/S1357-2725(98)00058-2, PMID 9785465
- ↑ Jiang D, 외. (2005년 11월), “Regulation of lung injury and repair by Toll-like receptors and hyaluronan”, 《Nature Medicine》 11 (11): 1173–1179, doi:10.1038/nm1315, PMID 16244651
- ↑ McQuibban GA, 외. (2000년 8월 18일), “Inflammation Dampened by Gelatinase A Cleavage of Monocyte Chemoattractant Protein-3”, 《Science》 289 (5482): 1202–1206, doi:10.1126/science.289.5482.1202, PMID 10947989
- ↑ Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 58. Glucocorticoids〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ 가 나 다 Ortega-Gómez A, Perretti M, Soehnlein O (2013년 5월), “Resolution of inflammation: an integrated view”, 《EMBO Molecular Medicine》 5 (5): 661–674, doi:10.1002/emmm.201202382, PMC 3662311, PMID 23592557, 2019년 11월 2일에 확인함
- ↑ Fullerton JN, Gilroy DW (2016년 8월), “Resolution of inflammation: a new therapeutic frontier”, 《Nature Reviews Drug Discovery》 15 (8): 551–567, doi:10.1038/nrd.2016.39, PMID 27020098
- ↑ Sugimoto MA, 외. (2016년 4월 26일), “Resolution of Inflammation: What Controls Its Onset?”, 《Frontiers in Immunology》 7: 160, doi:10.3389/fimmu.2016.00160, PMC 4845539, PMID 27199985, 2019년 11월 3일에 확인함
- ↑ 가 나 Roy S, Bagchi D, Raychaudhuri SP, 편집. (2013), 〈Chapter 9. Resolution of Inflammation〉, 《Chronic Inflammation: Molecular Pathophysiology, Nutritional and Therapeutic Interventions》 1판, Taylor & Francis Group, LLC, ISBN 978-1-4398-7215-4
- ↑ Fujiwara N, Kobayashi K (2005), “Macrophages in Inflammation” 4 (3): 281-286, doi:10.2174/1568010054022024, PMID 16101534
- ↑ 가 나 Roy S, Bagchi D, Raychaudhuri SP, 편집. (2013), 〈Chapter 1. At the Interface between Acute and Chronic Inflammation: Insights from Computational Modeling〉, 《Chronic Inflammation: Molecular Pathophysiology, Nutritional and Therapeutic Interventions》 1판, Taylor & Francis Group, LLC, ISBN 978-1-4398-7215-4
- ↑ Hotamisligil GS (2006년 12월 14일), “Inflammation and metabolic disorders”, 《Nature》 444 (7121): 860–867, doi:10.1038/nature05485, PMID 17167474
- ↑ 가 나 다 Sarkar D, Fisher PB (2006), “Molecular mechanisms of aging-associated inflammation”, 《Cancer Letters》 236 (1): 13–23, doi:10.1016/j.canlet.2005.04.009, PMID 15978720
- ↑ Miyasaka M, Takatsu K, 편집. (2016), 〈Chapter 1. Prostaglandins in Chronic Inflammation〉, 《Chronic Inflammation: Mechanisms and Regulation》 1판, Springer Japan, doi:10.1007/978-4-431-56068-5, ISBN 978-4-431-56066-1
- ↑ 가 나 Roy S, Bagchi D, Raychaudhuri SP, 편집. (2013), 〈Chapter 2. The Cellular Component of Chronic Inflammation〉, 《Chronic Inflammation: Molecular Pathophysiology, Nutritional and Therapeutic Interventions》 1판, Taylor & Francis Group, LLC, ISBN 978-1-4398-7215-4
- ↑ Ito A, 외. (1995년 5월), “Expression of vascular permeability factor (VPF/VEGF) messenger RNA by plasma cells: Possible involvement in the development of edema in chronic inflammation”, 《Pathology International》 45 (10): 715-720, doi:10.1111/j.1440-1827.1995.tb03387.x, PMID 8563931
- ↑ Multhoff G, Molls M, Radons J (2012년 1월 12일), “Chronic inflammation in cancer development”, 《Frontiers in Immunology》 12 (2): 98, doi:10.3389/fimmu.2011.00098, PMC 3342348, PMID 22566887, 2019년 11월 3일에 확인함
- ↑ Straub RH, Schradin C (2016), “Chronic inflammatory systemic diseases: An evolutionary trade-off between acutely beneficial but chronically harmful programs”, 《Evolution, Medicine & Public Health》 2016 (1): 37–51, doi:10.1093/emph/eow001, PMC 4753361, PMID 26817483, 2019년 11월 3일에 확인함
- ↑ Kushner I, Samols D, Magrey M (2010년 3월 30일), “A unifying biologic explanation for “high‐sensitivity” C‐reactive protein and “low‐grade” inflammation”, 《Arthritis Care & Research (Hoboken)》 62 (4): 442-446, doi:10.1002/acr.20052, PMID 20391496
- ↑ 가 나 다 라 마 Antonelli M, Kushner I (2017년 5월), “It’s time to redefine inflammation”, 《The FASEB Journal》 31 (5): 1787–1791, doi:10.1096/fj.201601326R, PMID 28179421, 2019년 10월 28일에 확인함
- ↑ Pearson TA, 외. (2003년 1월 28일), “Markers of inflammation and cardiovascular disease: application to clinical and public health practice: A statement for healthcare professionals from the Centers for Disease Control and Prevention and the American Heart Association”, 《Circulation》 107 (3): 499–511, doi:10.1161/01.cir.0000052939.59093.45, PMID 12551878
- ↑ Fliser D, 외. (2004년 8월 31일), “Antiinflammatory Effects of Angiotensin II Subtype 1 Receptor Blockade in Hypertensive Patients With Microinflammation”, 《Circulation》 110 (9): 1103–1107, doi:10.1161/01.CIR.0000140265.21608.8E, PMID 15313950
- ↑ 가 나 Kushner I, Rzewnicki D, Samols D (2006년 2월), “What Does Minor Elevation of C-Reactive Protein Signify?”, 《American Journal of Medicine》 119 (2): 166.e17–166.e28, doi:10.1016/j.amjmed.2005.06.057, PMID 16443421
- ↑ Lee S, 외. (2019년 2월 13일), “Sex Difference in the Association between High-sensitivity C-reactive Protein and Depression: The 2016 Korea National Health and Nutrition Examination Survey”, 《Scientific Reports》 9 (1): 1913, doi:10.1038/s41598-018-36402-3, PMC 6374396, PMID 30760746, 2019년 11월 3일에 확인함
- ↑ Ko YJ, 외. (2012년 11월), “High-Sensitivity C-Reactive Protein Levels and Cancer Mortality”, 《Cancer Epidemiology, Biomarkers & Prevention》 21 (11): 2076–2086, doi:10.1158/1055-9965.EPI-12-0611, PMID 23136255
- ↑ Pietzner M, 외. (2017), “Comprehensive metabolic profiling of chronic low-grade inflammation among generally healthy individuals”, 《BMC Medicine》 15: 210, doi:10.1186/s12916-017-0974-6, PMC 5708081, PMID 29187192, 2019년 10월 28일에 확인함
- ↑ Minihane AM, 외. (2015년 10월 14일), “Low-grade inflammation, diet composition and health: current research evidence and its translation”, 《The British Journal of Nutrition》 114 (7): 999–1012, doi:10.1017/S0007114515002093, PMC 4579563, PMID 26228057, 2019년 10월 28일에 확인함
- ↑ Lacourt TE, 외. (2018년 4월 26일), “The High Costs of Low-Grade Inflammation: Persistent Fatigue as a Consequence of Reduced Cellular-Energy Availability and Non-adaptive Energy Expenditure”, 《Frontiers in Behavioral Neuroscience》 12: 78, doi:10.3389/fnbeh.2018.00078, PMC 5932180, PMID 29755330, 2019년 11월 3일에 확인함
- ↑ Duncan BB, 외. (2003년 7월), “Low-Grade Systemic Inflammation and the Development of Type 2 Diabetes: The Atherosclerosis Risk in Communities Study”, 《Diabetes》 52 (7): 1799–1805, doi:10.2337/diabetes.52.7.1799, PMID 12829649
- ↑ Chandra Gupta S, 외. (2018년 9월 27일), “Inflammation, a Double-Edge Sword for Cancer and Other Age-Related Diseases”, 《Frontiers in Immunology》 9: 2160, doi:10.3389/fimmu.2018.02160, PMC 6170639, PMID 30319623, 2019년 11월 3일에 확인함
- ↑ Goldfine AB, Shoelson SE (2017년 1월 3일), “Therapeutic approaches targeting inflammation for diabetes and associated cardiovascular risk”, 《The Journal of Clinical Investigation》 127 (1): 83–93, doi:10.1172/JCI88884, PMC 5199685, PMID 28045401, 2019년 10월 29일에 확인함
- ↑ Brissett AE, Sherris DA (2001), “Scar Contractures, Hypertrophic Scars, and Keloids”, 《Facial Plastic Surgery》 17 (4): 263-272, doi:10.1055/s-2001-18827, PMID 11735059
- ↑ 최은광 (2016), “직장 주위 농양 배액술” (PDF), 《제55회 대한소화기내시경학회 세미나》: 295-299, 2019년 10월 23일에 확인함
- ↑ 조성범 (2012), “화농성 및 아메바 간농양” (PDF), 《2012년 대한간학회 추계 Single Topic Symposium》: 21-28, 2019년 7월 12일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 23일에 확인함
- ↑ 한현호, 오득영 (2015년 9월), “만성창상의 치료에 쓰이는 치료제재” (PDF), 《Journal of the Korean Medical Association》 (대한의사협회) 58 (9): 809-813, doi:10.5124/jkma.2015.58.9.809, 2019년 5월 2일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 23일에 확인함
- ↑ Mehta AC, Ali SR (2017), “Mnemonic for the Differential Diagnosis of Noncaseating Granulomas”, 《Sarcoidosis Vasculitis and Diffuse Lung Diseses》 34 (2), 2019년 10월 22일에 확인함
- ↑ Kumar V, Cotran RS, Robbins SL (1997), 〈Chapter 2. Acute and Chronic Inflammation〉, 《Basic Pathology》 6판, W.B. Saunders Co., ISBN 978-0-7216-5122-4
- ↑ Carapetis JR, 외. (2016), “Acute rheumatic fever and rheumatic heart disease”, 《Nature Reviews Disease Primers》 14 (2): 15084, doi:10.1038/nrdp.2015.84, PMC 5810582, PMID 27188830, 2019년 10월 22일에 확인함
- ↑ Bond CJ (1917년 12월 8일), “On the haemagglutinin reaction as a test of the toxicity of various antiseptic reagents, and on the association (if any) between the haemagglutinin content of the blood serum and pus, and capacity to resist infection”, 《British Medical Journal》 2 (2971): 751–755, doi:10.1136/bmj.2.2971.751, PMC 2349551, PMID 20768840, 2019년 10월 22일에 확인함
- ↑ “염증성 장질환”. 《세브란스병원》. 2015년 10월 1일. 2019년 10월 23일에 원본 문서에서 보존된 문서. 2019년 10월 23일에 확인함.
- ↑ “류마티스 관절염”. 《서울아산병원》. 2019년 10월 23일에 원본 문서에서 보존된 문서. 2019년 10월 23일에 확인함.
- ↑ 가 나 다 Germolec DR, 외. (2018), 〈Chapter 5. Markers of Inflammation〉, DeWitt JC, Rockwell CE, Bowman CC, 《Immunotoxicity Testing》 2판, Springer, doi:10.1007/978-1-4939-8549-4, ISBN 978-1-4939-8548-7
- ↑ Jain S, 외. (2011), “Acute-phase proteins: As diagnostic tool”, 《Journal of Pharmacy and Bioallied Sciences》 3 (1): 118–127, doi:10.4103/0975-7406.76489, PMC 3053509, PMID 21430962, 2019년 10월 23일에 확인함
- ↑ Tidy, Colin (2018년 7월 18일). “Blood Tests to Detect Inflammation”. 《patient.info》. 2019년 10월 23일에 원본 문서에서 보존된 문서. 2019년 10월 23일에 확인함.
- ↑ 가 나 Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 53. Pentraxins in the Orchestration of Defense and Tissue Repair during the Acute Phase Response〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156
- ↑ Du Clos TW (2000), “Function of C-reactive protein”, 《Annals of Medicine》 32 (2): 274-278, doi:10.3109/07853890009011772, PMID 10852144
- ↑ “ESR (L2016)”. 《서울아산병원》. 2019년 10월 23일에 원본 문서에서 보존된 문서. 2019년 10월 23일에 확인함.
- ↑ Xu H, 외. (2003년 12월), “Chronic inflammation in fat plays a crucial role in the development of obesity-related insulin resistance”, 《Journal of Clinical Investigation》 112 (12): 1821–1830, doi:10.1172/JCI200319451, PMC 296998, PMID 14679177, 2019년 10월 28일에 확인함
- ↑ 가 나 Monteiro R, Azevedo I (2010), “Chronic Inflammation in Obesity and the Metabolic Syndrome”, 《Mediators of Inflammation》 2010 (12): 289645, doi:10.1155/2010/289645, PMC 2913796, PMID 20706689, 2019년 10월 23일에 확인함
- ↑ 가 나 Ellulu MS, 외. (2017년 6월), “Obesity and inflammation: the linking mechanism and the complications”, 《Circulation》 13 (4): 851–863, doi:10.5114/aoms.2016.58928, PMC 5507106, PMID 28721154, 2019년 10월 28일에 확인함
- ↑ Petersen AM, Pedersen BK (2005년 4월), “The anti-inflammatory effect of exercise”, 《Journal of Applied Physiology》 98 (4): 1154–1162, doi:10.1152/japplphysiol.00164.2004, PMID 15772055
- ↑ Rogowski O, 외. (2010), “Waist circumference as the predominant contributor to the micro-inflammatory response in the metabolic syndrome: a cross sectional study”, 《Journal of Inflammation》 7: 35, doi:10.1186/1476-9255-7-35, PMC 2919526, PMID 20659330, 2019년 10월 28일에 확인함
- ↑ 김미경, 박정현 (2010), “대사증후군” (PDF), 《Journal of the Korean Medical Association》 (대한의사협회) 55 (10): 1005–1013, doi:10.5124/jkma.2012.55.10.1005, 2018년 7월 26일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 28일에 확인함
- ↑ Makki K, 외. (2013), “Adipose Tissue in Obesity-Related Inflammation and Insulin Resistance: Cells, Cytokines, and Chemokines”, 《ISRN Inflammation》 2013: 139239, doi:10.1155/2013/139239, PMC 3881510, PMID 24455420, 2019년 10월 28일에 확인함
- ↑ Lauterbach MA, Wunderlich FT (2017), “Macrophage function in obesity-induced inflammation and insulin resistance”, 《Pflügers Archiv: European Journal of Physiology》 469 (3): 385–396, doi:10.1007/s00424-017-1955-5, PMC 5362664, PMID 28233125, 2019년 10월 28일에 확인함
- ↑ Subramanian, V.; Ferrante, A.W., Jr. (2009), “Obesity, Inflammation, and Macrophages”, 《63rd Nestlé Nutrition Institute Workshop, Pediatric Program》 63: 151–162, doi:10.1159/000209979, PMID 19346774
- ↑ Parimisetty A, 외. (2016), “Secret talk between adipose tissue and central nervous system via secreted factors—an emerging frontier in the neurodegenerative research”, 《Journal of Neuroinflamamtion》 13: 67, doi:10.1186/s12974-016-0530-x, PMC 4806498, PMID 27012931, 2019년 10월 28일에 확인함
- ↑ Esposito K, 외. (2002년 10월 15일), “Inflammatory Cytokine Concentrations Are Acutely Increased by Hyperglycemia in Humans: Role of Oxidative Stress”, 《Circulation》 106 (16): 2067–2072, doi:10.1161/01.CIR.0000034509.14906.AE, PMID 12379575
- ↑ Choi J, 외. (2013년 3월), “Obesity and C‐reactive protein in various populations: a systematic review and meta‐analysis”, 《Obesity Reviews》 14 (3): 232-244, doi:10.1111/obr.12003, PMID 23171381
- ↑ 성상현 (2019년 6월 13일). “노화에 대한 분자 생물학적 이해와 응용 동향”. 《BRIC》. 2019년 10월 29일에 원본 문서에서 보존된 문서. 2019년 10월 30일에 확인함.
- ↑ 가 나 성보경, 정해영 (2005), “노화과정에서 분자염증 반응과 에너지 대사의 중요성” (PDF), 《대한암예방학회지》 10: 6-17, 2019년 10월 30일에 확인함
- ↑ Stone WL, Basit H, Burns B (2019년 4월 25일), 〈Pathology, Inflammation〉, 《StatPearls [Internet]》, StatPearls Publishing, 2019년 10월 30일에 확인함
- ↑ 가 나 다 Woods JA, 외. (2012년 2월), “Exercise, Inflammation and Aging”, 《Aging and Disease》 3 (1): 130–140, PMC 3320801, PMID 22500274, 2019년 10월 24일에 확인함
- ↑ Brüünsgaard H, Pedersen BK (2003년 2월), “Age-related inflammatory cytokines and disease”, 《Immunology and Allergy Clinics of North America》 23 (1): 15-39, doi:10.1016/S0889-8561(02)00056-5, PMID 12645876
- ↑ Ferrucci L, 외. (2005년 3월 15일), “The origins of age-related proinflammatory state”, 《Blood》 105 (6): 2294-2299, doi:10.1182/blood-2004-07-2599, PMID 15572589
- ↑ Sanada F, 외. (2018년 2월 22일), “Source of Chronic Inflammation in Aging”, 《Frontiers in Cardiovascular Medicine》 5: 12, doi:10.3389/fcvm.2018.00012, PMC 5850851, PMID 29564335, 2019년 10월 29일에 확인함
- ↑ Duggal NA (2018년 12월), “Reversing the immune ageing clock: lifestyle modifications and pharmacological interventions”, 《Biogerontology》 19 (6): 481–496, doi:10.1007/s10522-018-9771-7, PMC 6223743, PMID 30269199, 2019년 11월 3일에 확인함
- ↑ Bäck M, 외. (2019년 3월 7일), “Inflammation and its resolution in atherosclerosis: mediators and therapeutic opportunities”, 《Nature Reviews Cardiology》 16 (2): 389–406, doi:10.1038/s41569-019-0169-2, PMID 30846875
- ↑ 가 나 Libby P, Ridker PM, Maseri A (2002년 3월 5일), “Inflammation and Atherosclerosis”, 《Circulation》 105 (9): 1135–1143, doi:10.1161/hc0902.104353, PMID 11877368
- ↑ Espinola-Klein C, 외. (2007년 12월), “Inflammation, atherosclerotic burden and cardiovascular prognosis”, 《Clinical Medicine Insights: Cardiology》 195 (2): e126–e134, doi:10.1016/j.atherosclerosis.2007.01.021, PMID 17336309
- ↑ Ridker PM (2003년 1월 28일), “Clinical Application of C-Reactive Protein for Cardiovascular Disease Detection and Prevention”, 《Clinical Medicine Insights: Cardiology》 107 (3): 363–369, doi:10.1161/01.CIR.0000053730.47739.3C, PMID 12551853
- ↑ Antonopoulos AS, 외. (2012년 4월), “Statins as Anti-Inflammatory Agents in Atherogenesis: Molecular Mechanisms and Lessons from the Recent Clinical Trials”, 《Current Pharmaceutical Design》 18 (11): 1519–1530, doi:10.2174/138161212799504803, PMC 3394171, PMID 22364136, 2019년 10월 31일에 확인함
- ↑ 우리들내과의원 (2016년 11월 14일). “[암과 염증]염증이 암의 원인?”. 《휘경 우리들내과의원》. 2019년 10월 31일에 원본 문서에서 보존된 문서. 2019년 10월 31일에 확인함.
- ↑ 바이오휴머니스트 (2017년 7월 31일). “[암(癌)에게서 배우다] <15회> Tumor microenvironment(2) ; 여행, 그 변화의 유익함에 관하여”. 《BRIC》. 2019년 10월 31일에 원본 문서에서 보존된 문서. 2019년 10월 31일에 확인함.
- ↑ Ungefroren H, Sebens S, Seidl D, Lehnert H, Hass R (2011), “Interaction of tumor cells with the microenvironment”, 《Cell Communication and Signaling》 9: 1, doi:10.1186/1478-811X-9-18, PMC 3180438, PMID 21914164, 2019년 10월 31일에 확인함
- ↑ Colotta F, 외. (2009년 7월), “Cancer-related inflammation, the seventh hallmark of cancer: links to genetic instability”, 《Carcinogenesis》 30 (7): 1073–1081, doi:10.1093/carcin/bgp127, PMID 19468060
- ↑ Kawanishi S, 외. (2017년 8월), “Crosstalk between DNA Damage and Inflammation in the Multiple Steps of Carcinogenesis”, 《International Journal of Molecular Sciences》 18 (8): 1808, doi:10.3390/ijms18081808, PMC 5578195, PMID 28825631, 2019년 10월 31일에 확인함
- ↑ Coussens LM, Werb Z (2002년 12월 19일), “Inflammation and cancer”, 《Nature》 420 (6917): 860–867, doi:10.1038/nature01322, PMC 2803035, PMID 12490959, 2019년 10월 31일에 확인함
- ↑ Gunn L, 외. (2012년 9월 15일), “Opposing Roles for Complement Component C5a in Tumor Progression and the Tumor Microenvironment”, 《The Journal of Immunology》 189 (6): 2985–2994, doi:10.4049/jimmunol.1200846, PMC 3436956, PMID 22914051, 2019년 10월 31일에 확인함
- ↑ Copland JA, 외. (2012년 9월 15일), “Sex steroid receptors in skeletal differentiation and epithelial neoplasia: is tissue-specific intervention possible?”, 《BioEssays》 31 (6): 629–641, doi:10.1002/bies.200800138, PMID 19382224
- ↑ Yamamoto Y, Gaynor RB (2001년 1월 15일), “Therapeutic potential of inhibition of the NF-κB pathway in the treatment of inflammation and cancer”, 《Journal of Clinical Investigation》 107 (2): 135–142, doi:10.1002/bies.200800138, PMC 199180, PMID 11160126, 2019년 10월 31일에 확인함
- ↑ Roxburgh CS, McMillan DC (2014), “Cancer and systemic inflammation: treat the tumour and treat the host”, 《British Journal of Cancer》 110: 1409–1412, doi:10.1038/bjc.2014.90, PMC 3960633, PMID 24548867, 2019년 10월 31일에 확인함
- ↑ Najafi M, 외. (2019년 5월), “Tumor microenvironment: Interactions and therapy”, 《Journal of Cellular Physiology》 234 (5): 5700–5721, doi:10.1002/jcp.27425, PMID 30378106
- ↑ 가 나 다 김희규 (2017년 9월), “알레르기 염증에서의 비만세포 역할과 비만세포 관련 질환” (PDF), 《Allergy, Asthma & Respiratory Disease》 (대한천식알레르기학회) 5 (5): 248–255, doi:10.4168/aard.2017.5.5.248, 2018년 7월 18일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 31일에 확인함
- ↑ 조상헌 (2005). “과민반응 (Hypersensitivity Reaction)”. 《BRIC》. 2019년 10월 31일에 확인함.
- ↑ Miller AH, Raison CL (2016년 1월), “The role of inflammation in depression: from evolutionary imperative to modern treatment target”, 《Nature Reviews Immunology》 16 (1): 22–34, doi:10.1038/nri.2015.5, PMC 5542678, PMID 26711676, 2019년 10월 31일에 확인함
- ↑ Canli T (2014), “Reconceptualizing major depressive disorder as an infectious disease”, 《Biology of Mood & Anxiety Disorders》 4: 10, doi:10.1186/2045-5380-4-10, PMC 4215336, PMID 25364500, 2019년 10월 31일에 확인함
- ↑ Raison CL, Miller AH (2016년 1월), “Pathogen–Host Defense in the Evolution of Depression: Insights into Epidemiology, Genetics, Bioregional Differences and Female Preponderance”, 《Neuropsychopharmacology》 42 (1): 5–27, doi:10.1038/npp.2016.194, PMC 5143499, PMID 27629366, 2019년 10월 31일에 확인함
- ↑ Williams, Caroline (2015년 1월 4일). “Is depression a kind of allergic reaction?”. 《The Guardian》. 2019년 6월 12일에 원본 문서에서 보존된 문서. 2019년 10월 31일에 확인함.
- ↑ Maes M, 외. (2012), “Depression and sickness behavior are Janus-faced responses to shared inflammatory pathways”, 《BMC Medicine》 10: 66, doi:10.1186/1741-7015-10-66, PMC 3391987, PMID 22747645, 2019년 10월 31일에 확인함
- ↑ Brietzke E, 외. (2009년 8월), “Comparison of cytokine levels in depressed, manic and euthymic patients with bipolar disorder”, 《Journal of Affective Disorders》 116 (3): 214–217, doi:10.1016/j.jad.2008.12.001, PMID 19251324
- ↑ Müller N, 외. (2006년 7월), “The cyclooxygenase-2 inhibitor celecoxib has therapeutic effects in major depression: results of a double-blind, randomized, placebo controlled, add-on pilot study to reboxetine”, 《Molecular Psychiatry》 11 (7): 680–684, doi:10.1038/sj.mp.4001805, PMID 16491133
- ↑ Feltes PK, 외. (2017년 6월 27일), “Anti-inflammatory treatment for major depressive disorder: implications for patients with an elevated immune profile and non-responders to standard antidepressant therapy”, 《Journal of Psychopharmacology》 31 (9): 1149-1165, doi:10.1177/0269881117711708, PMC 5606303, PMID 28653857, 2019년 10월 31일에 확인함
- ↑ Paiardini M, Müller-Trutwin M (2013년 7월), “HIV-associated chronic immune activation”, 《Immunological Reviews》 254 (1): 78–101, doi:10.1111/imr.12079, PMC 3729961, PMID 23772616, 2019년 10월 30일에 확인함
- ↑ Klatt NR, 외. (2013년 7월), “Immune activation and HIV persistence: implications for curative approaches to HIV infection”, 《Immunological Reviews》 254 (1): 326-342, doi:10.1111/imr.12065, PMC 3694608, PMID 23772629, 2019년 10월 30일에 확인함
- ↑ Deeks SG (2011), “HIV Infection, Inflammation, Immunosenescence, and Aging”, 《Annual Review of Medicine》 62: 141–155, doi:10.1146/annurev-med-042909-093756, PMC 3759035, PMID 21090961, 2019년 10월 30일에 확인함
- ↑ Ipp H, Zemlin A (2013년 2월), “The paradox of the immune response in HIV infection: When inflammation becomes harmful”, 《Clinica Chimica Acta》 416: 96-99, doi:10.1016/j.cca.2012.11.025, PMID 23228847
- ↑ Erlandson KM, Campbell TB (2015년 8월), “Inflammation in Chronic HIV Infection: What Can We Do?”, 《The Journal of Infectious Diseases》 212 (3): 339–342, doi:10.1093/infdis/jiv007, PMID 25583171
- ↑ Zicari S, 외. (2019년 3월), “Immune Activation, Inflammation, and Non-AIDS Co-Morbidities in HIV-Infected Patients under Long-Term ART”, 《Viruses》 11 (3): 200, doi:10.3390/v11030200, PMC 6466530, PMID 30818749, 2019년 10월 30일에 확인함
- ↑ Nasi M, 외. (2014년 10월), “Persistent inflammation in HIV infection: established concepts, new perspectives”, 《Immunology Letters》 161 (2): 184–188, doi:10.1016/j.imlet.2014.01.008, PMID 24487059
- ↑ Tenorio AR, 외. (2014년 10월), “Soluble Markers of Inflammation and Coagulation but Not T-Cell Activation Predict Non–AIDS-Defining Morbid Events During Suppressive Antiretroviral Treatment”, 《The Journal of Infectious Diseases》 210 (8): 1248–1259, doi:10.1093/infdis/jiu254, PMC 4192039, PMID 24795473, 2019년 10월 31일에 확인함
- ↑ 강성욱 (2013년 12월), “Rituximab: 염증성 근병증 치료의 새로운 전망” (PDF), 《대한류마티스학회지》 20 (6): 345-347, doi:10.4078/jrd.2013.20.6.345, 2018년 7월 25일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 30일에 확인함
- ↑ Milanski M, 외. (2009년 1월 14일), “Saturated Fatty Acids Produce an Inflammatory Response Predominantly through the Activation of TLR4 Signaling in Hypothalamus: Implications for the Pathogenesis of Obesity”, 《Journal of Neuroscience》 29 (2): 359-370, doi:10.1523/JNEUROSCI.2760-08.2009, PMC 6664935, PMID 19144836, 2019년 10월 23일에 확인함
- ↑ van Dijk SJ, 외. (2009년 12월), “A saturated fatty acid-rich diet induces an obesity-linked proinflammatory gene expression profile in adipose tissue of subjects at risk of metabolic syndrome”, 《The American Journal of Clinical Nutrition》 90 (6): 1656–1664, doi:10.3945/ajcn.2009.27792, PMID 19828712
- ↑ Marsland AL, 외. (2010), “Systemic inflammation and the metabolic syndrome among middle-aged community volunteers”, 《Metabolism》 59 (12): 1801–1808, doi:10.1016/j.metabol.2010.05.015, PMC 2955187, PMID 20619428, 2019년 10월 23일에 확인함
- ↑ 가 나 나우리, 외. (2017), “대사성 질환자의 영양평가를 위한 한국형 식사염증지표 개발 및 타당성 검증: 한국인 유전체역학조사자료를 활용하여”, 《Korean Journal of Human Ecology》 (한국생활과학회) 26 (4): 369-381, doi:10.5934/kjhe.2017.26.4.369, 2019년 10월 23일에 확인함
- ↑ 양선희 (2009). “지중해식 식단 심장·뇌에 좋아”. 《서울아산병원》. 2019년 10월 23일에 확인함.
- ↑ 고승희 (2017년 6월 5일). “그 좋다는 ‘지중해 식단’, 어떻게 먹는 건가요?”. 《리얼푸드》. 2019년 10월 23일에 확인함.
- ↑ Calle MC, Andersen CJ (2019), “Assessment of Dietary Patterns Represents a Potential, Yet Variable, Measure of Inflammatory Status: A Review and Update”, 《Disease Markers》 2019: 3102870, doi:10.1155/2019/3102870, PMC 6360584, PMID 30805036, 2019년 10월 23일에 확인함
- ↑ Sureda A, 외. (2018년 1월), “Adherence to the Mediterranean Diet and Inflammatory Markers”, 《Nutrients》 10 (1): 62, doi:10.3390/nu10010062, PMC 5793290, PMID 29320413, 2019년 10월 23일에 확인함
- ↑ 이해나; 정선유 (2018년 12월 10일). “지중해식 식단, 왜 좋은지 밝혀져… "염증 줄이고, 당 분해 도와"”. 《헬스조선》. 2019년 10월 23일에 확인함.
- ↑ Lankinen M, Uusitupa M, Schwab U (2019년 6월), “Nordic Diet and Inflammation—A Review of Observational and Intervention Studies”, 《Nutrients》 11 (6): 1369, doi:10.3390/nu11061369, PMC 6627927, PMID 31216678, 2019년 10월 23일에 확인함
- ↑ Schwingshackl L, Hoffmann G (2015년 5월), “Diet Quality as Assessed by the Healthy Eating Index, the Alternate Healthy Eating Index, the Dietary Approaches to Stop Hypertension Score, and Health Outcomes: A Systematic Review and Meta-Analysis of Cohort Studies”, 《Journal of the Academy of Nutrition and Dietetics》 115 (5): 780–800.e5, doi:10.1016/j.jand.2014.12.009, PMID 25680825
- ↑ 육성민, 박소희, 문현경, 김기랑, 심재은, 황지윤 (2015), “국민건강영양조사 자료를 이용한 한국 성인의 식생활평가지수 개발” (PDF), 《Journal of Nutrition and Health》 (한국영양학회) 48 (5): 419–428, doi:10.4163/jnh.2015.48.5.419, 2019년 4월 30일에 원본 문서 (PDF)에서 보존된 문서, 2019년 10월 23일에 확인함
- ↑ Shivappa N, 외. (2014년 8월), “Designing and developing a literature-derived, population-based dietary inflammatory index”, 《Public Health Nutrition》 17 (8): 1689-1696, doi:10.1017/S1368980013002115, PMC 3925198, PMID 23941862, 2019년 10월 23일에 확인함
- ↑ Abramson JL, Vaccarino V (2002), “Relationship Between Physical Activity and Inflammation Among Apparently Healthy Middle-aged and Older US Adults”, 《Archives of Internal Medicine》 162 (11): 1286–1292, doi:10.1001/archinte.162.11.1286, PMID 12038947
- ↑ Hamer M, 외. (2012년 8월 21일), “Physical activity and inflammatory markers over 10 years follow up in men and women from the Whitehall II cohort study”, 《Circulation》 126 (8): 928–933, doi:10.1161/CIRCULATIONAHA.112.103879, PMC 3890998, PMID 22891048, 2019년 10월 24일에 확인함
- ↑ 가 나 Ploeger HE, 외. (2009), “The effects of acute and chronic exercise on inflammatory markers in children and adults with a chronic inflammatory disease: a systematic review”, 《Exercise immunology review》 15: 6–41, PMID 19957870
- ↑ Khazaei M (2012), “Chronic Low-grade Inflammation after Exercise: Controversies”, 《Iranian Journal of Basic Medical Sciences》 15 (5): 1008–1009, PMC 3586919, PMID 23495361, 2019년 10월 27일에 확인함
- ↑ Gleeson M, 외. (2011), “The anti-inflammatory effects of exercise: mechanisms and implications for the prevention and treatment of disease”, 《Nature Reviews Immunology》 11 (9): 607–615, doi:10.1038/nri3041, PMID 21818123
- ↑ Mathur N, Pedersen BK (2008), “Exercise as a Mean to Control Low-Grade Systemic Inflammation”, 《Mediators of Inflammation》 2008: 109502, doi:10.1155/2008/109502, PMC 2615833, PMID 19148295, 2019년 10월 27일에 확인함
- ↑ Beavers KM, 외., “Effect of exercise training on chronic inflammation”, 《Clinica Chimica Acta》 411 (11–12): 785–793, doi:10.1016/j.cca.2010.02.069, PMC 3629815, PMID 20188719, 2019년 10월 27일에 확인함
- ↑ 가 나 다 Ertek S, Cicero A (2012년 11월 9일), “Impact of physical activity on inflammation: effects on cardiovascular disease risk and other inflammatory conditions”, 《Archive of Medical Sciences》 8 (5): 794–804, doi:10.5114/aoms.2012.31614, PMC 3506236, PMID 23185187, 2019년 10월 27일에 확인함
- ↑ Zheng G, 외. (2019년 4월), “Effect of Aerobic Exercise on Inflammatory Markers in Healthy Middle-Aged and Older Adults: A Systematic Review and Meta-Analysis of Randomized Controlled Trials”, 《Frontiers in Aging Neuroscience》 11: 98, doi:10.3389/fnagi.2019.00098, PMC 6497785, PMID 31080412, 2019년 10월 24일에 확인함
- ↑ Suzuki K (2019년 6월), “Chronic Inflammation as an Immunological Abnormality and Effectiveness of Exercise”, 《Biomolecules》 9: 223, doi:10.3390/biom9060223, PMC 6628010, PMID 31181700, 2019년 10월 27일에 확인함
- ↑ Suzuki K (2003년 2월), “Impact of a Competitive Marathon Race on Systemic Cytokine and Neutrophil Responses”, 《Medicine & Science in Sports & Exercise》 35 (2): 348–355, doi:10.1249/01.MSS.0000048861.57899.04, PMID 12569227
- ↑ Abd El-Kader SM, 외. (2013년 12월), “Impact of moderate versus mild aerobic exercise training on inflammatory cytokines in obese type 2 diabetic patients: a randomized clinical trial”, 《African Health Sciences》 13 (4): 857–863, doi:10.4314/ahs.v13i4.1, PMC 4056484, PMID 24940305, 2019년 10월 27일에 확인함
- ↑ Pedersen BK, Hoffman-Goetz L (2000년 7월), “Exercise and the Immune System: Regulation, Integration, and Adaptation”, 《Physiological Reviews》 80 (3): 1055–1081, doi:10.1152/physrev.2000.80.3.1055, PMID 10893431
- ↑ Gleeson M (2006년 11월), “Immune system adaptation in elite athletes”, 《Current Opinion in Clinical Nutrition and Metabolic Care》 9 (6): 659–665, doi:10.1097/01.mco.0000247476.02650.18, PMID 17053416
- ↑ LaStayo PP, 외. (2007년 12월), “Elderly Patients and High Force Resistance Exercise—A Descriptive Report: Can an Anabolic, Muscle Growth Response Occur Without Muscle Damage or Inflammation?”, 《Journal of Geriatric Physical Therapy》 30 (53): 128–134, PMID 18171497
- ↑ Marimuthu K, Murton AJ, Greenhaff PL (2011년 2월), “Mechanisms regulating muscle mass during disuse atrophy and rehabilitation in humans”, 《Journal of Applied Physiology》 110 (2): 555-560, doi:10.1152/japplphysiol.00962.2010, PMID 21030670
- ↑ 가 나 Cannon JG, St Pierre BA (1998년 2월), “Cytokines in exertion-induced skeletal muscle injury”, 《Molecular and Cellular Biochemistry》 179 (1-2): 159-167, doi:10.1023/a:1006828425418, PMID 9543358
- ↑ Peake J, 외. (2005), “Characterization of inflammatory responses to eccentric exercise in humans”, 《Exercise Immunology Review》 11: 64-85, PMID 16385845
- ↑ 가 나 Fatouros IG, Jamurtas AZ (2016), “Insights into the molecular etiology of exercise-induced inflammation: opportunities for optimizing performance”, 《Journal of Inflammation Research》 9: 175–186, doi:10.2147/JIR.S114635, PMC 5085309, PMID 27799809, 2019년 10월 23일에 확인함
- ↑ 가 나 Staron RS, Hikida RS (2000), 〈Chapter 11. Muscular Response to Exercise and Training〉, Garrett WE, Kirkendall DT, 《Exercise and Sport Science》 1판, LWW, ISBN 978-0683034219
- ↑ 가 나 Peake JM, 외. (2017), “Muscle damage and inflammation during recovery from exercise”, 《Journal of Applied Physiology》 122 (3): 559-570, doi:10.1152/japplphysiol.00971.2016, PMID 28035017
- ↑ Armstrong RB (1984년 12월), “Mechanisms of exercise-induced delayed onset muscular soreness: a brief review”, 《Medicine & Science in Sports & Exercise》 16 (6): 529–538, PMID 6392811
- ↑ 김주영; 스포츠둥지 기자단 (2011년 9월 2일). “근육안에 자고있는 위성세포를 깨우자.”. 《국민체육진흥공단》. 2019년 10월 23일에 원본 문서에서 보존된 문서. 2019년 10월 23일에 확인함.
- ↑ Hawke T (2005년 4월), “Muscle Stem Cells and Exercise Training”, 《Exercise and Sport Sciences Reviews》 33 (2): 63-68, PMID 15821426
- ↑ McKay BR, 외. (2009년 6월), “Association of Interleukin-6 Signalling with the Muscle Stem Cell Response Following Muscle-Lengthening Contractions in Humans”, 《PLoS One》 4 (6): e6027, doi:10.1371/journal.pone.0006027, PMC 2696599, PMID 19554087, 2019년 10월 24일에 확인함
- ↑ D'Souza RF, 외. (2017), “MicroRNAs in Muscle: Characterizing the Powerlifter Phenotype”, 《Frontiers in Physiology》 8: 383, doi:10.3389/fphys.2017.00383, PMC 5461344, PMID 28638346, 2019년 10월 24일에 확인함
- ↑ Louis E, 외. (2007년 11월), “Time course of proteolytic, cytokine, and myostatin gene expression after acute exercise in human skeletal muscle”, 《Journal of Applied Physiology》 103 (5): 1744-1751, doi:10.1152/japplphysiol.00679.2007, PMID 17823296
- ↑ Pedersen BK, 외. (2007년 9월), “Role of myokines in exercise and metabolism”, 《Journal of Applied Physiology》 103 (3): 1093-1098, doi:10.1152/japplphysiol.00080.2007, PMID 17347387
- ↑ Toth MJ, 외. (2005년 5월), “Age-related differences in skeletal muscle protein synthesis: relation to markers of immune activation”, 《American Journal of Physiology-Endocrinology and Metabolism》 288 (5): E883–E891, doi:10.1152/ajpendo.00353.2004, PMID 15613683
- ↑ Visser M, 외. (2002년 5월), “Relationship of Interleukin-6 and Tumor Necrosis Factor-α With Muscle Mass and Muscle Strength in Elderly Men and Women: The Health ABC Study”, 《The Journals of Gerontology: Series A》 57 (5): M326–M332, doi:10.1093/gerona/57.5.M326, PMID 11983728
- ↑ Schiaffino S, Mammucari C (2011), “Regulation of skeletal muscle growth by the IGF1-Akt/PKB pathway: insights from genetic models”, 《Skeletal Muscle》 1 (1): 4, doi:10.1186/2044-5040-1-4, PMC 3143906, PMID 21798082, 2019년 10월 27일에 확인함
- ↑ Mee-Sup Y (2011), “mTOR as a Key Regulator in Maintaining Skeletal Muscle Mass”, 《Frontiers in Physiology》 8: 788, doi:10.3389/fphys.2017.00788, PMC 5650960, PMID 29089899, 2019년 10월 27일에 확인함
- ↑ 가 나 Lang CH, Frost RA (2007년 1월), “Sepsis-induced suppression of skeletal muscle translation initiation mediated by tumor necrosis factor alpha”, 《Metabolism》 56 (1): 49–57, doi:10.1016/j.metabol.2006.08.025, PMID 17161226
- ↑ Lang CH, Hong-Brown L, Frost RA (2005년 3월), “Cytokine inhibition of JAK-STAT signaling: a new mechanism of growth hormone resistance”, 《Pediatric Nephrology》 20 (3): 306–312, doi:10.1007/s00467-004-1607-9, PMID 15549417
- ↑ Henselmans M, “Inflammation: the major regulator of muscle growth nobody talks about”, 《mennohenselmans.com》, 2019년 10월 28일에 원본 문서에서 보존된 문서, 2019년 10월 28일에 확인함
- ↑ 가 나 다 Broz P, Dixit VM (2016년 7월), “Inflammasomes: mechanism of assembly, regulation and signalling”, 《Nature Reviews Immunology》 16 (7): 407–420, doi:10.1038/nri.2016.58, PMID 27291964
- ↑ Tang D, 외. (2012년 9월), “PAMPs and DAMPs: Signal 0s that Spur Autophagy and Immunity”, 《Immunological Reviews》 249 (1): 158–175, doi:10.1111/j.1600-065X.2012.01146.x, PMC 3662247, PMID 22889221, 2019년 11월 1일에 확인함
- ↑ Franchi L, 외. (2009년 3월), “The Inflammasome: A Caspase-1 Activation Platform Regulating Immune Responses and Disease Pathogenesis”, 《Nature Immunology》 10 (3): 241, doi:10.1038/ni.1703, PMC 2820724, PMID 19221555, 2019년 11월 1일에 확인함
- ↑ 민경우 (2019년 6월 18일). “세포사멸의 분자 기전들: 세포사멸 명칭위원회의 제안”. 《BRIC》. 2019년 11월 1일에 확인함.
- ↑ Boxberger N, Hecker M, Zettl UK (2019년 4월 15일), “Dysregulation of Inflammasome Priming and Activation by MicroRNAs in Human Immune-Mediated Diseases”, 《The Journal of Immunology》 202 (8): 2177-2187, doi:10.4049/jimmunol.1801416, PMID 30962309
- ↑ Barnes PJ (2006년 6월), “How corticosteroids control inflammation: Quintiles Prize Lecture 2005”, 《British Journal of Pharmacology》 148 (3): 245–254, doi:10.1038/sj.bjp.0706736, PMC 1751559, PMID 16604091, 2019년 11월 1일에 확인함
- ↑ Payne DN, Adcock IM (2001년 6월), “Molecular mechanisms of corticosteroid actions”, 《Paediatric Respiratory Reviews》 2 (2): 145–150, doi:10.1053/prrv.2000.0122, PMID 12531061
- ↑ Barnes PJ, Adcock IM (2003년 9월 2일), “How do corticosteroids work in asthma”, 《Annals of Internal Medicine》 139 (5 Pt 1): 359–370, doi:10.7326/0003-4819-139-5_part_1-200309020-00012, PMID 12965945
- ↑ 송영준, 하철원 (2009년 6월), “골관절염의 치료에서 COX-2 선택적 비스테로이드성 소염진통제의 이용”, 《대한슬관절학회지》 21 (2): 84–92, 2019년 11월 1일에 확인함
- ↑ Dinarello CA (2010년 3월 19일), “Anti-inflammatory Agents: Present and Future”, 《Cell》 140 (6): 935–950, doi:10.1016/j.cell.2010.02.043, PMC 3752337, PMID 20303881, 2019년 11월 1일에 확인함
- ↑ Malottki K, 외. (2011), 〈Adalimumab, etanercept, infliximab, rituximab and abatacept for the treatment of rheumatoid arthritis after the failure of a tumour necrosis factor inhibitor: a systematic review and economic evaluation〉, 《NIHR Health Technology Assessment programme: Executive Summaries》, Southampton (UK): NIHR Journals Library, 2019년 11월 1일에 확인함
- ↑ Jain MK, Ridker PM (2005년 12월), “Anti-Inflammatory Effects of Statins: Clinical Evidence and Basic Mechanisms”, 《Nature Reviews Drug Discovery》 4 (12): 977–987, doi:10.1038/nrd1901, PMID 16341063
- ↑ 가 나 WebMD Medical Reference (2018). “Vitamins That Fight Inflammation”. 《WebMD》. 2019년 11월 1일에 확인함.
- ↑ Wiedermann U, 외. (1996년 11월), “Vitamin A deficiency increases inflammatory responses”, 《Scandinavian Journal of Immunology》 44 (6): 578-584, doi:10.1046/j.1365-3083.1996.d01-351.x, PMID 8972739
- ↑ Ellulu MS, 외. (2004년 3월 15일), “Effect of vitamin C on inflammation and metabolic markers in hypertensive and/or diabetic obese adults: a randomized controlled trial”, 《Drug Design, Development and Therapy》 9: 3405–3412, doi:10.2147/DDDT.S83144, PMC 4492638, PMID 26170625, 2019년 11월 1일에 확인함
- ↑ Hargrave BY, 외. (2003년 6월), “Cocaine, not morphine, causes the generation of reactive oxygen species and activation of NF-kappaB in transiently cotransfected heart cell”, 《Cardiovascular Toxicology》 3 (2): 141–151, doi:10.1385/CT:3:2:141, PMID 14501032
- ↑ Montiel-Duarte C, 외. (2004년 3월 15일), “Role of reactive oxygen species, glutathione and NF-κB in apoptosis induced by 3,4-methylenedioxymethamphetamine (“Ecstasy”) on hepatic stellate cells”, 《Biochemical Pharmacology》 67 (6): 1025–1033, doi:10.1016/j.bcp.2003.10.020, PMID 15006539
- ↑ Bascones-Martinez A, 외. (2014년 1월), “Immunomodulatory drugs: Oral and systemic adverse effects”, 《Medicina Oral Patologia Oral y Cirugia Bucal》 19 (1): e24–e31, doi:10.4317/medoral.19087, PMC 3909428, PMID 23986016, 2019년 11월 2일에 확인함
- ↑ Sanmamed MF, Chen L (2014년 1월), “A Paradigm Shift in Cancer Immunotherapy: From Enhancement to Normalization”, 《Cell》 19 (1): 313–326, doi:10.1016/j.cell.2018.09.035, PMC 6538253, PMID 30290139, 2019년 11월 2일에 확인함
- ↑ Nakamura K, Smyth MJ (2017년 4월), “Targeting cancer‐related inflammation in the era of immunotherapy”, 《Immunology & Cell Biology》 95 (4): 325-332, doi:10.1038/icb.2016.126, PMID 27999432
- ↑ Gajewski TF, 외. (2017), “Cancer Immunotherapy Targets Based on Understanding the T Cell-Inflamed Versus Non-T Cell-Inflamed Tumor Microenvironment”, 《Advances in Experimental Medicine and Biology》 1036: 19–31, doi:10.1007/978-3-319-67577-0_2, PMC 6693322, PMID 29275462, 2019년 11월 2일에 확인함
- ↑ Zhong J, Shi G (2019년 4월 12일), “Editorial: Regulation of Inflammation in Chronic Disease”, 《Frontiers in Immunology》 10: 737, doi:10.3389/fimmu.2019.00737, PMC 6473051, PMID 31031750, 2019년 11월 3일에 확인함
- ↑ “Immunotherapies for autoimmune diseases”, 《Nature Biomedical Engineering》 3: 247, 2019, doi:10.1007/978-3-319-67577-0_2, 2019년 11월 2일에 확인함
- ↑ Jutel M (2014), “Allergen-Specific Immunotherapy in Asthma”, 《Current Treatment Options in Allergy》 1 (2): 213–219, doi:10.1007/s40521-014-0013-1, PMC 4032467, PMID 24900950, 2019년 11월 2일에 확인함
- ↑ Bucktrout SL, Bluestone JA, Ramsdell F (2018), “Recent advances in immunotherapies: from infection and autoimmunity, to cancer, and back again”, 《Genome Medicine》 10: 79, doi:10.1186/s13073-018-0588-4, PMC 6208073, PMID 30376867, 2019년 11월 2일에 확인함
- ↑ 김경록 (2016년 5월 3일). “면역조절 기능성 식품의 구조 및 작용”. 《BRIC》. 2019년 11월 1일에 확인함.
- ↑ Huaux F (2018년 11월 19일), “Emerging Role of Immunosuppression in Diseases Induced by Micro- and Nano-Particles: Time to Revisit the Exclusive Inflammatory Scenario”, 《Frontiers in Immunology》 9: 2364, doi:10.3389/fimmu.2018.02364, PMC 6252316, PMID 30510551, 2019년 11월 3일에 확인함
- ↑ Ashley NT, Weil ZM, Nelson RJ (2012), “Inflammation: Mechanisms, Costs, and Natural Variation”, 《Annual Review of Ecology, Evolution, and Systematics》 43: 385–406, doi:10.1146/annurev-ecolsys-040212-092530
- ↑ 가 나 Iqbal AJ, Fisher EA, Greaves DR (2016년 10월), “Inflammation – a critical appreciation of the role of myeloid cells”, 《Microbiology Spectrum》 4 (5), doi:10.1128/microbiolspec.MCHD-0027-2016, PMC 5119645, PMID 27780018, 2019년 10월 31일에 확인함
- ↑ Flajnik MF, Du Pasquier L (2004년 12월), “Evolution of innate and adaptive immunity: can we draw a line?”, 《Annual Review of Ecology, Evolution, and Systematics》 25 (12): 640–644, doi:10.1016/j.it.2004.10.001, PMID 15530832
- ↑ Boehm T (2012년 9월 11일), “Evolution of Vertebrate Immunity”, 《Current Biology》 22 (17): R722–R732, doi:10.1016/j.cub.2012.07.003, PMID 22975003
- ↑ 《글로벌세계대백과사전》, 도서출판 범한, 2004, ISBN 89-8048-325-2, 2019년 10월 31일에 확인함
- ↑ Melillo D, 외. (2018년 8월 22일), “Innate Immune Memory in Invertebrate Metazoans: A Critical Appraisal”, 《Frontiers in Immunology》 9: 1915, doi:10.3389/fimmu.2018.01915, PMC 6113390, PMID 30186286, 2019년 10월 31일에 확인함
- ↑ 이인희 (2000). “곤충의 생체방어체제에서의 Prophenoloxidase Activating System의 역할”. 《BRIC》. 2019년 10월 31일에 확인함.
- ↑ Nyholm SV, Graf J (2012년 12월), “Knowing your friends: invertebrate innate immunity fosters beneficial bacterial symbioses”, 《Nature Reviews Microbiology》 10 (12), doi:10.1038/nrmicro2894, PMC 3870473, PMID 23147708, 2019년 10월 31일에 확인함
- ↑ Loof TG, 외. (2011), “Coagulation Systems of Invertebrates and Vertebrates and Their Roles in Innate Immunity: The Same Side of Two Coins?”, 《Journal of Innate Immunity》 3: 34–40, doi:10.1159/000321641, PMID 21051879
- ↑ Tascedda F, Ottaviani E (2014), “Tumors in invertebrates”, 《Invertebrate Survival Journal》 11 (1): 197-203, 2019년 10월 31일에 확인함
- ↑ De Vico G, Carella F (2015), “Tumors in invertebrates: molluscs as an emerging animal model for human cancer”, 《Invertebrate Survival Journal》 12 (1): 19-21, 2019년 10월 31일에 확인함
- ↑ Robert J (2010년 9월), “Comparative study of tumorigenesis and tumor immunity in invertebrates and nonmammalian vertebrates”, 《Developmental & Comparative Immunology》 34 (9): 915–925, doi:10.1016/j.dci.2010.05.011, PMC 2900388, PMID 20553753, 2019년 10월 31일에 확인함
- ↑ 가 나 Wilson-Sanders SE (2011), “Invertebrate Models for Biomedical Research, Testing, and Education”, 《ILAR Journal》 52 (2): 126–152, doi:10.1093/ilar.52.2.126, PMID 21709307
- ↑ Zimmerman LM, Bowden RM, Vogel LA (2014년 10월), “A vertebrate cytokine primer for eco‐immunologists”, 《Functional Ecology》 28 (5): 1061–1073, doi:10.1111/1365-2435.12273
- ↑ Doolittle RF (2011), “Coagulation in Vertebrates with a Focus on Evolution and Inflammation”, 《Journal of Innate Immunity》 3: 9–16, doi:10.1159/000321005, PMID 20980726
- ↑ Richardson RJ (2018), “Parallels between vertebrate cardiac and cutaneous wound healing and regeneration”, 《npj Regenerative Medicine》 3: 21, doi:10.1038/s41536-018-0059-y, PMC 6220283, PMID 30416753, 2019년 11월 1일에 확인함
- ↑ Webb DR (2014년 1월), “Animal models of human disease: Inflammation”, 《Biochemical Pharmacology》 87 (1): 121–130, doi:10.1016/j.bcp.2013.06.014, PMID 23811309
- ↑ Ward JM, 외. (2016년 3월), “Why Animals Die: An Introduction to the Pathology of Aging”, 《Veterinary Pathology》 53 (2): 229–232, doi:10.1177/0300985815612151, PMID 26936750
- ↑ Bellows J, 외. (2015년 1월), “Defining healthy aging in older dogs and differentiating healthy aging from disease”, 《Journal of the American Veterinary Medical Association》 246 (1): 77–89, doi:10.2460/javma.246.1.77, PMID 25517329
- ↑ Panko, Ben (2017년 8월 17일). “What a 6,000-Year-Old Knee Can Teach Us About Arthritis”. 《Smithsonian.com》. 2019년 5월 13일에 원본 문서에서 보존된 문서. 2019년 10월 11일에 확인함.
- ↑ Rocha e Silva M (1978), 〈A Brief History of Inflammation〉, 《Inflammation. Handbook of Experimental Pharmacology (Continuation of Handbuch der experimentellen Pharmakologie)》 50판, Berlin, Heidelberg: Springer, doi:10.1007/978-3-642-66888-3_2, ISBN 978-3-642-66890-6
- ↑ 신창우 (2017년 4월 6일). “자극과 항상성 함께 봐야 염증 해소 가능”. 《한국의약통신》. 2019년 10월 11일에 확인함.
- ↑ 가 나 다 라 D Neil G, Senchenkova E (2010), 〈Chapter 2. Historical Perspectives〉, 《Inflammation and the Microcirculation》, Morgan & Claypool Life Sciences, ISBN 9781615041657, 2019년 10월 11일에 확인함
- ↑ Scott A, 외. (2004년 6월), “What is “inflammation”? Are we ready to move beyond Celsus?”, 《British Journal of Sports Medicine》 38 (3): 248–249, doi:10.1136/bjsm.2003.011221, PMC 1724817, PMID 15155418, 2019년 10월 11일에 확인함
- ↑ 가 나 다 Rocha e Silva M (1978년 1월), “A brief survey of the history of inflammation”, 《Agents Actions》 8 (1-2): 45-49, doi:10.1007/bf01972401, PMID 76437
- ↑ Rocha e Silva M, Leme JG (1972), 〈Chapter 1. Natural History of the Inflammatory Reaction〉, 《Chemical Mediators of the Acute Inflammatory Reaction》, Pergamon, doi:10.1016/C2013-0-02523-6, ISBN 978-0-08-017040-4
- ↑ 가 나 Cavaillon JM, Singer M, 편집. (2017년 10월), 〈Chapter 1. Inflammation through the Ages: A Historical Perspective〉, 《Inflammation: From Molecular and Cellular Mechanisms to the Clinic》, Wiley‐VCH Verlag GmbH & Co. KGaA., doi:10.1002/9783527692156, ISBN 9783527692156