G 단백질 연결 수용체
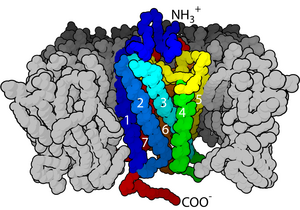
G 단백질 연결 수용체(G protein coupled receptor, GPCR)는 7-막관통 수용체(7-Transmembrane receptor, 7TMR)라고도 불린다. 이름에서 알 수 있듯이 [그림 1]에서 살펴보면 이것의 구조는 세포막 혹은 세포 내의 기관의 세포막에서 세포질 면과 세포 외면에 걸쳐있고 막을 7번 통과하는 구조이다. 생체내에서 800~1000개 정도의 수용체의 종류가 존재 하고, 사실상 생체내의 거의 모든 생리적 반응을 촉매한다 이것의 종류는 크게 5 가지로 나뉘며 (type A, B, C, D, E, F), type A에는 빛을 감지하는 로돕신, 냄새를 감지하는 후감각 수용체, 아드레날린 혹은 노르아드레날린을 감지하는 아드레날린 수용체가 있다. Type B에는 펩티드 수용체가 존재하며, Type C에는 글루타메이트 수용체 그리고 미감각 수용체가 존재한다고 알려져 있다. 이때 수용체에 붙는 물질을 리간드라고 정의하며 리간드는 수용체의 반응을 촉진하는 수용체 작용제와 반응을 촉진하지 않는 수용체 대항제로 나뉘게 된다.
신호전달[편집]

G-단백질 매개 신호 전달[편집]
GPCR의 신호전달체계는 수 십년 동안 많은 연구의 결과로 일반적으로 밝혀져 있다. [그림 2]에서 그러한 전달체계를 간략히 소개하고자 한다. 리간드 혹은 수용체 작용제가 수용체에 결합 하게 되면 수용체는 구조가 바뀌게 된다. 구조가 바뀐 수용체는 G-단백질과 연결되고 이러한 접촉에 의해 G-단백질은 Gα 와 Gβ-Gγ 이중체 구조로 나뉜다. 각기 나뉜 물질은 세포 혹은 기관내의 2차 메신저의 반응을 촉매하고 그러한 연쇄적인 반응에 의해 다양한 세포 반응이 일어나게 된다.
β-어레스틴(arrestin) 매개 신호 전달[편집]
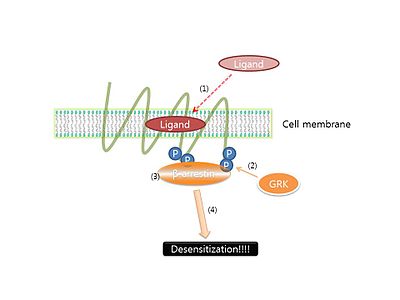
그러나 거의 모든 GPCR 반응에서는 리간드가 반응을 지속적으로 하게 되어 일정한 시간이 지나게 되면 반응의 결과물이 오히려 줄어든다는 결론이 많은 논문에서 밝혀졌다. 이것을 세포내 일종의 항상성을 유지하기 위한 기작으로서, GPCR의 경우 이것을 Desensitization이라 불린다. 이러한 Desensitization은 GPCR이 단백질 키나아제 protein kinase GRK에 의해 인산화되어 일어난다고 알려져있다. 인산화된 GPCR은 β-arrestin과 결합하게 되고, 결합된 β-arrestin이 GPCR이 G-단백질과 접촉하는 것을 방해하여 신호전달이 일어나지 않게 되는 것이다. 그렇기에 β-arrestin에 의한 새로운 신호전달체계는 다음 [그림 3]과 같다. β-arrestin은 desensitization 신호전달체계외에 식작용(혹은 internalization)과 그것 자체의 신호전달체계가 있다고 많은 논문에서 밝혀졌다. 간략히 살펴보면 식작용이 일어나는 기작은 먼저 수용체에 결합된 β-arrestin이 유비퀴티네이트가 되고 그 후에 β-arrestin에 GO 단백질과 같은 중매제가 결합하게 된다. 결합한 GO 단백질은 여러 모터단백질과 접촉하게 되어 리간드, 수용체, 막의 응집을 촉진한다. 이런 기작으로 형성된 버블은 세포내 수용체 혹은 리간드가 필요한 곳으로 이동하거나 리소좀에 의해 분해된다. 그리고 β-arrestin의 신호전달체계는 최근에 많은 논문에서 밝혀졌지만 아직까지 많은 기작이 밝혀지지 않았기에 연구가 현재진행형이라고 알려져 있다.
G-단백질의 구조[편집]
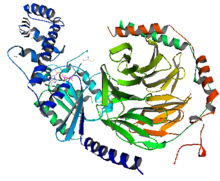

왼쪽의 그림과 같이 G-protein은 Gα와 Gβγ로 이루어져있다. Gα는 파란색으로 표시되어 있고,Gβγ는 빨간색과 녹색으로 표시되어 있다. Gβγ는 이량체를 이루고 있으며,Gα는 GαsAH와 GαsRas로 이루어져있다. 비활성화 상태에서는 Gα는 GDP와 Gβγ에 단단히 결합되어 있다. 수용체에 리간드(ligand)가 결합하게 되면 활성화상태로 바뀌면서 GPCR과 G-protein의 구조가 바뀌게 된다. GαsRas가 GTP 가수분해에 필요한 촉매역할의 residue를 포함하고 있으며 또한 effector protein과 Gβγ의 결합부위도 가지고 있다. GαsAH는 뉴클레오티드(nucleotide) 방출에서 조개껍집과 같이 열리는 역할을 한다. G-protein이 활성화 될 때 구조적인 변화를 좀 더 구체적으로 분석하기 위해서 결정구조(Crystal structure)가 제시하는 정적인 통찰과 함께 DXMS(peptide amide hydrogen-deuterium exchange mass spectrometry)라는 분석법을 이용하였고, 이러한 보안을 통해서 좀 더 역동적인 통찰을 제시할 수 있었다. 기존의 결정구조(Crystal structure)에서 알고 있던 사실 뿐만 아니라 결정구조가 밝혀낼 수 없었던 것까지 밝혀낼 수 있었다.
DXMS분석법 이용[편집]
G단백질이 이질삼합체를 이루고 있을 시에 비해 Gα와 수용체가 복합체를 이루고 있을 때를 비교했을 때(그림5,a) , Gα 단위체에서 α5-helix의 카복시말단(C-terminus)은 감소된 수소-중수소 교환을 보였다. 이를 통해 α5-helix가 복합체를 이룰 시에 수용체를 관통한다는 것을 알았다. 또한 α5-helix의 아미노말단은 증가된 교환을 보였다. 이는 α5-helix의 아미노말단이 뉴클레오티드 결합부분에 관여하고 있기 때문인데, 복합체를 이루면서 GDP가 떨어져나가기 때문에 뉴클레오티드 결합 지역은 열리게 되고 그러므로 수소-중수소 교환은 증가하게 되는 것이다. 복합체를 이루었을 때와 GDP+AlF3를 첨가했을 때를 비교하는 경우(그림5,b)에서 GDP+AlF3는 G단백질과 결합했을 때, GTP와 구조적으로 기능적으로 거의 같은 역할을 한다. GTP가 결합된 G단백질은 수용체와 Gβγ 단위체으로부터 떨어지게 된다. 그러므로 Gα의 α5-helix는 노출이 되게 되고 수소-중수소 교환은 증가하게 된다. 당연히 GDP+Al3의 결합으로 인해 뉴클레오티드 결합 부분은 닫히게 되고, 그에 따라 α5-helix의 아미노말단은 수소-중수소 교환이 감소하게 되는 것이다. GDP를 첨가했을 시에는 GDP+AlF3를 첨가했을 때와 거의 유사한 양상을 보였다(그림5,c). 하지만 GDP+AlF3을 첨가했을 때 만큼의 비율만큼 변화된 양상은 보이지 않았다. 이러한 결과는 GDP가 결합된 G단백질의 α5-helix가 수용체와 약하게 결합하고 있다는 것을 암시한다.
DXMS분석이 밝혀낸 가장 두드러진 부분은 바로 β1-strand의 구조적인 변화이다. β1-strand은 ICL2와 GDP의 β-phosphate를 조정하는 P-loop를 연결한다. 이 β1-strand의 부분은 결정구조에서는 작은 변화를 보여주기 때문에, GDP방출을 위해 필요한 구조적인 변화를 잘 반영하지 못했다. 하지만 DXMS분석법에서는 P-loop,α1,β1,그리고 α5의 아미노말단은 GDP방출시 수소-중수소의 높은 교환비율을 보였다. 결과적으로 DXMS의 연구는 β1-P-loop-α1 구역이 amide backbone 수소결합을 변경시키는 구조적인 변화를 겪는다는 것을 알아냈다. 이를 통해서 이들 지역이 뉴클레오티드 결합에 관여하고 있다는 것을 알게 된 것이다.
또한 DXMS 분석을 통해 뉴클레오티드 결합과 관련하여 GαsAH와 GαsRas(G단백질GαsAH와 GαsRas로 구성되어 있다)는 조개껍질같은 구조적인 변화를 겪는다는 것을 알아냈다. 뉴클레오티드가 없을 시에 이러한 조개껍질같은 열림이 일어나는데, 이때 GαsAH가 그 자체로는 접힘과 구조가 거의 그대로이며 위치적으로만 재배열이 일어나는 것을 알아냈다.
결론적으로 DXMS 분석법은 결정구조의 정적인 통찰을 보충하여 좀 더 자세하고 역동적인 통찰을 제시하였다. 이를 통해 G-단백질의 구조가 더 구체화되었다.
의학적 가치[편집]
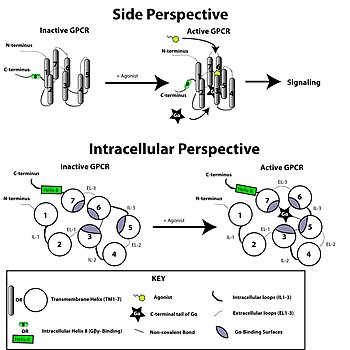
의학적 가치에서는 이전에 살펴본 신호 전달 체계 및 구조적인 관점을 통해 GPCR을 목적지로 하는 약 개발 가능성을 모색해보자 한다. 앞에서의 신호전달체계와 구조분석에서 말했듯이, GPCR은 외부에 존재하는 리간드에 담겨 있는 신호를 받아들여서 세포 내의 반응을 유도하여 리간드에 특정 반응을 유도한다. 이는 곧 구조적인 관점에서 보았을 때 리간드가 GPCR의 특정 구조적인 변화를 유도하여 G-단백질이 세포내의 위치에서 더 잘 결합하도록 도와주거나, GRK를 통해 GPCR의 C-말단을 인산화시켜 β-arrestin-중재 신호전달체계를 유도시킨다.(혹은 β-arrestin은 GPCR의 구조적인 변화가 나타났을 때 GRK를 거치지 않더라도 직접 GPCR과 상호작용을 가져 세포 내의 신호전달, desensitization, 식작용 등의 반응을 유도할 수 있다.) 즉, 세포 내의 변화를 일으키는 리간드 혹은 agonist는 특정 신호전달체계만을 활성화시키는, “biased agonist”의 특성을 가진다. 어떤 논문에서는 이 특성을 “efficacy is pluridimensional rather than linear”라 정리하기도 한다.
리간드는 친화력(리간드와 수용체간의 상호 작용의 세기)와 내부적 효험 (수용체에 결합한 리간드가 얼마나 반응을 잘 유도할 수 있는가)의 특성에 따라서 크게 4개의 종류로 나눌 수 있다.(full agonist, partial agonist, neutral agonist, inverse agonist) full agonist와 partial agonist는 GPCR의 활성화된 형태를 안정화시키며, inverse agonist, 즉 antagonist는 비활성화된 형태를 안정화시킨다. 특히 GPCR에 특정한 결합을 하는 약을 개발하는 데에 있어서 후보 약물이 어느 그룹에 속하는지 실험적으로 확인하는 것은 매우 중요한 과정이다. 어느 실험실에서는 각각의 리간드 족이 GPCR에 결합하였을 때 생기는 구조적인 차이, 그 중에서도 ECL 2/3간의 염다리 연결의 세기에 차이가 난다는 것에 착안하여 Lys305와 Asp192 간의 상호작용을 마커로 사용하여 동위원소 표시를 통해 Lys305 최고점의 위치를 파악하여 리간드의 특성을 파악하는 연구가 진행되었다.
최근에는 위의 신호전달체계를 이용한 분석뿐만이 아니라 구조기반적인 약 개발 기법 또한 많이 이용되고 있다. 구조를 기반으로 한 약의 탐색은 후보 중에서의 최적화 및 새로운 약을 찾을 수 있다. 이의 대표적인 예가 바로 In silico docking method이다. 이 기법은 full agonist와 partial agonist가 활성화 된 형태를 안정화시키고 antagonist가 비활성화된 형태를 안정화시킨다는 것에 착안하여 리간드에 결합한 GPCR을 정제하는 방법이다. 물론, 이 방법은 아직 한계점을 가지고 있다. 우선 리간드를 통해 GPCR을 정제해내는 데에 있어서 GPCR과 약한 상호작용을 하는 리간드를 이용할 수는 없다. 또한 앞에서도 살펴보았듯이 G-단백질의 결합, 리간드와 GPCR의 종류 등에 따라서 구조의 다양성을 가진다는 점에서 In silico docking은 한계점을 지니고 있다. 따라서 GPCR을 표적으로 하는 약을 개발할 때에는 단순히 결합만 생각할 뿐만이 아니라 GPCR의 역동적인 특성 이해하여야 할 것이다.
같이 보기[편집]
참고 자료[편집]
- “The Nobel Prize in Chemistry 2012” (PDF). 2012년 10월 10일에 확인함.
- “A phylogenetic tree of all human GPCRs” (PDF). 2008년 8월 11일에 확인함.
- Vassilatis DK; Hohmann JG; Zeng H; Li F; Ranchalis JE; Mortrud MT; Brown A; Rodriguez SS; Weller JR; Wright AC; Bergmann JE; Gaitanaris GA (2003). “The G protein-coupled receptor repertoires of human and mouse”. 《Proc Natl Acad Sci USA》 100 (8): 4903–8. doi:10.1073/pnas.0230374100. PMC 153653. PMID 12679517.
- “GPCR Reference Library”. 2008년 8월 11일에 확인함.
Reference for molecular and mathematical models for the initial receptor response
- GPCR structures in the Protein Data Bank
외부 링크[편집]
- 의학주제표목 (MeSH)의 G-protein-coupled+receptors
- en:MeSH D12.776#MeSH D12.776.543.750.100 --- receptors.2C g-protein-coupled
- “GPCR Database”. 《IUPHAR Database》. International Union of Basic and Clinical Pharmacology. 2008년 9월 15일에 원본 문서에서 보존된 문서. 2008년 8월 11일에 확인함.
- Vriend G; Horn F (2006년 6월 29일). “GPCRDB: Information system for G protein-coupled receptors (GPCRs)”. Molecular Class-Specific Information System (MCSIS) project. 2019년 4월 25일에 원본 문서에서 보존된 문서. 2008년 8월 11일에 확인함.
- “G Protein-Coupled Receptors on the NET”. 2010년 11월 10일에 확인함.
a classification of GPCRs
- “PSI GPCR Network Center”. 2013년 7월 25일에 원본 문서에서 보존된 문서. 2013년 7월 11일에 확인함.
a Protein Structure Initiative:Biology Network Center aimed at determining the 3D structures of representative GPCR family proteins
- GLASS: A comprehensive database for experimentally-validated GPCR-ligand associations
