삼투
이 문서는 참고 문헌 목록을 포함하고 있으나, 각주가 불충분하거나 존재하지 않아 출처가 모호합니다. |
삼투(滲透, 문화어: 스밈압력, 프랑스어, 독일어: Osmose, 영어, 라틴어, 스페인어: Osmosis) 또는 삼투현상이란 묽은 용액과 진한 용액이 반투막을 사이에 두고 있을 때, 용질은 상대적으로 입자의 크기가 크기 때문에 반투막을 통과할 수 없게 되는데 이 때 농도가 더 진한 쪽으로 용질 대신 용매(일반적 물)가 이동하는 현상이다. 이때 발생하는 압력의 크기를 삼투압이라고 한다. 수동운반(passive transport).
삼투압 공식[편집]
π(삼투압)=MRTip_e^2
{M: 용액의 몰농도(mol/L), R:기체 상수(0.0821 L·atm/mol·K), T:절대 온도(K), i:반트호프 인자(수용액이 전해질인 경우에 필요, i>1이며 값은 물질의 종류와 농도에 따라 다르다.)}
J. H. 반트호프는 삼투압의 원인은 용액 속에 녹아 있는 물질의 분자가 기체분자와 같은 법칙으로 운동하여 반투막에 압력을 미치기 때문이라 생각하고, 이 현상을 이론적으로 설명하였다. 즉, 삼투압을 P 기압, 용질 n mol을 용해하는 용액의 부피를 VL, 용액의 절대온도를 T, 기체상수를 R이라 하면, 용액의 농도가 그다지 크지 않은 범위에서 PV = nRT라는 식이 성립된다.
따라서 P=nRT/V라는 식이 성립되는데, 이때 P= π이고, n/V=M 이라 π(삼투압)=MRT 다음과 같은 간단한 식으로 나타낼 수 있다.
예시 문제) 25°C 바닷물의 평균 삼투압은 30.0 atm이다. 바닷물과 등장액인 설탕 수용액의 몰농도를 계산하시오.
π=MRTi
M= π/RTi = 30.0 atm/(0.0821 L·atm/mol·K)(298K)(1) <비전해질인 설탕의 경우 i=1>
= 1.23mol/L
= 1.23M
삼투압에 의한 현상의 예인체 내의 삼투 현상 : 체액의 삼투압은 체액의 농도에 비례하며 체액을 구성하는 수분과 무기 염류량에 의해 결정된다.[편집]
1. 체내 수분량 조절(체내의 삼투압이 변하면 콩팥(신장)에서 수분의 흡수를 조절)
삼투압 변화를 조절하는 중추는 간뇌의 시상 하부로, 뇌하수체 후엽에서 분비되는 항이뇨 호르몬(ADH)에 의해 조절된다
<항이뇨 호르몬>
- 뇌하수체 후엽에서 분비되는 호르몬으로 팥의 집합관에서 수분의 재흡수를 촉진한다.
- 혈관을 수축시켜 혈압을 상승시키는 역할도 하므로 바소프레신이라고도 한다
<혈장 삼투압>
체내에 흐르는 피의 양, 즉 혈류량과 혈압 역시 일정하게 유지되어야 한다. 하지만 체내의 수분은 상시 변할 수 밖에 없고 그로 인해 혈류량이 변하여 혈압 역시 변하게 된다. 체내는 이런 변화를 삼투압을 통해 일정하게 유지시킨다.
만약 체내의 수분이 많아지면 수분의 증가로 혈류량이 증가한다. 혈류량이 증가하면 당연히 혈압 역시 증가하기에 뇌의 항상성을 담당흡수량을 증가시켜 수분량은 증가하고, 소변량은 감소한다.
-수분이 과다할 때(삼투압 하강)
시상 하부에서 조절을 받아 뇌하수체 후엽에서 ADH 분비가 감소하여 물의 재흡수가 억제되어 수분은 감소하고 소변량은 증가한다.
2. 체내 무기 염류량 조절
무기 염류의 농도는 수분의 이동과 삼투압에 큰 영향을 미친다. 혈중 K+의 농도가 높거나 Na+의 농도가 낮을 때는 뇌하수체 전엽에서 부신 겉질 자극 호르몬(ACTH)의 분비량이 증가하여 부신 겉질에서 알도스테론의 분비가 촉진되고, 이에 따라 콩팥의 세뇨관과 집합관에서 K+의 분비와 Na+의 재흡수량이 증가하여 혈액 속의 Na+의 농도가 높아진다. 또한 비타민, 미네랄의 부족은 세포에 필요한 단백질의 합성이 제대로 되지 않는다. 그리고 단백질의 부족은 세포의 삼투압에도 영향을 미치게 된다. 세포는 삼투압을 유지해야 세포의 크기를 유지할 수 있다. 만약 세포내에 단백질이 부족하게 되면 세포내의 음이온이 부족하게 된다. 세포내 부족한 음이온은 삼투압에 의해 세포외액에 있는 대표적인 음이온인 염소가 세포내로 들어오게 된다.(세포내 물질의 합이 일정해야 세포의 크기를 유지하게 된다.) 염소의 증가는 세포내의 나트륨의 증가를 가져오고 세포내에 나트륨이 증가를 하게 되면 삼투압을 조절에 필수인 Na+/K+ 펌프가 제대로 작동을 하지 못하게 된다. Na+/K+ 펌프가 제대로 작동을 하지 못하면 세포의 전위차에 변화와 물질의 이동에 문제가 발생한다.
3. 삼투압 조절로 세포 모형 일정하게 유지
인체 내의 많은 세포는 물질대사를 하며 세포외액은 세포에 영양의 공급과 노폐물의 배설을 도와준다. 세포에서 대사를 통해서 단백질을 합성하는 순간 세포내의 물질의 농도는 올라간다. 또 음식을 섭취함으로서 세포외액에 염분, 포도당, 아미노산의 농도가 올라간다. 이러한 변화는 삼투압에 변화를 가져오고 인체는 삼투압의 변화에 대응하기 위해서 농도의 차이에 역행하는 Na/K pump를 작동해서 삼투압을 조절을 하여 원래의 삼투압으로 다시 설정한다. 이로 인해 세포는 더 이상 팽창이나 수축을 하지 않고 기존의 세포의 크기를 그대로 유지할 수 있다. (삼투압=흡수력 )
- 삼투압을 활용한 고분자의 분자량 측정
반트호프의 법칙 [van’t Hoff’s law] : 묽은 용액의 삼투압에 관한 법칙.
「이상적인 용액의 삼투압은 일정한 온도에서 용질의 농도에 비례한다」는 W. 페퍼의 실험적 결과에 입각해서 1887년 반트호프가 제출한 법칙이며 용질의 몰농도를 c, 절대 온도를 T, 기체상수를 R라 하면 용액의 삼투압의 크기 π는 다음과 같다.
π = RTc 여기서 R값은 (0.0821L·atm/mol·K)이다.
이 때 용액의 부피를 V, 용액에 포함된 용질의 몰수를 n이라 할 때 c=n/V이므로 위의 관계식은 πV = nRT=wRT/M가 된다. (w : 고분자물질의 질량, M : 분자량) 이 식을 통해 고분자 물질의 분자량 M을 구할 수 있다.
- 배추를 소금에 절여두면 배추의 수분이 밖으로 빠져나간다.
- 오이를 식초에 넣으면 오이에서 수분이 빠져나가면서 피클이 된다.
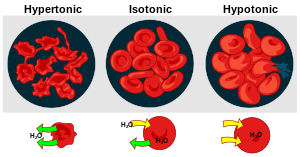
- 적혈구를 고장액(Hypertonic)에 넣으면 적혈구에서 물이 빠져나가 쪼그라든다.
- 적혈구를 저장액(Hypotonic)에 넣으면 바깥에서 적혈구로 물이 들어오면서 세포가 파괴된다. (용혈, hemolysis)
참고 문헌[편집]
- Florian Horn, 《Biochemie des Menschen: Das Lehrbuch für das Medizinstudium》, Auflage 6, Thieme (2012)
- Armin Baur, 《Humanbiologie für Lehramtsstudierende: Ein Arbeits- und Studienbuch》, Springer Spektrum (2015)
- Christa Pews-Hocke, Edeltraud Kemnitz, Annelore Bilsing, Karl-Heinz Firtzlaff, 《Basiswissen Schule - Biologie 5. bis 10. Klasse》, Auflage 5, Bibliographisches Institut (2014)
- Theodord L. Brown,《Chemistry: The Central Science》,10th Ed.,Pearson (2007)
- Carlos Romero Magdalena, Esther Yáñez Conde, Isabel Blasco Castiñeyra, Carlota García-Hoz Jiménez Elena Feduchi Canosa, 《Bioquímica. Conceptos esenciales》, Edición 2, Editorial Médica Panamericana S.A. (2014)
