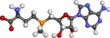
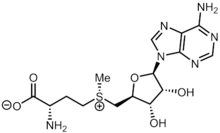
S-아데노실메티오닌
| |||
|
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
(S)-2-amino-4-((SS)-(((2S,3S,4R,5R)-5-(6-amino-9H-purin-9-yl)-3,4-dihydroxytetrahydrofuran-2-yl)methyl)(methyl)sulfonio)butanoate
| |||
| 별칭
S-Adenosyl-L-methionine; SAM-e; SAMe, AdoMet, ademethionine
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.045.391 | ||
| KEGG | |||
| MeSH | S-Adenosylmethionine | ||
PubChem CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C15H22N6O5S | |||
| 몰 질량 | 398.44 g·mol−1 | ||
| 약리학 | |||
| A16AA02 (WHO) | |||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
S-아데노실메티오닌(영어: S-adenosylmethionine)은 메틸기 전이, 황전환 및 아미노프로필화에 관여하는 일반적인 보조 인자이다. 이러한 동화작용은 몸 전체에서 일어나지만, 대부분의 S-아데노실메티오닌은 간에서 생성되고 소비된다.[1] S-아데노실메티오닌으로부터 40가지 이상의 메틸기 전이 반응이 핵산, 단백질, 지질 및 이차 대사산물과 같은 다양한 기질에서 일어나는 것으로 알려져 있다. S-아데노실메티오닌은 메티오닌 아데노실트랜스퍼레이스(EC 2.5.1.6)에 의해 아데노신 삼인산(ATP)과 메티오닌으로부터 생성된다. S-아데노실메티오닌은 1952년에 줄리오 칸토니에 의해 처음 발견되었다.[1]
세균에서 S-아데노실메티오닌은 SAM 리보스위치에 의해 결합되어, 메티오닌 생합성 또는 시스테인 생합성에 관여하는 유전자들을 조절한다. 진핵세포에서 S-아데노실메티오닌은 DNA, tRNA, rRNA의 메틸화, 면역 반응,[2] 아미노산 대사, 황전환 등을 포함한 다양한 과정의 조절 인자로 작용한다. 식물에서 S-아데노실메티오닌은 중요한 식물 호르몬 및 신호전달 분자인 에틸렌의 생합성에 중요하다.[3]
화학적으로, S-아데노실메티오닌은 친전자성 메틸기의 공급원 또는 5'-디옥시아데노실 라디칼의 공급원으로 작용하는 설포늄 베타인이다.
생화학[편집]
S-아데노실메티오닌 회로(활성 메틸 회로)[편집]
 |
S-아데노실메티오닌을 생성, 소비, 재생하는 반응을 S-아데노실메티오닌 회로(활성 메틸 회로)라고 한다. 회로의 첫 번째 단계에서 메티오닌은 메티오닌 아데노실트랜스퍼레이스에 의해 ATP와 반응하여 S-아데노실메티오닌을 생성한다.[4] 두 번째 단계에서 S-아데노실메티오닌을 기질로 사용하는 S-아데노실메티오닌 의존적 메틸트랜스퍼레이스(EC 2.1.1)는 생성물로 S-아데노실호모시스테인을 생성한다.[5] S-아데노실메티오닌은 생물학적 다양성에도 불구하고 거의 모든 S-아데노실메티오닌 의존적 메틸트랜스퍼레이스의 강력한 음성 조절 인자이다. 세 번째 단계에서 S-아데노실호모시스테인은 아데노실호모시스테네이스(EC 3.3.1.1)에 의해 아데노신과 호모시스테인으로 가수분해된다. 네 번째 단계에서 호모시스테인은 메티오닌 생성효소(EC 2.1.1.13)에 의해 5-메틸테트라하이드로폴산으로부터 메틸기를 전달받아 메티오닌을 생성해서 다시 회로를 재순환하게 되어 회로를 완성한다. S-아데노실메티오닌 회로의 속도 제한 단계에서 메틸렌테트라하이드로폴산 환원효소(MTHFR)는 5,10-메틸렌테트라하이드로폴산을 5-메틸테트라하이드로폴산으로 비가역적으로 환원시킨다.[6]
라디칼 S-아데노실메티오닌 효소[편집]
다수의 철-황 클러스터 함유 효소들은 S-아데노실메티오닌을 환원적으로 절단하여 5'-디옥시아데노실 5'-라디칼을 중간생성물로 생성하는 데, 이러한 효소들을 라디칼 S-아데노실메티오닌 효소라고 한다.[7] 이러한 능력을 가지고 있는 대부분의 효소들은 CxxxCxxC 모티프 또는 근접 변이체를 포함하는 서열상 상동 영역을 공유한다. 라디칼 중간체는 효소가 광범위하고 특이한 화학 반응을 수행할 수 있게 한다. 라디칼 S-아데노실메티오닌 효소의 예로는 포자 광생성물 분해효소, 폼산 C-아세틸트랜스퍼레이스 및 혐기성 설파테이트의 활성화효소, 리신 2,3-아미노뮤테이스, 다양한 효소들의 보조 인자 생합성, 펩타이드 변형, 금속 단백질 클러스터 형성, tRNA 변형, 지질 대사 등에 관여하는 효소들이 있다. 일부 라디칼 S-아데노실메티오닌 효소는 두 번째 S-아데노실메티오닌을 메틸기 공여체로 사용한다. 라디칼 S-아데노실메티오닌 효소는 호기성 생물보다 혐기성 세균에 더 풍부하다. 라디칼 S-아데노실메티오닌 효소는 모든 생물에서 발견될 수 있으며, 이에 대해선 대부분 연구되지 않았다. 최근의 생물정보학 연구는 라디칼 S-아데노실메티오닌 효소 계열이 65가지의 독특한 반응을 수행하며, 최소한 114,000개의 염기 서열을 포함하고 있다고 결론지었다.[8]
폴리아민 생합성[편집]
S-아데노실메티오닌의 또 다른 주요 역할은 폴리아민 생합성이다. 폴리아민 생합성에서 S-아데노실메티오닌은 아데노실메티오닌 탈카복실화효소(EC 4.1.1.50)에 의해 탈카복실화되어 S-아데노실메티오닌아민을 형성한다. 이어서 S-아데노실메티오닌아민은 n-프로필아민기를 푸트레신으로부터의 스페르미딘 및 스페르민과 같은 폴리아민의 생합성 과정에 공여한다.[9]
세포의 생장과 복구에는 S-아데노실메티오닌이 필요하다. S-아데노실메티오닌은 또한 에피네프린과 같이 기분에 영향을 미치는 여러 호르몬과 신경전달물질의 생합성에 관여한다. 메틸트랜스퍼레이스는 또한 mRNA에서 5' 캡에 있는 첫 번째 뉴클레오타이드와 두 번째 뉴클레오타이드의 2'-하이드록실기에 메틸기를 첨가하는 역할을 한다.[10][11]
치료용[편집]
2012년 시점까지 S-아데노실메티오닌이 골관절염의 통증을 완화시킬 수 있는지에 대한 증거는 결정적이지 않다. 수행된 임상 시험은 일반화하기에는 표본이 너무 적다.[12] 2016년 연구에 따르면 주요 우울 장애인 경우 "높이 신뢰할 증거가 없고 그러한 증거에 근거한 확실한 결론을 도출할 수 없기 때문에 성인의 우울증 치료에 S-아데노실메티오닌의 사용에 대해 추가로 조사해야 한다"고 결론지었다.[13]
알코올성 간경변 환자는 혈액에 메티오닌을 다량으로 축적하기 때문에 간과 밀접한 관련이 있다.[14] 세포 및 동물 모델에 대한 실험실 테스트에서 나온 여러 증거들은 S-아데노실메티오닌이 다양한 간질환들을 치료하는 데 유용할 수 있음을 시사하지만, 2012년을 기준으로 S-아데노실메티오닌은 그 효능과 안전성을 평가할 수 있는 대규모 무작위 위약 대조 임상 시험에서 연구되지 않았다.[15][16]
약물동태학[편집]
S-아데노실메티오닌은 장용정(400–1000 mg)으로 경구 섭취 후 3~5시간 후에 최대 혈장 농도에 도달한다. 반감기는 약 100분이다.[17]
부작용[편집]
위장관 장애, 소화 불량 및 불안은 S-아데노실메티오닌의 섭취로 일어날 수 있다.[17] 장기적인 복용의 효과는 알려져 있지 않다. S-아데노실메티오닌은 약한 DNA 알킬화제이다.[18]
S-아데노실메티오닌의 또 다른 부작용은 불면증이다. 따라서 보충제는 보통 아침에 섭취한다. 경미한 부작용에 대한 다른 보고서에는 식욕 부진, 변비, 메스꺼움, 구강 건조, 발한 및 불안, 신경과민이 포함되지만 위약 대조 연구에서 이러한 부작용은 위약 그룹에서 거의 동일한 발병률로 발생한다.
S-아데노실메티오닌은 최근 후성유전적 조절에 중요한 역할을 하는 것으로 나타났다. DNA 메틸화는 포유류 세포의 발생 및 분화 동안 후성유전적 변형의 중요한 조절인자이다. 쥐에 대한 실험에서 과도한 수준의 S-아데노실메티오닌은 당뇨병성 신경병증과 관련된 잘못된 메틸화 패턴과 연루되어 있다. S-아데노실메티오닌은 주요 후성유전적 조절 과정인 사이토신 메틸화에서 메틸기 공여체 역할을 한다.[19] 후성유전적 조절에 대한 이러한 영향으로 인해 S-아데노실메티오닌은 항암 치료제로 테스트되었다. 암 세포의 증식은 낮은 수준의 DNA 메틸화에 의존한다. 시험관 내 첨가는 프로모터 서열을 재메틸화하고 원종양유전자의 생성을 감소시키는 것으로 나타났다.[20]
라디칼 S-아데노실메티오닌 효소의 결핍은 선천성 심장병, 근위축성 측색 경화증 및 증가된 바이러스 감수성을 포함한 다양한 질병과 관련되어 있다.[8]
상호작용 및 금기사항[편집]
일부 약물과 동시에 S-아데노실메티오닌을 복용하면 세로토닌이 너무 많이 생성되어 세로토닌 증후군의 위험이 높아질 수 있다. 이러한 약물에는 덱스트로메토르판(로비투신), 페티딘(데메롤), 펜타조신(탈윈), 트라마돌(울트람) 등이 있다. S-아데노실메티오닌은 또한 항우울제와 상호작용하여 부작용의 가능성을 증가시키고, 파킨슨병에 대한 레보도파의 효과를 감소시킬 수 있다.
양극성 장애가 있는 사람은 S-아데노실메티오닌을 사용하면 조증의 위험이 높아질 수 있기 때문에 사용하지 말아야 한다.[21]
사용가능한 국가들[편집]
미국과 캐나다에서 S-아데노실메티오닌은 "SAM-e"라는 이름의 식이 보충제로 판매되고 있다.[22] S-아데노실메티오닌은 1994년 식이보충건강 및 교육법(Dietary Supplement Health and Education Act of 1994)이 통과된 후 1999년에 미국에 도입되었다.[23]
S-아데노실메티오닌은 1979년 이탈리아, 1985년 스페인, 1989년 독일에서 처방 의약품으로 소개되었다.[23] 2012년을 기준으로 S-아데노실메티오닌은 러시아, 인도, 중국, 이탈리아, 독일, 베트남, 멕시코에서 처방 의약품으로 판매되고 있다.[16]
같이 보기[편집]
- 메티오닌
- S-아데노실호모시스테인
- DNA 메틸트랜스퍼레이스
- SAM-I 리보스위치
- SAM-II 리보스위치
- SAM-III 리보스위치
- SAM-IV 리보스위치
- SAM-V 리보스위치
- SAM-VI 리보스위치
- 임상시험용 항우울제의 목록
각주[편집]
- ↑ 가 나 Cantoni, GL (1952). “The Nature of the Active Methyl Donor Formed Enzymatically from L-Methionine and Adenosinetriphosphate”. 《J Am Chem Soc》 74 (11): 2942–3. doi:10.1021/ja01131a519.
- ↑ Ding, Wei; Smulan, Lorissa J.; Hou, Nicole S.; Taubert, Stefan; Watts, Jennifer L.; Walker, Amy K. (2015년 10월 6일). “S-Adenosylmethionine Levels Govern Innate Immunity through Distinct Methylation-Dependent Pathways”. 《Cell Metabolism》 22 (4): 633–645. doi:10.1016/j.cmet.2015.07.013. PMC 4598287. PMID 26321661.
- ↑ Wang, X.; Oh, M. W.; Komatsu, S. (2016년 6월 1일). “Characterization of S-adenosylmethionine synthetases in soybean under flooding and drought stresses”. 《Biologia Plantarum》 (영어) 60 (2): 269–278. doi:10.1007/s10535-016-0586-6. ISSN 0006-3134.
- ↑ Födinger M, Hörl W, Sunder-Plassmann G (Jan–Feb 2000). “Molecular biology of 5,10-methylenetetrahydrofolate reductase”. 《J Nephrol》 13 (1): 20–33. PMID 10720211.
- ↑ Finkelstein J, Martin J (2000). “Homocysteine”. 《Int J Biochem Cell Biol》 32 (4): 385–9. doi:10.1016/S1357-2725(99)00138-7. PMID 10762063.
- ↑ Goyette, P.; Sumner, J. S.; Milos, R.; Duncan, A. M.; Rosenblatt, D. S.; Matthews, R. G.; Rozen, R. (1994년 6월 1일). “Human methylenetetrahydrofolate reductase: isolation of cDNA, mapping and mutation identification”. 《Nature Genetics》 7 (2): 195–200. doi:10.1038/ng0694-195. ISSN 1061-4036. PMID 7920641.
- ↑ Booker, SJ; Grove, TL (2010). “Mechanistic and functional versatility of radical SAM enzymes”. 《F1000 Biology Reports》 2: 52. doi:10.3410/B2-52. PMC 2996862. PMID 21152342.
- ↑ 가 나 Landgraf, Bradley J.; McCarthy, Erin L.; Booker, Squire J. (2016년 6월 13일). “Radical S-Adenosylmethionine Enzymes in Human Health and Disease”. 《Annual Review of Biochemistry》 (영어) 85: 485–514. doi:10.1146/annurev-biochem-060713-035504. PMID 27145839.
- ↑ Roje S (2006). “S-Adenosyl-L-methionine: beyond the universal methyl group donor”. 《Phytochemistry》 67 (15): 1686–98. doi:10.1016/j.phytochem.2006.04.019. PMID 16766004.
- ↑ Loenen W (2006). “S-Adenosylmethionine: jack of all trades and master of everything?”. 《Biochem Soc Trans》 34 (Pt 2): 330–3. doi:10.1042/BST20060330. PMID 16545107.
- ↑ Chiang P, Gordon R, Tal J, Zeng G, Doctor B, Pardhasaradhi K, McCann P (1996). “S-Adenosylmethionine and methylation”. 《FASEB J》 10 (4): 471–80. doi:10.1096/fasebj.10.4.8647346. PMID 8647346.
- ↑ Rutjes, AW; Nüesch, E; Reichenbach, S; Jüni, P (2009년 10월 7일). “S-Adenosylmethionine for osteoarthritis of the knee or hip.” (PDF). 《The Cochrane Database of Systematic Reviews》 (4): CD007321. doi:10.1002/14651858.CD007321.pub2. PMID 19821403.
- ↑ Galizia, I; Oldani, L; Macritchie, K; Amari, E; Dougall, D; Jones, TN; Lam, RW; Massei, GJ; Yatham, LN; Young, AH (2016년 10월 10일). “S-Adenosyl methionine (SAMe) for depression in adults.”. 《The Cochrane Database of Systematic Reviews》 10: CD011286. doi:10.1002/14651858.CD011286.pub2. PMC 6457972. PMID 27727432.
- ↑ Mato, Jose M (1997). “S-adenosylmethionine synthesis: Molecular mechanisms and clinical implications”. 《Pharmacology & Therapeutics》 73 (3): 265–280. doi:10.1016/s0163-7258(96)00197-0. hdl:10261/79246. PMID 9175157.
- ↑ Anstee, QM; Day, CP (November 2012). “S-Adenosylmethionine (SAMe) therapy in liver disease: a review of current evidence and clinical utility”. 《Journal of Hepatology》 57 (5): 1097–109. doi:10.1016/j.jhep.2012.04.041. PMID 22659519.
- ↑ 가 나 Lu, SC; Mato, JM (October 2012). “S-Adenosylmethionine in liver health, injury, and cancer”. 《Physiological Reviews》 92 (4): 1515–42. doi:10.1152/physrev.00047.2011. PMC 3698976. PMID 23073625.
- ↑ 가 나 Najm WI, Reinsch S, Hoehler F, Tobis JS, Harvey PW (February 2004). “S-Adenosyl methionine (SAMe) versus celecoxib for the treatment of osteoarthritis symptoms: A double-blind cross-over trial. ISRCTN36233495”. 《BMC Musculoskelet Disord》 5: 6. doi:10.1186/1471-2474-5-6. PMC 387830. PMID 15102339.
- ↑ Rydberg B, Lindahl T (1982). “Nonenzymatic methylation of DNA by the intracellular methyl group donor S-adenosyl-L-methionine is a potentially mutagenic reaction”. 《EMBO J.》 1 (2): 211–6. doi:10.1002/j.1460-2075.1982.tb01149.x. PMC 553022. PMID 7188181.
- ↑ Varela-Rey, Marta (2014). “S-Adenosylmethionine Levels Regulate the Schwann Cell DNA Methylome”. 《Neuron》 81 (5): 1024–1039. doi:10.1016/j.neuron.2014.01.037. PMC 3960855. PMID 24607226.
- ↑ Schmidt, Thomas; Leha, Andreas; Salinas-Riester, Gabriela (2016년 12월 31일). “Treatment of prostate cancer cells with S-adenosylmethionine leads to genome-wide alterations in transcription profiles”. 《Gene》 595 (2): 161–167. doi:10.1016/j.gene.2016.09.032. PMID 27688072.
- ↑ “S-Adenosyl-L-Methionine (SAMe): In Depth” (영어). NCCIH. 2017년 1월 11일.
- ↑ Woolston, Chris. "What is SAM-e?" Archived 2022년 12월 7일 - 웨이백 머신 1 January 2019. Retrieved on 14 November 2019.
- ↑ 가 나 Bottiglieri, T (November 2002). “S-Adenosyl-L-methionine (SAMe): from the bench to the bedside--molecular basis of a pleiotrophic molecule”. 《The American Journal of Clinical Nutrition》 76 (5): 1151S–1157S. doi:10.1093/ajcn/76.5.1151S. PMID 12418493.
외부 링크[편집]
- EINECS 번호 249-946-8
- Shippy, R Andrew; Mendez, Douglas; Jones, Kristina; Cergnul, Irene; Karpiak, Stephen E (2004). “S-Adenosylmethionine (SAM-e) for the treatment of depression in people living with HIV/AIDS”. 《BMC Psychiatry》 4: 38. doi:10.1186/1471-244X-4-38. PMC 535560. PMID 15538952.