크레아티닌
| |

| |
| 이름 | |
|---|---|
| 우선명 (PIN)
2-Amino-1-methyl-5H-imidazol-4-one | |
| 체계명
2-Amino-1-methyl-1H-imidazol-4-ol | |
| 별칭
2-Amino-1-methylimidazol-4-ol
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| 3DMet | |
| 112061 | |
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.424 |
| EC 번호 |
|
| KEGG | |
| MeSH | Creatinine |
PubChem CID
|
|
| UNII | |
| UN 번호 | 1789 |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C4H7N3O | |
| 몰 질량 | 113.120 g·mol−1 |
| 겉보기 | White crystals |
| 밀도 | 1.09 g cm−3 |
| 녹는점 | 300 °C (572 °F; 573 K)[1] (decomposes) |
| 1 part per 12[1]
90 mg/mL at 20° C[2] | |
| log P | -1.76 |
| 산성도 (pKa) | 12.309 |
| 염기도 (pKb) | 1.688 |
| 등전점 | 11.19 |
| 열화학 | |
열용량 (C)
|
138.1 J K−1 mol−1 (at 23.4 °C) |
표준 몰 엔트로피 (S
|
167.4 J K−1 mol−1 |
표준 생성 엔탈피 (ΔfH⦵298)
|
−240.81–239.05 kJ mol−1 |
표준 연소 엔탈피 (ΔcH⦵298)
|
−2.33539–2.33367 MJ mol−1 |
| 위험 | |
| NFPA 704 (파이어 다이아몬드) | |
| 인화점 | 290 °C (554 °F; 563 K) |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
크레아티닌(영어: creatinine)은 근육에서 포스포크레아틴의 분해 산물이며, 일반적으로 신체에 의해 상당히 일정한 속도로(근육의 질량에 따라 다름) 생성된다.[3][4] 크레아티닌이란 용어는 "살, 고기(flesh)"를 의미하는 그리스어 "κρέας"에서 파생되었다.
생물학적 관련성[편집]
혈청 크레아티닌(혈액 측정)은 콩팥에 의해 변하지 않고 배설되는 근육 대사의 부산물로 쉽게 측정되므로 콩팥 건강의 중요한 지표이다. 크레아티닌 자체는 크레아틴, 포스포크레아틴 및 아데노신 삼인산(ATP, 신체에 즉각적으로 에너지를 공급함)을 포함하는 생물학적 시스템을 통해 생성된다.[5]
크레아틴은 주로 간에서 S-아데노실메티오닌에 의해 글리코사이아민(콩팥에서 아미노산인 아르지닌과 글리신으로부터 구아니디노아세트산으로 합성됨)의 메틸화로부터 합성된다. 그런 다음, 혈액을 통해 다른 기관들, 근육 및 뇌로 운반되며, 운반된 기관에서 인산화를 통해 고에너지 화합물인 포스포크레아틴이 생성된다.[6] 크레아틴은 크레아틴 키네이스에 의해 포스포크레아틴으로 전환된다. 크레아티닌의 자발적인 형성은 반응 중에 일어난다.[7]
크레아티닌은 콩팥, 주로 사구체에서의 여과 뿐만 아니라 근위 세뇨관에서의 분비에 의해 혈액에서 제거된다. 크레아티닌의 세뇨관에서의 재흡수는 거의 또는 전혀 일어나지 않는다. 콩팥에서 여과가 잘 일어나지 않으면 혈액의 크레아틴의 농도가 높아진다. 따라서 혈액과 소변의 크레아티닌 농도를 이용하여 크레아티닌 청소율(CrCl)을 계산할 수 있으며, 이는 사구체 여과율(GFR)과 관련이 있다. 혈액의 크레아티닌 농도는 또한 추정된 사구체 여과율(eGFR)을 계산하기 위해 단독으로 사용될 수 있다.
사구체 여과율(GFR)은 콩팥의 기능을 측정하기 때문에 임상적으로 중요하다. 그러나 심각한 콩팥 기능 장애인 경우, 근위 세뇨관에 의한 크레아티닌의 과분비가 제거된 총 크레아티닌의 많은 부분을 차지하기 때문에 크레아티닌 청소율(CrCl)이 사구체 여과율(GFR)을 과대평가할 것이다.[8] 케토산, 시메티딘, 트리메소프림은 크레아티닌의 세뇨관 분비를 감소시키기 때문에, 특히 심각한 콩팥 기능 장애에서 사구체 여과율(GFR) 추정치의 정확도를 증가시킨다. 분비가 없으면 크레아티닌은 이눌린처럼 행동한다.
크레아티닌의 혈중 농도와 요소의 혈중 농도를 해석할 때 콩팥의 기능의 대체 평가를 할 수 있다. 혈액요소질소 대 크레아티닌의 비율은 콩팥에 내재된 것 이외에 다른 문제들을 나타낼 수 있다. 예를 들어, 크레아티닌에 비례하여 높아진 요소 농도는 부피 감소와 같은 신장전(前) 문제를 나타낼 수 있다.
매일 근육 크레아틴의 1~2%가 크레아티닌으로 전환된다.[6] 이러한 전환 과정은 비효소적이며, 비가역적이다.[9] 일반적으로 골격근의 질량이 더 크기 때문에, 남성은 여성보다 크레아티닌의 농도가 높은 경향이 있다.[6] 크레아틴의 식이 섭취 증가 또는 육류와 같은 많은 단백질의 섭취는 크레아티닌의 배설을 증가시킬 수 있다.[6]
항균 및 잠재적 면역억제 특성[편집]
연구에 따르면 크레아티닌은 그람 양성 세균, 그람 음성 세균 뿐만 아니라 다양한 항생제 내성 세균 균주에서 많은 종의 세균을 죽이는 데 효과적일 수 있다.[10] 크레아티닌은 균류와 효모의 성장에 영향을 미치지 않는 것으로 보인다. 크레아티닌은 대부분의 환경 시료에서 발견되는 정상적인 세균 개체군으로부터 느리게 자라는 균류를 분리하는 데 사용될 수 있다. 크레아티닌이 세균을 죽이는 메커니즘은 현재 알려져 있지 않다. 최근의 보고서는 또한 크레아티닌이 면역억제 특성을 가질 수 있음을 시사한다.[11][12]
진단용[편집]
혈청 크레아티닌은 콩팥 기능에 대해 가장 일반적으로 사용되는 지표(직접 측정은 아님)이다. 크레아티닌의 증가가 항상 사구체 여과율(GFR)의 진정한 감소를 나타내는 것은 아니다. 높은 수치는 신장 기능 감소, 분석 방해 또는 크레아티닌의 세뇨관 분비 감소로 인한 것이 아니라 크레아티닌의 생성 증가로 인한 것 일 수 있다. 혈청 크레아티닌의 증가는 조리된 고기(요리로 인한 열에 의해 크레아틴에서 전환된 크레아티닌을 함유함)의 섭취 증가 또는 운동 능력을 향상시키기 위해 단백질 및 크레아틴 보충제의 과도한 섭취로 인한 것 일 수 있다. 격렬한 운동은 근육 파괴를 증가시켜 크레아티닌을 증가시킬 수 있다. 열이 나는 염증 과정에 이차적인 탈수는 담낭염의 경우와 같이 실제 콩팥 손상과 관련이 없는 크레아티닌 농도의 잘못된 증가를 유발할 수 있다. 여러 약물 및 색소원이 분석을 방해할 수 있다. 세뇨관에 의한 크레아티닌 분비는 몇몇 약물에 의해 차단될 수 있으며, 다시 측정된 크레아티닌을 증가시킨다.[13]
혈청 크레아티닌[편집]
진단 혈청 크레아티닌 연구는 콩팥 기능을 결정하는 데 사용된다.[4] 기준 간격은 0.6 ~ 1.3 mg/dL (53 ~ 115 µmol/L)이다.[4] 혈청 크레아티닌 측정은 간단한 검사이며, 콩팥 기능에 대해 가장 일반적으로 사용되는 지표이다.[6]
혈액의 크레아티닌 농도의 증가는 늦은 마커이며, 기능하는 네프론에 현저한 손상이 있는 것으로 관찰된다. 따라서 이 검사는 초기 신장 질환을 발견하기에 적합하지 않다. 추정 사구체 여과율(eGFR)을 계산하여 콩팥 기능을 더 잘 추정할 수 있다. 혈청 크레아티닌 농도 및 미국 당뇨병학회가 제안한 성별, 연령, 체중, 인종과 같은 변수들을 사용하여 24시간 소변 수집없이 추정 사구체 여과율 eGFR을 정확하게 계산할 수 있다.[14] 많은 실험실에서는 크레아티닌 검사가 요청될 때 추정 사구체 여과율(eGFR)을 자동으로 계산한다. 크레아티닌 농도 및 기타 매개 변수들로부터 사구체 여과율(GFR)을 추청하는 알고리즘은 콩팥 기능에 대한 논문에서 논의된다.
2010년 후반의 우려는 새로운 분석 방법론의 채택과 이것이 임상 의학에 미칠 수 있는 영향에 관한 것이다. 대부분의 임상 실험실은 크레아티닌 측정치를 새롭게 표준화된 동위원소 희석 질량분석법(IDMS)과 대조하여 혈청 크레아티닌을 측정한다. 혈청 크레아티닌 값이 비교적 낮은 경우, 예를 들어 0.7 mg/dL인 경우, 동위원소 희석 질량분석법(IDMS)은 이전의 방법들보다 낮은 값을 제공하는 것으로 보인다. 동위원소 희석 질량분석법(IDMS)은 정상적인 콩팥 기능을 가지고 있는 일부 환자에서 상응하는 사구체 여과율(GFR)의 비교 과대 평가를 초래할 수도 있다. 유도된 사구체 여과율(GFR)의 정상적인 콩팥 기능에서도 몇 가지 약물이 투여된다. 추가로 변형되지 않는 한, 용량은 원하는 것보다 많을 수 있고, 잠재적으로 약물 관련 독성을 증가시킬 수 있다. 동위원소 희석 질량분석법(IDMS)로의 변경 효과에 대응하기 위해, 새로운 미국 식품의약국(FDA)의 지침은 화학요법 약물인 카보플라틴으로 특정 최대 용량을 제한할 것을 제안했다.[15]
2009년 일본의 연구에서는 낮은 혈청 크레아티닌 농도가 일본 남성의 제2형 당뇨병 발병 위험 증가와 관련이 있다는 것을 발견했다.[16]
소변의 크레아티닌[편집]
남성은 하루에 체중의 킬로그램 당 약 150~200 μmol의 크레아티닌을 생성하는 반면 여성은 약 100~150 μmol의 크레아티닌을 생성한다. 정상적인 상황에서는 하루에 생성되는 모든 크레아티닌은 소변으로 배설된다.
크레아티닌 농도는 표준 소변 약물 검사 중에 확인된다. 예상 크레아티닌 농도는 시험 샘플이 희석되지 않았음을 나타내며, 소변 중 소량의 크레아티닌은 처리된 시험 또는 초기 기준선 크레아티닌 농도를 나타낸다. 낮은 크레아티닌으로 인해 처리된 것으로 간주되는 테스트 샘플은 테스트되지 않으며 때로는 테스트가 실패한 것으로 간주된다.
해석[편집]
미국과 대부분의 유럽 국가에서 크레아티닌은 보통 mg/dL이 일반적인 단위인 반면, 캐나다, 오스트레일리아[17] 및 몇몇 유럽 국가에서는 μmol/L이 일반적인 단위이다. 1 mg/dL은 88.4 μmol/L이다.
혈청 크레아티닌의 전형적인 사람 기준 범위는 여성의 경우 0.5 mg/dL ~ 1.0 mg/dL (약 45 μmol/L ~ 90 μmol/L)이며, 남성의 경우 0.7 mg/dL ~ 1.2 mg/dL (60 μmol/L ~ 110 μmol/L)이다. 단일 크레아티닌 값의 중요성은 환자의 근육 질량에 비추어 해석되어야 한다. 근육량이 많은 환자는 크레아티닌 농도가 더 높다. 2.0 mg/dL (177 μmol/L)의 기준치 혈청 크레아티닌은 남성 보디 빌더에서 정상적인 콩팥 기능을 나타낼 수 있지만, 1.6 mg/dL (110 μmol/L)의 혈청 크레아티닌은 노인 여성에서 심각한 신장 질환을 나타내는 것일 수도 있다.
 |
시간에 따른 혈청 크레아티닌 농도의 경향은 절대 크레아티닌 농도보다 중요하다.
심부전 및 만성 신부전에 대해 안지오텐신 전환효소 저해제(ACE 억제제)를 복용하면 혈청 크레아티닌의 농도가 증가할 수 있다. 안지오텐신 전환효소 저해제는 심부전 환자에게 생존에 대한 이점을 제공하고 만성 심부전 환자의 질병 진행 속도를 늦춘다. 안지오텐신 전환효소 저해제 사용시 혈청 크레아티닌이 30%를 초과하지 않는 증가가 예상된다. 따라서 혈청 크레아티닌의 증가가 30%를 초과하거나 고칼륨혈증이 발생하지 않는 한 안지오텐신 전환효소 저해제의 사용을 중단해서는 안된다.[18]
화학[편집]
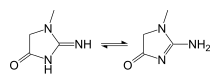
화학적으로 크레아티닌은 자발적으로 형성된 크레아틴의 고리형 유도체이다. 크레아티닌의 몇몇 호변 이성질체가 존재하며, 기여도에 따른 순서는 다음과 같다.
- 2-아미노-1-메틸-1H-이미다졸-4-올 (또는 2-아미노-1-메틸이미다졸-4-올)
- 2-아미노-1-메틸-4,5-다이하이드로-1H-이미다졸-4-온
- 2-이미노-1-메틸-2,3-다이하이드로-1H-이미다졸-4-올 (또는 2-이미노-1-메틸-3H-이미다졸-4-올)
- 2-이미노-1-메틸이미다졸리딘-4-온
- 2-이미노-1-메틸-2,5-다이하이드로-1H-이미다졸-4-올 (또는 2-이미노-1-메틸-5H-이미다졸-4-올)
크레아티닌은 약 300 °C에서 분해되기 시작한다.
같이 보기[편집]
각주[편집]
- ↑ 가 나 Merck Index, 11th Edition, 2571
- ↑ “Creatinine, anhydrous - CAS 60-27-5”. 《Scbt.com》.
- ↑ Creatinine in Mayo Clinic
- ↑ 가 나 다 Lewis, Sharon Mantik; Dirksen, Shannon Ruff; Heitkemper, Margaret M.; Bucher, Linda; Harding, Mariann. 《Medical-surgical nursing : assessment and management of clinical problems》 9판. St. Louis, Missouri. ISBN 978-0-323-10089-2. OCLC 228373703.
- ↑ “What Is a Creatinine Blood Test? Low & High Ranges”. 《Medicinenet.com》. 2018년 9월 21일에 확인함.
- ↑ 가 나 다 라 마 Taylor, E. Howard (1989). 《Clinical Chemistry》. New York: John Wiley and Sons. 4, 58–62쪽.
- ↑ Allen PJ (May 2012). “Creatine metabolism and psychiatric disorders: Does creatine supplementation have therapeutic value?”. 《Neurosci Biobehav Rev》 36 (5): 1442–62. doi:10.1016/j.neubiorev.2012.03.005. PMC 3340488. PMID 22465051.
- ↑ Shemesh O, Golbetz H, Kriss JP, Myers BD (November 1985). “Limitations of creatinine as a filtration marker in glomerulopathic patients”. 《Kidney Int.》 28 (5): 830–8. doi:10.1038/ki.1985.205. PMID 2418254.
- ↑ Hosten, Adrian O. (1990). Walker, H. Kenneth; Hall, W. Dallas; Hurst, J. Willis, 편집. 《Clinical Methods: The History, Physical, and Laboratory Examinations》 3판. Boston: Butterworths. ISBN 978-0409900774. PMID 21250147.
- ↑ McDonald, Thomas; Drescher, Kristen M.; Weber, Annika; Tracy, Steven (2012년 3월 1일). “Creatinine inhibits bacterial replication”. 《The Journal of Antibiotics》 65 (3): 153–156. doi:10.1038/ja.2011.131. PMID 22293916.
- ↑ Smithee, Shane; Tracy, Steven; Drescher, Kristen M.; Pitz, Lisa A.; McDonald, Thomas (2014년 10월 1일). “A novel, broadly applicable approach to isolation of fungi in diverse growth media”. 《Journal of Microbiological Methods》 105: 155–161. doi:10.1016/j.mimet.2014.07.023. PMID 25093757.
- ↑ Leland, Korey M.; McDonald, Thomas L.; Drescher, Kristen M. (2011년 9월 1일). “Effect of creatine, creatinine, and creatine ethyl ester on TLR expression in macrophages”. 《International Immunopharmacology》 11 (9): 1341–1347. doi:10.1016/j.intimp.2011.04.018. PMC 3157573. PMID 21575742.
- ↑ Samra M, Abcar AC (2012). “False estimates of elevated creatinine.”. 《Perm J》 16 (2): 51–2. doi:10.7812/tpp/11-121. PMC 3383162. PMID 22745616.
- ↑ Gross JL, de Azevedo MJ, Silveiro SP, Canani LH, Caramori ML, Zelmanovitz T (January 2005). “Diabetic nephropathy: diagnosis, prevention, and treatment”. 《Diabetes Care》 28 (1): 164–76. doi:10.2337/diacare.28.1.164. PMID 15616252.
- ↑ “Carboplatin dosing”. Center for Drug Evaluation and Research. 2011년 11월 19일에 원본 문서에서 보존된 문서.
- ↑ Harita N, Hayashi T, Sato KK, 외. (March 2009). “Lower serum creatinine is a new risk factor of type 2 diabetes: the Kansai healthcare study”. 《Diabetes Care》 32 (3): 424–6. doi:10.2337/dc08-1265. PMC 2646021. PMID 19074997.
- ↑ Faull R (2007). “Prescribing in renal disease”. 《Australian Prescriber》 30 (1): 17–20. doi:10.18773/austprescr.2007.008.
- ↑ Ahmed, Ali (July 2002). “Use of Angiotensin-Converting Enzyme Inhibitors in Patients with Heart Failure and Renal Insufficiency: How Concerned Should We Be by the Rise in Serum Creatinine?”. 《Journal of the American Geriatrics Society》 50 (7): 1297–1300. doi:10.1046/j.1532-5415.2002.50321.x.
외부 링크[편집]
- Creatinine at Lab Tests Online Archived 2017년 7월 28일 - 웨이백 머신
- Creatinine: analyte monograph Archived 2017년 4월 28일 - 웨이백 머신 – The Association for Clinical Biochemistry and Laboratory Medicine

