아스파르트산
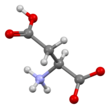
 L-아스파르트산의 골격 구조식
| |||
| |||
| 이름 | |||
|---|---|---|---|
IUPAC 이름
| |||
별칭
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
| ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank |
| ||
| ECHA InfoCard | 100.000.265 | ||
| EC 번호 |
| ||
| KEGG |
| ||
PubChem CID
|
|||
| UNII |
| ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C4H7NO4 | |||
| 몰 질량 | 133.103 g·mol−1 | ||
| 겉보기 | 무색 결정 | ||
| 밀도 | 1.7 g/cm3 | ||
| 녹는점 | 270 °C (518 °F; 543 K) | ||
| 끓는점 | 324 °C (615 °F; 597 K) (decomposes) | ||
| 4.5 g/L[2] | |||
| 산성도 (pKa) |
| ||
| 짝염기 | aspartate | ||
자화율 (χ)
|
-64.2·10−6 cm3/mol | ||
| 위험 | |||
| NFPA 704 (파이어 다이아몬드) | |||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
아스파르트산(영어: aspartic acid) (기호: Asp or D)[4]은 단백질의 생합성에 사용되는 α-아미노산이다.[5] 아스파트산이라고도 하며, 이온형은 아스파르트산염(영어: aspartate)으로 알려져 있다. 다른 모든 아미노산과 마찬가지로 아스파르트산은 아미노기와 카복실기를 가지고 있다. 아스파르트산은 α-아미노기(생물학적 조건에서 양성자화된 –NH+
3 형태), α-카복실기(생물학적 조건에서 탈양성자화된 −COO− 형태) 및 체내의 다른 아미노산, 효소 및 단백질과 반응할 수 있는 산성 곁사슬(CH2COOH)을 포함하고 있다.[5] 단백질의 생물학적 조건(pH 7.4)에서 아스파르트산의 곁사슬은 일반적으로 음전하를 띠는 아스파르트산염(−COO−)의 형태로 존재한다.[5] 아스파르트산은 사람에서 비필수 아미노산이며, 신체의 필요에 따라 합성될 수 있다. 아스파르트산은 GAU, GAC 코돈에 의해 암호화되어 있다.
D-아스파르트산은 포유류에서 흔히 발견되는 두 가지 D-아미노산 중 하나이다.[3]
단백질에서 아스파르트산의 곁사슬은 보통 α-나선의 N-말단에서 자주 발견되는 Asx 턴 또는 Asx 모티프를 형성하기 위해 수소 결합된다.
L-아스파르트산은 22가지의 단백질생성성 아미노산들 중 하나로, 단백질을 구성하는 단위체이다. 아스파르트산은 pKa가 3.9로 글루탐산과 마찬가지로 산성 아미노산으로 분류되며, 펩타이드에 존재시에는 국부적인 주변 환경에 크게 영향을 받으며 14까지 높아질 수도 있다. 아스파르트산은 생합성에서 널리 발견된다.
발견
[편집]아스파르트산은 1806년에 아스파라거스 주스로부터 분리된 아스파라긴을 가수분해하여[6] 1827년 오귀스트 아르튀르 플리송과 에띠엔 오시앙 앙리에 의해 처음으로 발견되었다.[7][8] 이들이 사용한 방법은 수산화 납을 사용하는 것이었지만, 이제는 다양한 다른 산이나 염기가 보다 더 일반적으로 사용된다.
형태 및 명명법
[편집]아스파르트산에는 두 가지 형태 또는 두 가지 거울상 이성질체가 존재한다. "아스파르트산"이라는 이름은 각각의 거울상 이성질체 또는 이 둘의 혼합물을 나타내는 것일 수 있다.[9] 두 가지 형태의 거울상 이성질체 중 "L-아스파르트산"만 단백질 생합성에 사용된다. "D-아스파르트산"의 생물학적 역할은 보다 더 제한적이다. 효소적 합성이 두 가지 거울상 이성질체 중 하나를 생성하는 반면, 대부분의 화학적 합성은 라세미 혼합물로 알려진 "DL-아스파르트산"이라는 두 가지 형태의 거울상 이성질체를 모두 생성한다.
합성
[편집]생합성
[편집]인체에서 아스파르트산은 옥살로아세트산의 아미노기 전이반응을 통해 가장 빈번하게 합성된다. 아스파르트산의 생합성은 아스파르트산 아미노기전이효소에 의해 촉매된다. 글루탐산으로부터 옥살로아세트산으로 아미노기가 전이되면 α-케토글루타르산과 아스파르트산이 생성된다.[5]
아스파르트산은 또한 요소 회로에서 중요한 역할을 한다.
화학 합성
[편집]산업적으로 아스파르트산은 아스파르트산 암모니아 분해효소에 의해 촉매되는 푸마르산의 아미노화에 의해 생성된다.[10]
라세미 아스파르트산은 다이에틸 나트륨 프탈이미도말로네이트(C6H4(CO)2NC(CO2Et)2)로부터 합성될 수 있다.[11]
물질대사
[편집]식물과 미생물에서 아스파르트산은 사람에게 필수적인 4가지 아미노산(메티오닌, 트레오닌, 아이소류신, 리신)을 포함한 여러 아미노산들의 전구체이다. 이러한 다른 아미노산으로의 아스파르트산의 전환은 아스파르트산의 세미알데하이드인 O2CCH(NH2)CH2CHO로 환원되면서 시작된다.[12] 아스파라긴은 아미노기 전이반응을 통해 아스파르트산으로부터 유도된다.
- -O2CCH(NH2)CH2CO2- + GC(O)NH3+ O2CCH(NH2)CH2CONH3+ + GC(O)O
(여기서 GC(O)NH2는 글루타민, 및 GC(O)OH는 글루탐산이다.)
요소 회로에 참여
[편집]요소 회로에서 아스파르트산과 암모니아는 아미노기를 제공하여 요소를 형성한다.[13]
기타 생물학적 역할
[편집]아스파르트산은 다른 많은 생화학적 역할을 한다. 아스파르트산은 요소 회로에서의 대사 산물이며,[14] 포도당신생합성에 참여한다. 아스파르트산은 말산의 산화된(탈수소화된) 유도체인 옥살로아세트산과 아스파르트산 사이의 즉각적인 상호전환을 활용하는 말산-아스파르트산 셔틀에서 환원 당량을 운반한다. 아스파르트산은 퓨린 염기의 전구체인 이노신의 생합성에서 1개의 질소 원자를 제공한다. 식이 L-아스파르트산은 빌리루빈과 담즙산의 장간 순환을 조절하는 역할을 하는 β-글루쿠로니데이스의 저해제로 작용하는 것으로 나타났다.[15]
신경전달물질
[편집]아스파르트산은 NMDA 수용체를 자극하지만, 아미노산 신경전달물질인 글루탐산만큼 강력하지는 않다.[16]
활용 및 시장
[편집]아스파르트산의 전세계 시장 규모는 2014년에 35,700톤[17] 또는 연간 약 1억 1,700만 달러[18]였으며, 잠재적 성장 규모는 87억 8,000만 달러로 추정되었다.[19] 아스파르트산의 세계 3대 시장은 미국, 서유럽, 중국이다. 현재 활용 분야로는 생분해성 고분자(폴리아스파르트산), 저칼로리 감미료(아스파탐), 스케일 및 부식 방지제, 수지 등이 있다.
고흡수성 고분자
[편집]아스파르트산 시장의 성장 분야는 생분해성 고흡수성 고분자(SAP)와 하이드로젤이다.[20] 고흡수성 고분자 시장은 2014년부터 2019년까지 연평균 성장률 5.51%로 전세계적으로 87억 8,000만 달러 규모로 성장할 것으로 예상되었다.[19] 고흡수성 고분자의 약 75%는 일회용 기저귀에 사용되며, 20%는 성인용 요실금 용품 및 여성용 위생용품에 사용된다. 아스파르트산의 중합 생성물인 폴리아스파르트산은 폴리아크릴레이트의 생분해성 대체물이다.[20][21][22] 폴리아스파르트산 시장은 전체 고흡수성 고분자 시장의 작은 부분(1% 미만으로 추정)을 차지한다.
추가 용도
[편집]고흡수성 고분자 외에도 아스파르트산은 190억 달러 규모의 비료 산업에 적용되며, 여기서 폴리아스파르트산은 수분 보유 및 질소 흡수를 개선한다.[23] 2020년 기준 11억 달러 규모의 콘크리트 바닥 코팅 시장에서 폴리아스파르트산은 기존의 에폭시 수지에 대한 저 VOC, 저에너지 대안이다.[24] 마지막으로 50억 달러 이상의 스케일 및 부식 방지제 시장이 있다.[25]
공급원
[편집]식이 공급원
[편집]아스파르트산은 필수 아미노산이 아니며, 사람에서 대사 경로의 대사 중간생성물로부터 합성될 수 있다.[26] 아스파르트산은 다음과 같은 것들에서 발견된다.
- 동물성 공급원: 굴, 런천 미트, 소시지 고기
- 식물성 공급원: 새싹 씨앗, 귀리 플레이크, 아보카도,[27] 아스파라거스,[28] 어린 사탕수수, 사탕무의 당밀[1]
- 식이 보충제: 아스파르트산 자체 또는 염(예: 아스파르트산 마그네슘)
- 아스파르트산, 페닐알라닌으로부터 만들어지는 감미료인 아스파탐
같이 보기
[편집]각주
[편집]- ↑ 가 나 Budavari, Susan; Co, Merck (1989). 〈862. Aspartic acid〉. 《The Merck Index》 11판. 132쪽. ISBN 978-0-911910-28-5.
- ↑ “ICSC 1439 - L-ASPARTIC ACID”. 《inchem.org》.
- ↑ Haynes, William M., 편집. (2016). 《CRC Handbook of Chemistry and Physics》 97판. CRC Press. 5–89쪽. ISBN 978-1498754286.
- ↑ “Nomenclature and Symbolism for Amino Acids and Peptides”. IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. 2008년 10월 9일에 원본 문서에서 보존된 문서. 2018년 3월 5일에 확인함.
- ↑ 가 나 다 라 G., Voet, Judith; W., Pratt, Charlotte (2016년 2월 29일). 《Fundamentals of biochemistry : life at the molecular level》. ISBN 9781118918401. OCLC 910538334.
- ↑ Plimmer, R.H.A. (1912) [1908]. Plimmer, R.H.A.; Hopkins, F.G., 편집. 《The chemical composition of the proteins》. Monographs on Biochemistry. Part I. Analysis 2판. London: Longmans, Green and Co. 112쪽. 2010년 1월 18일에 확인함.
- ↑ Plisson, A. (October 1827). “Sur l'identité du malate acide d'althéine avec l'asparagine (1); et sur un acide nouveau” [On the identity of altheine acid malate with asparagine (1); and on a new acid]. 《Journal de Pharmacie》 (프랑스어) 13 (10): 477–492.
- ↑ Berzelius, Jöns Jakob; Öngren, Olof Gustaf (1839). 《Traité de chimie》 (프랑스어) 3. Brussels: A. Wahlen et Cie. 81쪽. 2015년 8월 25일에 확인함.
- ↑ “Nomenclature and symbolism for amino acids and peptides (IUPAC-IUB Recommendations 1983)”, 《Pure Appl. Chem.》 56 (5), 1984: 595–624, doi:10.1351/pac198456050595.
- ↑ Karlheinz Drauz, Ian Grayson, Axel Kleemann, Hans-Peter Krimmer, Wolfgang Leuchtenberger, Christoph Weckbecker (2006), 《울만 공업화학 백과사전(Ullmann's Encyclopedia of Industrial Chemistry)》, Weinheim: Wiley-VCH, doi:10.1002/14356007.a02_057.pub2
- ↑ Dunn, M. S.; Smart, B. W. (1950). “DL-Aspartic Acid”. 《Organic Syntheses》 30: 7.; 《Collective Volume》 4, 55쪽.
- ↑ 틀:Lehninger3rd
- ↑ “Biochemistry - Biochemistry”. 《www.varsitytutors.com》 (영어). 2022년 2월 18일에 확인함.
- ↑ “Biochemistry - Biochemistry”. 《www.varsitytutors.com》 (영어). 2022년 2월 18일에 확인함.
- ↑ Kreamer, Siegel, & Gourley (Oct 2001). “A novel inhibitor of beta-glucuronidase: L-aspartic acid.”. 《Pediatric Research》 50 (4): 460–466. doi:10.1203/00006450-200110000-00007. PMID 11568288.
- ↑ Chen PE, Geballe MT, Stansfeld PJ, Johnston AR, Yuan H, Jacob AL, Snyder JP, Traynelis SF, Wyllie DJ (May 2005). “Structural features of the glutamate binding site in recombinant NR1/NR2A N-methyl-D-aspartate receptors determined by site-directed mutagenesis and molecular modeling”. 《Molecular Pharmacology》 67 (5): 1470–84. doi:10.1124/mol.104.008185. PMID 15703381. S2CID 13505187.
- ↑ “Global Aspartic Acid Market By Application”. Grand View Research. 2019년 11월 30일에 확인함.
- ↑ Evans J (2014). 《Commercial Amino Acids》. BCC Research. 101–103쪽.
- ↑ 가 나 Transparency Market Research. Superabsorbent polymers market - global industry analysis, size, share, growth, trends and forecase, 2014-2020. (2014).
- ↑ 가 나 Adelnia, Hossein; Blakey, Idriss; Little, Peter J.; Ta, Hang T. (2019). “Hydrogels Based on Poly(aspartic acid): Synthesis and Applications”. 《Frontiers in Chemistry》 (영어) 7: 755. Bibcode:2019FrCh....7..755A. doi:10.3389/fchem.2019.00755. ISSN 2296-2646. PMC 6861526. PMID 31799235.
- ↑ Adelnia, Hossein; Tran, Huong D.N.; Little, Peter J.; Blakey, Idriss; Ta, Hang T. (2021년 6월 14일). “Poly(aspartic acid) in Biomedical Applications: From Polymerization, Modification, Properties, Degradation, and Biocompatibility to Applications”. 《ACS Biomaterials Science & Engineering》 7 (6): 2083–2105. doi:10.1021/acsbiomaterials.1c00150. hdl:10072/404497. PMID 33797239. S2CID 232761877.
- ↑ Alford DD, Wheeler AP, Pettigrew CA (1994). “Biodegradation of thermally synthesized polyaspartate”. 《J Environ Polym Degr》 2 (4): 225–236. doi:10.1007/BF02071970.
- ↑ Kelling K (2001). 《Crop Responses to Amisorb in the North Central Region》. University of Wisconsin-Madison.
- ↑ Global concrete floor coatings market will be worth US$1.1Bn by 2020. Transparency Market Research (2015).
- ↑ Corrosion inhibitors market analysis by product, by application, by end-use industry, and segment forecasts to 2020. Grand View Research (2014)
- ↑ Kozlowski LP (January 2017). “Proteome-pI: proteome isoelectric point database”. 《Nucleic Acids Research》 45 (D1): D1112–D1116. doi:10.1093/nar/gkw978. PMC 5210655. PMID 27789699.
- ↑ Salunkhe, D. K.; Kadam, S.S. (1995년 8월 18일). 《Handbook of Fruit Science and Technology: Production, Composition, Storage, and Processing》. CRC Press. 368–쪽. ISBN 978-0-8247-9643-3.
- ↑ Considine, Douglas M. (2012년 12월 6일). 《Foods and Food Production Encyclopedia》. Springer Science & Business Media. 114–쪽. ISBN 978-1-4684-8511-0.
외부 링크
[편집]- GMD MS Spectrum
- American Chemical Society (2010년 4월 21일). “Ancestral Eve' Crystal May Explain Origin of Life's Left-Handedness”. 《ScienceDaily》. 2010년 4월 23일에 원본 문서에서 보존된 문서. 2010년 4월 21일에 확인함.