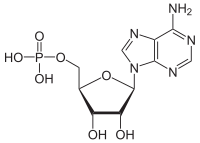
아데노신 일인산
| |

| |
| 이름 | |
|---|---|
| IUPAC 이름
[(2R,3S,4R,5R)-5-(6-aminopurin-9-yl)-3,4-dihydroxyoxolan-2-yl]methyl dihydrogen phosphate
| |
| 별칭
Adenosine 5'-monophosphate, 5'-Adenylic acid
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.455 |
| KEGG | |
| MeSH | Adenosine+monophosphate |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C10H14N5O7P | |
| 몰 질량 | 347.22 g/mol |
| 겉보기 | white crystalline powder |
| 밀도 | 2.32 g/mL |
| 녹는점 | 178 to 185 °C (352 to 365 °F; 451 to 458 K) |
| 끓는점 | 798.5 °C (1,469.3 °F; 1,071.7 K) |
| 산성도 (pKa) | 0.9, 3.8, 6.1 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
아데노신 일인산(영어: adenosine monophosphate, AMP)은 RNA에서 단위체로 사용되는 뉴클레오타이드의 한 종류이다. 5'-아데닐산 또는 아데닐산이라고도 한다. 아데노신 일인산은 뉴클레오타이드인 아데노신과 인산의 에스터이다. 아데노신 일인산은 핵염기인 아데닌, 5탄당인 리보스, 인산으로 구성되므로 리보뉴클레오사이드 일인산이다. 치환기로 사용될 때는 접두사 "아데닐릴-"로 나타낸다.
AMP는 ADP 또는 ATP로 상호 변환됨으로써 많은 세포 내 물질대사 과정에서 중요한 역할을 하며, RNA 합성에 있어 중요한 구성 요소이다.[1]
생성 및 분해[편집]
AMP는 ADP, ATP와는 달리 고에너지 인산 결합을 가지지 않는다. AMP는 ADP로부터 생성되기도 한다.
- 2 ADP → ATP + AMP
또는 AMP는 ADP의 고에너지 인산 결합이 가수분해되면서 생성될 수도 있다.
- ADP + H2O → AMP + Pi
AMP는 또한 ATP가 AMP와 피로인산으로 가수분해되면서 생성될 수도 있다.
- ATP + H2O → AMP + PPi
생명체에서 RNA가 분해되면 아데노신 일인산을 포함한 뉴클레오사이드 일인산이 생성된다.
AMP는 다음과 같이 ATP로 재생성될 수 있다.
- AMP + ATP → 2 ADP (아데닐산 키네이스에 의해 촉매된다.)
- ADP + Pi → ATP (이러한 과정은 호기성 생물에서 산화적 인산화가 일어나는 동안 ATP 생성효소에 의해서 수행되는 경우가 가장 많다.)
AMP는 AMP 탈아미노효소에 의해 이노신 일인산(IMP)으로 전환되며, 이 과정에서 아미노기가 유리된다.
포유류는 체내에서 아데노신 일인산을 이화작용을 통해 요산으로 전환시켜 배출할 수 있다.[2]
생리학적 조절[편집]
AMP-활성 단백질 키네이스 조절[편집]
진핵생물이 가지고 있는 효소인 AMP-활성 단백질 키네이스(AMPK)는 운동과 같이 세포의 에너지 소비가 많아질 때, 에너지 항상성을 유지하기 위해 AMP를 이용한다.[3] ATP의 가수분해 반응은 생체 내의 다양한 과정에서 에너지원으로 활용되기 때문에 세포 호흡을 통한 ATP의 생성은 중요하다. AMP-활성 단백질 키네이스는 세포에 있는 에너지 센서로, ATP의 양이 감소함에 따라 사용 가능한 에너지가 적어지면 AMP에 의해 활성화되며, ATP의 소비를 억제하고 ATP의 생산을 증가시킨다.[4]
인산화가 AMP-활성 단백질 키네이스의 주된 활성인자인 것처럼 보이지만, 일부 연구에서는 AMP가 다른 자리 입체성 조절인자 일 뿐만 아니라, AMP-활성 단백질 키네이스의 직접적인 작용제라고 보고하고 있다.[5] 한편 다른 연구들에서는 AMP 뿐만 아니라 AMP 대 ATP의 비율이 세포내에서 AMP-활성 단백질 키네이스를 활성화시킨다는 메커니즘을 제안한 바 있다. 예를 들어, 예쁜꼬마선충과 노랑초파리의 AMP-활성 단백질 키네이스는 AMP에 의해 활성화된다는 것이 발견된 반면, 효모와 식물의 AMP-활성 단백질 키네이스는 AMP에 의해 다른 자리 입체성 조절로 활성화되지 않았다.[6] 이것은 AMP 대 ATP의 비율에서 ATP가 상대적으로 낮거나 AMP가 상대적으로 높을 때 활성화를 전제할 수 있다는 의미로 가정해볼 수 있다. 이러한 맥락은 ATP의 전환과정이 포도당의 해당과정과 포도당재합성의 가역적 반응의 일예에서처럼 생명체의 에너지대사나 물질대사가 얼마나 정교하고 섬세하게 조절되는지를 설명하고 있다고 할 수 있다.
AMP는 AMP-활성 단백질 키네이스의 γ-소단위체와 결합하여 키네이스의 활성화를 유도하고, 이는 이화경로의 활성화 및 동화경로의 억제와 같은 다른 과정의 캐스케이드를 통해 ATP를 재생성한다. 분자의 분해로 인한 에너지 방출을 통해 ATP를 생성하는 이화작용은 AMP-활성 단백질 키네이스에 의해 활성화되는 반면, ATP의 에너지를 물질 합성에 사용하는 동화작용은 억제된다.[7] γ-소단위체는 AMP/ADP/ATP와 결합할 수 있지만, AMP/ADP와 결합할 때만 효소의 구조적인 변화를 일으킨다. 이러한 AMP/ADP 결합과 ATP 결합의 차이는 효소에 대한 탈인산화 상태의 변화로 이어진다.[8] 다양한 단백질 포스파테이스를 통한 AMP-활성 단백질 키네이스의 탈인산화는 촉매 기능을 완전히 비활성화시킨다. AMP/ADP는 γ-소단위체에 결합하고 탈인산화 상태를 유지함으로써 AMP-활성 단백질 키네이스가 불활성화되지 않도록 보호한다.[9]
cAMP[편집]
아데노신 일인산(AMP)은 또한 고리형 아데노신 일인산(cAMP)으로 알려진 고리 구조로도 존재할 수 있다. 특정 세포 내에서 아데닐산 고리화효소는 ATP로부터 cAMP를 만드는데, 이 반응은 일반적으로 에피네프린이나 글루카곤과 같은 호르몬에 의해 조절된다. cAMP는 세포 내 신호 전달에서 중요한 역할을 한다.[10]
같이 보기[편집]
각주[편집]
- ↑ Jauker, Mario; Griesser, Helmut; Richert, Clemens (2015년 11월 23일). “Spontaneous Formation of RNA Strands, Peptidyl RNA, and Cofactors”. 《Angewandte Chemie》 54 (48): 14564–9. doi:10.1002/anie.201506593. PMC 4678511. PMID 26435376.
- ↑ Maiuolo, Jessica; Oppedisano, Francescs; Gratteri, Santo; Muscoli, Carolina; Mollace, Vincenzo (2016년 6월 15일). “Regulation of uric acid metabolism and excretion”. 《International Journal of Cardiology》 213: 8–14. doi:10.1016/j.ijcard.2015.08.109. PMID 26316329.
- ↑ Richter, Erik A.; Ruderman, Neil B. (2009년 2월 11일). “AMPK and the biochemistry of exercise: implications for human health and disease”. 《The Biochemical Journal》 (영어) 418 (2): 261–75. doi:10.1042/BJ20082055. PMC 2779044. PMID 19196246. 2019년 3월 31일에 확인함.
- ↑ Carling, David; Mayer, Faith V.; Sanders, Matthew J.; Gamblin, Steven J. (2011년 7월 18일). “AMP-activated protein kinase: nature's energy sensor”. 《Nature Chemical Biology》 (영어) 7 (8): 512–8. doi:10.1038/nchembio.610. PMID 21769098.
- ↑ Faubert, Brandon; Vincent, Emma E.; Poffenberger, Maya C.; Jones, Russell G. (2015년 1월 28일). “The AMP-activated protein kinase (AMPK) and cancer: many faces of a metabolic regulator”. 《Cancer Letters》 (영어) 356 (2 Pt A): 165–70. doi:10.1016/j.canlet.2014.01.018. PMID 24486219.
- ↑ Hardie, D. Grahame (2011년 9월 15일). “AMP-activated protein kinase—an energy sensor that regulates all aspects of cell function”. 《Genes & Development》 (영어) 25 (18): 1895–1908. doi:10.1101/gad.17420111. ISSN 0890-9369. PMC 3185962. PMID 21937710.
- ↑ Hardie, Grahame (2011년 2월). “Energy sensing by the AMP-activated protein kinase and its effects on muscle metabolism”. 《The Proceedings of the Nutrition Society》 (영어) 70 (1): 92–9. doi:10.1017/S0029665110003915. PMID 21067629.
- ↑ Krishan, Sukriti; Richardson, Des R.; Sahni, Sumit (2015년 3월 1일). “Adenosine monophosphate-activated kinase and its key role in catabolism: structure, regulation, biological activity, and pharmacological activation”. 《Molecular Pharmacology》 (영어) 87 (3): 363–77. doi:10.1124/mol.114.095810. PMID 25422142.
- ↑ Xiao, Bing; Sanders, Matthew J.; Underwood, Elizabeth; Heath, Richard; Mayer, Faith V.; Carmena, David; Jing, Chun; Walker, Philip A.; Eccleston, John F.; Haire, Lesley F.; Saiu, Peter; Howell, Steven A.; Aasland, Rein; Martin, Stephen R.; Carling, David; Gamblin, Steven J. (2011년 4월 14일). “Structure of mammalian AMPK and its regulation by ADP”. 《Nature》 (영어) 472 (7342): 230–3. doi:10.1038/nature09932. PMC 3078618. PMID 21399626.
- ↑ Ravnskjaer, Kim; Madiraju, Anila; Montminy, Marc (2015). 《Metabolic Control》. Handbook of Experimental Pharmacology (영어) 233. Springer, Cham. 29–49쪽. doi:10.1007/164_2015_32. ISBN 9783319298047. PMID 26721678.
참고 문헌[편집]
- Ming D, Ninomiya Y, Margolskee RF (1999년 8월). “Blocking taste receptor activation of gustducin inhibits gustatory responses to bitter compounds”. 《Proceedings of the National Academy of Sciences of the United States of America》 96 (17): 9903–8. doi:10.1073/pnas.96.17.9903. PMC 22308. PMID 10449792.
