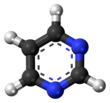
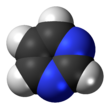
피리미딘
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Pyrimidine[1] | |||
| 체계명
1,3-Diazabenzene | |||
| 별칭
1,3-Diazine
m-Diazine 1,3-Diazacyclohexa-1,3,5-triene | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.005.479 | ||
| KEGG | |||
| MeSH | pyrimidine | ||
PubChem CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C4H4N2 | |||
| 몰 질량 | 80.088 g mol−1 | ||
| 밀도 | 1.016 g cm−3 | ||
| 녹는점 | 20 to 22 °C (68 to 72 °F; 293 to 295 K) | ||
| 끓는점 | 123 to 124 °C (253 to 255 °F; 396 to 397 K) | ||
| Miscible (25 °C) | |||
| 산성도 (pKa) | 1.10[2] (protonated pyrimidine) | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
피리미딘(영어: pyrimidine)은 피리딘과 유사한 방향족 헤테로고리 유기 화합물이다.[3] 피리미딘은 3가지의 다이아진(고리에 2개의 질소 원자를 가지고 있는 6원자 헤테로고리 화합물)들 중 하나로 고리의 1번 위치와 3번 위치에 질소 원자를 가지고 있다.[4] 다른 다이아진들은 피라진(고리의 1번 위치와 4번 위치에 질소 원자를 가지고 있음)과 피리다진(고리의 1번 위치와 2번 위치에 질소 원자를 가지고 있음)이다. 핵산에서 3가지 핵염기는 피리미딘 유도체인 사이토신(C), 티민(T), 유라실(U)이다.
생성 및 역사
[편집]
피리미딘 고리 체계는 핵염기인 사이토신, 티민, 유라실과 티아민(비타민 B1) 및 알록산을 포함하는 치환된 화합물 및 고리가 융합된 화합물 및 유도체로 자연에서 광범위하게 생성된다.[5] 또한 피리미딘은 바르비투르산계 및 HIV 약물인 지도부딘과 같은 많은 합성 화합물에서 발견된다. 요산 및 알록산과 같은 피리미딘 유도체는 19세기 초에 알려져 있었지만,[5]그리모(Grimaux)가 염화 포스포릴의 존재 하에서 요소 및 말론산으로부터 바르비투르산의 제조를 보고한 1879년까지 실험실에서 피리미딘의 합성은 수행되지 않았다.[6] 피리미딘의 체계적인 연구는 1884년에 아세토아세트산 에틸과 아미딘을 축합하여 유도체를 합성한[7] 아돌프 피너[8]와 함께 시작되었다. 피너는 1885년에 "피리미딘"이라는 이름을 최초로 제안했다.[9] 모체 화합물은 1900년 지그문트 가브리엘과 콜먼(Colman)에 의해 바르비투르산을 2,4,6-트라이클로로피리미딘으로 전환시킨 다음, 뜨거운 물에서 아연 분말을 사용하여 환원시키는 방법으로 처음으로 제조되었다.[10][11]
명명법
[편집]피리미딘의 명명법은 간단하다. 그러나 다른 헤테로고리 화합물들과 같이 호변이성질체의 하이드록실기는 이들이 고리형 아마이드 형태로 주로 존재하기 때문에 문제를 발생시킨다. 예를 들어, 2-하이드록시피리딘은 2-피리미돈으로 보다 적절하게 명명된다. 다양한 피리미딘의 관용명의 일부 목록이 존재한다.[12]
물리적 특성
[편집]물리적 특성이 정보 상자에 표시되어 있다. 스펙트럼을 포함한 보다 광범위한 논의는 브라운(Brown) 외에서 확인할 수 있다.[12]
화학적 특성
[편집]앨버트(Albert)에 의한 6원자 헤테로고리 화합물의 분류[13]는 π-결핍으로 기술될 수 있다. 고리에서 음전하 그룹 또는 추가적인 질소 원자에 의한 치환은 π-결핍을 상당히 증가시킨다. 이러한 효과는 또한 염기성도를 감소시킨다.[13]
피리딘과 마찬가지로, 피리미딘에서 π-전자 밀도는 훨씬 더 감소된다. 따라서 친전자성 방향족 치환은 보다 어려운 반면, 친핵성 방향족 치환은 촉진된다. 마지막 반응 유형의 예로는 염소에 의한 2-아미노피리미딘의 아미노기의 변위[14]와 그 역반응[15]을 들 수 있다.
고립 전자쌍의 가용성(염기성도)는 피리딘에 비해 감소한다. 피리딘에 비해, 피리미딘의 N-알킬화 및 N-산화는 더 어렵다. 양성자화된 피리미딘의 pKa 값은 1.23이며, 피리딘의 pKa 값은 5.30이다. 양성자화 및 다른 친전자성 첨가는 제2의 질소에 의한 추가적인 비활성화로 인해 오직 하나의 질소에서만 일어난다.[4] 피리미딘 고리 상의 2번, 4번, 6번 위치는 피리딘, 나이트로벤젠, 다이나이트로벤젠의 경우와 유사하게 전자 결핍이다. 5번 위치는 전자 결핍이 적고, 치환기가 상당히 안정적이다. 그러나 친전자성 치환은 나이트로화 및 할로젠화를 포함하여 5번 위치에서 비교적 용이하다.[12]
피리미딘의 공명 안정화 감소는 치환보다는 첨가 및 고리 절단 반응을 야기할 수 있다. 그러한 징후 중 하나는 딤로드 자리옮김에서 관찰된다.
피리미딘은 운석에서도 발견되지만, 과학자들은 그 기원에 대해 알지 못한다. 피리미딘은 또한 자외선 하에서 유라실로 광분해된다.[16]
합성
[편집]모체가 되는 헤테로고리 체계에서 종종 그러하듯이, 피리미딘의 합성은 일반적이지 않으며, 보통 유도체로부터 작용기를 제거함으로써 수행된다. 폼아마이드와 관련된 1차 합성이 보고되었다.[12]
피리미딘은 전형적으로 β-다이카보닐 화합물과 N-C-N 화합물의 고리화를 포함하는 주요 합성 과정에 의해 생성된다. β-다이카보닐 화합물과 아미딘과의 반응으로 2-치환된 피리미딘을 생성하고, β-다이카보닐 화합물과 요소와의 반응으로 2-피리미돈을 생성하며, β-다이카보닐 화합물과 구아니딘과의 반응으로 2-아미노피리미딘을 생성하는 것이 전형적이다.[12]
피리미딘은 비지넬리 반응을 통해 제조될 수 있다. 많은 다른 방법들은 카보닐기와 다이아민의 축합에 의존하는 데 예를 들어, 싸이오요소와 아세토아세트산 에틸로부터 2-싸이오-6-메틸유라실의 합성,[17] 4,4-다이메톡시-2-뷰탄올과 폼아마이드로부터 4-메틸피리미딘의 합성 반응이 있다.[18]
새로운 방법은 아마이드를 2-클로로-피리딘 및 트라이플루오로메테인설폰산 무수물과 친전자성 활성화 하에서 N-바이닐 아마이드 및 N-아릴 아마이드를 카보나이트릴과 반응시키는 것이다.[19]
 |
반응
[편집]피리딘에 비해 감소된 염기성도로 인해 피리미딘의 친전자성 치환은 덜 용이하다. 양성자화 또는 알킬화는 전형적으로 고리의 질소 원자들 중 하나에서만 일어난다. 과산(過酸, peracid)과의 반응에 의해 모노-N-산화가 일어난다.[4]
피리미딘의 친전자성 C-치환은 전자 결핍이 가장 적은 5번 위치에서 일어난다. 치환된 피리미딘에 대한 나이트로화, 나이트로소화, 아조 커플링, 할로젠화, 설폰화, 폼일화, 하이드록시메틸화, 아미노메틸화가 관찰되었다.[12]
피리미딘의 친핵성 C-치환은 2번, 4번, 6번 위치에서 촉진되어야 하지만, 단지 몇 가지 예시만이 존재한다. 치환된 피리미딘에 대한 아미노화 및 하이드록실화가 관찰되었다. 그리냐르 반응 또는 알킬 리튬 시약과의 반응은 방향족화 후에 4-알킬 피리미딘 또는 4-아릴 피리미딘을 생성한다.[12]
피리미딘에 대한 자유 라디칼 공격이 관찰되었으며, 치환된 피리미딘에 대한 광화학 반응이 관찰되었다.[12] 피리미딘은 수소화되어 테트라하이드로피리미딘을 생성할 수 있다.[12]
뉴클레오타이드
[편집]
핵산에서 발견되는 3가지 핵염기인 사이토신(C), 티민(T), 유라실(U)은 피리미딘 유도체이다.

Chemical structure of cytosine 
Chemical structure of thymine 
Chemical structure of uracil 사이토신 (C) 티민 (T) 유라실 (U)
DNA와 RNA에서 이들 피리미딘 계열 염기는 퓨린 계열 염기와 상보적인 수소 결합을 형성한다. 따라서 DNA에서 아데닌(A)은 티민(T)과, 구아닌(G)은 사이토신(C)과 염기쌍을 형성한다.
RNA에서 아데닌(A)은 티민(T)이 아닌 유라실(U)과, 구아닌(G)은 사이토신(C)과 염기쌍을 형성한다.
아주 드물게 티민이 RNA에 나타나거나 유라실이 DNA에 나타날 수도 있다. 이들 3가지 주요 피리미딘 염기 외에도, 소수의 다른 피리미딘 염기들도 핵산에 존재할 수 있다. 이러한 소수의 피리미딘들은 일반적으로 주요 피리미딘 염기들의 메틸화된 버전이며, 조절 기능을 가지고 있는 것으로 추정된다.[20]
이러한 수소 결합은 고전적인 왓슨-크릭 염기쌍을 형성하게 한다. RNA의 추가적인 2'-하이드록실기가 입체 배치를 확장시켜서 RNA가 수소 결합을 형성할 수 있지만, 다른 수소 결합 모드(동요 염기)는 DNA와 RNA에서 모두 이용가능하다.
이론적 측면
[편집]2015년 3월에 미국 항공우주국(NASA)의 에임스 연구센터의 과학자들은 유라실, 사이토신, 티민을 포함한 DNA 및 RNA와 같은 생물에 존재하는 복잡한 유기 화합물들이 운석에서 발견되는 피리미딘과 같은 출발 물질들을 사용하여 우주 공간과 같은 조건 하의 실험실에서 생성되었다고 보고했다. 우주에서 가장 탄소가 풍부한 화학물질인 다환 방향족 탄화수소와 같이 피리미딘은 적색거성이나 우주진 및 가스 구름에서 형성되었을 수 있다.[21][22][23]
같이 보기
[편집]각주
[편집]- ↑ 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 141쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ Brown, H. C.; 외. (1955). Baude, E. A.; F. C., Nachod, 편집. 《Determination of Organic Structures by Physical Methods》. New York, NY: Academic Press.
- ↑ Gilchrist, Thomas Lonsdale (1997). 《Heterocyclic chemistry》. New York: Longman. ISBN 978-0-582-27843-1.
- ↑ 가 나 다 Joule, John A.; Mills, Keith, 편집. (2010). 《Heterocyclic Chemistry》 5판. Oxford: Wiley. ISBN 978-1-405-13300-5.
- ↑ 가 나 Lagoja, Irene M. (2005). “Pyrimidine as Constituent of Natural Biologically Active Compounds” (PDF). 《Chemistry and Biodiversity》 2 (1): 1–50. doi:10.1002/cbdv.200490173. PMID 17191918. 2017년 2월 15일에 원본 문서 (PDF)에서 보존된 문서. 2020년 9월 14일에 확인함.
- ↑ Grimaux, E. (1879). “Synthèse des dérivés uriques de la série de l'alloxane” [Synthesis of urea derivatives of the alloxan series]. 《Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences》 88: 85–87.

- ↑ Kenner, G. W.; Todd, Alexander (1957). Elderfield, R.C., 편집. 《Heterocyclic Compounds》 6. New York: Wiley. 235쪽.
- ↑ Pinner, A. (1884). “Ueber die Einwirkung von Acetessigäther auf die Amidine” [On the effect of acetylacetonate ester on amidines]. 《Berichte der Deutschen Chemischen Gesellschaft》 A17 (2): 2519–2520. doi:10.1002/cber.188401702173.

- ↑ Pinner, A. (1885). “Ueber die Einwirkung von Acetessigäther auf die Amidine. Pyrimidin” [On the effect of acetylacetonate ester on amidines. Pyrimidine]. 《Berichte der Deutschen Chemischen Gesellschaft》 A18: 759–760. doi:10.1002/cber.188501801161.

- ↑ Gabriel, S. (1900). “Pyrimidin aus Barbitursäure” [Pyrimidine from barbituric acid]. 《Berichte der Deutschen Chemischen Gesellschaft》 A33 (3): 3666–3668. doi:10.1002/cber.190003303173.

- ↑ Lythgoe, B.; Rayner, L. S. (1951). “Substitution Reactions of Pyrimidine and its 2- and 4-Phenyl Derivatives”. 《Journal of the Chemical Society》 1951: 2323–2329. doi:10.1039/JR9510002323.
- ↑ 가 나 다 라 마 바 사 아 자 Brown, D. J.; Evans, R. F.; Cowden, W. B.; Fenn, M. D. (1994). 《The Pyrimidines》. New York, NY: John Wiley & Sons. ISBN 978-0-471-50656-0.
- ↑ 가 나 Albert, Adrien (1968). 《Heterocyclic Chemistry, an Introduction》. London: Athlone Press.
- ↑ Kogon, Irving C.; Minin, Ronald; Overberger, C. G. “2-Chloropyrimidine”. 《Organic Syntheses》 35: 34. doi:10.15227/orgsyn.035.0034.; 《Collective Volume》 4, 182쪽
- ↑ Overberger, C. G.; Kogon, Irving C.; Minin, Ronald. “2-(Dimethylamino)pyrimidine”. 《Organic Syntheses》 35: 58. doi:10.15227/orgsyn.035.0058.; 《Collective Volume》 4, 336쪽
- ↑ Nuevo, M.; Milam, S. N.; Sandford, S. A.; Elsila, J. E.; Dworkin, J. P. (2009). “Formation of uracil from the ultraviolet photo-irradiation of pyrimidine in pure H2O ices”. 《Astrobiology》 9 (7): 683–695. Bibcode:2009AsBio...9..683N. doi:10.1089/ast.2008.0324. PMID 19778279.
- ↑ Foster, H. M.; Snyder, H. R. “4-Methyl-6-hydroxypyrimidine”. 《Organic Syntheses》 35: 80. doi:10.15227/orgsyn.035.0080.; 《Collective Volume》 4, 638쪽
- ↑ Bredereck, H. “4-methylpyrimidine”. 《Organic Syntheses》 43: 77. doi:10.15227/orgsyn.043.0077.; 《Collective Volume》 5, 794쪽
- ↑ Movassaghi, Mohammad; Hill, Matthew D. (2006). “Single-Step Synthesis of Pyrimidine Derivatives”. 《J. Am. Chem. Soc.》 128 (44): 14254–14255. doi:10.1021/ja066405m. PMID 17076488.
- ↑ Nelson, David L.; Cox, Michael M. (2008). 《Principles of Biochemistry》 5판. W. H. Freeman. 272–274쪽. ISBN 978-1429208925.
- ↑ Marlaire, Ruth (2015년 3월 3일). “NASA Ames reproduces the building blocks of life in laboratory” (보도 자료). NASA. 2015년 3월 5일에 원본 문서에서 보존된 문서. 2015년 3월 5일에 확인함.
- ↑ Nuevo, M.; Chen, Y. J.; Hu, W. J.; Qiu, J. M.; Wu, S. R.; Fung, H. S.; Yih, T. S.; Ip, W. H.; Wu, C. Y. R. (2014). “Photo-irradiation of pyrimidine in pure H2O ice with high-energy ultraviolet photons” (PDF). 《Astrobiology》 14 (2): 119–131. Bibcode:2014AsBio..14..119N. doi:10.1089/ast.2013.1093. PMC 3929345. PMID 24512484.
- ↑ Sandford, S. A.; Bera, P. P.; Lee, T. J.; Materese, C. K.; Nuevo, M. (2014년 2월 6일). 《Photosynthesis and photo-stability of nucleic acids in prebiotic extraterrestrial environments》 (PDF). 《Topics of Current Chemistry》. Topics in Current Chemistry 356. 123–164쪽. doi:10.1007/128_2013_499. ISBN 978-3-319-13271-6. PMC 5737941. PMID 24500331., also published as Barbatti, M.; Borin, A. C.; Ullrich, S. (편집.). 〈14: Photosynthesis and photo-stability of nucleic acids in prebiotic extraterrestrial environments〉. 《Photoinduced phenomena in nucleic acids》. Berlin, Heidelberg: Springer-Verlag. 499쪽.