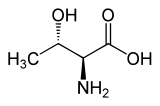
트레오닌
 L-트레오닌의 골격 구조식
| |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
threonine
| |||
| 별칭
2-amino-3-hydroxybutanoic acid
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
| ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider |
| ||
| DrugBank |
| ||
| ECHA InfoCard | 100.000.704 | ||
| EC 번호 |
| ||
| |||
| KEGG |
| ||
PubChem CID
|
| ||
| UNII |
| ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C4H9NO3 | |||
| 몰 질량 | 119.120 g·mol−1 | ||
| (H2O, g/dl) 10.6(30°),14.1(52°),19.0(61°) | |||
| 산성도 (pKa) | 2.63 (카복실기), 10.43 (아미노기)[1] | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
트레오닌(영어: threonine) (기호: Thr 또는 T)[2]은 단백질의 생합성에 사용되는 α-아미노산이다. 트레오닌은 α-아미노기(생물학적 조건에서 양성자화된 −NH+
3 형태), α-카복실기(생물학적 조건에서 탈양성자화된 −COO− 형태) 및 곁사슬인 하이드록실기를 포함하고 있다. 트레오닌은 극성 비전하 아미노산으로 분류된다. 트레오닌은 필수 아미노산으로 인체에서 합성되지 않으며 음식을 통해 섭취해야 한다. 트레오닌은 대장균과 같은 세균에서 아스파르트산으로부터 합성된다.[3] 트레오닌은 AC로 시작하는 모든 코돈(ACU, ACC, ACA, ACG)에 의해 암호화되어 있다.
트레오닌의 곁사슬은 보통 수소 결합되어 있다. 형성되는 가장 일반적인 작은 모티프는 ST 턴, ST 모티프(보통 α 나선의 시작 부분) 및 ST 스테이플(일반적으로 α 나선의 중간 부분)이며, 이들은 세린과의 상호작용을 기반으로 한다.
변형
[편집]트레오닌 잔기는 수 많은 번역 후 변형에 민감하다. 곁사슬의 하이드록실기는 O-결합 글리코실화를 겪을 수 있다. 또한 트레오닌 잔기는 트레오닌 키네이스에 의해 인산화된다. 트레오닌의 인산화된 형태는 포스포트레오닌이라고 할 수 있다. 포스포트레오닌은 3개의 잠재적인 배위 자리(카복실기, 아미노기, 인산기)를 가지고 있으며, 생물에서 생성되는 인산화된 리간드와 금속 이온 사이의 배위 방식을 결정하는 것은 생물학적 과정에서 포스포트레오닌의 기능을 설명하는 데 중요하다.[4]
역사
[편집]트레오닌은 20가지의 단백질생성성 아미노산들 중에서 가장 나중에 발견되었다. 트레오닌은 1936년에 커티스 마이어(Curtis Meyer)와 윌리엄 커밍 로즈[5]가 공동으로 발견했다. 4탄당인 트레오스의 유도체로 분자식이 C4H8O5인 트레온산과 구조가 유사하기 때문에 트레오닌이라고 명명되었다.[6]
입체 이성질체
[편집]트레오닌은 아이소류신과 함께 2개의 입체 중심이 있는 2가지 단백질생성성 아미노산 중 하나이다. 트레오닌은 (2S,3R), (2R,3S), (2S,3S), (2R,3R)의 입체배치를 갖는 4가지 가능한 입체 이성질체로 존재할 수 있다. 그러나 L-트레오닌이라는 이름은 하나의 단일 입체 이성질체인 (2S,3R)-2-아미노-3-하이드록시뷰탄산에 사용된다. 자연계에는 거의 존재하지 않는 두 번째 입체 이성질체 (2S,3S)를 L-알로트레오닌이라고 한다.[7] 2가지 다른 입체 이성질체인 (2R,3S)-2-아미노-3-하이드록시뷰탄산과 (2R,3R)-2-아미노-3-하이드록시뷰탄산은 그다지 중요하지 않다.
생합성
[편집]트레오닌은 필수 아미노산으로 인체에서 합성되지 않으며, 식사를 통해 섭취해야 한다. 성인의 경우 매일 체중 1 kg당 20 mg의 트레오닌이 필요하다.[8] 식물과 미생물에서 트레오닌은 α-아스파르틸-세미알데하이드 및 호모세린을 거쳐 아스파르트산으로부터 합성된다. 호모세린은 O-인산화를 겪는다. 이 인산 에스터는 하이드록실기의 재배치와 함께 가수분해를 겪는다.[9] 트레오닌의 일반적인 생합성에 관여하는 효소는 다음과 같다.
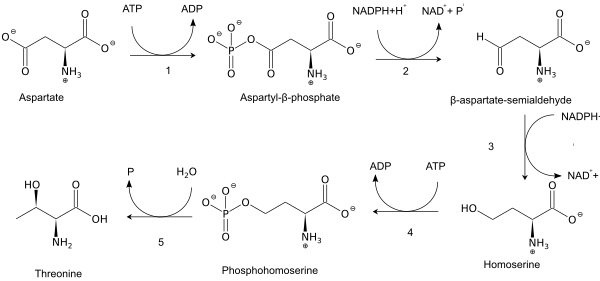 |
물질대사
[편집]트레오닌은 적어도 세 가지 방식으로 대사된다.
- 많은 동물에서 트레오닌은 L-트레오닌 3-탈수소효소에 의해 피루브산으로 전환된다. 이 경로의 대사 중간생성물은 CoA와 싸이올분해를 거쳐 아세틸-CoA와 글리신을 생성할 수 있다.
- 사람에서 L-트레오닌 3-탈수소효소 유전자는 비활성 위유전자이므로[10] 트레오닌은 α-케토뷰티르산으로 전환된다. 첫 번째 단계의 메커니즘은 세린 탈수효소에 의해 촉매되는 것과 유사하며, 세린 탈수효소 및 트레오닌 탈수효소 반응은 아마도 동일한 효소에 의해 촉매된다.[11]
- 많은 생물에서 이는 추가적인 대사를 준비하는 키네이스에 의해 O-인산화된다. 이것은 세균에서 코발라민(비타민 B12) 생합성의 일부로 특히 중요하다. 그 이유는 대사산물이 비타민의 곁사슬에 결합되기 위해 1-아미노프로판-2-올로 전환되기 때문이다.[12]
- 트레오닌은 쥐의 뇌와 간에서 L-카르니틴의 내인성 생성 동안 글리신을 합성하는 데 사용된다.[13][14]
공급원
[편집]트레오닌이 많이 함유된 식품으로는 코티지 치즈, 가금류, 생선, 고기, 렌즈콩, 검정거북콩,[15] 및 참깨가 있다.[16]
라세미 트레오닌은 아세트산 수은(II)을 사용하여 알파-기능화에 의해 크로톤산으로부터 제조할 수 있다. threonine can be prepared from crotonic acid by alpha-functionalization using mercury(II) acetate.[17]
같이 보기
[편집]각주
[편집]- ↑ Dawson, R.M.C., et al., Data for Biochemical Research, Oxford, Clarendon Press, 1959.
- ↑ “Nomenclature and Symbolism for Amino Acids and Peptides”. IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. 2008년 10월 9일에 원본 문서에서 보존된 문서. 2018년 3월 5일에 확인함.
- ↑ Raïs, Badr; Chassagnole, Christophe; Lettelier, Thierry; Fell, David; Mazat, Jean-Pierre (2001). “Threonine synthesis from aspartate in Escherichia coli cell-free extracts: pathway dynamics”. 《Biochem J》 356 (Pt 2): 425–32. doi:10.1042/bj3560425. PMC 1221853. PMID 11368769.
- ↑ Jastrzab, Renata (2013). "Studies of new phosphothreonine complexes formed in binary and ternary systems including biogenic amines and copper(II)". Journal of Coordination Chemistry. 66 (1): 98–113. doi 10.1080/00958972.2012.746678
- ↑ 《A Dictionary of scientists.》. Daintith, John., Gjertsen, Derek. Oxford: Oxford University Press. 1999. 459쪽. ISBN 9780192800862. OCLC 44963215.
- ↑ Meyer, Curtis (1936년 7월 20일). “The Spatial Configuation of Alpha-Amino-Beta-Hydroxy-n-Butyric Acid” (PDF). 《Journal of Biological Chemistry》 115 (3): 721–729. doi:10.1016/S0021-9258(18)74711-X.
- ↑ “Nomenclature and symbolism for amino acids and peptides (Recommendations 1983)”. 《Pure and Applied Chemistry》 56 (5): 601, 603, 608. 1984년 1월 1일. doi:10.1351/pac198456050595.
- ↑ Institute of Medicine (2002). 〈Protein and Amino Acids〉. 《Dietary Reference Intakes for Energy, Carbohydrates, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids》. Washington, DC: The National Academies Press. 589–768쪽. doi:10.17226/10490. ISBN 978-0-309-08525-0.
- ↑ 틀:Lehninger3rd.
- ↑ Stipanuk, Martha H.; Caudill, Marie A. (2013). 《Biochemical, Physiological, and Molecular Aspects of Human Nutrition – E-Book》 (영어). Elsevier Health Sciences. ISBN 9780323266956.
- ↑ Bhardwaj, Uma; Bhardwaj, Ravindra. 《Biochemistry for Nurses》 (영어). Pearson Education India. ISBN 9788131795286.
- ↑ Fang, H; Kang, J; Zhang, D (2017년 1월 30일). “Microbial production of vitamin B12: a review and future perspectives.”. 《Microbial Cell Factories》 16 (1): 15. doi:10.1186/s12934-017-0631-y. PMC 5282855. PMID 28137297.
- ↑ Adeva-Andany, M; Souto-Adeva, G; Ameneiros-Rodríguez, E; Fernández-Fernández, C; Donapetry-García, C; Domínguez-Montero, A (January 2018). “Insulin resistance and glycine metabolism in humans.”. 《Amino Acids》 50 (1): 11–27. doi:10.1007/s00726-017-2508-0. PMID 29094215. S2CID 3708658.
- ↑ Dalangin, R; Kim, A; Campbell, RE (2020년 8월 27일). “The Role of Amino Acids in Neurotransmission and Fluorescent Tools for Their Detection.”. 《International Journal of Molecular Sciences》 21 (17): 6197. doi:10.3390/ijms21176197. PMC 7503967. PMID 32867295.
- ↑ “Error”. 《ndb.nal.usda.gov》. 2018년 11월 16일에 원본 문서에서 보존된 문서. 2013년 5월 29일에 확인함.
- ↑ “SELF Nutrition Data - Food Facts, Information & Calorie Calculator”. 《nutritiondata.self.com》. 2018년 3월 27일에 확인함.
- ↑ Carter, Herbert E.; West, Harold D. (1940). “dl-Threonine”. 《Organic Syntheses》 20: 101.; 《Collective Volume》 3, 813쪽.