인간면역결핍 바이러스
|
| ||
|---|---|---|
 | ||
| 생물 분류ℹ️ | ||
| 군: | VI (ssRNA-RT 바이러스) | |
| 과: | 레트로바이러스과 | |
| 속: | 렌티바이러스속 | |
| 종 | ||
| ||
인간면역결핍 바이러스(人間免疫缺乏 바이러스, human immunodeficiency virus, HIV)는 발병하게 되면 AIDS로 진행하는, 인간의 면역체계를 파괴하는 레트로바이러스이다. 기회감염에 의한 사망에 이를 수 있게끔 인간의 면역체계를 무너뜨리는 AIDS를 일으키는 병원체이다.
질병관리본부의 '문답으로 알아보는 에이즈 상식' 자료에 따르면 HIV와 에이즈(AIDS)는 다른 말이다. HIV는 바이러스를 말하며 에이즈는 면역이 결핍돼 나타나는 상태를 뜻한다. HIV에 걸린 사람을 에이즈 환자라고 부르지 않는다. HIV 감염인이란 HIV에 걸린 모든 사람을 말하며 이 중에서 질병이 나타난 사람을 에이즈 환자라고 부른다. 아무런 치료를 받지 않아도 면역결핍으로 사망에 이르기까지 10~12년 정도 걸린다. 올바른 관리를 한다면 30년 이상 살 수 있다. 현재 에이즈는 만성질환으로 분류되고 있다.[1] 한국인 최초의 HIV 감염자는 현재 28년째 살아있다.[2]
(이전에는 인간 T-세포 림프종 바이러스-III(Human T-Lymphotropic Virus-III, HTLV-III), 림프절 종창 연관 바이러스(Lymphadenopathy-Associated Virus, LAV), AIDS 연관 레트로바이러스(AIDS-Associated Retrovirus, ARV)라고도 불렸으나, 현재에는 이 명칭들은 거의 사용되지 않는다.)
HIV는 수혈, 정액, 질액, 쿠퍼액, 모유 등의 체액으로 전염된다. HIV는 자유롭게 떠다니는 바이러스 상태나 체액속에서 감염된 백혈구의 형태로 존재한다. HIV의 가장 주요한 4가지 감염경로는 감염된 사람과의 성적 행위, 오염된 주사바늘, 수직감염(모유로 인한 감염과 임신 중 모체에서 태아로의 감염), 감염된 혈액제재 투여이다.(혈액에 대한 검사는 수혈이나 혈액제제로 인한 HIV감염을 대부분 막을 수 있다.)
세계보건기구(WHO)는 HIV 감염추세가 세계적인 유행(판데믹)이라고 하였다. 1981년부터 2006년까지 AIDS로 인하여 2천 5백만 명 이상의 사람이 사망했으며 세계인구의 0.6%가 HIV에 감염되어 있다고 발표했다.[3] 2005년 한 해만 AIDS는 약 2천4백–3천3백만(그 중 57만 이상이 어린이)의 목숨을 앗아간 것으로 추정된다. 사망자의 1/3이 경제성장이 없고 빈곤이 극심한 아프리카의 사하라 이남지방에 집중되어 있다.[4] 또한 HIV는 아프리카에서 9천만명을 감염시켜 최소 천8백만명의 고아를 생기게 한 원인이라고 한다.[5] 항레트로바이러스제 처방은 HIV감염으로 인한 사망률을 낮춘다. 하지만 모든 국가에서 항레트로바이러스제의 주기적인 투약이 가능한 것은 아니다.[6]
HIV는 주로 헬퍼 T 세포(T세포의 CD4+ 부위), 대식세포, 수지상 세포 등의 살아있는 면역세포들을 감염시킨다. HIV에 감염되면 CD4+를 가진 T 세포의 개체 수가 현격히 감소하고 감소되는 3가지의 원인기작은 다음과 같다. 첫 번째, 감염된 세포의 바이러스성 괴사. 두 번째, 감염된 T세포의 아포토시스(세포자살) 확률 증가. 세 번째, CD8 세포독성 림프구가 감염된 CD4+ T 세포를 인지하여 파괴. CD4+ T 세포의 수가 치명적인 수준 이하로 내려가면 세포매개성 면역이 상실되어 점차 기회감염에 쉽게 노출된다.[7] HIV가 AIDS로 진행되는 데는 바이러스, 숙주, 환경의 요인에 의해 영향을 받는다. HIV 치료는 AIDS 진행을 지체시킨다. 대체로 HIV감염 10년 안에 AIDS로 진행되며 이보다 느릴 수도 빠를 수도 있다.[8][9] 에이즈 환자의 생존기간을 연장시켜줄 수 있는 약제로는 항레트로바이러스제가 있다. HIV감염자의 생존기대치를 높이는 효과가 있으며, AIDS로 진행되더라도 평균 5년 이상 생존기간을 연장할 수 있다고 알려져 있다.(2005년 기준)[10] AIDS환자가 레트로바이러스제를 처방받지 않으면 보통 1년이내 사망하는 것으로 알려져 있다.[11] 2010년 처음으로 AIDS 완치에 성공한 사례가 발표되었다. 이 환자는, HIV 감염에 저항력이 있는 T세포를 생산하는 기증자로부터 골수 줄기세포 이식을 받았는데, 그 이후 저항력이 있는 T세포를 스스로 생산하기 시작하면서 HIV를 몸속으로부터 퇴치하는데 성공하였다.[12]
분류
[편집]HIV는 레트로바이러스과의 렌티바이러스속에 속한다.[13][14] 렌티바이러스는 형태학적인 측면이나 생물학적 특징에서 많은 공통점을 가지고 있다. 렌티바이러스는 많은 생물종을 감염시킬 수 있으며, 긴 잠복기를 가진 만성 질환의 원인이라는 특징을 공통적으로 가지고 있다.[15] 또 이들은 모두 한 가닥의 활성(positive-sense)을 가진 RNA 바이러스이며 외피에 싸여있다. 일단 목표 세포에 침입하게 되면, 바이러스의 RNA는 바이러스 입자에 포함된 역전사효소를 통해 두 가닥의 DNA로 변환된다. 이 바이러스 DNA는 인테그레이스를 암호화하고 있어 이 효소를 만들어 효소와 숙주세포의 공통인자와의 작용에 의해 숙주의 DNA와 결합한다.[16] 결합된 DNA를 숙주 세포가 전사하면 새로운 바이러스가 생산되는 것이다. 바이러스가 세포를 감염시키면 두 가지 경로가 있다. 첫째는 잠복하여 세포가 정상적인 기능을 하게끔 하는 것이고, 둘째는 활성을 띄고 다른 세포를 감염시키도록 많은 수의 바이러스 입자를 복제하여 퍼뜨리는 것이다.
HIV에는 HIV-1, HIV-2 2종류가 있는 것으로 알려져 있다. HIV-1은 처음 발견되었을 당시 LAV라고 불렸으며 독성과 감염력이 더 강하고, 전 세계 HIV감염의 주요원인 바이러스이다.[17] HIV-2는 HIV-1보다 노출되었을 때 감염될 확률이 상대적으로 낮아 대체로 서아프리카에 한정되어 분포하고 있다.[18]
HIV종 비교
[편집]| 종 | 독성 | 감염력 | 유행지역 | 유래한 것으로 추정되는 생물 |
|---|---|---|---|---|
| HIV-1 | 높음 | 높음 | 전 세계 | 침팬지 |
| HIV-2 | 낮음 | 낮음 | 서아프리카 | 검은망가베이원숭이(sooty mangabey) |
증세 및 증상
[편집]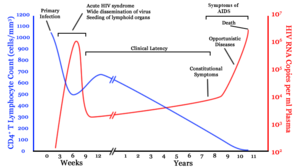
HIV-1의 감염은 CD4+ T 세포 수의 점진적인 감소와 바이러스 양의 증가를 수반한다. 감염단계는 CD4+ T세포 수와 혈액 내 HIV 수준에 따라 결정된다.
감염 단계
[편집]HIV 감염은 기본적으로 배양기, 급성감염, 잠복기, AIDS 4단계로 나뉜다.
- 배양기 :무증상이며 2~4주 정도 지속된다.
- 급성감염 : 평균 28일 정도 지속되며 발열, 림프절증, 인두염, 발진(뾰루지), 근육통, 오한, 구강과 식도의 통증 등의 증상이 나타날 수 있다.
- 잠복기 : 증상이 거의 없으며 무증상일 수도 있다. 2주에서 20년 이상 지속될 수 있다.
- AIDS : HIV감염의 마지막 단계로 다양한 기회감염의 증상을 보인다.
프랑스 병원 환자를 대상으로 한 연구에서 HIV-1 감염자의 약 0.5%가 항레트로바이러스 재제의 투약없이도 높은 수준의 CD4 T세포와 임상적으로 측정할 수 없을 정도로 낮은 수준의 바이러스 양을 가진 상태를 유지한다는 것을 밝혀냈다. 이러한 사람들을 HIV조절자 또는 장기 비진행자로 분류한다.[19]
급성 HIV 감염
[편집]
HIV감염은 보통 감염자에서 비감염자로 체액이 이동함으로써 발생한다. 급성감염기는 바이러스 복제가 빠르게 일어나는 시기로 HIV에 노출된 사람의 말초혈액 중 바이러스의 수가 1 mL 당 수백만개에 이르게 된다.[20] 이러한 바이러스의 증가는 체내에서의 CD4+ T세포 수의 현저한 감소를 동반하고 HIV감염세포를 죽이는 CD8+ T세포의 활성화를 가져와 항체를 생산하게끔 하고 혈청전환이 일어난다. 바이러스 수가 증가하다 감소하고 CD4+ T세포 수 또한 감소하다 1 µL 당 800개 정도를 회복하기 때문에 (정상수치는 1 µL 당 1200개) CD8+ T세포의 활성화가 바이러스 수준을 조절하는 데 중요한 역할을 한다고 여겨지고 있다. CD8+ T세포가 제대로 기능을 하면 바이러스를 제거하지는 못해도 질병의 진전을 막고 보다 나은 예측을 가능하게끔 한다.[21] 급성감염기간 동안(바이러스 노출 후 보통 2~4주) 대부분의 감염자(80~90%)는 급성HIV감염이라 불리는 독감이나 전염성단구증가증과 같은 증상을 앓는다. 주요 증상은 발열, 림프절증, 인후염, 발진, 근육통, 입과 식도의 통증이며 덜 일반적이지만 두통, 메스꺼움, 구토, 간/비장의 비대, 몸무게감소, 칸디다증, 신경장애 증상이 있다. 사람에 따라 경험하는 증상은 각각 다르며 모든 증상을 경험하기도 하고, 또 일부를 경험하기도 하며, 혹은 증상이 없을 수도 있다. 증상의 지속기간 또한 다른데 최소 일주일이고 평균 28일정도 유지된다.[22] 증상들의 비특이적인 속성 때문에 감염자들은 HIV감염 증상이라고 인지하지 못하는 경우가 많다. 병원에서 감염자들이 진료를 받더라도 일반적인 전염병으로 인한 같은 증상으로 오진되는 경우가 많다. 모든 경우에 있어 증상이 나타나는 것은 아니며 다른 일반적인 전염병에 의해 증상이 나타나기도 하기 때문에 결론적으로 초기 증상은 HIV감염 진단에 사용되지 않는다. 하지만 감염자는 급성감염기간 동안 쉽게 질병을 앓기 때문에 HIV 증후군으로 인지하는 것은 치료를 위해 중요하다.[23]
잠복기
[편집]강한 면역적인 방어로 인해 혈중 바이러스 수는 줄어들고 임상적인 잠복기로 들어서기 시작한다. 잠복기는 2주에서 20년으로 개인별로 매우 다르다. 감염초기에 HIV는 난포성 수지상세포(FDC)에 붙잡혀 림프계에서 활성을 띈다.[24] CD4+ T세포가 풍부한 조직은 감염되고 바이러스 조각은 감염된 세포와 자유로운 바이러스 형태로 축적된다. 잠복기의 감염자는 여전히 다른 사람을 전염시킬 수 있다. CD4+ CD45RO+ T세포는 대부분의 전바이러스(proviral load)를 운반한다.[25]
- 더 자세한 사항은 AIDS 진단, AIDS 증상, HIV감염과 질병에 대한 WHO 질병단계체계 참조
CD4+ T세포의 수가 µL당 200개 이하의 치명적인 수준까지 떨어지면 세포매개성 면역은 사라지고 다양한 미생물에 의한 기회감염 가능성이 높아진다. 일반적인 기회감염과 종양은 대부분 CD4+ T세포의 강력한 세포매개성 면역에 의해 조절되지만 AIDS환자의 경우 조절능력이 떨어져 기회감염에 쉽게 노출되는 것이다. 주요 증상으로 완만하고 이유를 알 수 없는 체중감소, 기도감염의 재발(부비강염, 기관지염, 기관염, 인후염), 전립선염, 피부발진, 구강궤양이 자주 나타난다. 일반적으로 구강 칸디다균과 Mycobacterium tuberculosis에 대한 저항력이 떨어져 구강칸디다증, 결핵에 쉽게 걸리게 된다. 이후 잠복해있던 헤르페스 바이러스가 단순 헤르페스 발진, 대상포진, 엡스타인바 바이러스에 유도된 림프종이나 카포시육종을 재발시켜 악화시킬 수 있다. Pneumocystis jirovecii에 의해 진균성 폐렴이 일반적으로 나타나며 때때로 치명적이다. AIDS의 마지막단계는 사이토메갈로바이러스 또는 미코박테리움아비움균 등이 더욱 두드러진다. 모든 AIDS환자가 앞에서 열거한 질병이나 종양에 한정되어 발병하는 것은 아니며 덜 우세하지만 중요한 종양이 생기거나 전염병들에 걸리기도 한다.
병태생리학
[편집]전염
[편집]| 감염경로 | 만번 노출당 감염 추정치 | |||
|---|---|---|---|---|
| 수혈 | 9,000[27] | |||
| 출산 | 2,500[28] | |||
| 주사제 바늘 공동사용 | 67[29] | |||
| 주사침상해(경피주사바늘) | 30[30] | |||
| 항문성교(피삽입)* | 50[31][32] | |||
| 항문성교(삽입)* | 6.5[31][32] | |||
| 이성성관계(피삽입)* | 10[31][32][33] | |||
| 이성성관계(삽입)* | 5[31][32] | |||
| 구강성교(피삽입)*§ | 1†[32] | |||
| 구강성교(삽입)*§ | 0.5†[32] | |||
| * 콘돔사용이 없다고 가정 § 구강성교는 남자의 경우를 의미 | ||||
| † "가장 나은 추정치" | ||||
주로 3가지의 HIV 감염경로가 알려져 있다. HIV-1에 비해 HIV-2는 성관계나 출산으로 인한 전염이 매우 적게 이루어진다.
성관계
[편집]HIV감염의 주된 원인은 안전하지 않은 성적 행위이다. 성관계로 인한 전염은 감염자의 체액이 비감염자의 생식기, 구강, 항문, 점막에 접촉하면서 이루어진다. 소득이 높은 국가에서는 여자에서 남자로 전염이 행위당 0.04%이고 남자에서 여자로의 전염이 행위당 0.08%이다. 다양한 이유로 소득이 낮은 국가에서는 이들 비율이 4배에서 10배정도 높다.[34] 올바르고 지속적인 콘돔의 사용은 성행위로 인한 HIV감염위험을 85%정도 줄일 수 있다.[35] 하지만 살정제는 감염비율을 높일 수 있다.[36][37][38]
1999년 이전 아프리카 남부사하라지역에서 수행된 27개의 관찰연구를 메타분석한 결과 남자의 할례(포경수술)가 HIV감염위험을 줄이는 것으로 보였다.[39] 하지만 HIV와 할례와의 상관관계를 재조사 결과 혼란변인에 의한 것으로 밝혀졌다.[40] 더불어 할례 중 살균되지 않은 칼날에 의한 HIV 확산가능성도 제기되었다.[41] 할례를 받지 않은 남성을 대상으로 무작위적으로 살균된 환경에서 포경을 하도록 하고 일부는 하지 않도록 실험을 하였다. 서아프리카,[42] 케냐,[43] 우간다[44]에서 실험을 실행하였으며 이성간 성관계로 인한 HIV전염이 각각 60%, 53%, 51%씩 감소하는 것으로 나타났다. 결론적으로 WHO와 UNAIDS 사무국에 의해 소집된 전문가 집단은 이 사실을 이성관계로 인한 남성의 HIV 감염위험을 낮출 수 있는 중요한 발견으로 인지하고 남성의 포경수술을 권고했다.[45]
혈액과 혈액제제
[편집]일반적으로 감염된 혈액이 상처에 접촉하면 HIV가 전염될 수 있다고 알려져있다. 이 경우 정맥주사, 혈우병, 수혈 수해자(대부분의 선진국에서 수혈 전 HIV검사를 함에도 불구하고)가 감염될 수 있다. 주사침의 재사용과 같은 주사도구의 위생기준이 지켜지지 않는 의료서비스를 받는 지역에 있는 사람 또한 감염될 수 있다. 간호사, 연구자, 의사들과 같은 의료종사자도 감염되기도 하지만, 보편적인 예방책으로 혈액접촉을 피하도록 요구되므로 혈액에 의한 HIV감염은 드물다. 문신, 피어싱, 난절법 또한 시술자와 피시술자에게 모두 감염위험이 존재한다.
HIV는 낮은 농도로 감염자의 침, 눈물, 소변속에 존재하며 이들 분비물에 의해 감염된 기록은 없고 감염가능성 또한 무시할 정도로 낮다.[46] 모기에 의한 HIV 전염은 불가능하다.[47]
수직 감염
[편집]어머니에게서 아이에게로 임신 중이나 분만, 수유시 바이러스 전염이 일어날 수 있다. 치료없이 출산시 전염비율은 2.5%에 이른다.[28] 하지만 항레트로바이러스제 처방과 제왕절개를 병행하면 전염비율은 1%수준으로 낮아진다.[28] 출생 후 수직감염은 수유를 피함으로써 막을 수 있다. 이환률이 현저하게 낮아지지만 수유를 배제하고 아이에게까지 약물치료를 병행하면 임상적으로 전염을 막는 데 효과가 있다고 알려져 있다.[48]
여러번 감염
[편집]다른 바이러스와 다르게 HIV감염은 특히 유전적으로 먼 바이러스의 경우 추가적인 감염에 대하여 면역력이 결여되어 있다. 계통분기군간(inter-clade) 계통분기군내(intra-clade) 여러번감염이 보고된 바 있고[49] 병의 진행이 보다 빨리 진행되는 것과 연관되어 있다.[50] 여러번 감염은 두 번째 병원체의 획득 시기에 따라 2가지 범주로 분류된다. 동시감염은 두 가지 병원체에 동시에 감염되는 것(또는 감염시기가 분간되지 않을 정도로 비슷한 경우)이고, 재감염 또는 중복감염은 두 번째 병원체가 첫 번째 병원체감염과 상당한 시간적인 간격이 있는 경우이다. 두 경우 모두 HIV의 급성감염과 만성감염의 경우에 있어 여러번감염이 보고된 바 있다.[51][52][53][54]
HIV의 구조와 유전체
[편집]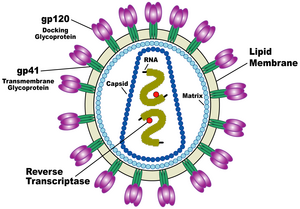

HIV의 구조는 다른 레트로바이러스와 다르며 아주 복잡하다. 전체적으로 구형에 가까우며,[55] 지름은 약 120nm로 적혈구보다 60배 정도 작지만, 바이러스 중에서는 큰 편이다.[56] 유전체는 아홉 개의 바이러스 유전인자를 암호화하고 있는 2벌의 양성 단일가닥 RNA로 구성되어 있다. RNA는 바이러스 단백질 p24[57] 2,000개 가량으로 구성된 원뿔형의 캡시드로 둘러싸여 있다. 바이러스 내부는 단일가닥 RNA와 핵캡시드 단백질 p7과 비리온단백질 형성에 필수적 효소(역전사효소, 단백질분해효소, 리보뉴클레이스, 인테그레이스)로 꽉 들어차있다. 바이러스 단백질 p17로 구성된 기질이 비리온의 보전을 위해 다시 캡시드를 둘러싸고 있다.[57] 기질은 다시 인지질(지방산의 일종)2중층으로 이루어진 바이러스막에 둘러 싸여 있다. 바이러스막은 숙주세포로부터 새로 바이러스가 출아되어 나올 때 가장 먼저 형성된다. 생성 중인 바이러스막은 숙주세포의 세포막에 묻혀있는 형태로 숙주세포의 단백질과 바이러스 입자 표면으로 비어져 나오는 70여개의 복합 HIV단백질로 구성된다.[57] Env라고 알려진 복합HIV단백질은glycoprotein120 3분자로 구성된 모자와 gp41 3분자로 구성된 줄기(단백질 구조물을 바이러스막에 고정하는 역할을 함)로 구성되어 있다.[58] 당단백질 결합체는 감염주기를 시작하는데 중요한데 바이러스가 목표세포에 부착하여 융합하는 것을 가능하게 한다.[58] 바이러스의 2가지 표면당단백질 특히 gp120은 향후 치료제나 백신의 개발대상으로 여겨진다.[59] RNA유전체는 최소 7개의 구조적 경계(LTR, TAR, RRE, PE, SLIP, CRS, INS)를 가지고 9kB 정도의 사이즈로 5'에서 3'쪽으로부터 9개의 유전인자(gag, pol, env, tat, rev, nef, vif, vpr, vpu, tev)를 가진다. 9개의 유전인자는 19종의 단백질을 암호화하고 있으며, gag, pol, env 이 3개의 유전자는 새로운 바이러스를 만드는 데 필요한 구조 단백질을 만드는 데 필요한 정보를 가지고 있다.[57] env는 gp160(이후 바이러스 효소에 의해 gp120, gp41로 쪼개진다. 바이러스막 단백질 구성요소)으로 불리는 단백질을 암호화하고 있다. 나머지 6개의 유전자(tat, rev, nef, vif, vpr, vpu (HIV-2의 경우 vpx))는 HIV의 세포를 감염시키거나 바이러스를 복제하거나 병을 유발하는 능력을 조절하는 단백질에 대한 조절인자이다.[57] 2개의 Tat 단백질(p14, p16)은 TAR RNA에 결합하여 작동하는 LTR 프로모터인자에 대한 활성제이다. TAR은 아포토시스 유전자(ERCC1과 IER3)를 조절하는 마이크로RNA에 의해 처리될 수도 있다.[60][61] Rev 단백질(p19)는 RNA를 PRE RNA 분자에 결합하여 핵에서 세포질로 옮기는 데 관련이 있다. Vif단백질(p23)은 APOBEC3G(DNA:RNA 하이브리드의 아민을 제거하거나 Pol 단백질을 간섭하는 세포 단백질)의 기능을 저해하며 Vpr단백질(p14)는 숙주세포를 G2/M단계에서 묶어 세포분열을 막는다. Nef단백질(p27)은 T세포의 CD4(주요 바이러스 수용체)뿐만 아니라 MHC class I, MHC class II분자를 저해한다.[62][63][64] Nef는 또한 SH3도메인과 상호작용한다. Vpu단백질(p16)은 감염된 세포로부터 새로운 바이러스 입자를 방출하는 데 영향을 준다.[57] Gag 유전자는 바이러스 입자를 만드는 중심이 되는 매트릭스 단백질 (MA, Gag p17)과 캡시드 단백질 (CA, Gag p24), 핵산캡시드 (NC, Gag p7)등을 발현하는 유전자이며, Pol 유전자는 바이러스 증식 관련 효소 유전자를 포함하는데, 바이러스 RNA의 역전사효소 발현에 관여하는 RT 부분과 단백질 분해효소를 담당하는 PR, 인티그라제 관련 부분인 IN등으로 구성된다. 이 외에 Tat 유전자는 감염 과정에서 바이러스의 증식을 활성화시키는 조절인자를 발현하는 것으로 알려져 있으며, Nef 유전자는 반대로 LTR 부분과 함께 바이러스의 증식을 억제시키는 역할을 하는 것으로 알려져 있다. 전체 HIV RNA의 양쪽 끝부분에는 같은 염기 서열이 반복적으로 존재하는 LTR (Long Term Repeat)가 붙어있다. LTR부위는 새로운 바이러스의 생산을 조절하는 스위치 역할을 하거나 HIV나 숙주세포의 단백질에 의해 유발될 수 있다. 레트로바이러스 Psi요소는 바이러스 유전체를 포장하고 Gag와 Rev단백질에 의해 인지되는 데 관련이 있다. SLIP 요소(TTTTTT)는 기능적인 Pol을 만들기 위해 필요한 Gag-Pol 해독구조에서 구조이동과 관련이 있다.[57]
에이즈 음모론
[편집]HIV분야에 저명한 전문가가 아닌 과학자[65]를 포함한 일부의 사람들은 HIV와 AIDS의 관계나[66] HIV진단과 치료방법의 유효성[65][67]에 대하여 의문을 가지고 있다. AIDS 부정론이라 불리는 이러한 주장은 전 세계 과학단체가 조사해왔으며 부정되었다.[68][모호한 표현]
남아프리카 지역 국가에서 AIDS 부정론이 공식적으로 정부의 옹호를 받고 있는 만큼 AIDS 부정론은 정치적인 영향력을 가지고 있다. [69][70][71][모호한 표현]
같이 보기
[편집]각주
[편집]- ↑ <키스만 해도 HIV감염?…에이즈에 대한 오해와 진실>[깨진 링크(과거 내용 찾기)]
- ↑ 국내 첫 HIV 감염 환자, 28년째 치료받으며 생존
- ↑ Joint United Nations Programme on HIV/AIDS (2006). 〈Overview of the global AIDS epidemic〉 (PDF). 《2006 Report on the global AIDS epidemic》 (PDF). 2006년 6월 8일에 확인함.
- ↑ Greener, R. (2002). 〈AIDS and macroeconomic impact〉. S, Forsyth (ed.). 《State of The Art: AIDS and Economics》. IAEN. 49–55쪽. 2010년 1월 31일에 원본 문서에서 보존된 문서. 2021년 3월 10일에 확인함.
- ↑ Joint United Nations Programme on HIV/AIDS. “AIDS epidemic update, 2005” (PDF). 2006년 4월 4일에 원본 문서 (PDF)에서 보존된 문서. 2006년 2월 28일에 확인함.
- ↑ Palella, F. J. Jr, Delaney, K. M., Moorman, A. C., Loveless, M. O., Fuhrer, J., Satten, G. A., Aschman and D. J., Holmberg, S. D. (1998). “Declining morbidity and mortality among patients with advanced human immunodeficiency virus infection. HIV Outpatient Study Investigators”. 《N. Engl. J. Med》 338 (13): 853–860. doi:10.1056/NEJM199803263381301. PMID 9516219.
- ↑ Lawn SD (2004). “AIDS in Africa: the impact of coinfections on the pathogenesis of HIV-1 infection”. 《J. Infect. Dis.》 48 (1): 1–12. doi:10.1016/j.jinf.2003.09.001. PMID 14667787.
- ↑ Buchbinder SP, Katz MH, Hessol NA, O'Malley PM, Holmberg SD. (1994). “Long-term HIV-1 infection without immunologic progression”. 《AIDS》 8 (8): 1123–8. doi:10.1097/00002030-199408000-00014. PMID 7986410.
- ↑ “Time from HIV-1 seroconversion to AIDS and death before widespread use of highly-active antiretroviral therapy: a collaborative re-analysis. Collaborative Group on AIDS Incubation and HIV Survival including the CASCADE EU Concerted Action. Concerted Action on SeroConversion to AIDS and Death in Europe”. 《Lancet》 355 (9210): 1131–7. 2000년 4월. doi:10.1016/S0140-6736(00)02061-4. PMID 10791375.
- ↑ Schneider MF, Gange SJ, Williams CM, Anastos K, Greenblatt RM, Kingsley L, Detels R, Munoz A (2005). “Patterns of the hazard of death after AIDS through the evolution of antiretroviral therapy: 1984–2004”. 《AIDS》 19 (17): 2009–18. PMID 16260908.
- ↑ Morgan D, Mahe C, Mayanja B, Okongo JM, Lubega R, Whitworth JA (2002). “HIV-1 infection in rural Africa: is there a difference in median time to AIDS and survival compared with that in industrialized countries?”. 《AIDS》 16 (4): 597–632. PMID 11873003.
- ↑ “보관된 사본”. 2011년 1월 19일에 원본 문서에서 보존된 문서. 2011년 7월 21일에 확인함.
- ↑ International Committee on Taxonomy of Viruses. “61.0.6. Lentivirus”. 미국 국립 보건원. 2006년 2월 28일에 확인함.
- ↑ International Committee on Taxonomy of Viruses. “61. Retroviridae”. 미국 국립 보건원. 2006년 2월 28일에 확인함.
- ↑ Lévy, J. A. (1993). “HIV pathogenesis and long-term survival”. 《AIDS》 7 (11): 1401–10. doi:10.1097/00002030-199311000-00001. PMID 8280406.
- ↑ Smith, Johanna A.; Daniel, René (Division of Infectious Diseases, Center for Human Virology, Thomas Jefferson University, Philadelphia) (2006). “Following the path of the virus: the exploitation of host DNA repair mechanisms by retroviruses”. 《ACS Chem Biol》 1 (4): 217–26. doi:10.1021/cb600131q. PMID 17163676.
- ↑ Gilbert, PB; 외. (2003년 2월 28일). “Comparison of HIV-1 and HIV-2 infectivity from a prospective cohort study in Senegal”. 《Statistics in Medicine》 22 (4): 573–593. PMID 12590415.
- ↑ Reeves, J. D. and Doms, R. W (2002). “Human Immunodeficiency Virus Type 2”. 《J. Gen. Virol.》 83 (Pt 6): 1253–65. PMID 12029140.
- ↑ Grabar, S., Selinger-Leneman, H., Abgrall, S., Pialoux, G., Weiss, L., Costagliola, D. (2009). “Prevalence and comparative characteristics of long-term nonprogressors and HIV controller patients in the French Hospital Database on HIV”. 《AIDS》 23 (9): 1163–1169. doi:10.1097/QAD.0b013e32832b44c8. PMID 19444075.
- ↑ Piatak, M., Jr, Saag, M. S., Yang, L. C., Clark, S. J., Kappes, J. C., Luk, K. C., Hahn, B. H., Shaw, G. M. and Lifson, J.D. (1993). “High levels of HIV-1 in plasma during all stages of infection determined by competitive PCR”. 《Science》 259 (5102): 1749–1754. doi:10.1126/science.8096089. PMID 8096089.
- ↑ Pantaleo G, Demarest JF, Schacker T, Vaccarezza M, Cohen OJ, Daucher M, Graziosi C, Schnittman SS, Quinn TC, Shaw GM, Perrin L, Tambussi G, Lazzarin A, Sekaly RP, Soudeyns H, Corey L, Fauci AS. (1997). “The qualitative nature of the primary immune response to HIV infection is a prognosticator of disease progression independent of the initial level of plasma viremia”. 《Proc Natl Acad Sci U S A.》 94 (1): 254–258. doi:10.1073/pnas.94.1.254. PMID 8990195.
- ↑ Kahn, J. O. and Walker, B. D. (1998). “Acute Human Immunodeficiency Virus type 1 infection”. 《N. Engl. J. Med.》 331 (1): 33–39. doi:10.1056/NEJM199807023390107. PMID 9647878.
- ↑ Daar ES, Little S, Pitt J; 외. (2001). “Diagnosis of primary HIV-1 infection. Los Angeles County Primary HIV Infection Recruitment Network”. 《Ann. Intern. Med.》 134 (1): 25–9. PMID 11187417.
- ↑ Burton GF, Keele BF, Estes JD, Thacker TC, Gartner S. (2002). “Follicular dendritic cell contributions to HIV pathogenesis”. 《Semin Immunol.》 14 (4): 275–284. doi:10.1016/S1044-5323(02)00060-X. PMID 12163303.
- ↑ Clapham PR, McKnight A. (2001). “HIV-1 receptors and cell tropism”. 《Br Med Bull.》 58 (4): 43–59. doi:10.1093/bmb/58.1.43. PMID 11714623.
- ↑ Smith DK, Grohskopf LA, Black RJ; 외. (2005년 1월). “Antiretroviral postexposure prophylaxis after sexual, injection-drug use, or other nonoccupational exposure to HIV in the United States: recommendations from the U.S. Department of Health and Human Services”. 《MMWR Recomm Rep》 54 (RR-2): 1–20. PMID 15660015. 2009년 3월 31일에 확인함.
- ↑ Donegan E, Stuart M, Niland JC; 외. (1990). “Infection with human immunodeficiency virus type 1 (HIV-1) among recipients of antibody-positive blood donations”. 《Ann. Intern. Med.》 113 (10): 733–739. PMID 2240875.
- ↑ 가 나 다 Coovadia H (2004). “Antiretroviral agents—how best to protect infants from HIV and save their mothers from AIDS”. 《N. Engl. J. Med.》 351 (3): 289–292. doi:10.1056/NEJMe048128. PMID 15247337.
- ↑ Kaplan EH, Heimer R (1995). “HIV incidence among New Haven needle exchange participants: updated estimates from syringe tracking and testing data”. 《J. Acquir. Immune Defic. Syndr. Hum. Retrovirol.》 10 (2): 175–176. PMID 7552482.
- ↑ Bell DM (1997). “Occupational risk of human immunodeficiency virus infection in healthcare workers: an overview.”. 《Am. J. Med.》 102 (5B): 9–15. PMID 9845490.
- ↑ 가 나 다 라 European Study Group on Heterosexual Transmission of HIV (1992). “Comparison of female to male and male to female transmission of HIV in 563 stable couples”. 《BMJ.》 304 (6830): 809–813. PMC 1881672. PMID 1392708.
- ↑ 가 나 다 라 마 바 Varghese B, Maher JE, Peterman TA, Branson BM,Steketee RW (2002). “Reducing the risk of sexual HIV transmission: quantifying the per-act risk for HIV on the basis of choice of partner, sex act, and condom use”. 《Sex. Transm. Dis.》 29 (1): 38–43. PMID 11773877.
- ↑ Leynaert B, Downs AM, de Vincenzi I (1998). “Heterosexual transmission of human immunodeficiency virus: variability of infectivity throughout the course of infection. European Study Group on Heterosexual Transmission of HIV”. 《Am. J. Epidemiol.》 148 (1): 88–96. PMID 9663408.
- ↑ Boily M-C, Baggaley RF, Wang L; 외. (2009). “Heterosexual risk of HIV-1 infection per sexual act: systematic review and meta-analysis of observational studies”. 《Lancet Infect Dis》 9 (2): 118–129. doi:10.1016/S1473-3099(09)70021-0. PMID 19179227.
- ↑ National Institute of Allergy and Infectious Diseases; National Institutes of Health, Department of Health and Human Services (2001년 7월 20일). 《Workshop Summary: Scientific Evidence on Condom Effectiveness for Sexually Transmitted Disease (STD) Prevention》 (PDF). Hyatt Dulles Airport, Herndon, Virginia. 13–15쪽. 2010년 3월 15일에 원본 문서 (PDF)에서 보존된 문서. 2009년 1월 8일에 확인함.
- ↑ “Should spermicides be used with condoms?”. 《Condoms and Sexually Transmitted Diseases, Brochure》. United States Food and Drug Administration. 2009년 4월 30일. 2009년 7월 23일에 확인함.
- ↑ Global Campaign for Microbicides : Rectal Use of N-9 Archived 2012년 8월 21일 - 웨이백 머신 checked 2009-07-22
- ↑ Nonoxynol-9 Spermicide on HIV Risk List Archived 2012년 8월 21일 - 웨이백 머신 checked 2009-07-22
- ↑ Weiss, H.A.; M.A. Quigley, R.J. Hayes (2000). “Male circumcision and risk of HIV infection in sub-Saharan Africa: A systematic review and meta-analysis”. 《AIDS》 14 (15): 2361–70. doi:10.1097/00002030-200010200-00018. PMID 11089625.
- ↑ Siegfried, N., Muller, M., Deeks, J., Volmink, J., Egger, M., Low, N., Walker, S. and Williamson, P. (2005). “HIV and male circumcision--a systematic review with assessment of the quality of studies”. 《Lancet Infect. Dis.》 5 (3): 165–73. PMID 15766651.
- ↑ Various (2005). “Repeated Use of Unsterilized Blades in Ritual Circumcision Might Contribute to HIV Spread in S. Africa, Doctors Say”. Kaisernetwork.org. 2006년 9월 28일에 원본 문서에서 보존된 문서. 2006년 3월 28일에 확인함.
- ↑ Williams BG, Lloyd-Smith JO, Gouws E, Hankins C, Getz WM, Hargrove J, de Zoysa I, Dye C, Auvert B. (2006). “The Potential Impact of Male Circumcision on HIV in Sub-Saharan Africa.”. 《PLoS Med》 3 (7): e262. doi:10.1371/journal.pmed.0030262. PMID 16822094.
- ↑ Bailey RC, Moses S, Parker CB; 외. (2007). “Male circumcision for HIV prevention in young men in Kisumu, Kenya: a randomised controlled trial”. 《Lancet》 369 (9562): 643–56. doi:10.1016/S0140-6736(07)60312-2. PMID 17321310.
- ↑ Gray RH; 외. (2007년 2월 24일). “Male circumcision for HIV prevention in men in Rakai, Uganda: a randomised trial”. 《Lancet》 369 (9562): 657–66. doi:10.1016/S0140-6736(07)60313-4. PMID 17321311.
- ↑ WHO (2007). “WHO and UNAIDS announce recommendations from expert consultation on male circumcision for HIV prevention”. WHO.int. 2007년 7월 13일에 확인함.
- ↑ Lifson AR (1988). “Do alternate modes for transmission of human immunodeficiency virus exist? A review”. 《JAMA》 259 (9): 1353–6. doi:10.1001/jama.1988.03720090043032. PMID 2963151.
- ↑ “Why Mosquitoes Cannot Transmit AIDS”. 2014년 3월 29일에 원본 문서에서 보존된 문서. 2014년 3월 29일에 확인함.
- ↑ Cochrane Systematic Review on interventions for prevention of late postnatal mother-to-child transmission of HIV
- ↑ Smith D, Richman D, Little S (2005). “HIV Superinfection”. 《Journal of Infectious Diseases》 192: 438–44. doi:10.1086/431682. PMID 15995957.
- ↑ Gottlieb; 외. (2004). “Dual HIV-1 infection associated with rapid disease progression”. 《Lancet》 363 (9049): 619–22. doi:10.1016/S0140-6736(04)15596-7. PMID 14987889.
- ↑ Smith; 외. (2004). “Incidence of HIV superinfection following primary infection”. 《JAMA》 292 (10): 1177–8. doi:10.1001/jama.292.10.1177. PMID 15353529.
- ↑ Chohan B, Lavreys L, Rainwater SM, Overbaugh J (2005년 8월). “Evidence for frequent reinfection with human immunodeficiency virus type 1 of a different subtype”. 《J. Virol.》 79 (16): 10701–8. doi:10.1128/JVI.79.16.10701-10708.2005. PMC 1182664. PMID 16051862.
- ↑ Piantadosi A, Chohan B, Chohan V, McClelland RS, Overbaugh J (2007년 11월). “Chronic HIV-1 infection frequently fails to protect against superinfection”. 《PLoS Pathog.》 3 (11): e177. doi:10.1371/journal.ppat.0030177. PMC 2077901. PMID 18020705.
- ↑ Hu DJ, Subbarao S, Vanichseni S; 외. (2005년 2월). “Frequency of HIV-1 dual subtype infections, including intersubtype superinfections, among injection drug users in Bangkok, Thailand”. 《AIDS》 19 (3): 303–8. PMID 15718841. 2013년 9월 16일에 원본 문서에서 보존된 문서. 2009년 3월 31일에 확인함.
- ↑ McGovern SL, Caselli E, Grigorieff N, Shoichet BK (2002). “A common mechanism underlying promiscuous inhibitors from virtual and high-throughput screening”. 《J Med Chem》 45 (8): 1712–22. doi:10.1021/jm010533y. PMID 11931626.
- ↑ Compared with overview in: Fisher, Bruce; Harvey, Richard P.; Champe, Pamela C. (2007). 《Lippincott's Illustrated Reviews: Microbiology (Lippincott's Illustrated Reviews Series)》. Hagerstown, MD: Lippincott Williams & Wilkins. ISBN 0-7817-8215-5. Page 3
- ↑ 가 나 다 라 마 바 사 Various (2008). 《HIV Sequence Compendium 2008 Introduction》 (PDF). 2009년 3월 31일에 확인함.
- ↑ 가 나 Chan, DC., Fass, D., Berger, JM., Kim, PS. (1997). “Core Structure of gp41 from the HIV Envelope Glycoprotein” (PDF). 《Cell》 89: 263–73. PMID 9108481. 2009년 3월 31일에 확인함.
- ↑ 미국 국립 보건원 (1998년 6월 17일). “Crystal Structure of Key HIV Protein Reveals New Prevention, Treatment Targets”. 2006년 2월 19일에 원본 문서에서 보존된 문서. 2006년 9월 14일에 확인함.
- ↑ Ouellet DL, Plante I, Landry P; 외. (2008년 4월). “Identification of functional microRNAs released through asymmetrical processing of HIV-1 TAR element”. 《Nucleic Acids Res.》 36 (7): 2353–65. doi:10.1093/nar/gkn076. PMC 2367715. PMID 18299284.
- ↑ Klase Z, Winograd R, Davis J; 외. (2009). “HIV-1 TAR miRNA protects against apoptosis by altering cellular gene expression”. 《Retrovirology》 6: 18. doi:10.1186/1742-4690-6-18. PMC 2654423. PMID 19220914.
- ↑ Garcia JV, Miller AD (1991년 4월). “Serine phosphorylation-independent downregulation of cell-surface CD4 by nef”. 《Nature》 350 (6318): 508–11. doi:10.1038/350508a0. PMID 2014052.
- ↑ Schwartz O, Maréchal V, Le Gall S, Lemonnier F, Heard JM (1996년 3월). “Endocytosis of major histocompatibility complex class I molecules is induced by the HIV-1 Nef protein”. 《Nat. Med.》 2 (3): 338–42. doi:10.1038/nm0396-338. PMID 8612235.
- ↑ Stumptner-Cuvelette P, Morchoisne S, Dugast M; 외. (2001년 10월). “HIV-1 Nef impairs MHC class II antigen presentation and surface expression”. 《Proc. Natl. Acad. Sci. U.S.A.》 98 (21): 12144–9. doi:10.1073/pnas.221256498. PMC 59782. PMID 11593029.
- ↑ 가 나 Kalichman, Seth (2009). 《Denying AIDS: Conspiracy Theories, Pseudoscience, and Human Tragedy》. New York: Copernicus Books (Springer Science+Business Media). ISBN 978-0-387-79475-4.
- ↑ Duesberg, P. H. (1988). “HIV is not the cause of AIDS”. 《Science》 241 (4865): 514, 517. doi:10.1126/science.3399880. PMID 3399880.
- ↑ Smith TC, Novella SP (2007년 8월). “HIV denial in the Internet era”. 《PLoS Med.》 4 (8): e256. doi:10.1371/journal.pmed.0040256. PMID 17713982. 2008년 5월 6일에 원본 문서에서 보존된 문서. 2009년 11월 7일에 확인함.
- ↑ HIV는 AIDS의 원인이라는 증거는 다음의 예에서 알 수 있다.
- , (2000). “The Durban Declaration”. 《Nature》 406 (6791): 15–6. doi:10.1038/35017662. PMID 10894520..
- Cohen, J. (1994). “The Controversy over HIV and AIDS” (PDF). 《Science》 266 (5191): 1642–1649. doi:10.1126/science.7992043. PMID 7992043. 2009년 3월 31일에 확인함.
- Various. “Resources and Links, HIV-AIDS Connection”. National Institute of Allergy and Infectious Diseases. 2009년 4월 25일에 원본 문서에서 보존된 문서. 2009년 2월 22일에 확인함.
- O'Brien SJ, Goedert JJ (1996). “HIV causes AIDS: Koch's postulates fulfilled”. 《Curr. Opin. Immunol.》 8 (5): 613–8. doi:10.1016/S0952-7915(96)80075-6. PMID 8902385.
- Galéa P, Chermann JC (1998). “HIV as the cause of AIDS and associated diseases”. 《Genetica》 104 (2): 133–42. doi:10.1023/A:1003432603348. PMID 10220906.
- ↑ Watson J (2006). “Scientists, activists sue South Africa's AIDS 'denialists'”. 《Nat. Med.》 12 (1): 6. doi:10.1038/nm0106-6a. PMID 16397537.
- ↑ Baleta A (2003). “S Africa's AIDS activists accuse government of murder”. 《Lancet》 361 (9363): 1105. doi:10.1016/S0140-6736(03)12909-1. PMID 12672319.
- ↑ Cohen J (2000). “South Africa's new enemy”. 《Science》 288 (5474): 2168–70. doi:10.1126/science.288.5474.2168. PMID 10896606.
외부 링크
[편집]- HIV Medicine 2005 Archived 2019년 6월 7일 - 웨이백 머신, a medical textbook, >700 pages (free download)
- The Mechanism of HIV-1 Core Assembly: Insights from Three-Dimensional Reconstructions of Authentic Virions
- AIDS.ORG: Educating - Raising HIV Awareness - Building Community
- Be the Generation - Information on HIV Vaccine Clinical Research in 20 American Cities Archived 2017년 9월 25일 - 웨이백 머신
- Capital Area Vaccine Effort
- AEGiS.org: AIDS Education Global Information System- Patient/clinician information & Historical news and treatment database
- AIDS/HIV Education Archived 2006년 6월 18일 - 웨이백 머신
- Watch an animated tutorial on the life cycle of HIV Archived 2006년 6월 16일 - 웨이백 머신
- Continuing medical education about HIV for healthcare providers
- FightAIDS@Home Archived 2019년 10월 8일 - 웨이백 머신
- Everything you wanted to know about HIV and AIDS — Provided by New Scientist.
- Free HIV Images
- HIV/AIDS Treatment Information Service Archived 2020년 10월 28일 - 웨이백 머신
- HIV/AIDS Education in Teacher Preparation Programs Archived 2006년 6월 18일 - 웨이백 머신
- HIV InSite Archived 2005년 8월 9일 - 웨이백 머신
- How Aids Works (with animation)
- Medecins Sans Frontieres/Doctors Without Borders HIV/AIDS Pages
- NIH/NIAD/DAIDS
- History of AIDS research at the NIH
- "The Molecules of HIV" information resource Archived 2006년 6월 14일 - 웨이백 머신
- Unsafe Health Care and the HIV/AIDS Pandemic 2003
- HIV/AIDS: global trends, global funds and delivery bottlenecks
- UNAIDS document regarding three scenarios for HIV/AIDS in Africa for the year 2025 (Large PDF file)
- UNAIDS - Joint United Nations Programme on HIV/AIDS webpage
- Media Campaign: HIV leads to AIDS Archived 2021년 1월 26일 - 웨이백 머신
- CSA54 - AIDS Cure News
- The role of dendritic cells in HIV pathogenesis
- HIV overview
- video ofTreatment Update 2006 from the Conference on Retrovirus'
뉴스
[편집]- Nov 2005 - Progress in HIV vaccine research -Recorded interview with Prof. Robert Gallo (HIV researcher) Archived 2005년 12월 11일 - 웨이백 머신
- Jan 2006 - 3D structure of HIV is revealed - 3D map of AIDS causing virus revealed
- May 2006—HIV origin 'found in wild chimps'—HIV origin 'found in wild chimps'
