탄탈럼
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 개요 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 영어명 | Tantalum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 표준 원자량 (Ar, standard) | 180.94788(2) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기율표 정보 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 번호 (Z) | 73 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 족 | 5족 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기 | 6주기 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 구역 | d-구역 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 화학 계열 | 전이 금속 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전자 배열 | [Xe] 4f14 5d3 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 준위별 전자 수 | 2, 8, 18, 32, 11, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 물리적 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 겉보기 | 청회색 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 상태 (STP) | 고체 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 녹는점 | 3290 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 끓는점 | 5731 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 밀도 (상온 근처) | 16.69 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 융해열 | 36.51 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기화열 | 732.8 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 몰열용량 | 25.36 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 증기 압력 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자의 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 산화 상태 | −3, −1, +1, +2, +3, +4, +5 (약산성 산화물) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기 음성도 (폴링 척도) | 1.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이온화 에너지 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 반지름 | 146 pm (실험값) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 공유 반지름 | 170±8 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 그 밖의 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
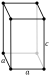
| 결정 구조 (α-Ta) | 체심 입방정계 (bcc) [1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 결정 구조 (β-Ta) | 단순 정방정계 [1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 음속 (얇은 막대) | 3400 m/s (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열팽창 | 6.3 µm/(m·K) (25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열전도율 | 57.5 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기 저항도 | 131 Ω·m (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자기 정렬 | 상자성[2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 영률 | 186 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전단 탄성 계수 | 69 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 부피 탄성 계수 | 200 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 푸아송 비 | 0.34 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 모스 굳기계 | 6.5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 비커스 굳기 | 870-1200 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 브리넬 굳기 | 440-3430 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS 번호 | 7440-25-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 역사 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 발견 | 안데르스 에셰베리 (1802) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
탄탈럼, 탄탈룸(←영어: Tantalum 탠털럼[*]) 또는 탄탈(←독일어: Tantal 탄탈[*])은 화학 원소로 기호는 Ta(←라틴어: Tantalum 탄탈룸[*]), 원자 번호는 73이다. 희귀하고 단단하며, 청회색의 광택을 띠는 전이 금속으로 부식에 매우 강하다. 난융 금속의 하나로, 합금의 첨가물로 널리 이용된다. 화학적으로 비활성이므로 각종 실험실 장비와 휴대 전화, 컴퓨터 등의 전자 기기들에 커패시터(콘덴서)의 원료로 사용되거나 백금 대체물, 의료용 등으로 사용되기도 한다. 화학적으로 나이오븀과 매우 유사하므로 나이오븀의 영어식 이름인 콜롬븀과 탄탈륨의 첫 글를 따서 콜탄이라고 불리기도 한다. 컬럼바이트 등의 광물에 같이 들어 있는 경우가 많다.
특성[편집]
물리적 특성[편집]
탄탈럼은 어두운 청회색의 광택을 가진 전이 금속으로, 무겁고 매우 단단하며 연성이 뛰어나고 가공성이 좋은 금속이다. 열전도율과 전기 전도율이 매우 좋고 산에 거의 부식되지 않는다. 150°C 이하에서는 왕수와도 잘 반응하지 않으며 플루오린 이온이나 삼산화 황 등을 포함한 산성 용액에서 녹는다. 녹는점은 3017°C, 끓는점은 5458°C로 매우 높으며, 이는 텅스텐, 탄소, 레늄, 오스뮴에 이어 원소들 중 5번째로 높은 것이다. 또, 탄탈럼은 두 종류의 동소체가 존재한다. α 구조일 때는 연성이 뛰어나며 결정형은 체심 입방정계 구조이다. β 구조일 때는 단단하지만 부서지기 쉬우며 결정형은 정방정계 구조이다. 결정형이 β 구조일 때 준안정하며, 750°C 이상으로 가열하면 α 구조로 전환된다. 자연에 존재하는 탄탈럼은 대부분 체심입방구조이다.
화학적 특성[편집]
탄탈럼은 +4와 +5의 산화 상태를 가질 수 있으며, 각각 이산화 탄탈럼(TaO2)과 오산화 탄탈럼(Ta2O5)을 만들 수 있다. 산화수가 +5일 때 가장 안정하며, 이들 외에 +3, -1의 산화수를 가지기도 한다.
동위 원소[편집]
자연에는 180mTa(0.012%)와 181Ta(99.988%) 두 종류의 탄탈럼 동위 원소가 존재한다. 이 중 준안정한 180mTa은 방사성인 것으로 추정되지만 아직 방사성 붕괴가 관찰된 적은 없으며, 반감기가 1.2×1015년 이상인 것으로 추정된다. 또, 180mTa은 자연에 존재하는 모든 동위 원소들 중 유일한 이성질핵이기도 하다. 바닥상태의 180Ta은 반감기가 약 8시간이다.
한편, 탄탈럼은 이론적으로 핵무기의 외피에 씌워 더 많은 방사선을 내는 폭탄의 제조에 사용할 수 있다. 이는 코발트 폭탄과 비슷한 개념으로 181Ta이 핵무기가 폭발하면서 방출하는 중성자로 인해 강력한 감마선을 방출하는 방사성 동위 원소 182Ta(반감기 114.4일)이 되는 점을 이용한다. 그러나 아직까지 공식적으로 이러한 폭탄이 개발된 적은 없는 것으로 알려져 있다.
존재[편집]
탄탈럼은 지각 속에 약 1~2ppm 정도 포함된 것으로 추정된다. 주로 탄탈석, 콜탄, 컬럼바이트 등에 포함되어 있으며 주된 산지는 호주, 중국, 에티오피아, 모잠비크 등이며, 이외에 브라질, 캐나다, 태국 등지에서는 나이오븀이나 주석 채굴 과정에서 부산물로 함께 얻는 경우도 있다.
한편, 탄탈럼 광석 중의 하나인 콜탄은 중앙아프리카 지역에서 주로 생산되는데, 이는 콩고 민주 공화국의 내전과도 관련이 있었다. 이 내전으로 인해 540만 명 이상이 사망하였고, 제2차 세계대전 이후 가장 많은 사망자를 낸 전쟁이 되었다.
용도[편집]
전자 제품[편집]
탄탈럼은 주로 전자 회로의 부품을 제조하는데 사용되며, 특히 고성능 저항기와 축전기와 같은 부품 제조에 주로 사용된다. 특히 탄탈럼 축전기는 탄탈럼 분말이 산화 피막을 형성하려는 경향을 이용한 것으로, 여기서 생성된 탄탈럼 산화물이 유전체의 역할을 한다. 이러한 축전기는 작은 부피에 비해 큰 용량을 저장할 수 있으므로 휴대 전화, 컴퓨터, 자동차 내 전기 부품 등에 사용된다. 또, 질소나 산소와 잘 결합하는 성질이 있어 과거에 고주파 라디오 송신기의 진공관 내부의 진공을 유지하는데 쓰이기도 하였다.
합금[편집]
탄탈럼을 합금에 첨가하면 녹는점이 높아지고 강도가 증가하며, 연성이 좋아지는 장점이 있어 제트 엔진, 핵반응로, 미사일 등에 들어가는 초합금의 재료로 이용된다. 탄화 탄탈럼은 고강도의 장비를 만드는데 이용된다. 또, 탄탈럼은 연성이 매우 뛰어나므로 얇게 늘여서 얇은 철사나 필라멘트 등을 제조하는데 사용하기도 하며, 반응성이 낮아 체액과도 잘 반응하지 않고 생체 적합성이 뛰어나므로 의료용 목적으로도 많이 사용한다.
포탄
매우 단단하기에 날개안정분리철갑탄의 관통자로 쓰인다
하지만 비싸서 요즘에는 텅스텐 합금으로 대체되었다.
각주[편집]
- ↑ 가 나 Moseley, P. T.; Seabrook, C. J. (1973). “The crystal structure of β-tantalum”. 《Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry》 29 (5): 1170–1171. doi:10.1107/S0567740873004140.
- ↑ Lide, D. R., 편집. (2005). 〈Magnetic susceptibility of the elements and inorganic compounds〉. 《CRC Handbook of Chemistry and Physics》 (PDF) 86판. Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5.
외부 링크[편집]
- “탄탈럼”. 《네이버캐스트》.
- (영어) 탄탈럼 - WebElements.com