이터븀
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 개요 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 영어명 | Ytterbium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 표준 원자량 (Ar, standard) | 173.045(10) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기율표 정보 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 번호 (Z) | 70 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 족 | n/a | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 주기 | 6주기 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 구역 | f-구역 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 화학 계열 | 란타넘족 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전자 배열 | [Xe] 4f14 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 준위별 전자 수 | 2, 8, 18, 32, 8, 2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 물리적 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 겉보기 | 은백색 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 상태 (STP) | 고체 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 녹는점 | 1097 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 끓는점 | 1469 K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 밀도 (상온 근처) | 6.90 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 융해열 | 7.66 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 기화열 | 159 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 몰열용량 | 26.74 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 증기 압력 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자의 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 산화 상태 | 3 (염기성 산화물) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기 음성도 (폴링 척도) | ? 1.1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 이온화 에너지 |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 원자 반지름 | 176 pm (실험값) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 공유 반지름 | 187±8 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 그 밖의 성질 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
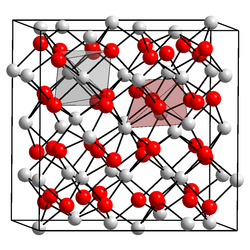
| 결정 구조 | 면심 입방정계 (fcc) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 음속 (얇은 막대) | 1590 m/s (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열팽창 | (실온) (β, poly) 26.3 µm/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 열전도율 | 38.5 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전기 저항도 | (실온) (β, poly) 0.250 μ Ω·m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 자기 정렬 | 상자성 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 영률 | (β form) 23.9 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 전단 탄성 계수 | (β form) 9.9 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 부피 탄성 계수 | (β form) 30.5 GPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 푸아송 비 | (β form) 0.207 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 비커스 굳기 | 206 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 브리넬 굳기 | 343 MPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS 번호 | 7440-64-4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
이터븀(←영어: ytterbium 이터비엄[*]) 또는 이테르븀(문화어: 이테르비움←독일어: Ytterbium 위테르비움[*])은 화학 원소로 기호는 Yb(←라틴어: Ytterbium 이테르비움[*]), 원자 번호는 70이다.
주기율표상으로 란타넘족 원소 중 14번째이며 끝에서 두 번째에 위치해 있다. 이는 이터븀이 다른 란타넘족 원소들과 다르게 비교적 안정한 +2의 산화수를 가질 수 있는 이유이다. 하지만 다른 모든 란타넘족 원소들처럼 화합물(할로젠화물, 산화물 등) 내에서 가지는 주요 산화수는 +3으로 나타난다. 이터븀의 수용성인 화합물은 다른 원자번호가 큰 란타넘족 원소들의 수용성 화합물처럼 수용액 내에서는 9개의 물 분자와 배위화합물(coordination complex)를 형성한다. 꽉 찬 전자 배치에 의해, 이터븀의 녹는점과 끓는점은 대부분 란타넘족 원소들의 경우와 눈에 보일 만한 차이를 보인다.
이터븀은 많은 희토류 원소의 혼합물인 이트리아(Yttria)에 포함된 9가지 원소들 중 하나이다. 이트리아에서 스칸듐과 어븀을 포함하는 에르비아(Erbia)가 분리되었고 에르비아는 이터븀과 루테튬(Lu)을 포함하는 이테르비아(Ytterbia), 툴륨(Tm)을 포함하는 툴리아(Thulia), 디스프로슘과 홀뮴이 들어있던 홀미아(Holmia)로 분리되었다. 이터븀과 함께 분리된 루테튬은 처음에는 루테슘(Lutecium)으로 불리다가 후에 루테튬(Lutetium)으로 바뀌었다.
현재 이터븀은 스테인리스 스틸에 추가하는 불순물이나 레이저, 흔하지 않지만 감마선원으로도 사용된다. 자연적으로 7개의 안정 동위원소로 존재하며 중국, 미국, 브라질, 인도 등의 나라에서 광물에 포함되어 산출된다. 추출되었을 때 이터븀은 눈과 피부를 다소 자극할 수 있으며 특히 가루 형태일 때 가연성이고 폭발의 위험이 있다.
물리적 성질[편집]
이터븀은 찬물과 천천히 반응하며 공기 중에서 서서히 산화한다. 이터븀은 3가지 결정 구조를 가지는데 알파 결정 구조는 -13 °C이하에서 존재하고 낮은 온도에서 안정하며 육방정계 결정 구조를 가지고 있고, 감마 결정 구조는 795 °C이상에서 존재하고 체심입방격자 구조를 갖는다. 베타 결정 구조는 상온에서 존재하며 면심입방격자 구조를 가지고 있다. 베타 결정 구조는 금속적인 전기전도도를 갖는데 16000 기압(1.6 GPa)에서는 반도체가 되고 39000기압(3.9 GPa)에서는 10배나 전기저항이 상승한다. 하지만 신기하게도 40000기압에서는(4.0 GPa) 전기 저항이 1기압일 때의 전기 저항의 90 %밖에 되지 않는다. 저온에서 강자성이나 반강자성을 가지는 다른 란타넘족들과는 달리 이터븀은 1 K 위의 낮은 온도에서 상자성을 가진다. 예외로 알파 동소체는 반자성체이다. 이터븀은 녹는점이 824 °C, 끓는점이 1196 °C로 액체로 존재하는 온도 범위가 가장 작은 금속이다.
조밀육방격자를 가지는 대부분의 란타넘족 원소들과 달리 이터븀은 면심입방격자 구조를 갖는다. 이터븀의 밀도는 6.973 g/cm^(3)로 이웃한 툴륨 (9.32 g/cm^(3))과 루테튬 (9.841 g/cm^(3))에 비해 상당히 낮다. 밀도 뿐만 아니라 녹는점과 끓는점도 이들에 비해 상당히 낮다. 이는 이터븀의 채워진 전자 배치([Xe] 4f14 6s2)와 관련이 있는데 이터븀은 두개의 6s전자로 금속결합이 가능하고 (다른 란타넘족들은 3개로 가능하다)이는 최종적으로 이터븀의 금속성 반지름을 증가시킨다.
화학적 성질[편집]
이터븀 금속은 공기 중에서 느리게 광택을 잃는다. 고운 분말 형태라면 공기 중에서 산소의 존재 하에 쉽게 산화된다. 이터븀 가루를 폴리테트라플루오로에틸렌 이나 헥사클로로에탄과 섞어 태우면 밝은 에메랄드 색 빛으로 탄다. 또한 이터븀은 수소와 화학량적이지 않은 수소화물을 생성한다. 이터븀은 물과 천천히 반응하지만 산성 용액 안에서는 수소 기체를 생성하며 빠르게 반응한다.
이터븀은 꽤 전기 양성적인 금속이다. 찬물과 천천히, 따뜻한 물과는 꽤 빠르게 반응하며 수소 기체를 생성시킨다.
2 Yb (s) + 6 H2O (l) → 2 Yb(OH)3 (aq) + 3 H2
이터븀은 모든 할로젠 원소들과 반응해서 흰색 이온결합 화합물을 생성한다.
2 Yb (s) + 3 F2 (g) → 2 YbF3
2 Yb (s) + 3 Cl2 (g) → 2 YbCl3
2 Yb (s) + 3 Br2 (g) → 2 YbBr3
2 Yb (s) + 3 I2 (g) → 2 YbI3
이터븀(III) 이온은 적외선과 비슷한 파장을 가지는 빛(전자기파)를 흡수하지만 가시광선 영역의 빛은 흡수하지 않기 때문에 산화이터븀(Yb2O3)인 이테르비아(Ytterbia)는 흰색을 띤다. 마찬가지로 여러 이터븀 염도 흰색이다(뚜렷한 색을 나타내지 않는다). 이터븀은 묽은 황산과 쉽게 반응해 색깔 없는 이터븀(III) 이온을 만드는데, 이는 9수화물 복합체로 존재한다.
2 Yb (s) + 3 H2SO4 (aq) + 18 H2O (l) → 2 [Yb(H2O)9]3+ (aq) + 3 SO2−4 (aq) + 3 H2 (g)
Yb2+와 Yb3+[편집]
이터븀의 주요 산화수는 +3이지만 쉽게 +2의 산화수도 가질 수 있다. 이러한 성질은 란타넘족 원소로써는 예외적인데, 이들은 거의 오직 +3의 산화수를 가지며 화합물을 형성하기 때문이다. 이터븀(II) 이온은 [Xe] 4f14의 전자 배치를 가지는데, 이는 꽉 찬 4f 껍질이 이온을 안정하게 만들기 때문이다. 연두색 이터븀(II) 이온 Yb2+은 매우 강한 환원제로, 물을 분해하여 수소 기체를 발생시킨다. 그렇게 때문에 이터븀은 이터븀(III) 이온 형태로만 수용액 상태로 존재할 수 있다. 사마륨(Sm)과 툴륨(Tm)도 +2의 산화수를 가지는 이온 상태일 때 이런 성질을 나타내지만 유로퓸(Eu)의 경우, Eu2+는 수용액 상태에서 안정하다. 이터븀 금속은 유로퓸이나 알칼리토금속 원소들처럼 암모니아와 반응해 전자가 음이온 역할을 하는 파란색 염을 만든다. (이런 화합물을 Electride, 즉 '전자화물'이라고 한다)
예: 알칼리금속 원소인 소듐의 경우, Na + 6 NH3 → [Na(NH3)6]+,e−
바로 여기서 음전하를 띠는 전자가 바로 음이온 역할을 한다. 이러한 전자화물(Electride)에서 양이온은 배위결합이 포함된 배위화합물이다.
동위원소[편집]
자연적으로 이터븀은 7가지의 안정 동위원소(168Yb, 170Yb, 171Yb, 172Yb, 173Yb, 174Yb 그리고 176Yb) 형태로 존재한다. 이들 중 174Yb가 31.8 %로 가장 존재비가 높다. 27개의 방사성 동위원소도 알려져 있으며 가장 반감기가 긴 것들은 169Yb (32.0 일), 175Yb (4.18 일), 그리고 166Yb (56.7 시간)이다. 나머지 방사성 동위원소들은 반감기가 2시간을 넘지 않으며 대부분 20분 이하이다. 이터븀은 12개의 준안정 상태(meta state)의 원자핵 역시 가지는데, 이 중 가장 반감기가 긴 것은 169mYb (반감기 46초)이다.
이터븀의 동위원소들은 148Yb의 경우인 147.9674 u에서부터 181Yb의 경우인 182.9562 u의 원자량 범위를 가진다. 이터븀의 가장 안정한 동위원소 174Yb보다 중성자수가 적은 방사성 동위원소들의 일반적인 방사성 붕괴 형식은 전자 포획이고 174Yb 보다 중성자수가 더 많은 방사성 동위원소의 일반적인 붕괴 형식은 베타 붕괴이다. 그렇기 때문에 전자 포획을 일반적인 붕괴 형식으로 가지는 174Yb보다 중성자수가 적은 방사성 동위원소의 붕괴 산물은 툴륨(Tm) 동위원소이고 174Yb 보다 중성자수가 더 많은 방사성 동위원소의 붕괴 산물은 루테튬(Lu) 동위원소이다.
생산[편집]
이터븀은 다른 란타넘족 원소들과 화학적 성질이 비슷하기 때문에 분리하기 힘든 편이다. 이터븀은 이온 교환 방법을 쓰거나 소듐 아말감(소듐과 수은으로 이루어진 합금)으로 환원시켜서 다른 희토류 금속들로부터 분리된다. 3가의 희토류 금속 이온들이 녹아있는 산성 용액에 용융 상태의 소듐-수은 합금(소듐 아말감)을 부으면 이는 Yb3+를 환원시켜서 녹이게 된다. 이터븀 금속은 용액 안에서 수산염(oxalate) 형태로 분리되고 가열해서 산화물 형태로 바꾼다. 이터븀 금속은 그 산화물을 란타넘(La), 알루미늄(Al), 세륨(Ce), 지르코늄(Zr)과 고진공 상태에서 가열함으로써 생성된다.
화합물[편집]
이터븀의 화학적 성질은 나머지 란타넘족 원소들과 비슷하다. 이터븀은 화합물 내에서 대부분 +3의 산화수를 가지며 3가의 이터븀 이온을 포함한 염은 대부분 흰색이다.(뚜렷한 색깔을 나타내지 않는다) 유로퓸, 사마륨, 툴륨과 같게, 이터븀의 삼할로젠화물(YbX3 형태로 나타나는)은 수소나 아연 가루, 이터븀 금속에 의해 이할로젠화물(YbX2 형태로 나타나는)로 환원될 수 있다. 이터븀은 고체 화합물 내에서만 +2의 산화수를 가지며 이런 화합물은 알칼리 토금속 화합물과 비슷한 양상을 보인다. 예를 들어 YbO, 산화이터븀(II)은 산화칼슘(CaO) 와 같은 구조를 보인다.
할로젠화물[편집]
이터븀은 할로젠 원소인 플루오린(F), 염소(Cl), 브로민(Br), 아이오딘(I)과 삼할로젠화물, 이할로젠화물을 생성할 수 있으며 이할로젠화물은 상온에서 삼할로젠화물로 산화되거나 고온에서 삼할로젠화물과 이터븀 금속으로 분해될 수 있다.
3 YbX2 → 2 YbX3 + Yb (X = F, Cl, Br, I)
일부 이터븀 할로젠화물은 유기합성(organic synthesis) 분야에서 시약(reagent)으로 사용된다. 예를 들어 염화 이터븀(III) 즉 YbCl3는 루이스 산으로 알돌 반응(탄소-탄소 결합을 만드는 반응), 딜스-알더 반응에 촉매로 사용된다. 그리고 아이오딘화 이터븀(II) YbI2는 염화 사마륨(II)처럼 두 객체를 촉매를 사용하여 결합시키는 유기화학 반응인 coupling reaction에서 환원제로 사용된다. 플루오린화 이터븀(III)은 반응성이 낮고 독성이 없는 치아 수복에 사용되는데, 이는 지속적으로 플루오린화 이온을 내놓아 치아 건강에 도움이 된다.
산화물[편집]
이터븀은 산소와 반응해 '희토류 C형 2,3 산화물(Rare-earth C-type sesquioxide)'이라는 결정 구조를 가지는 산화이터븀(III) Yb2O3을 만드는데, 이의 결정 구조는 형석의 결정 구조와 연관이 있다. Yb2O3는 원소 상태의 이터븀에 의해 YbO, 즉 산화이터븀(II)로 환원될 수 있다.
산화이터븀(II)은 염화 소듐(NaCl), 즉 소금과 같은 형태로 결정화된다.
용도[편집]
감마선원[편집]
32일의 반감기를 가지는 169Yb는 감마선을 방출하기 때문에 방사선 촬영에 사용된다. 이 방사성 동위원소는 175Yb와 함께 원자로에서 이터븀에 중성자가 흡수될 때 생성된다. X선처럼 감마선은 부드러운 조직은 통과하지만 뼈와 밀도가 높은 물체에 가로막히는 성질이 있다. 그래서 조그만 169Yb의 샘플은 작은 X선 촬영장치와 같아서 작은 물질을 방사선 촬영하는 데 쓰일 수 있다. 여러 실험 결과는 이 동위원소로 찍은 방사선 촬영 사진이 250~350 kev의 에너지를 가지는 X선 사진과 거의 맞먹는다는 것을 보여준다. 169Yb은 핵의학에도 활용된다.
스테인리스 강 도핑 재료[편집]
이터븀은 스테인리스 강의 강도, 결정립 미세화, 그리고 다른 공학적인 성질을 높이는 데 쓰인다. 몇몇 이터븀 합금은 치과의학에서 사용되기도 한다.
레이저 분야[편집]
Yb3+ 이온은 레이저 분야에서 도핑재료로 쓰인다. 특히 고체 레이저, 이중 클래드 광섬유 레이저(Double clad optical fiber) 같은 종류의 레이저에서 사용된다. 이터븀 레이저는 고효율이고 수명이 길며 짧은 펄스광을 발생시킬 수 있다. 이로 인해 이터븀은 레이저 재료에 많이 포함된다. 이터븀 레이저는 일반적으로 1.06 - 1.12 마이크로미터의 선에서 파장 900 nm~1 마이크로미터의 빛을 발생시킨다. (광섬유 레이저의 도핑 재료로 사용된다.)
정확도 높은 원자 시계[편집]
이터븀 광시계는 가장 높은 안정성을 가지는 시계로 오차가 2 × 10-18밖에 나지 않는다고 알려져 있다. 미국 국립 표준기술 연구소(NIST)가 개발한 이터븀 광시계는 10 마이크로켈빈까지 냉각시킨 이터븀 원자 10,000개를 레이저광으로 만든 광격자(optical lattice, 레이저광으로 만든의 연속)안에 가둔 뒤에 이터븀 원자의 두 에너지 준위 사이의 전이를 유발하는, 1초에 518조 번 '째깍거리는' 또 다른 레이저를 쏘는 방식으로 작동된다. 이터븀의 높은 원자번호는 시계의 높은 안정성의 열쇠이다.
세슘 원자시계의 경우에 쓰이는 마이크로파보다 가시광선이 더 높은 진동수를 가지므로 광시계는 세슘 원자시계보다 더 높은 정확도를 가질 수 있다. 이터븀 광시계는 미래에 더 정밀한 시간표준이 될 수 있는 가능성이 있다.
기타 용도[편집]
이터븀은 압력을 받으면 전기 저항이 커지는 성질이 있는데, 이런 성질을 이용해서 지하에서 발생한 지진이나 폭발을 감지할 수 있다. (지진 감시 장치 등에 이용된다.)
주의할 점[편집]
이터븀은 알칼리 금속 원소들처럼 반응성이 그렇게 높지는 않으나 공기와 수분과 접촉하지 않게 질소처럼 비활성적인 기체가 들어있는 밀봉된 용기 안에 보관한다. 몇몇 이터븀 화합물이 인간의 눈과 피부에 자극을 줄 수 있어서다. 분말 상태로는 자발적으로 발화할 수 있다. 대부분 금속 관련된 화재처럼 이를 진화할 때 물을 사용하지 말고 금속 화재 전용 소화기를 사용해야 한다.
외부 링크[편집]
- “이터븀”. 《네이버캐스트》.
- (영어) 이터븀 - WebElements.com
- (영어) 이터븀 - It's Elemental



