일산화 탄소
| |||
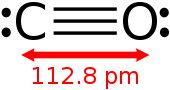
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Carbon monoxide | |||
| 별칭
Carbon monooxide
Carbonous oxide Carbon(II) oxide Carbonyl Flue gas Monoxide | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3587264 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.010.118 | ||
| EC 번호 |
| ||
| 421 | |||
| KEGG | |||
| MeSH | Carbon+monoxide | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1016 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| CO | |||
| 몰 질량 | 28.010 g/mol | ||
| 겉보기 | 무색 기체 | ||
| 냄새 | odorless | ||
| 밀도 | 789 kg/m3, liquid 1.250 kg/m3 at 0 °C, 1 atm 1.145 kg/m3 at 25 °C, 1 atm | ||
| 녹는점 | −205.02 °C (−337.04 °F; 68.13 K) | ||
| 끓는점 | −191.5 °C (−312.7 °F; 81.6 K) | ||
| 27.6 mg/L (25 °C) | |||
| 용해도 | 클로로포름, 아세트산, 아세트산 에틸, 에탄올, 암모니아수, 벤젠에 가용성 | ||
헨리 상수 (kH)
|
1.04 atm·m3/mol | ||
자화율 (χ)
|
−9.8·10−6 cm3/mol | ||
굴절률 (nD)
|
1.0003364 | ||
| 0.122 D | |||
| 열화학 | |||
열용량 (C)
|
29.1 J/(K·mol) | ||
표준 몰 엔트로피 (S
|
197.7 J/(mol·K) | ||
표준 생성 엔탈피 (ΔfH⦵298)
|
−110.5 kJ/mol | ||
표준 연소 엔탈피 (ΔcH⦵298)
|
−283.4 kJ/mol | ||
| 약리학 | |||
| V04CX08 (WHO) | |||
| 위험 | |||
| 물질 안전 보건 자료 | ICSC 0023 | ||
| GHS 그림문자 |   
| ||
| 신호어 | 위험 | ||
| H220, H331, H360, H372 | |||
| P201, P202, P210, P260, P261, P264, P270, P271, P281, P304+340, P308+313, P311, P314, P321, P377, P381, P403, P403+233, P405, P501 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | −191 °C (−311.8 °F; 82.1 K) | ||
| 609 °C (1,128 °F; 882 K) | |||
| 폭발 한계 | 12.5–74.2% | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LC50 (median concentration)
|
8636 ppm (rat, 15 min) 5207 ppm (rat, 30 min) 1784 ppm (rat, 4 h) 2414 ppm (mouse, 4 h) 5647 ppm (guinea pig, 4 h)[1] | ||
LCLo (lowest published)
|
4000 ppm (human, 30 min) 5000 ppm (human, 5 min)[1] | ||
| NIOSH (미국 건강 노출 한계):[3] | |||
PEL (허용)
|
TWA 50 ppm (55 mg/m3) | ||
REL (권장)
|
TWA 35 ppm (40 mg/m3) C 200 ppm (229 mg/m3) | ||
IDLH (직접적 위험)
|
1200 ppm | ||
| 관련 화합물 | |||
관련 carbon oxides
|
이산화 탄소 아산화 탄소 산화 탄소 | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
일산화 탄소(一酸化炭素, 영어: carbon monoxide)는 탄소와 산소로 구성된 화합물이다. 분자식은 CO이다. 석탄이나 석유를 다량 연소시키는 공업지대의 대기에 포함되어 있는 경우가 있으며, 가정에 공급되고 있는 도시가스에도 포함되어 있다.[5] 탄소 화합물이 불완전 연소되면 발생한다. 가연성이며 독성이 있어서 취급에 주의가 필요하다. 산소보다 헤모글로빈과의 친화력이 200배 정도 더 좋기 때문에 소량 흡입시에도 호흡 대사를 방해하여 생명 유지가 어려울 수 있으므로 주의해야 한다.담배 속에 들어있는 인체에 해로운 대표적 물질 3가지 중 하나이다.(타르,니코틴,일산화탄소)
역사[편집]
18세기 후반에 프랑스의 화학자 J. M. F. Lassone에 의해 처음으로 얻어졌다. 19세기 초에 J. B. Desormes와 W. Cruickshank는 일산화 탄소를 연소시키면 같은 부피의 이산화 탄소가 발생하는 것을 통해 일산화 탄소의 조성을 결정하였다.[5]
성질[편집]
물리적 성질[편집]
상온에서 무색, 무취, 무미의 기체로 존재한다. 끓는점은 -191.5°C, 녹는점은 -205.0°C이다. 임계 온도는 -139°C이며 임계 압력은 35atm이다. 25°C에서 생성열은 26.62cal/mole, 연소열은 67.62cal/mole이다. 물에는 잘 녹지 않아, 0°C에서 1atm의 일산화 탄소와 평형상태에 있는 물 100ml는 0.0044g의 일산화 탄소를 포함한다. 알코올, 염화 구리(II) 수용액에는 잘 녹는다. 활성탄에 쉽게 흡착된다.
일산화 탄소는 다음의 세 공명 구조를 가지고 있다고 볼 수 있다.
C 원자와 O 원자간의 결합 길이는 1.13Å이다.[5]
화학적 성질[편집]
공기 중에서 점화하면 푸른 불꽃을 내며 연소하여 이산화 탄소를 생성한다. 반응식은 다음과 같다.
일산화 탄소가 다음과 같이 분해되는 일은 온도가 수천도 이상으로 올라가지 않는 한은 잘 일어나지 않는다.
다음과 같은 분해는 상온에서는 팔라듐 촉매 존재 하에 가능하며, 400~700°C에서는 많은 물질의 표면이 다음 분해 반응의 촉매 역할을 한다.
수증기와는 가역적으로 반응하여 다음과 같은 반응을 일으킨다.
그 외에 일산화 탄소가 관여하는 대표적인 반응으로는 다음과 같은 것이 있다.[5][6]
- 코발트, 구리, 철, 납, 망가니즈, 몰리브덴, 니켈, 은, 주석 등의 산화물을 환원시켜 금속의 형태로 만들거나 저급 산화물로 만든다.
- 리간드로서 작용하여 니켈, 철, 코발트, 몰리브덴, 루테늄, 로듐, 오스뮴, 이리듐 등의 금속과 금속 카보닐을 생성한다. 대표적인 것으로는 니켈 카보닐(Ni(CO)4)이 있다.
- 염소와 반응하여 포스젠을 만든다.
- 수산화 나트륨과 반응하여 폼산 나트륨을 생성한다.
- 적절한 조건, 반응물, 촉매 존재 하에 반응하면 메탄올, 폼산 메틸, 프로피온산, 프로필 알코올 등의 매우 많은 종류의 알코올, 알데하이드,
만드는 방법[편집]
모든 유기체에 포함되어 있는 탄소를 태울 때 불완전연소하면 일산화탄소가 생긴다. 따라서, 시체를 태우거나, 동식물의 사체로부터 만들어진 숯, 석탄, 석유 등을 태우면 발생한다.
공업적으로는 석탄이나 코크스와 공기 또는 가열 수증기를 반응시킨 후 이를 정제하여 일산화 탄소를 얻어낼 수 있는데, 대부분의 공업적 용도로는 질소와 수소가 포함된 채로 사용되는 경우가 많다.
실험실에서는 포름산을 진한 황산이나 진한 인산으로 탈수시켜 얻는다.[5]
또한, 카바이드 제조 시에 부산물로 얻어지기도 한다.
용도[편집]
일산화 탄소는 주로 연료, 화학공정의 원료로 사용된다.
일산화 탄소가 화학공정의 원료로 사용된 예는 다음과 같다.[6]
- CO + CH3OH → CH3COOH
이 반응은 특정 금속의 분리에 사용된다.
오염[편집]
일산화 탄소는 대기오염물질의 일종이다. 특히 공장지대나 차량, 항공기가 많이 사용되는 지역에서의 농도가 높다.[6]
안전성[편집]
일산화 탄소는 인화성이 강하기 때문에 취급에 주의를 요한다. 또한 일산화 탄소는 인체 내에서 독성을 가진다.
흡입된 일산화 탄소는 혈액의 헤모글로빈과 결합하여 카복시헤모글로빈을 생성한다. 카복시헤모글로빈은 산소 운반의 기능이 없기 때문에, 이는 혈액의 산소운반능력을 크게 떨어트린다. 흡입된 양에 따라서 두통, 어지러움, 심계항진증, 나른함, 혼란, 구역질이 나타날 수 있으며 심할 경우 경련, 의식 없음, 죽음에까지 이를 수 있다.[7]
일산화 탄소 중독[편집]
각주[편집]
- ↑ 가 나 “Carbon monoxide”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
- ↑ Richard, Pohanish (2012). 《Sittig's Handbook of Toxic and Hazardous Chemicals and Carcinogens》 2판. Elsevier. 572쪽. ISBN 978-1-4377-7869-4. 2015년 9월 5일에 확인함.
- ↑ NIOSH Pocket Guide to Chemical Hazards. “#0105”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ GOV, NOAA Office of Response and Restoration, US. “CARBON MONOXIDE - CAMEO Chemicals - NOAA”. 《cameochemicals.noaa.gov》.
- ↑ 가 나 다 라 마 化學大辭典編集委員會 편, 성용길, 김창홍 역, 〈일산화탄소〉, 《화학대사전》(Vol.7), 서울: 世和, 2001, 576쪽.
- ↑ 가 나 다 Considine, G. D. et al., "CARBON MONOXIDE", Van Nostrand's encyclopedia of chemistry, 5th edition, Hoboken : Wiley-Interscience, 2005, p. 293.
- ↑ 일산화 탄소 MSDS{{ Archived 2006년 10월 20일 - 웨이백 머신
참고 문헌[편집]
- Considine, G. D. et al., Van Nostrand's encyclopedia of chemistry, 5th edition, Hoboken : Wiley-Interscience, 2005.
- 化學大辭典編集委員會 편, 성용길, 김창홍 역, 《화학대사전》, 서울: 世和, 2001.
같이 보기[편집]
- 강릉 펜션 유독가스 질식 사고
- 일산화탄소 감지기(en:Carbon monoxide detector, CO detector)



