세로토닌
이 문서는 참고 문헌 목록을 포함하고 있으나, 각주가 불충분하거나 존재하지 않아 출처가 모호합니다. |
| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
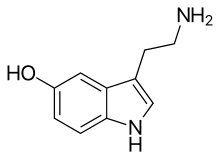
| 3-(2-Aminoethyl)-1H-indol-5-ol | |
| 식별 정보 | |
| CAS 등록번호 | 50-67-9 |
| ATC 코드 | ? |
| PubChem | 5202 |
| ChemSpider | 5013 |
| 화학적 성질 | |
| 화학식 | ? |
| 분자량 | ? |
| 유의어 | 5-HT, 5-Hydroxytryptamine, Enteramine, Thrombocytin, 3-(β-Aminoethyl)-5-hydroxyindole, Thrombotonin |
| 약동학 정보 | |
| 생체적합성 | ? |
| 동등생물의약품 | ? |
| 약물 대사 | MAO |
| 생물학적 반감기 | ? |
| 배출 | ? |
| 처방 주의사항 | |
| 임부투여안전성 | ? |
| 법적 상태 | |
| 투여 방법 | ? |

| |
| 이름 | |
|---|---|
| IUPAC 이름
5-Hydroxytryptamine or
3-(2-Aminoethyl)indol-5-ol | |
| 별칭
5-Hydroxytryptamine, 5-HT, Enteramine; Thrombocytin, 3-(β-Aminoethyl)-5-hydroxyindole, Thrombotonin
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.000.054 |
| KEGG | |
| MeSH | Serotonin |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C10H12N2O | |
| 몰 질량 | 176.215 g/mol |
| 겉보기 | White powder |
| 녹는점 | 167.7 °C (333.9 °F; 440.8 K) 121–122 °C (ligroin)[3] |
| 끓는점 | 416 ± 30 °C (at 760 Torr)[1] |
| slightly soluble | |
| 산성도 (pKa) | 10.16 in water at 23.5 °C[2] |
| 2.98 D | |
| 위험 | |
| 물질 안전 보건 자료 | External MSDS |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose)
|
750 mg/kg (subcutaneous, rat),[4] 4500 mg/kg (intraperitoneal, rat),[5] 60 mg/kg (oral, rat) |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
세로토닌(영어: serotonin, 5-Hydroxytryptamine (5-HT))은 모노아민 신경전달 물질의 하나이며, 생화학적으로 필수아미노산중 하나인 트립토판에서 유도되는 세로토닌은 주로 인간을 포함한 동물의 위장관, 혈소판, 중추신경계에서 볼 수 있다. 세로토닌은 행복감을 포함한 광범위한 감정을 느끼는 데에 기여한다고 보고되고 있는 복잡한 신경전달물질이다.[6]
생물학적 역할[편집]
세로토닌은 수면, 체온조절, 학습, 기억, 고통, 사회적 행동,[7] 성관계, 수유, 동작 활동, 바이오 리듬 등 다양한 생리적 과정에 관여한다.[8] 무척추동물처럼 복잡성이 덜한 동물들에게 세로토닌은 수유와 기타 과정을 조정한다.[9] 식물에서 세로토닌 합성물은 스트레스 신호와 연결된 것으로 보인다.[10][11]
심리적 영향[편집]
세로토닌은 인지, 기분, 불안, 정신병에 관여하지만 그 기전이 명료하지 못하다.[12][13]
자폐 스펙트럼 장애[편집]
신경전달물질과 자폐 스펙트럼 장애(Autism Spectrum Disorder, ASD) 환자에게 미치는 영향에 관한 연구에서, 5-HT는 가장 많이 연구 대상이 되어 왔다.[14] 언급하였듯, 5-HT 신호(signaling)는 신경발생(neurogenesis), 세포 이동(cell migration)과 생존, 시냅스발생(synaptogenesis), 시냅스 가소성(synaptic plasticity) 등 신경 과정을 용이하게 한다.[14] 실험에 참가한 자폐스펙트럼장애 환자 45%는 혈액에 5-HT 농도가 높다고 한다.[14] 또한 비슷한 장애가 있는 동물들에게 수행한 연구에서는 세로토닌 과도현상(hyperserotonemia)이 분리 불안(separation distress)을 억제하는 것을 통하여, 사교적 관심에 대한 동기를 상당히 감소시킨다고 보고하였다. 이는 사회적으로 지장이 있는 자폐스펙트럼장애 환자에게 관련이 있울 수 있다.[14]
세로토닌의 기능[편집]
두뇌 오케스트라의 지휘자[편집]
세로토닌 신경은 뇌줄기(brainstem) 가운데 솔기핵(raphe nucleus)이라는 곳에 위치하며 그 수는 수만 개 정도이다. 이는 뇌 전체 신경세포(약 150억 개)에 비해 아주 적은 수이지만 세로토닌은 뇌 전체에 광범위한 영향을 미친다. 하나의 세로토닌이 수많은 신경을 상대로 하는 모습은 오케스트라의 지휘자가 지휘봉을 휘두르며 곡 전체 분위기를 형성하는 것과 비슷할 것으로 비유할 수 있는 세로토닌 시스템을 갖는다. 구체적으로 세로토닌은 의식수준이나 건강상태 등에 영향을 미친다.
참고로 마음(컨디션, 기분 등을 포함한 개념으로 사용) 상태는
- 도파민 신경: 쾌락의 정열적 움직임, 긍정적인 마음, 성욕과 식욕 등을 관장
- 노르아드레날린 신경: 불안, 부정적 마음, 스트레스 반응 등을 관장
- 세로토닌 신경: 위의 두 가지 신경을 억제하고 너무 흥분하지도 않고 불안한 감정도 갖지 못하게 평온함을 만듦
이 세 가지 신경들이 서로 영향을 주고받으며 형성되는 것이다. 세로토닌 신경이 활성화된 사람은 평상심을 잘 유지할 수 있다는 것을 알 수 있다.
대뇌피질에의 영향[편집]
각성에는 격렬한 각성과 조용한 각성이 있다. 격렬한 각성은 노르아드레날린 신경이 연출하는 것으로서, 외부로부터의 스트레스 자극과 신체 내부 변화에 반응하여 흥분하고 대뇌피질을 강화시켜 각성수준을 올리는 것이다. 이에 반해 세로토닌이 만들어내는 조용한 각성은 스트레스 자극에는 전혀 반응을 보이지 않고 마치 좌선할 때의 각성상태와 같은 조용한 각성이다.
자율 신경에 영향[편집]
각성하면 세로토닌 신경은 낮은 빈도로 규칙적인 임펄스(신경이 정보를 전달할 때 사용하는 전기 신호)를 내보내는데, 이것은 차 엔진의 시동을 걸면 저속으로 규칙적인 회전이 시작되는 것과 같다. 몸을 움직이기 위한 준비상태로 만든다는 것이다. 따라서 아침에 기상과 동시에 세로토닌 신경에서 임펄스가 잘 발생하면 쉽게 일어나 상쾌한 심신상태를 맞이할 수 있다.
근육에 영향[편집]
항중력근(중력 방향에 대항해서 서서 자세를 유지하는 데 필요한 근육: 목덜미, 척추주변, 하지 근육군 뿐만 아니라 눈꺼풀 안면의 근육군도 포함됨) 은 수면 시에는 이완된 상태로 쉬고 있다가 잠에서 깨어남과 동시에 지속적인 수축을 통해 자세나 표정을 만들게 된다. 항중력근을 직접적으로 흥분시키는 것은 척수의 운동신경으로, 세로토닌 신경은 이 운동신경에 자극을 주어 흥분 수준을 올리게 한다. 그렇게 되면 항중력근의 긴장이 높아져 척추 근육이 반듯해져 자세가 좋아지고 얼굴 표정이 팽팽해져 사람이 생기 있어 보인다.
감각에 영향[편집]
약간의 통증에도 아픔을 호소하는 사람이 있는데, 이것은 세로토닌 신경에 문제가 있기 때문이다. 세로토닌 신경을 단련시키면 통증을 전달하는 경로를 억제하여 진통효과가 나타난다.
정서행동장애 간의 연관성[편집]
세로토닌의 분비량이 적어져서 세로토닌 기능이 저하되면 여러 가지 정서․행동장애가 생길 수 있다. 단, 앞으로 언급할 장애들은 몇 가지 상태가 여러 개월 이상 지속적으로 나타나며, 약물이나 의학적 상태 또는 주변 환경에 대한 일시적인 반응이 아니어야 한다.
우울장애[편집]
- 우울장애: 전반적인 슬픈 기분 및 무력감, 무능감, 고립감, 허무감, 죄책감 등을 느끼며 그로 인해 자살충동, 불면증, 체중감소, 식욕과 성욕 감퇴, 일상에서의 즐거움과 흥미 상실 등의 특성이 나타나는 장애이다.
- 우울장애 세로토닌: 우울장애를 갖고 있는 사람은 뉴런과 뉴런 사이에 신경전달물질의 활성도가 떨어져서 세로토닌의 수치가 낮게 나타난다. 따라서 웃음치료나 선택적 세로토닌 흡수 억제제의 한 종류인 '플루옥세틴(fluoxetine, 프로작)'이라는 약의 처방 등의 방법이 널리 쓰이고 있다.
성격장애[편집]
성격장애란?: 인지능력이나 정서, 대인관계, 충동조절 등의 부분에서 각 개인이 속한 사회의 일반적인 사회문화적 기대에서 심하게 이탈된 행동이나 내적 경험이 지속적으로 나타나는 장애이다.
반사회적 성격장애[편집]
- 반사회적 성격장애란?: 사회의 정상적이고 일반적인 규범에 맞추지 못하고 만성적, 반복적으로 비이성적, 비도덕적, 충동적, 반사회적 또는 범죄적 행동을 하고 남의 권리를 무시하거나 침해하고 더 나아가 남을 해치는 행동 등을 나타내는 장애이다. 충동적이고 잦은 거짓말을 하는 등의 사기성을 보이며 공격성, 무책임함을 보이고 양심의 가책이 결여되어 있다. 이는 18세 이후에 나타나고 15세 이전에는 품행장애의 증거가 있어야 한다.
- 반사회적 성격장애와 세로토닌: 이 장애를 갖고 있는 사람은 다른 이에 비하여 세로토닌의 활동수준이 비정상적으로 저하 되어있다. 이러한 세로토닌 분비 저하는 성염색체(X염색체)의 결함으로 인해 MAO라는 효소가 결핍되어 있기 때문이다. 또 최근 연구에는 세로토닌 자체보다는 세로토닌 전달체를 구성하는 유전자(17번 염색체: 5-HTT)의 영향을 받는다는 의견도 있다.
- 세로토닌 과다의 분노양상: 최근의 연구에 따르면, 신경 생물학적 요인으로 신경전달물질인 세로토닌이 비정상적으로 과다 분비되었거나 남성 호르몬인 안드로겐이 높은 경우 공격적 행동에 중요한 요소가 된다. 이런 기질을 선천적으로 타고난 사람은 스트레스를 유발하는 상황에 대해 통제력이 약하기 때문에 일반적이고 평범한 스트레스에도 폭력적이고 공격적인 행동을 보일 수 있다.
경계선 성격장애[편집]
- 경계선 성격장애란?: 정서, 자아상, 행동 및 대인관계 등에 있어서 불안정성을 나타내고 심한 충동성을 갖고 있어서 모든 면에서 변동이 심한 장애이다. 불안정한 주체성으로 인해 대인관계에 있어서도 극과 극을 오가며 낭비, 성관계, 도박, 폭식 등의 부분에서 충동성을 보이고 자살충동이나 자해행위 등을 반복적으로 행하기도 한다.
- 경계선 성격장애와 세로토닌: 경계선급 성격장애를 가진 사람은 세로토닌 시스템이 작동하는 우리 뇌의 앞부분 즉, 전두엽에 장애가 오거나 기능 저하가 와서 세로토닌 분비가 현저히 떨어지는 양상을 보인다.
섭식장애[편집]
섭식장애란?: 섭식장애란 음식을 먹는 데에 있어서 심한 장애를 보이는 장애이다.
신경성 식욕상실증(거식증)[편집]
- 거식증이란?: 현재 체중미달임에도 불구하고 체중이 증가하는 것에 대한 비정상적인 두려움을 갖고 나이와 키에 맞는 최소한의 정상체중으로 유지하는 것조차 거부하는 장애이다. 왜곡된 신체상을 가지고 있고 체중이나 몸매가 자신에 대한 평가기준에 과도한 영향을 미치며 여성의 경우 그로 인한 무월경증이 나타난다. 또한 항상 우울한 기분을 느끼고 충동적으로 행동한다.
- 거식증과 세로토닌: 거식증은 세로토닌 분비량에 직접적으로 영향을 받는다고 보기보다는 거식증으로 인한 우울감이 두드러지게 나타나므로 세로토닌 기능 향상을 위한 노력이 필요하다고 본다. 세로토닌 기능 활성화를 통해 우울감에서 벗어나고 긍정적이고 밝은 사고를 이끌어내어 거식증을 극복하는 데 도움을 줄 수 있다.
신경성 식욕항진증(폭식증)[편집]
- 폭식증이란?: 반복적으로(최소 1주일에 2회, 3개월 동안) 일정시간동안 다른 사람들이 보통 먹는 양에 비해 과도하게 많은 양의 음식을 섭취하고 먹는 것에 대한 조절능력이 현저하게 떨어지는 장애이다. 폭식에 대한 죄책감을 덜기 위해 과도한 운동, 금식, 스스로 유도하는 구토, 이뇨제, 관장제 복용 등의 부적절한 보상행동을 하며 왜곡된 신체상을 갖고 있고 몸매와 체중이 자기평가에 과도하게 영향을 미친다.
- 폭식증과 세로토닌: 세로토닌은 포만감을 느끼게 하고 음식 섭취량을 줄이려는 욕구를 일으키게 한다. 세로토닌이 부족하면 배고픈 상태를 유지하게 되고 달고 기름진 음식에 대한 욕구가 강해져 이로 인해 폭식을 하게 된다. 단 음식을 먹으면 세로토닌이 증가해 포만감을 느끼게 되므로 폭식을 멈추게 되는 것이다. 따라서 선택적 세로토닌 흡수 억제제(SSRI)를 통해 음식을 먹지 않아도 포만감을 느낄 수 있도록 한다.
불안장애[편집]
공황장애[편집]
- 공황장애란?: 갑자기 비정기적으로 공황발작(심장박동수가 심하게 빨라지고 숨이 가쁘고 질식할 것 같은 기분이 들며 현기증, 흉부 또는 복부의 통증, 비현실감, 심한 두려움, 감각이상 등의 증상이 갑작스럽게 나타나고 10분 이내에 그 증상들이 최고조에 달하는 것)이 반복적으로 일어나고 그에 대해 심한 걱정과 특정한 행동의 변화를 보이는 장애이다. 그리고 공황장애는 우울증과 굉장히 밀접한 관련이 있다고 알려져 있다.
- 공황장애와 세로토닌: 뇌 전두엽의 이상으로 인해 세로토닌 기능이 저하되어 공황장애가 나타난다. 따라서 세로토닌의 재흡수를 억제하는 SSRI를 복용함으로써 공황장애 뿐만 아니라 주로 동반되는 우울장애 극복에도 도움을 줄 수 있다.
강박장애[편집]
- 강박장애란?: 강박적 사고나 강박적 행동이 지속적이고 반복적으로 나타나는 장애이다. 강박적 사고란 반복적이고 지속적인 특정 사고, 충동, 심상 등을 부적절하고 침입적으로 경험하며 이로 인해 심한 불안이나 고통을 느끼는 것이다. 그리고 강박적 행동은 주로 강박적 사고에 대한 반응(강박적 사고로 인한 것은 아니다)으로, 어떤 압박감 때문에 외현적인 행동을 하거나 정신적인 활동을 하는 것이다. 이러한 강박적 행동은 고통을 예방하거나 감소시키고 강박적 사고를 중화시키기 위한 행동인데 현실적이거나 합리적이지 못한 것이다.
- 강박장애와 세로토닌: 뇌 전두엽과 기저핵 부분의 혈류 이상으로 인해 세로토닌의 기능이 저하되거나 혹은 세로토닌 수용체의 감수성 증가가 강박장애의 원인으로 알려져 있다. 따라서 세로토닌 재흡수 억제제인 SSRI를 복용하는 것이 일차적인 처방이다.
세로토닌 기능을 이용한 의약품[편집]
- 조루증 치료제(다폭세틴): 짧은시간 동안 사정중추에 세로토닌 농도를 높여 사정을 지연시킨다.
- 우울증 치료제(프로작, 졸로푸트, 렉사프로, 레메론 등): 세로토닌을 활성화하거나 뇌에 더 오래 머물게 한다. 은행잎 추출물 영양제도 효과적이라고 한다.[출처 필요]
- 비만 치료제(시부트라민): 세로토닌의 분비를 증가시킨다
- 금연 치료제(웰부트린): 직접 세로토닌을 증가시키지는 않지만 노르에피네프린 증가를 통해 간접적으로 세로토닌을 증가시키고 식욕과 흡연 충동을 억제한다.
- 과민성 대장증후군 치료제(젤막, 로트로넥스): 장내 세로토닌 수용체에 작용해 장운동을 개선시킨다.
세로토닌과 생체주기[편집]
생체리듬은 인체의 한정된 자원의 한계를 전제하며 따라서 도파민, 노르에피네프린,세로토닌등 신경전달물질을 매우 복잡하고 정교하게 경쟁하에 사용해야할뿐만아니라 이들의 균형을 유지하는 항상성에 에너지를 쏟고있다. 휴식과 음식섭취 그리고 걷기운동과 같은 신체활동은 이러한 생체주기를 안정되게 유지하는 필수적인 요인으로 알려져있다. 또한 뇌 유도성 신경영양인자의 맥락에서처럼 '새로운 학습'(new learning)도 주요한 요인으로 보고되고있다.[15][16]
5-HTP[편집]
5-HTP(5-Hydroxytryptophan) 또는 옥시트립탄(oxitriptan)은 세로토닌(5-HT)의 전구물질이 될수있다.
같이 보기[편집]
각주[편집]
- ↑ Calculated using Advanced Chemistry Development (ACD/Labs) Software V11.02 (©1994–2011 ACD/Labs)
- ↑ Mazák K, Dóczy V, Kökösi J, Noszál B (April 2009). “Proton speciation and microspeciation of serotonin and 5-hydroxytryptophan”. 《Chemistry & Biodiversity》 6 (4): 578–90. doi:10.1002/cbdv.200800087. PMID 19353542. S2CID 20543931.
- ↑ Pietra S (1958). “[Indolic derivatives. II. A new way to synthesize serotonin]”. 《Il Farmaco; Edizione Scientifica》 (이탈리아어) 13 (1): 75–9. PMID 13524273.
- ↑ Erspamer V (1952). “Ricerche preliminari sulle indolalchilamine e sulle fenilalchilamine degli estratti di pelle di Anfibio”. 《Ricerca Scientifica》 22: 694–702.
- ↑ Tammisto T (1967). “Increased toxicity of 5-hydroxytryptamine by ethanol in rats and mice”. 《Annales Medicinae Experimentalis et Biologiae Fenniae》 46 (3, Pt. 2): 382–4. PMID 5734241.
- ↑ Young SN (2007). “How to increase serotonin in the human brain without drugs”. 《Rev. Psychiatr. Neurosci.》 32 (6): 394~99. PMC 2077351. PMID 18043762.
- ↑ Kravitz EA (September 1988). “Hormonal control of behavior: amines and the biasing of behavioral output in lobsters”. 《Science》 241 (4874): 1775–81. Bibcode:1988Sci...241.1775K. doi:10.1126/science.2902685. PMID 2902685.
- ↑ Zifa E, Fillion G (September 1992). “5-Hydroxytryptamine receptors”. 《Pharmacological Reviews》 44 (3): 401–458. PMID 1359584.
- ↑ Srinivasan S, Sadegh L, Elle IC, 외. (June 2008). “Serotonin regulates C. elegans fat and feeding through independent molecular mechanisms”. 《Cell Metabolism》 7 (6): 533–44. doi:10.1016/j.cmet.2008.04.012. PMC 2495008. PMID 18522834.
- ↑ Ramakrishna A, Giridhar P, Ravishankar GA (June 2011). “Phytoserotonin: a review”. 《Plant Signaling & Behavior》 6 (6): 800–9. doi:10.4161/psb.6.6.15242. PMC 3218476. PMID 21617371.
- ↑ Ramakrishna A, Ravishankar GA (November 2011). “Influence of abiotic stress signals on secondary metabolites in plants”. 《Plant Signaling & Behavior》 (Informa) 6 (11): 1720–1731. doi:10.4161/psb.6.11.17613. PMC 3329344. PMID 22041989.
- ↑ Chilmonczyk Z, Bojarski AJ, Pilc A, Sylte I (August 2015). “Functional Selectivity and Antidepressant Activity of Serotonin 1A Receptor Ligands”. 《International Journal of Molecular Sciences》 16 (8): 18474–506. doi:10.3390/ijms160818474. PMC 4581256. PMID 26262615.
- ↑ Blier P, El Mansari M (2013). “Serotonin and beyond: therapeutics for major depression”. 《Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences》 368 (1615): 20120536. doi:10.1098/rstb.2012.0536. PMC 3638389. PMID 23440470.
- ↑ 가 나 다 라 Eissa N, Al-Houqani M, Sadeq A, Ojha SK, Sasse A, Sadek B (2018년 5월 16일). “Current Enlightenment About Etiology and Pharmacological Treatment of Autism Spectrum Disorder”. 《Frontiers in Neuroscience》 12: 304. doi:10.3389/fnins.2018.00304. PMC 5964170. PMID 29867317.
- ↑ [참고](The role of BDNF and its receptors in depression and antidepressant drug action: Reactivation of developmental plasticity Eero Castrén Tomi Rantamäki First published:22 February 2010 https://doi.org/10.1002/dneu.20758Citations: 484)https://onlinelibrary.wiley.com/doi/abs/10.1002/dneu.20758
- ↑ [참고](Nat Neurosci. 2015 Nov;18(11):1606-16. doi: 10.1038/nn.4116. Epub 2015 Sep 21. 5-HT1A Receptors on Mature Dentate Gyrus Granule Cells Are Critical for the Antidepressant Response Benjamin Adam Samuels 1, Christoph Anacker 1, Alice Hu 1, Marjorie R Levinstein 1, Anouchka Pickenhagen 1, Theodore Tsetsenis 2, Noelia Madroñal 2, Zoe R Donaldson 1, Liam John Drew 1, Alex Dranovsky 1, Cornelius T Gross 2, Kenji F Tanaka 3, René Hen 1 Affiliations expand PMID: 26389840 PMCID: PMC4624493 DOI: 10.1038/nn.4116)https://pubmed.ncbi.nlm.nih.gov/26389840/ Archived 2020년 11월 8일 - 웨이백 머신
참고 문헌[편집]
- 김청송(2006). 이상심리학. 서울: 영진.COM
- 김청송(2007). 정신장애 사례연구. 서울: 학지사
- 김용식 외(2008). 비정형 항정신병제의 임상. 서울: 서울대학교 출판부
- 아리타 히데오(2007). 뇌를 행복하게 하라. 성기홍 외(역). 서울: 푸른솔
- ERIC J.MASH 외(2007). 아동이상심리학. 조현춘 외(역). 서울: 시그마프레스
- RITA WICKS NELSON 외(2005). 아동기 행동장애. 정명숙 외(역). 서울: 시그마프레스
- 다음 백과사전. 선택적 세로토닌 재흡수 억제제. http://enc.daum.net
- 청소년 아이프랜드. 이상심리학^^. https://web.archive.org/web/20180318180555/http://i-friend.org/
- 연세대학교 원주기독병원 정신과. 성격장애. http://psychiatry.yonsei.ac.kr/
- [참고](Cell Volume 157, Issue 7, 19 June 2014, Pages 1535-1551, Natural Neural Projection Dynamics Underlying Social Behavior
Author links open overlay panelLisa A.Gunaydin15LoganGrosenick125Joel C.Finkelstein15Isaac V.Kauvar15Lief E.Fenno12AvishekAdhikari1StephanLammel3Julie J.Mirzabekov1Raag D.Airan1Kelly A.Zalocusky12Kay M.Tye1PolinaAnikeeva1Robert C.Malenka3KarlDeisseroth134 DOI https://doi.org/10.1016/j.cell.2014.05.017)https://www.sciencedirect.com/science/article/pii/S009286741400659X
