의공학
| 의공학 | |
|---|---|
 초음파진단기 모습 | |
| 학문명 | 의공학 |
의공학(醫工學, 의용생체공학/생체의공학, biomedical engineering)은 보건진료의 용도를 위해 의료와 생물학의 설계 개념 및 공학원리가 융합된 응용분야이다. 이 분야는 공학과 의료 사이의 간극을 줄이도록 노력하고 있다. 진단, 관찰 및 치료를 포함하는 보건 치료를 개선하기 위해 의학과 생물학과 함께 공학의 기법으로 설계하고 문제를 푼다. 최근에 떠오르는 정밀의료를 의공학 및 빅데이터로 구현하여, 저렴한 비용으로 100세까지 건강한 삶을 누릴 수 있도록 목표를 확대하고 있다.
의공학은 다른 많은 공학 분야에 비해, 비교적 최근에 독자적인 학문으로 떠오르고 있다. 이러한 진화는 그 자체가 한 분야로 간주되기에, 이미 확립된 분야 간의 학제적 전문이 되는 새로운 분야로 전환이 되는게 일반적이다. 의공학에서의 작업의 대부분은 서브필드의 광범위한 분야에 걸친 연구개발로 이루어져 있다. 의공학 응용 프로그램은 임상 장비로부터 재생조직의 성장, 제약 및 치료 생물학적 제제, MRI와 EEG 같은 일반적인 영상기기, 작은 이식장비까지의 범위인 생체적합, 보철물, 다양한 진단과 치료 의료기기의 개발을 포함하고 있다.
의용 생체 공학의 주목할만한 하위 학문분야는 의료 응용 프로그램 측에서과 엔지니어링 측면에서, 두 개의 각도에서 볼 수 있다. 의공학 엔지니어는 양쪽의 시각(능력)을 가지고 있어야 한다. 많은 의료 전문분야 (예 : 심장과, 신경과)와 같은 일부 BME 하위 분야는 다음과 같은 인체의 특정 시스템과의 관계에 의해 구별된다 :
- 심장 혈관 기술 - 심장 혈관 시스템의 진단 및 치료에 관련된 모든 약물, 생물학적 제제 및 장치를 포함한다.
- 신경 기술 - 뇌와 신경 시스템의 진단 및 치료에 관련된 모든 의약품, 생물학적 제제 및 장치를 포함한다.
- 정형 외과 기술 - 골격 시스템의 진단 및 치료에 관련된 모든 약물, 생물학적 제제 및 장치를 포함한다.
그 예는 해부학이나 생리학의 특정 측면에 초점을 맞춘다.
약간의 변형된 접근법은 신체의 특정 부위(시스템)와는 달리 해결하고자 병리생리학(기전)의 종류에 기초하여 기술의 종류를 식별할 수 있다 : 예를 들면
- 암 기술 - 암의 진단과 치료와 관련된 모든 의약품, 생물학적 제제 및 장치를 포함한다.
추가로, BME 내 하위 분야는 (넓은 수준)를 포함 할 수 있는 또다른 기본 공학 분야의 협회에 의해 분류된다 :
- 화학 공학에 기초 생화학-BME : 생화학 세포, 분자 및 조직 공학, 생체 재료 및 biotransport(생체내 변화)와 관련됨.
- 전기공학 및 컴퓨터 과학을 기반으로 생체 전기-BME : 생체 전기 및 신경 공학, 생체 계측, 바이오 메디컬 이미징 및 의료 기기와 관련됨. 이것은 또한 광학 및 광학 기술을 포함하기도 한다. - 생물 의학 광학, 생물 정보학, 이미징 및 관련 의료 기기.
- 기계 공학을 기반으로 생체 역학 - BME : 생체 역학, biotransport(생체내 변화), 의료 기기 및 연부 조직 역학과 같은 생물학적 시스템의 모델링과 관련됨.
분야를 하위 분류로 세분하는 또 하나의 방법은 만든 제품의 기준이다. 의료에 사용되는 치료 및 진단 제품은 일반적으로 다음과 같은 범주에 속한다. :
- 생물제재(Biologics) 및 바이오 의약품(Biopharmaceuticals)은 종종 합성 생물학의 원리를 사용하여 설계 (합성 생물학은 유전 공학의 연장이다). 생물학 및 바이오 제약 제품의 개발은 BME와 관련되거나 중복하는, 바이오 기술(biotechnology) 및 생명 공학(bioengineering)의 분야를 폭넓게 활용한다.
- 의약품 (작은 분자 또는 비생물학적)
- 전자및기계 장치
- 복합제품
의공학은 보건의료 전반의 기술에 포함되는데, 이 보건의료기술(HT; Health Technology)은 건강 증진과 질병의 방지를 위한 진단과 치료, 재활에 쓰이는 모든 기술 및 산업을 통칭하는 말이다. 의료에 사용되는 의약품, 의료기기, 치료법과 병원 조직 체계 등을 모두 포함한다.
역사
[편집]인간의 역사는 선사시대부터 시작하여 현대 문명에 이르기까지 실로 기술의 발전이라고 불러도 손색이 없을 만큼 기술의 발전과 함께해 왔다. 또한, 사람들의 질병의 시달림으로부터 벗어나기위한 수단으로서 의학의 발달이 이루어졌다. 기술의 발전은 공학(Engineering)으로 구체화되었고, 질병치료와 생명 구제는 의학(Medicine)으로 구체화되었다. 그리고 이 두 학문을 합하여 상호간의 발전을 도모하는 학문이 바로 의공학(Biomedical engineering)이다.
현대 의학과 기기
[편집]이탈리아의 과학자 갈릴레오 갈릴레이는 유리관에 눈금을 그은 온도계를 1593년에 발명하였다. 1592년 갈릴레이가 만든 온도계는 온도가 오르면 공기가 부풀어올라 수위가 내려갔다. 1714년, 독일의 파렌하이트는 정확한 온도 눈금이 붙은 (화씨) 온도계를 만들었다. 이것은 얼음이 녹는 온도를 32도, 체온을 96도, 물이 끓는 온도를 212도로 하고 있다. 1742년 스웨덴의 셀시우스가 만든 수은 온도계의 눈금은 현재에도 그대로 섭씨 온도 눈금으로 쓰여지고 있다.
의공학의 태동은 1750년대 취리히 대학의 생리학교수였던 요한 술저(Johann Sulzer)의 업적으로 평가된다. 그는 전기 자극이 근육 자극제로 작용할 수 있는지 관심을 가지고 실험을 해 금속 사이에 혀를 놓으면 짜릿한 신맛이 발생함을 알아냈다. 그리고 이탈리아 볼로고나(Bologona)대학의 해부학 교수 루이지 갈바니(Luigi Galvani)는 해부된 개구리의 근육에 전극의 가했을 때 근육의 수축을 관찰하여 생체전기(bioelectricity)를 발견한다.
이후 네덜란드의 빌럼 아인트호벤(Willem Einthoven)은 1903년 심전도(electrocardiogram,ECG)를 반조형 검류계(mirror type string galvanometer)를 이용하여 기록함으로써 최초로 생체전기를 기록하는데 성공한다. 또한, 1924년 드 포레스트(De Forest)의 3극 진공관을 이용하여, 독일의 한스 베르거(Hans Berger)가 뇌전도(electoencephalogram, EEG) 장치를 계발한다.
생체전기와는 다른 분야에서는 1927년 미국의 Dinker에 의해 최초의 인공호흡기(respirator)발명하였고, 1936년 J.Laurence는 감마선 등의 방사선을 이용하여 인체의 연조직 내부에 발생하는 암(cancer)을 효과적으로 진단, 치료하는 핵의학(Nuclear Medicine)의 기초를 마련하였다. 이후 1960년대 후반 의사이자 엔지니어인 Raymond Damadian은 NMR 스펙트로스코피가 정상조직과 악성 조식의 스펙트럼이 다르다는 것을 알아내고, 1974년 <사이언스>지에 쥐 종양 MRI 사진을 실었다.
체내에 넣어 질병을 치료하는 이식형 의료기기에 대한 기술도 상당히 빠르게 발전되어왔다. 1969년 D.A.Cooley 최초의 인공심장 이식실험이 실시되었으며 현재까지 수많은 인공장기가 만들어지고 있다. (출처: 의용생체전자공학개론, 조진호 외 3인)
의공학 분야의 정립과 학술단체
[편집]제2차 세계대전을 거치며 눈부신 발전을 계속하고 있던 전자공학 기술은 이러한 여러 가지 측면에서의 요구를 모두 충족시키면서 급속도로 의학 분야에 응용되기 시작하였다. 이에 따라 새로운 학문 분야의 정립과 그 개념 설정이 이루어지기에 이르렀는데, 1958년 파리에서 열린 국제회의에서 처음으로 의학에 전자공학 기술을 도입한 연구 분야를 ME(Medical Electronics, 의용전자공학)로 명명하기로 제창하였다. 이 학회가 IFMBE(International Federation for Medical and Biological Engineering)로 세계 최대 규모의 의공학 학술 집단이다. 본부는 파리에 있고 현재 30개국이 가입하고 있으며, 3년 마다 학회가 열린다. 세계 최초로 의용생체공학(Biomedical engineering)이라는 정식 명칭을 사용한 국제적 모임이다. [1]
그 다음 미국에 본부를 둔 국제전자전기학회(International Electrical Engineering Engineers, IEEE)의 산하 학술단 IEEE 의생물학공학협회(Engineering in Medicine and Biology Society,EMBS) 등이 있으며 [2], 일본, 영국, 독일 등도 모두 자국 내에 의공학 관련 학회를 가지고 있다.
대한민국에는 1979년 대한의용생체공학회(Korea Society of Medical and Biology Engineering,KOSOMBE)가 설립되어 현재 3000명의 회원이 등록되어 있다.[3]
생물 정보 공학 (Bioinformatics)
[편집]생물 정보학은 생물학적 데이터를 이해하기위한 방법과 소프트웨어 툴을 개발하는 융합적 분야이다. 여러 과학이 포함된 분야로서, 생물 정보공학은 생물학적 데이터를 분석하고 해석하기 위해 컴퓨터 과학, 통계, 수학, 공학이 결합되어 있다.
생물 정보공학은 방법론의 일환으로 컴퓨터 프로그램을 사용하여 생물학적 연구의 본체에 대한 포괄적 인 용어일 뿐만 아니라, 특히 유전체학(게놈)의 분야에서 반복적으로 사용되는 특정 분석 "파이프 라인"에 대한 기준이기도 하다. 생물 정보학의 일반적인 용도는 후보 유전자 및 뉴클레오티드(SNP)의 식별을 포함한다.
생체역학 (Biomechanics)
[편집]생체역학을 보세요.
생체 재료 (Biomaterial)
[편집]생체 재료는 인체 장기와 상호 작용하는 모든 물질, 표면 또는 구조물이다. 과학으로, 생체 재료는 오십년의 역사가 있다. 생체 재료의 연구는 생체 재료 과학 또는 생체 재료 공학이라고 한다. 그것은 새로운 제품의 개발에 거액의 돈을 투자하는 많은 기업들이 있는데, 그 역사를 통해 지속적으로 강한 성장을 경험하고있다. 생체 재료 과학은 의학, 생물학, 화학, 조직 공학 및 재료 과학의 분야를 포함한다.
의광학 (Biomedical Optics)
[편집]en:Biomedical Optics을 보세요.
조직 공학 (Tissue Engineering)
[편집]유전 공학 (아래 참조)과 같은 조직공학은 바이오 공학의 주요 세그먼트이며, BME와 상당히 겹친다. 조직공학의 목표 중 하나는 장기 이식이 필요한 환자를 위해 (생물학적 재료를 통해) 인공 장기를 만드는 것이다. 의공학 엔지니어는 그런 장기를 만드는 방법을 현재 연구하고 있다. 최근에는 3D printing 기술로 이들 장기를 만들어보고자하는 많은 노력을 하고 있다. 예를 들어, 현재 전 세계 보청기의 95%는 3D 프린터로 생산되고 있으며, 치아 보정물의 경우 하루 65만 쌍이 3D 프린터로 제작되고 있다.
유전 공학 (Genetic Engineering)
[편집]유전 공학, 재조합 DNA 기술, 유전자 변형 / 조작 (GM)과 유전자 접합은 유기체의 유전자의 직접 조작에 적용되는 용어이다. 유전 공학은 생물의 유전자가 간접적으로 조작하는 전통적인 육종과 다르다. 유전 공학은 직접 유전자의 구조 및 특성을 변화하는 분자 클로닝 및 변형 기술을 사용한다. 유전 공학 기술은 다양한 응용 프로그램에서 성공을 발견했다.
신경 공학 (Neural Engineering)
[편집]신경 공학(또한 Neuro engineering라고도 함)은 신경 시스템을 이해 수리, 교체 또는 향상시키기 위해 엔지니어링 기술을 사용하는 분야이다. 신경 엔지니어는 살이 있는 신경 조직과 인공 전자 장치와의 인터페이스에서 설계 문제를 해결할 수 있는 고유 한 기술을 보유하고 있다.
제약 공학 (Pharmaceutical Engineering)
[편집]제약 공학은 때때로 생물의공학의 한 분야, 때로는 화학 공학의 한 분야로 간주되며 실제로, 매우 하이브리드 하위 분야를 가진다.(많은 BME 분야처럼) 최근에 바이오시밀러(영어: biosimilar) 또는 동등생물의약품은 특허가 만료된 생물의약품에 대한 복제약 분야가 한참 뜨고 있다. 바이오 복제약, 바이오제네릭(Biogeneric)이라 부르기도 한다.
의료기기 (Medical Device)
[편집]
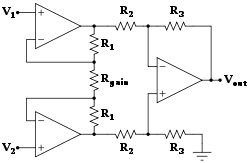
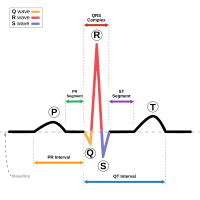
의료 기기라 함은 다음의 목적이 있어야 한다. (의료기기의 정의)
- 질병의 진단, 치료, 경감, 처치 또는 예방의 목적으로 사용되는 제품;
- 상해 또는 장애의 진단, 치료, 경감 또는 보정의 목적으로 사용되는 제품;
- 인체 구조 또는 기능의 검사. 대체 또는 변형의 목적으로 사용되는 제품;
- 임신조절의 목적으로 사용되는 제품
대한민국에서는 재활보조기구중 의지, 보조기기는 의료기기에서 제외한다.
의료 영상 (Medical Imaging)
[편집]의료 영상(생체의료영상)은 의료기기의 주요 부분이다. 이 분야는 임상의에게 직간접적으로 보통의 영상에 보이지 않는 것을 보이게 하는 것에 대해 다룬다. 이는 초음파, 자기, 자외선, 다른 방사선 및 기타 수단을 포함할 수 있다. 영상기술은 의료진단에 종종 필수이며, 전형적으로 병원에서 찾을 수 있는 복잡한 장비는 다음과 같다.
- en:Fluoroscopy (투시영상)
- en:Magnetic resonance imaging (자기공명영상/MRI)
- en:Nuclear medicine (핵의학)
- en:Positron emission tomography (양전자 방출 단층촬영/PET) PET scans PET-CT scans
- en:X-ray(엑스선)나 CT scans(엑스선 전산화 단층 촬영) 같은 Projection radiography
- en:Tomography (단층영상)
- en:Ultrasound (초음파진단기), 의료 초음파
- en:Optical microscopy (광학 현미경)
- en:Electron microscopy (전자 현미경)
- 의료영상저장전송시스템 (PACS)
이식 장치 (Implants)
[편집]임플란트는 없어진 생물학적 장기 구조를 대체하여 (생의학 조직 이식을 나타내는 이식과 비교하여) 그 역할을하도록 만든 의료 기기의 일종이다. 몸에 접촉한 임플란트 장치의 표면은 대부분의 기능이 무엇인지에 따라 티타늄, 실리콘 또는 인회석 등의 생물 의학 재료로 만들어질 수 있다. 어떤 경우에는 임플란트는 전자 장치(예를 들어 인공 심장 박동기와 인공 와우)를 포함한다. 일부 임플란트는 이식할 수 있는 알약이나 약물 방출 스텐트의 형태로 피하 약물 전달 장치로, 생리 활성화한다.
생체 공학 (Bionics)
[편집]Bionics라는 단어는 생명체를 뜻하는 그리스어 bion에서 유래하였으며, 1958년 미국국립항공우주국(en:NASA)의 잭 스틸(Jack E. Steele)이 처음으로 사용하였다.생체 공학은 간략히 말하자면 생명체의 기능을 모방하는 기술로 인간공학(Human Engineering)등이 포함된다. 우리 주변에서 흔히 볼 수 있는 인체공학적 상품들처럼 인체에 맞게 만들어진 물건들을 비롯하여, 물고기의 유선형 몸체를 이용한 잠수함, 새의 날개를 모방하여 만든 로봇 등이 모두 생체 공학의 범주에 들어간다고 볼 수 있다. 또한, 기계 팔과 같이 인체의 동작을 모방하여 그 대용물을 만들어 내는 것 역시 바이오닉스의 한 종류라 할 수 있겠다.
인공 신체 부위 교체는 바이오닉의 많은 응용 중 하나다. 인체 시스템의 특성과 기능에 대한 복잡하고 철저한 연구에 관심이 있는 바이오닉스는 엔지니어링 문제를 해결하기 위해 적용될 수 있다. 다양한 기능과 눈, 귀, 기타 기관의 과정을 면밀히 조사하여 카메라, TV, 라디오 송신기 및 수신기, 기타 여러 유용한 도구를 이용하여 개선 할 수 있다. 이러한 발전은 실제로 우리의 삶을 더 좋게 만들었지만 생체 공학이 만들어 낸 최고의 기여는 생물 의공학(인체의 여러 부분에 대한 유용한 대체물의 제조) 분야이다. 현대 병원은 부상이나 질병으로 심하게 손상된 신체 부위를 대체 할 수 있는 예비 부품을 보유하고 있다. 생물 의공학도는 의사와 손 잡고 인공 신체 부위를 만들고 있다.
모바일 헬스케어(Mobile Healthcare)
[편집]이는 Ubiquotous Healthcare(U-Healthcare), Smart Healthcare 또는 M-Health(Telehealth(원격의료), Telemedicine, eHealth)라고 불리는데, 병의 검출/치료보다는 병의 예후관리 분야 및 노인에 대한 만성질환 관리가 앞으로 훨씬 더 커지므로, 이를 해결하기 위해서는 병원을 벗어난 곳에서 모니터링을 할 수 있는 M-healthcare가 대세로 떠오르고 있다. 최근에 사물인터넷(IoT)과 함께 가정에서 나의 건강을 외부 환경, 나의 배설물들을 모니터링하는 것부터 나의 손목밴드나 착복할 수 있는(wearable) 옷들을 이용하여 신체 정보를 항상 모니터링하는 기술 및 제품들이 대세로 떠오르고 있다. 한국에서는 U-Healthcare 품목[4]으로 16가지를 지정한바 있다. 이는 원격 의료 기술을 활용하고 있다.
스마트 헬스케어(smart healthcare)는 4차산업혁명 또는 헬스케어 3.0에서 요구하는 연결성을 중요시한 개념의 모바일 및 가정용 의료기기를 말한다. 이 연결은 모바일을 가능하게 하기 위해 주로 wifi나 bluetooth를 의미하며, 결과를 핸드폰이나 pad를 통해 보고, 필요시 cloud computing system에 연결하여 인공지능의 도움으로 개인 맞춤, 정밀 진단을 지원하는 쪽으로 가고 있다. 2016년 CES에서는 이 분야가 완전 붐이었다. (생체기능을 측정하는 스마트 워치, 손목 밴드를 통한 바이오 리듬 측정 및 코치등..)
의료기기로서의 소프트웨어(Software as Medical Device)
[편집]Software as Medical device로 SaMD라 표기한다. 이는 2018년부터 미국 FDA가 허가하기 시작한 소프트웨어 약이다. 소프트웨어만으로도 질병을 고치는 의료기기의 역할로 인정한 것이다. 핸드폰의 앱이 나의 행동을 측정하고, 관리(예:식이요법등)하여 병이 나빠지지 않게 하고, 호전되도록 할 수 있는 의료기기이다. 기존의 의료기기에 들어가 있는 소프트웨어는 Software in Medical Device로 SiMD라 표기한다.
임상 공학 (Clinical Engineering)
[편집]임상 공학은 병원 또는 기타 임상 환경에서 의료장비 및 기술의 실제 구현을 다루는 의공학의 한 분야이다. 임상 엔지니어의 주요 역할은 다음과 같다.
- 생물의공학(Biomedical engineering) 장비 기술자(BMETs)의 교육과 감독,
- 기술 제품이나 서비스를 선택 및 의료장비 환경 구현 실행 관리
- 감독 / 감사에 대한 정부의 규제당국과의 협조
- 병원내의 다른 직원 (예 : 의사, 관리자, IT 등)을 위한 기술적 컨설팅
임상 엔지니어들은 임상 경험을 바탕으로 향후 디자인 개선에 관한 의료 기기 제조 업체와의 자문 및 협업은 물론 가장 최신의 기술의 장비가 도입이 되도록 구매 패턴을 재정립하거나 적절의 진행을 모니터링할 수 있다.
재활공학 (Rehabilitation engineering)
[편집]재활 공학은 장애인이 부딪히는 문제에 대한 기술 솔루션을 설계, 개발, 적용, 테스트, 평가, 적용 및 배포하는 엔지니어링 과학의 체계적인 응용 분야이다. 재활 공학을 통해 연결된 기능 영역은 이동성, 통신, 청각, 시각과인지 및 고용과 관련 활동, 독립적인 생활, 교육 및 일반사회와의 통합을 포함 할 수 있다. 일부 재활 엔지니어는 의용 생체 공학의 일반적으로 하위 전문분야인 재활 공학 석사 학위를 가지고 있지만, 대부분의 재활 엔지니어는 생물 의학 공학, 기계공학 또는 전기공학 학사 또는 석사 학위를 가지고 있다. 장애인(people with disabilities)의 재활 과정은 가끔 오락, 상거래, 주류 사회속으로 해당 사용자를 포함하는 것을 촉진하기 위한 산책 보조 같은 보조 장치의 설계디자인을 의미한다.
법적인 문제
[편집]의료 장치로 인한 많은 사건이 환자에게 발생했는데 이를 해결하기 위한 규제 문제는 지속적으로 지난 수십 년간 증가되었다. 예를 들어, 2008년에서 2011년까지, 미국에서 119건의 FDA 클래스 I으로 분류된 의료 기기의 리콜이 있었다. 미국 식품 의약국 (FDA)에 따르면, 클래스 I 리콜은 사용 또는 제품을 사용하거나 노출하면 심각한 건강상의 부작용이나 사망을 초래할 수 있는 가능성이 있는 상황과 관련되어 있다. 국가 별 법규에 관계없이, 주요 규제의 목표는 전 세계적으로 일치하고 있다. 예를 들어, 의료 기기 규정에서, 의료기기 제품은 다음을 지켜야 한다.
- 안전해야 하고
- 진단 및 치료하고자 하는 임상적 내용에 효과적이어야 하고
- 제조된 모든 장치에 적용 됨
환자, 사용자 및 제 3자가 의도 한 용도로 신체적 위험 (사망, 상해, ...)등의 용인 할 수 없는 위험이 없으면 제은 안전하다. 잔류 위험을 허용 수준에서 사용하는 데 따른 이익과 비교하여 잔류 위험을 줄이기 위해 장치에 보호 조치를 도입해야 한다.
제품이 의도된 용도로 제조업체가 지정한대로 작동하는 경우 제품의 효과가 있다. 효과는 임상 평가, 성능 표준 준수 또는 이미 판매된 장치와의 상당한 동등성 입증을 통해 달성된다.
이전 기능은 의료 기기의 모든 제조 품목에 대해 보장되어야 한다. 이를 위해서는 전체 의료 기기 수명주기 동안 안전성(safety)과 효과성(effectiveness)에 영향을 미칠 수 있는 모든 관련 단체 및 프로세스에 대한 품질 시스템이 마련되어야 한다.
의료 기기 엔지니어링 영역은 가장 엄격하게 규제되는 엔지니어링 분야이며, 의공학 엔지니어를 수행하는 것은 규제법관련 변호사 및 기타 전문가들과 정기적으로 협의하고 협조해야 한다. FDA (Food and Drug Administration)는 의료 기기, 의약품, 생물 제제 및 복합 제품에 대한 관할권을 가진 미국의 주요 보건 관리 당국이다. FDA의 정책 결정을 이끌어내는 주요 목표는 21 CFR 829 규정에 명시된 품질 시스템을 통해 보장되어야하는 건강 관리 제품의 안전성과 효율성이다. 또한 의공학 엔지니어는 물리적 치료 장치 ( "의료"장치이기도 함)와 같이 "소비자"용 장치 및 기술을 개발하기 때문에 소비자 제품 안전위원회 (Consumer Product Safety Commission)에서 일부면에서 관리 될 수 있다. 가장 큰 장애물은 510K "클리어런스"(일반적으로 클래스 2 디바이스 용) 또는 시판 전 "승인"(일반적으로 약물 및 클래스 3 디바이스 용)이 되는 경향이 있다.
유럽의 경우 의료기기 지침을 보면, 안전성과 품질은 "제조업체가 자사의 의료 기기가 유럽 의료기기 지침의 요구 사항을 준수 함을 입증하는 방법"으로 정의 된 "적합성 평가(Conformity Assessment)"를 통해 보장된다. 이 지침은 클래스 I 장치에 대한 간단한 준수 선언 (부록 VII)부터 EC 검증 (부속서 IV), 생산 품질 보증 (부속서 V), 제품 품질 보증 (부속서 VI), 전체 품질 보증 (부속서 II)까지의 장치 클래스에 따라 다른 절차를 규정한다. 의료 기기 지침은 인증을 위한 세부 절차를 규정한다. 일반적으로 이러한 절차에는 위험 관리 파일, 기술 파일 및 품질 시스템 납품과 같은 특정 납품에 포함될 테스트 및 검증이 포함된다. 위험 관리 파일은 다음과 같은 설계 및 제조 단계를 처리하는 첫 번째 산출물이다. 위험 관리 단계에서는 제품 사용에있어 환자에게 기대되는 이익과 관련하여 제품 위험이 허용 수준에서 감소되도록 제품을 동작시켜야 한다. 기술 파일에는 의료 기기 인증을 지원하는 모든 문서 데이터 및 기록이 들어 있다. FDA 기술 파일은 다른 구조로 구성되어 있지만 비슷한 내용을 가지고 있다. 품질 시스템 결과물에는 일반적으로 모든 제품 수명주기 동안 품질을 보장하는 절차가 포함된다. 동일한 표준 (ISO EN 13485)은 일반적으로 GMP라는 이름으로 미국 및 전 세계의 품질 관리 시스템에 적용된다.
유럽 연합에는 유럽 연합 회원국이 인정한 "인증 기관(Notified Bodies; NB)"이라는 인증 기관이 있다. 인증 기관은 클래스 I 장치를 제외한 모든 의료 장치에 대해 제조업체가 생산한 적합성 선언이 마케팅에 충분할 경우 인증 프로세스의 효율성을 보장해야하며 이를 위해 심사한다. 제품이 의료 기기 지침에서 요구하는 모든 단계를 거치면 기기는 의도 한대로 사용되었을 때 안전하고 효과적이라고 생각되는 CE 마크가 유럽 연합 지역내에서 표시 될 수 있다.
각 나라별로 규제가 다른 경우에, 더 유리한 규제 방식에 따라 미국이나 유럽에서 먼저 특정 기술이 개발되기도 한다. 각국이 국가 간 분배를 용이하게하기 위해 실질적인 조화(harmony)를 이루기 위해 노력하는 동안, 최적의 규제 범위에 대한 철학적 차이는 방해가 될 수 있다. 보다 제한적인 규제가 직관적인 수준에서 매력적으로 보이지만 일부 비평가들은 생명을 구하는 개발에 대한 액세스 속도를 늦추는 측면에서 잘못된 규제라고 비판한다.
대한민국의 의료기기법[5]과 유럽의 의료기기 지침, 미국의 FDA 법령은 같은 레벨의 법령(지침)이다.
RoHS II
[편집]더 나은 RoHS (로하스라 읽음) 준수 2로 알려진 지침 2011/65/EU는 원래 2002년에 도입된 법안의 재정리 버전이다. 원래의 EU 법률인 " 전기 및 전자 장비의 특정 유해 물질 사용 제한" (RoHS 지침 2002/95/EC )은 2011년 7월에 발표된 2011/65/EU, 즉 일반적으로 RoHS 준수 2로 알려진 지침으로 대체되었다. RoHS 지침으로 이러한 장치 가 재생 될 때 이후 환경으로 배출 되는 특정 독소와 중금속에, 전자 제품 유통에서 위험 물질을 제한하고자 한다. 이 RoHS 대응의 범위는 의료 기기 , 산업 기기 등의 이전에 별도의 제품을 포함하도록 넓혀진다. 추가적으로, 제조 업체는 이제 적합성 위험 평가 및 테스트 보고서를 제공 할 의무가 있고 또는 그들이 부족한 이유를 설명할 의무가 있다. 처음엔, 제조 업체 뿐만 아니라 수입 및 유통업체도 전기 및 전자 장비가 유해 물질 제한 규정을 준수하는 RoHS 범위 내에 있음을 확인하고 해당 제품 에CE 마크를 가질 책임을 공유한다. 2013년 1월 2일까지 회원국들은 이 법을 RoHS2로 바꾸어야 한다.
의료기기를 개발하여 판매를 하려면 반드시 허가를 받아야 한다. 그 허가를 받기 위해 필요한게 국가에서 공인한 시험성적서인데 그 시험성적서는 이 IEC60601-1 (의료전기기기 - part 1 : 기본 안전과 필수성능에 대한 일반적인 요구사항)을 기초로 평가한다. 유럽은 2012.7월부터 시작되었고, 미국은 2014.1월부터, 한국은 2015.1월부터 단계적으로 시행된다. (4등급은 2015.1.1부터, 3등급은 2015.7.1 부터, 2등급은 2016.1.1 부터, 1등급은 2016.7.1부터 적용)
- 대한민국의 전기.기계적 안전에 관한 공통기준규격[6] (2015.12.31)
- IEC60601-1 3.1판 [별표1] 의료기기의 전기기계적 안전에 관한 공통 기준 및 시험방법
- IEC 60601-1-3 [별표2] (의료기기의 방사선 안전에 관한 일반요구사항)
- IEC 60601-1-6 [별표3] (Usability; 의료기기의 사용적합성에 관한 보조기준규격)
- IEC 60601-1-8 [별표4] (Alarm; 의료기기의 경보시스템에 관한 보조기준규격)
- IEC 60601-1-11 (Home Healthcare; 의료기기의 홈헬스케어 환경에 관한 보조기준규격)
- 대한민국의 IEC 60601-1 3판 Guideline = [7] (2013.7)
- IEC 60601-1-2 (의료기기의 전자파안전에 관한 공통기준규격)[8]
- ISO 14971 (위험관리 가이드라인) = [9] (2007.1.1)
- ISO 10993 (생체적합성 : Bio-Compatibility) : 의료기기의 생물학적 안전에 관한 공통기준규격(인체 접촉에 의해 영향을 미치는 독성 시험) [10] (2014.4.24)
- IEC 62304 (의료기기 소프트웨어 - software life cycle process, 참조 의료 소프트웨어
GMP
[편집]회사로는 GMP (Good Manufacturing Practice)라는 품질시스템을 인증받아야, 그 시험성적서를 가지고 품목허가를 받을 수 있다.
- 식약처의 의료기기 제조 및 품질관리 기준(KGMP) = [11] (2016.12.30)
임상시험
[편집]의료기기 임상시험 계획 승인에 관한 규정 = [12] (2016.11.10)
의료기기 임상시험 길라잡이 = [13] (2017.06.01)
훈련 및 인증
[편집]교육
[편집]의공학 엔지니어는 공학 및 생물학에 대한 상당한 지식이 필요하며 일반적으로 BME (생물 의공학) 또는 다른 학문에서 석사 (MS, M.Tech, MSE 또는 M.Eng.) 또는 박사 (Ph.D.) BME가 중첩될 수있는 상당한 가능성을 지니고 있다. BME에 대한 관심이 높아짐에 따라 많은 기술 대학에는 현재 학부 (B.Tech, B.S., B.Eng 또는 B.S.E.)에서 박사급에 이르는 다양한 생물 의공학부 또는 프로그램이 있다. 생물 의공학은 최근 다른 학문 분야의 교차 학문적 하이브리드 전문화가 아닌, 자체 학문으로 부상하고 있다. 그리고 모든 수준의 BME 프로그램은 실제로 많은 학생들이 의학 학교 준비를위한 "예비 전공"으로 사용하는 많은 생물 과학 내용을 포함하는 생의학 공학 학사를 포함하여 더욱 널리 보급되고 있다. 생의공학 엔지니어의 수는 의료 기술 향상의 원인과 결과 모두로 상승 할 것으로 예상된다.[1]
미국에서는 공인 생명 공학 / 생물 의학 공학 프로그램(공학교육인증, en:ABET)을 받은 학부 프로그램의 수가 점점 더 많아지고 있다. 현재 65 개가 넘는 프로그램이 ABET의 인증을 받았다. 한국에선 공학인증을 받은 의공학과는 한군데도 없다.
많은 학위와 마찬가지로, 프로그램의 평판과 순위는 취업이나 대학원 입학을 위해 학위 소지자의 희망사항을 고려할 수 있다. 많은 학부 과정의 평판은 연구 자금 및 책자, 출판물 및 인용과 같은 평가에 대한 확실한 요소가 있는 대학원 또는 연구 프로그램과 관련이 있다. 특히 BME (의공학)이 있으면, BME 부서 / 프로그램의 명성에 의해 대학 병원 및 의대의 순위를 매기는데 중요한 요소가 될 수 있다.
대학원 교육은 BME에서 특히 중요한 측면이다. 많은 공학 분야 (예 : 기계 또는 전기공학)는 해당 분야에서 초급 직업을 얻기 위해서는 대학원 수준의 교육이 필요하지 않지만 대부분의 BME 직책은 이를 선호하거나 필요로 한다. 대부분의 BME 관련 직업은 제약 및 의료 기기 개발과 같은 과학 연구가 포함되기 때문에 대학원 교육은 거의 필수 사항이다. (일반적으로 학부 학위는 충분한 연구 훈련 및 경험이 필요하지 않기 때문에). 이 교육은 석사 또는 박사 학위일 수 있다. 의공학이라는 특정 전문 분야(학계 및 기업)에서는 다른 분야보다 Ph.D. 가 휠씬 더 많다.
다른 과학 분야와 마찬가지로 BME의 대학원 프로그램은 매우 다양하며 특정 프로그램은 해당 분야의 특정 측면을 강조한다. BME의 융합학문적 성격으로 인해 다른 분야 (예 : 의과 대학 또는 기타 엔지니어링 부서)의 프로그램을 통해 광범위한 협력 활동을 펼칠 수도 있다. 석사나 박사 학위는 일반적으로 지원자에게 BME 또는 다른 엔지니어링 분야 (특정 생명 과학 과정 포함) 또는 생명 과학 (특정 공학 과정 포함)에서 학사 학위를 취득하도록 요구한다.
전세계적으로 BME 교육은 크게 다르다. 미국은 광범위한 생명 공학 분야와 수많은 주요 대학, 내부 장벽이 비교적 적기 때문에, BME 교육 및 훈련 기회의 발전에 많은 노력을 기울였다. 대규모의 생명 공학 분야와 인상적인 교육 시스템을 갖춘 유럽에서도 유럽 공동체가 여전히 존재하는 국가 관할 장벽 중 일부를 대체하기 위해 통일된 표준을 만드는 데 어려움을 겪고 있다. 최근 유럽에서 BIOMEDEA[14] Archived 2017년 1월 9일 - 웨이백 머신와 같은 중요한 기획으로 BME 관련 교육 및 전문 표준 개발에 박차를 가하고 있다. 호주와 같은 다른 국가들은 BME 교육의 결함을 수정하고 인식하고 있다. 또한 고도의 기술 노력은 선진국의 흔적이기 때문에 일부 지역은 BME를 비롯하여 교육 개발의 속도가 느려지기도 한다.
한국내 의공학 연구 현황 정리 = [15]
한국내 의공학과가 있는 대학 = [16]
라이선스/증명서
[편집]한국에서는 의공기사 자격증제도가 있다.
대한생체공학회에서의 의공기사 자격 시험 안내 = [17] Archived 2013년 12월 17일 - 웨이백 머신
RA (regulatory Affair) 자격증 = 의료기기정보기술지원센터에서 교육하고 자격증을 준다. [18]
한국에서의 의공학 분야 정부 연구
[편집]2009.10 산업원천기술로드맵 = [19]
2011.12 신성장동력 장비 개발 로드맵 = [20]
2012.12 2012년 의료기기산업분석보고서 = [21]
대한민국 산업기술비전 2020 융합신산업편 = [22]
국민의료비 및 국내시장
[편집]2016년 : 1년 전체 국민의료비 = 2.9만$ (우리나라 1인당 GDP) * 5150만명 (우리나라 인구수) * 7.7% (GDP대비 의료비 비중) * 1156원 = 133조원
이중에 의료기기 소비자 시장 : 10% ; 133조원 * 10% = 13.3조원 [23]
2016년 식약처 의료기기 시장 통계 자료 = [24]
2016년 국내 의료기기 시장 분석[25]
전세계 의료기기 시장
[편집]다음은 Espicom이 2014년도에 발행한 Worldwide Medical Market Forecasts to 2019의 내용을 인용했다. (2014년 → 2019년 시장 크기 예측)
진단영상장치 857억$ -> 1160억$ (DIAGNOSTIC IMAGING)
의료소모품 529억$ -> 747억$ (CONSUMABLES)
치과제품 235억$ -> 315억$ (DENTAL PRODUCTS)
정형기구 403억$ -> 566억$ (ORTHOPAEDICS & PROSTHETICS)
환자 지원 424억$ -> 596억$ (PATIENT AIDS)
기타 954억$ -> 1294억$ (OTHERS)
계 3403억$ -> 4678억$
(참조로 타분야의 2020년의 시장을 보면, 휴대전화 4235억$, PC 1690억$ 보다 의료기기 시장이 크다[26])
같이 보기
[편집]각주
[편집]- ↑ U.S. Bureau of Labor Statistics - Profile for Engineers 보관됨 2월 19, 2006 - 웨이백 머신

