테스토스테론: 두 판 사이의 차이
Mark Marcus Marco (토론 | 기여) 편집 요약 없음 태그: m 모바일 웹 고급 모바일 편집 |
Mark Marcus Marco (토론 | 기여) 편집 요약 없음 태그: m 모바일 웹 고급 모바일 편집 |
||
| 131번째 줄: | 131번째 줄: | ||
안드로겐은 질 조직의 생리기능을 조절하고 여성의 성적 흥분에 기여한다.<ref name="pmid12007897">{{cite journal | vauthors = Traish AM, Kim N, Min K, Munarriz R, Goldstein I | title = Role of androgens in female genital sexual arousal: receptor expression, structure, and function | journal = Fertility and Sterility | volume = 77 Suppl 4 | pages = S11–8 | date = Apr 2002 | pmid = 12007897 | doi = 10.1016/s0015-0282(02)02978-3 }}</ref> 여성의 테스토스테론 수치는 포옹 전보가는 성교 전, 포옹 후 보다는 성교 후에 높다.<ref name="pmid17320881">{{cite journal | vauthors = van Anders SM, Hamilton LD, Schmidt N, Watson NV | s2cid = 5718960 | title = Associations between testosterone secretion and sexual activity in women | journal = Hormones and Behavior | volume = 51 | issue = 4 | pages = 477–82 | date = Apr 2007 | pmid = 17320881 | doi = 10.1016/j.yhbeh.2007.01.003 | hdl = 2027.42/83880 | hdl-access = free }}</ref> 여성의 성기 흥분 상태에 있어 테스토스테론이 작용할 때 시간 지연 효과가 있다. 게다가 질의 성적 흥분이 지속적으로 증가하는 것은 성기의 감각과 성적 욕구적 행동(sexual appetitive behavior)이 높아지는 결과를 낳는다.<ref name="pmid10665617">{{cite journal | vauthors = Tuiten A, Van Honk J, Koppeschaar H, Bernaards C, Thijssen J, Verbaten R | title = Time course of effects of testosterone administration on sexual arousal in women | journal = Archives of General Psychiatry | volume = 57 | issue = 2 | pages = 149–53; discussion 155–6 | date = Feb 2000 | pmid = 10665617 | doi = 10.1001/archpsyc.57.2.149 | doi-access = free }}</ref> |
안드로겐은 질 조직의 생리기능을 조절하고 여성의 성적 흥분에 기여한다.<ref name="pmid12007897">{{cite journal | vauthors = Traish AM, Kim N, Min K, Munarriz R, Goldstein I | title = Role of androgens in female genital sexual arousal: receptor expression, structure, and function | journal = Fertility and Sterility | volume = 77 Suppl 4 | pages = S11–8 | date = Apr 2002 | pmid = 12007897 | doi = 10.1016/s0015-0282(02)02978-3 }}</ref> 여성의 테스토스테론 수치는 포옹 전보가는 성교 전, 포옹 후 보다는 성교 후에 높다.<ref name="pmid17320881">{{cite journal | vauthors = van Anders SM, Hamilton LD, Schmidt N, Watson NV | s2cid = 5718960 | title = Associations between testosterone secretion and sexual activity in women | journal = Hormones and Behavior | volume = 51 | issue = 4 | pages = 477–82 | date = Apr 2007 | pmid = 17320881 | doi = 10.1016/j.yhbeh.2007.01.003 | hdl = 2027.42/83880 | hdl-access = free }}</ref> 여성의 성기 흥분 상태에 있어 테스토스테론이 작용할 때 시간 지연 효과가 있다. 게다가 질의 성적 흥분이 지속적으로 증가하는 것은 성기의 감각과 성적 욕구적 행동(sexual appetitive behavior)이 높아지는 결과를 낳는다.<ref name="pmid10665617">{{cite journal | vauthors = Tuiten A, Van Honk J, Koppeschaar H, Bernaards C, Thijssen J, Verbaten R | title = Time course of effects of testosterone administration on sexual arousal in women | journal = Archives of General Psychiatry | volume = 57 | issue = 2 | pages = 149–53; discussion 155–6 | date = Feb 2000 | pmid = 10665617 | doi = 10.1001/archpsyc.57.2.149 | doi-access = free }}</ref> |
||
여성이 |
여성이 테스토스테론 기본 수치가 상대적으로 높으면, 이들은 성적 흥분 수치 증가가 더 높디만 테스토스테론 증가치는 적다. 이는 여성의 테스토스테론 수치에 나타나는 천정효과(ceiling effect)이다. 성적인 사고 역시 테스토스테론 수치를 변화시키지만, 여성 신체 내 코르티솔 수치는 변화시키지 않으며, 호르몬 피임은 성적 사고에 대한 테스토스테론 반응의 변화에 효과를 끼칠 것이다.<ref name="pmid21185838">{{cite journal | vauthors = Goldey KL, van Anders SM | s2cid = 18691358 | title = Sexy thoughts: effects of sexual cognitions on testosterone, cortisol, and arousal in women | journal = Hormones and Behavior | volume = 59 | issue = 5 | pages = 754–64 | date = May 2011 | pmid = 21185838 | doi = 10.1016/j.yhbeh.2010.12.005 | hdl = 2027.42/83874 | url = https://deepblue.lib.umich.edu/bitstream/2027.42/83874/1/sexy_thoughts.pdf | hdl-access = free }}</ref> |
||
테스토스테론은 [[여성 성적 흥분 장애]](female sexual arousal disorder) 치료에도 효과가 있다고 밝혀졌다.<ref name="Bolour_2005">{{cite journal | vauthors = Bolour S, Braunstein G | title = Testosterone therapy in women: a review | journal = International Journal of Impotence Research | volume = 17 | issue = 5 | pages = 399–408 | year = 2005 | pmid = 15889125 | doi = 10.1038/sj.ijir.3901334 | doi-access = free }}</ref> 또한 피부 패치로도 사용 가능하다. [[미국식품의약국]](FDA)이 인정한 안드로겐 부족 치료를 위한 안드로겐 조제약은 없다. 그러나 노년 여성의 리비도 저하와 성적 기능 부전(sexual dysfunction) 치료를 위한 [[ |
테스토스테론은 [[여성 성적 흥분 장애]](female sexual arousal disorder) 치료에도 효과가 있다고 밝혀졌다.<ref name="Bolour_2005">{{cite journal | vauthors = Bolour S, Braunstein G | title = Testosterone therapy in women: a review | journal = International Journal of Impotence Research | volume = 17 | issue = 5 | pages = 399–408 | year = 2005 | pmid = 15889125 | doi = 10.1038/sj.ijir.3901334 | doi-access = free }}</ref> 또한 피부 패치로도 사용 가능하다. [[미국식품의약국]](FDA)이 인정한 안드로겐 부족 치료를 위한 안드로겐 조제약은 없다. 그러나 노년 여성의 리비도 저하와 성적 기능 부전(sexual dysfunction) 치료를 위한 [[오프라벨]](off-label use)로 사용되어 왔다. 테스토스테론은 갱년기 이후 여성들이 에스트로겐 분비가 원활하게 될 경우 좋은 치료제일 수 있다.<ref name="Bolour_2005"/> |
||
==== 이성 관계 ==== |
|||
남성은 사랑에 빠지면 테스토스테론 수치가 낮아지지만 여성은 반대로 증가한다. 이로 인해 남녀의 행동 간에 일시적으로 차이가 감소하게 된다.<ref name="pmid15177709">{{cite journal | vauthors = Marazziti D, Canale D | s2cid = 24651931 | title = Hormonal changes when falling in love | journal = Psychoneuroendocrinology | volume = 29 | issue = 7 | pages = 931–36 | date = Aug 2004 | pmid = 15177709 | doi = 10.1016/j.psyneuen.2003.08.006 }}</ref> 그러나 약 4년 동안의 "신혼기간(honeymoon phase)"이 끝난 후, 이러한 태스토스테론 수치 변화는 더이상 보이지 않는다.<ref name="pmid15177709" /> 테스토스테론 수치가 적은 남자는 관계에 머물 가능성이 더 높으며,<ref name="pmid16621328">{{cite journal | vauthors = van Anders SM, Watson NV | s2cid = 22477678 | title = Relationship status and testosterone in North American heterosexual and non-heterosexual men and women: cross-sectional and longitudinal data | journal = Psychoneuroendocrinology | volume = 31 | issue = 6 | pages = 715–23 | date = Jul 2006 | pmid = 16621328 | doi = 10.1016/j.psyneuen.2006.01.008 | hdl = 2027.42/83924 | hdl-access = free }}</ref> or married,<ref name = "Booth_Dabbs_1993"/> 수치가 높은 남자는 이혼할 가능성이 높다.<ref name = "Booth_Dabbs_1993">{{cite journal | vauthors = Booth A, Dabbs JM|title=Testosterone and Men's Marriages | journal = Social Forces | year = 1993 | volume = 72 | issue = 2 | pages = 463–77 | doi = 10.1093/sf/72.2.463}}</ref> 결혼 및 결혼생활 이행은 테스토스테론 수치를 떨어뜨릴 수 있다.<ref name=Mazur_Michalek_1998>{{cite journal | vauthors = Mazur A, Michalek J | title = Marriage, Divorce, and Male Testosterone | journal = Social Forces | year = 1998 | volume = 77 | issue = 1 | pages = 315–30 | doi = 10.1093/sf/77.1.315 }}</ref> |
|||
이성 관계가 없었던 독신 남성은 이성 관계가 있었던 남성에 비해 테스토스테론 수치가 낮다. 이는 이전의 이성 관계가 있던 경험이 그렇지 않은 경우보다 더 경쟁성 있다는 것을 시사한다.<ref name=Gray_2004>{{cite journal | vauthors = Gray PB, Chapman JF, Burnham TC, McIntyre MH, Lipson SF, Ellison PT | s2cid = 33812118 | title = Human male pair bonding and testosterone | journal = Human Nature | volume = 15 | issue = 2 | pages = 119–31 | date = Jun 2004 | pmid = 26190409 | doi = 10.1007/s12110-004-1016-6 }}</ref> 유부남의 경우, 배우자나 아이와 시간을 보내는 것 등의 연대 유지 활동을 하는 동안이나 그렇지 않은 동안이나 테스토스테론 수치에 차이가 없다. 종합적으로 이런 결과는 연대 유지 활동에 비해 경쟁 활동 상태가 테스토스테론 수치 변화에 더 관련있다는 것을 말한다.<ref name="pmid15219639">{{cite journal | vauthors = Gray PB, Campbell BC, Marlowe FW, Lipson SF, Ellison PT | s2cid = 18107730 | title = Social variables predict between-subject but not day-to-day variation in the testosterone of US men | journal = Psychoneuroendocrinology | volume = 29 | issue = 9 | pages = 1153–62 | date = Oct 2004 | pmid = 15219639 | doi = 10.1016/j.psyneuen.2004.01.008 }}</ref> |
|||
테스토스테론 수치가 높은 남성이 혼외정사를 벌일 가능성이 더 높다.<ref name=Booth_Dabbs_1993/> 테스토스테론 수치는 파트너의 물리적 존재에 영향받지 않는다. 같은 도시에 있거나 장거리 연애중이 있어도 수치는 비슷하다.<ref name="pmid16621328" /> 물리적 존재는 테스토스테론 파트너의 상호작용에 관한 관계에 있는 여성들에게 필요하다. 같은 도시에 사는 남성과 연애하는 여성은 장거리 연애 여성보다 테스토스테론 수치가 낮다.<ref name="pmid17196592">{{cite journal | vauthors = van Anders SM, Watson NV | s2cid = 30710035 | title = Testosterone levels in women and men who are single, in long-distance relationships, or same-city relationships | journal = Hormones and Behavior | volume = 51 | issue = 2 | pages = 286–91 | date = Feb 2007 | pmid = 17196592 | doi = 10.1016/j.yhbeh.2006.11.005 | hdl = 2027.42/83915 | hdl-access = free }}</ref> |
|||
== 의학적 사용 == |
== 의학적 사용 == |
||
2021년 10월 26일 (화) 14:23 판
| |

| |
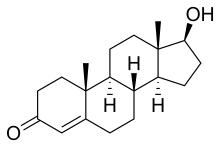
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
| (8R,9S,10R,13S,14S,17S)- 17-hydroxy-10,13-dimethyl- 1,2,6,7,8,9,11,12,14,15,16,17- dodecahydrocyclopenta[a]phenanthren-3-one | |
| 식별 정보 | |
| CAS 등록번호 | 58-22-0 57-85-2 (propionate ester) |
| ATC 코드 | G03BA03 |
| PubChem | 6013 |
| 드러그뱅크 | DB00624 |
| ChemSpider | 5791 |
| 화학적 성질 | |
| 화학식 | C19H28O2 |
| 분자량 | 288.42 |
| SMILES | eMolecules & PubChem |
| 물리적 성질 | |
| 녹는점 | 155 °C (311 °F) |
| 비선광도 | +110.2° |
| 연소 엔탈피 | −11080 kJ/mol |
| 약동학 정보 | |
| 생체적합성 | 낮음 (초회통과효과(first pass effect)가 크기 때문) |
| 동등생물의약품 | ? |
| 약물 대사 | 간, 고환, 전립선 |
| 생물학적 반감기 | 2–4시간 |
| 배출 | 소변 (90%), 배설물 (6%) |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | X(미국)기형아 출산 가능성으로 인해 금지됨 |
| 법적 상태 |
|
| 투여 방법 | 근육 내 투여, 피하 침투 (크림, 젤, 패치), sub-'Q' pellet |
테스토스테론(testosterone)은 남성 혹은 수컷(male)의 주요 성호르몬(sex hormone)이자 아나볼릭 스테로이드(anabolic steroid)이다.[1] 남성에게서 테스토스테론은 고환(testicles)이나 전립선(prostate) 등 남성의 생식 기관의 발달, 근골격 크기 증대나 체모(body hair) 성장 등 2차 성징(secondary sexual characteristic) 촉진에 중요한 역할을 한다.[2] 또한 남성과 여성 모두에게 있어 테스토스테론은 기분(mood)이나 행동 등에 관한 건강과 행복, 그리고 골다공증(osteoporosis) 예방에 관여한다.[3][4][5][6][7][8] 남성이 테스토스테론이 부족하면 허약(frailty)과 골손실(bone loss)을 야기한다.
테스토스테론은 케톤기(ketone group)과 하이드록시기(hydroxy group)를 각각 3위(positions three)와 17(positions seventeen)에 포함하고 있는 안드로스탄(androstane) 류의 스테로이드(steroid)이다. 콜레스테롤(cholesterol)로부터 유래하여 몇 단계에 걸쳐 생합성(biosynthesis)되어 간(liver)에서 비활성 대사물질(inactive metabolite)로 변환된다.[9] 안드로겐 수용체(androgen receptor)와의 연계 및 안드로겐 수용체 활성화를 통해 활동한다.[9] 인간 및 대부분의 척추동물(vertebrate)에서, 테스토스테론은 남성 혹은 수컷의 고환(testicles)에서 분비되며, 여성 혹은 암컷의 난소(ovaries)에서도 소량 분비된다. 평균적으로 성인 남성은 성인 여성에 비해 분비량이 7-8배에 달한다.[10] 남성에게서 테스토스테론 대사가 더 뚜렷해지면, 일일 분비량은 20배 더 커진다.[11][12] 여성이나 암컷 역시 호르몬에 더 예민해진다.[13]
천연호르몬 역할에 외에도, 테스토스테론은 남성의 생식기능저하증(hypogonadism) 및 여성의 유방암(breast cancer) 치료 약물로 사용한다.[14] 남성이 나이가 들면서 테스토스테론 수치가 떨어짐에 따라, 노인들에게 치료용으로 테스토스테론을 사용하기도 한다. 또한 운동선수들은 경기력 향상 약물(Performance-enhancing drug)로서 체격과 수행능력 향상을 위해 불법적으로 사용하기도 한다.[15] 세계반도핑기구(World Anti-Doping Agency)는 테스토스테론을 'S1 아나볼릭 약제, 항상 금지(S1 Anabolic agent substance prohibited at all times)'로 등재시키고 있다.[16]
생물학적 효과
보통 테스토스테론과 같은 안드로겐(androgen)은 안드로겐 수용체(androgen receptor)와 함께 단백질 합성(protein synthesis)과 조직의 성장을 촉진한다.[17] 테스토스테론은 남성화(virilization)와 아나볼릭 효과(anabolic effect)를 갖는다고 하지만, 이러한 범주 묘사는 임의적인데 이들 사이에는 상호 중첩이 있기 때문이다.[18]
- '아나볼릭 효과(Anabolic effects)'는 근육량(muscle mass) 및 근력(muscle strength) 성장, 골밀도(bone density) 및 골력(bone strength) 증가, 골성숙(bone maturation)과 선형 성장의 자극을 포함한다.
- '안드로겐 효과(Androgenic effects)'는 성기(sex organ)의 성숙, 특히 음경(penis) 성숙과 태아의 음낭(scrotum)의 형성, 탄생 후 사춘기(puberty)에 목소리 변성, 턱수염(beard) 등 수염 발달, 액모(axillary hair) 성장이 있다. 대부분은 남성의 2차 성징(secondary sex characteristics) 범주에 속한다.
테스토스테론 효과는 흔히 발생하는 연령에 따라 분류될 수 있다. 남녀의 출산 후 효과(postnatal effect)에 있어, 효과는 자유 테스토스테론(free testosterone) 순환의 수치와 지속에 대부분 종속되어 있다.
출산 전
출산 전 효과는 두 범주로 나뉘며, 발달 단계와 관련하여 분류된다.
첫 시기는 임신 4-6주차이다. 중심선 융합(midline fusion) 남성 요도(phallic urethra), 음낭이 얆아지고 주름이 생김, 음경 확대 등 생식기의 남성화가 발생한다. 테스토스테론 역할은 디하이드로테스토스테론(dihydrotestosterone) 역할보다 작다. 또한 전립선(prostate gland)과 정낭(seminal vesicle)도 발달한다.
임신 4-6개월차에 안드로겐 수치는 성별 형성과 연관된다.[19] 특히 테스토스테론은 반 뮐러 호르몬(anti-Müllerian hormone, AMH)과 함께 볼프관(Wolffian duct) 성장과 뮐러관(Müllerian duct) 퇴화를 촉진한다.[20] 이 시기동안 태아의 남성화나 여성화가 이뤄지며, 이때의 테스토스테론 수치는 성인 때의 그것보다 성유형별 행동 혹은 여성 혹은 남성적 행동을 예측하는데 있어 훨씬 좋은 지수가 될 수 있다. 출산 전 안드로겐은 성별 활동에 관한 흥미와 수행에 영향을 주며, 공간 능력에 효과를 끼친다.[21] 선천부신과다형성(Congenital adrenal hyperplasia, CAH)을 보이는 여성들은, 어려서부터 남성스러운 놀이를 하는 모습을 보이며, 이는 곧 여성이라는 것에 대한 만족도 저하 및 성인기 이성에 대한 흥미 감소로 이어진다.[22]
영아 초기
초기 영아 안드로겐 효과는 거의 규명되지 않았다. 남아는 생후 1주차에 테스토스테론 수치가 올라간다. 수치는 몇 달 동안 사춘기 범위에 남지만, 4-7개월까지 거의 탐지되지 않는 수준에 도달한다.[23][24] 이러한 테스토스테론 수치 상승의 기능은 알려져 있지 않다. 신체 다른 부분에서 유의미한 변화가 규명되지 않았기에 두뇌의 남성화는 발생한다.[25] 남성의 두뇌는 테스토스테론이 에스트로겐(estrogen)으로 방향족화(aromatization)하는 것을 통해 남성화된다. 에스트로겐은 혈액뇌장벽(blood–brain barrier)을 건너서 남성의 두뇌로 들어가지만, 여성 태아는 α-페토프로틴(α-fetoprotein)을 가지고 있는데, 이는 에스트로겐과 결합하여 여성 두뇌가 영향받지 않도록 한다.[26]
사춘기 이전
사춘기 이전에, 안드로겐 수치 상승 효과는 소년과 소녀 모두에게 발생한다. 이는 성인 유형 체취(body odor), 피부와 모발 기름기 증가, 여드름, 음모발생(pubarche), 겨드랑이털, 폭발적인 성장, 골성숙 증가, 수염 등이 있다.[27]
사춘기
안드로겐이 일반 성인 여성 수치보다 수개월 혹은 수년 동안 높을 때 사춘기(puberty)에의 테스토스테론 효과가 발생한다. 남성에게 있어 이러한 효과는 후기 사춘기 효과이며, 여성에게는 혈액 내 자유 테스토스테론(free testosterone) 수치가 높아진 시기가 지속된 이후에 발생한다. 효과는 다음과 같다.[27][28]
- 고환 내 정자형성 조직(spermatogenic tissue)의 성장, 남성 수정 능력(male fertility), 음경(penis) 혹은 음핵(clitoris) 크기 증가, 리비도(libido) 증가 및 발기(erection) 혹은 음핵 충혈(clitoral engorgement) 빈도 증가.
- 성장 호르몬(human growth hormone)의 발현과 함께 턱, 눈썹, 볼, 코 성장, 얼굴뼈 윤곽 재구축[29]
- 골성숙(bone maturation) 및 성장 완료, 이는 에스트라디올(estradiol) 대사산물(metabolite)을 통하여 간접적으로 진행하기에, 여성보다 남성에게 보다 점진적으로 발생
- 근력 및 근육량 증가, 어깨가 벌어지고 흉곽(rib cage)이 넓어지며, 목소리가 굵어지고 목젖(Adam's apple)이 성장함
- 피지샘(sebaceous glands) 확대. 이로 인해 얼굴에 여드름이 생기고, 얼굴의 피하지방(subcutaneous fat)이 줄어든다.
- 음모(pubic hair)가 허벅지와 배꼽으로 확장, 구레나룻이나 턱수염 등 얼굴 체모 발달, 두피모(머리털) 손실(탈모), 흉모(가슴털), 유선모(periareolar hair), 항모(perianal hair), 각모(다리털), 액모(겨드랑이털) 증가.
성인기
테스토스테론은 정상적인 정액(sperm) 생산에 필요하다. 정원세포(spermatogonia)의 구분을 촉진하는 세르톨리 세포(Sertoli cell) 내 유전자를 활성화한다. 지배 도전(dominance challenge) 하에 급성 HPA (hypothalamic–pituitary–adrenal axis) 반응을 조절한다.[30] 테스토스테론을 포함한 안드로겐은 근성장을 높인다. 또한 테스토스테론은 인간에게 있어 거핵구(megakaryocyte)와 혈소판(platelet)의 트롬복산 수용체(thromboxane A2 receptor) 개수를 조절하며, 이를 통해 혈소판응집(platelet aggregation)을 조절한다.[31][32]
성인 테스토스테론 효과는 여성보다 남성에게 분명 두드러지지만, 남녀에게 모두 중요하다. 테스토스테론 수치가 인생 후반부에 저하되면서 그 효과도 줄어든다.[33]
건강 위험
테스토스테론은 전립선암(prostate cancer) 발병 위험을 높이진 않는다. 테스토스테론 차단요법(testosterone deprivation therapy)을 받았음에도 거세된 경우의 테스토스테론 수치보다 높은 테스토스테론 수치 증가를 보이는 경우, 이는 보유하고 있는 전립선암 확산율을 증가시키게 된다.[34][35][36]
심혈관 건강 유지에 있어 테스토스테론의 중요성에 있어서는 상반된 결과를 보여 왔다.[37][38] 그럼에도, 노년기 정상 태스토스테론 수치를 유지하는 경우, 지방제외체중(lean body mass), 내장지방량 감소, 총 콜레스테롤 저하, 혈당 조절 등 심혈관 질환 발병률 감소와 관련된 지표들이 향상된다고 밝혀졌다.[39]
안드로겐 수치가 높으면 질병을 가지고 있는 여성은 물론 건강한 일반 여성도 생리불순을 보인다.틀:Better source needed[40]
성적 흥분
테스토스테론 수치는 성적 활력(sexual activity)과 상관 없이 매일 아침에 피크에 이르는 일주야 리듬(nycthemeral rhythm)을 따른다.[41]
여성의 심적 안정이 핵심인 긍정적 오르가즘 경험과 테스토스테론 수치 간에 정적 연관성이 있다. 테스토스테론과 남성의 오르가즘 경험 감지 간의 연관성은 없다. 또한 남녀 모두 테스토스테론 수치가 높을수록 성적 자기주장(sexual assertiveness)도 더 높다는 연관성 역시 없다.[42]
여성의 성적 흥분(sexual arousal)과 자위(masturbation)는 테스토스테론 농도의 소폭 증가를 가져온다.[43] 남성은 자위 이후 다양한 스테로이드의 혈장(blood plasma) 수치가 유의미하게 증가하며, 테스토스테론 수치는 이러한 스테로이드 수치들과도 연관되어 있다.[44]
영장류 연구
쥐 연구에 의하면, 쥐들의 성적 흥분 정도는 테스토스테론 감소에 영향받기 쉽다. 테스토스테론이 차단된 쥐들에게 테스토스테론 중간 수치를 투여하면 이 쥐들은 교미나 파트너 선택 등의 성적 행동을 재개하지만, 소량을 주입하면 그렇지 않다. 따라서 이러한 포유동물들은 불감증(hypoactive sexual desire disorder) 등의 환자들에게 하나의 모델을 제공한다.[45]
모든 포유종에게 있어, 남성은 새로운 여성을 만나면 테스토스테론 수치가 증가한다. 반응적 테스토스테론이 수컷 쥐에게서 증가하는 것은 남성의 성적 흥분 초기 수치와 관련된다.[46]
인간을 제외한 영장류 동물들에게서. 테스토스테론은 사춘기 성적흥분을 자극, 이로 인해 여성과의 성적 경험 탐색이 증가하게 되고 여성에 대한 성적 선호를 보인다.[47] 일부 연구에 의하면, 테스토스테론이 성인 남성이나 성인 남성 영장류 사이에서 사라지면 성적 동기(sexual motivation)가 감소하지만, 성적 활동 능력 자체가 감소하는 것과는 무관하다.[47]
정자 경쟁 이론(sperm competition theory) 입장에서, 성적으로 자극받은 수컷쥐는 이전에는 중립적이었던 자극에도 테스토스테론 수치가 오르는 반응을 보인다.[48] 이런 반응은 발기나 사정 등 하나 이상의 수컷이 짝짓기 대상을 만날 때 정자 경쟁에 도움 주는 음경 반사(penile reflex)를 보이게 하여, 정액 생산을 늘리고 번식 기회를 높이도록 한다.
남성
남성에게 테스토스테론 수치가 높은 것은 성적 활동 기간과 관련 있다.[49][50]
성적으로 노골적인 영화 한 편을 본 남성은 영화가 끝난 이후 60–90분 동안 테스토스테론 수치가 평균 35% 증가하지만, 성적이지 않은 영화를 본 남성은 증가하지 않는다.[51] 또한 성적인 장면이 노출된 영화를 본 남성들은 동기와 경쟁력이 증가하지만 피로는 감소하였다.[52] 성적 흥분 이후 이완과 테스토스테론 수치 간의 연관성도 밝혀졌다.[53]
남성의 짝짓기 행동에 효과를 끼친다는 남성의 테스토스테론 수치는 배란기 여성의 체취에 노출되었는지 여부에 따라 바뀐다. 배란기 여성 체취에 노출된 남성은 배란기가 아닌 여성의 체취에 노출된 경우보다 테스토스테론 수치가 안정되게 유지되었다. 남성은 여성의 호르몬 주기를 예민하게 알아차린다는 것이다.[54] 이는 '배란 전환 가설(ovulatory shift hypothesis)'과도 연계되어 있다.[55] 남성은 여성이 언제 가장 번식력이 강한지 알아차림으로써 여성의 배란 주기에 반응하도록 적응된다. 그로 인해 여성은 번식력이 가장 강할 때 선호하는 남성 대상을 찾는다. 양쪽 모두 호르몬에 따라 움직인다.
여성
안드로겐은 질 조직의 생리기능을 조절하고 여성의 성적 흥분에 기여한다.[56] 여성의 테스토스테론 수치는 포옹 전보가는 성교 전, 포옹 후 보다는 성교 후에 높다.[57] 여성의 성기 흥분 상태에 있어 테스토스테론이 작용할 때 시간 지연 효과가 있다. 게다가 질의 성적 흥분이 지속적으로 증가하는 것은 성기의 감각과 성적 욕구적 행동(sexual appetitive behavior)이 높아지는 결과를 낳는다.[58]
여성이 테스토스테론 기본 수치가 상대적으로 높으면, 이들은 성적 흥분 수치 증가가 더 높디만 테스토스테론 증가치는 적다. 이는 여성의 테스토스테론 수치에 나타나는 천정효과(ceiling effect)이다. 성적인 사고 역시 테스토스테론 수치를 변화시키지만, 여성 신체 내 코르티솔 수치는 변화시키지 않으며, 호르몬 피임은 성적 사고에 대한 테스토스테론 반응의 변화에 효과를 끼칠 것이다.[59]
테스토스테론은 여성 성적 흥분 장애(female sexual arousal disorder) 치료에도 효과가 있다고 밝혀졌다.[60] 또한 피부 패치로도 사용 가능하다. 미국식품의약국(FDA)이 인정한 안드로겐 부족 치료를 위한 안드로겐 조제약은 없다. 그러나 노년 여성의 리비도 저하와 성적 기능 부전(sexual dysfunction) 치료를 위한 오프라벨(off-label use)로 사용되어 왔다. 테스토스테론은 갱년기 이후 여성들이 에스트로겐 분비가 원활하게 될 경우 좋은 치료제일 수 있다.[60]
이성 관계
남성은 사랑에 빠지면 테스토스테론 수치가 낮아지지만 여성은 반대로 증가한다. 이로 인해 남녀의 행동 간에 일시적으로 차이가 감소하게 된다.[61] 그러나 약 4년 동안의 "신혼기간(honeymoon phase)"이 끝난 후, 이러한 태스토스테론 수치 변화는 더이상 보이지 않는다.[61] 테스토스테론 수치가 적은 남자는 관계에 머물 가능성이 더 높으며,[62] or married,[63] 수치가 높은 남자는 이혼할 가능성이 높다.[63] 결혼 및 결혼생활 이행은 테스토스테론 수치를 떨어뜨릴 수 있다.[64]
이성 관계가 없었던 독신 남성은 이성 관계가 있었던 남성에 비해 테스토스테론 수치가 낮다. 이는 이전의 이성 관계가 있던 경험이 그렇지 않은 경우보다 더 경쟁성 있다는 것을 시사한다.[65] 유부남의 경우, 배우자나 아이와 시간을 보내는 것 등의 연대 유지 활동을 하는 동안이나 그렇지 않은 동안이나 테스토스테론 수치에 차이가 없다. 종합적으로 이런 결과는 연대 유지 활동에 비해 경쟁 활동 상태가 테스토스테론 수치 변화에 더 관련있다는 것을 말한다.[66]
테스토스테론 수치가 높은 남성이 혼외정사를 벌일 가능성이 더 높다.[63] 테스토스테론 수치는 파트너의 물리적 존재에 영향받지 않는다. 같은 도시에 있거나 장거리 연애중이 있어도 수치는 비슷하다.[62] 물리적 존재는 테스토스테론 파트너의 상호작용에 관한 관계에 있는 여성들에게 필요하다. 같은 도시에 사는 남성과 연애하는 여성은 장거리 연애 여성보다 테스토스테론 수치가 낮다.[67]
의학적 사용
남성 성선기능저하증(male hypogonadism), 성별 불쾌감(gender dysphoria), 특정 유형의 유방암(breast cancer) 치료 약물로 사용한다.[14][68] 이는 호르몬 대체요법(hormone replacement therapy, HRT) 혹은 테스토스테론 대체요법(testosterone replacement therapy, TRT)이라고 한다. 요법은 혈청 테스토스테론(serum testosterone) 수치를 정상으로 유지한다. 남성갱년기(andropause)로 인한 테스토스테론 생산 저하는 안드로겐 대체요법(androgen replacement therapy)으로의 관심을 야기한다.[69] 노화로 인한 테스토스테론 수치가 낮은 사람에게 테스토스테론을 처방하는 것이 좋은지 나쁜지는 불분명하다.[70]
테스토스테론은 WHO 필수 의약품 목록(WHO Model List of Essential Medicines)에 등재되어 있다. 이는 기초의료제도에 필요한 가장 중요한 약이란 뜻이다.[71] 복제약(generic medication)으로 이용 가능하다.[14] 피부에 바르는 크림이나 피부 패치(transdermal patch), 혹은 근육 내 주사(intramuscular injection), 구강 점막 흡수 약물(buccal administration) 알약 형태, 혹은 경구 형태로 처방 가능하다.[14]
흔한 부작용은 여드름, 부종, 여성형유방증(gynecomastia)이 있다.[14] 심각한 부작용은 간독성(liver toxicity), 심혈관계 질환(heart disease), 행동 변화(behavioral change)가 있다.[14] 약물에 노출된 여성이나 아동은 남성화(virilization)가 보일 수 있다.[14] 전립선암(prostate cancer) 환자는 약물을 쓰지 않도록 권고한다.[14] 임신이나 수유 기간에는 해를 일으킬 수 있다.[14]
미국내과의사회(American College of Physicians) 2020년 가이드라인은 성 기능 장애(sexual dysfunction)가 있는 테스토스테론 저하 성인 남성에게 치료용으로 쓰는 것을 지지했다. 이들은 개선이 있는지 매년 평가하고, 그렇지 않으면 테스토스테론 사용을 중단할 것을 추천한다. 비용 문제와 두 방식의 효과 및 부작용이 비슷하다는 이유에서, 내과의사들은 피하 치료보다는 근육 내 주사를 고려해야 한다. 성 기능 장애 개선 외에 다른 이유로 시행하는 테스토스테론 치료는 권고하지 않는다.[72][73]
측정
태스토스테론의 생체이용성 농도(bioavailable concentration)는 베르묄렌 계산법(Vermeulen calculation)이나 더 정확히는 개량 베르묄렌 방식(modified Vermeulen method)을 이용하여 측정한다.[74][75] 이는 성 호르몬 결합 글로불린(sex-hormone-binding-globulin)의 이합체 형태를 고려한다.[76]
두 방식 모두 화학평형(chemical equilibrium)을 사용하여 생체이용 가능 테스토스테론 농도를 추론한다. 혈액 순환에서, 테스토스테론은 두 가지 결합 파트너(binding partner)를 가지고 있다. 즉 약한 결합의 알부민(albumin)과 강한 결합의 성 호르몬 결합 글로불린(sex-hormone-binding-globulin)이 그것이다. 측정수단들은 아래 그림에서 상세히 묘사된다.
-
테스토스테론 배위자(- 配位子, testosterone ligand)가 동반한 이합형 성 호르몬 결합 글로불린(dimeric sex-hormone-binding-globulin)
-
생물학적 이용성 테스토스테론 농도 측정 수단 2가지
역사

아놀드 아돌프 베르톨드(Arnold Adolph Berthold, 1803–1861)의 가금류의 거세 및 고환 이식에 관한 초기 연구에서, 고환 활동은 혈액 부분(blood fraction)의 순환과 연관지어졌다. 현재 이 혈액 부분은 안드로겐 호르몬군(family of androgenic hormones)으로 밝혀져 있다.[77] 1889년 하버드대학교(Harvard University) 교수 샤를-에두아르 브라운-세카르(Charles-Édouard Brown-Séquard, 1817–1894)가 1889년 프랑스 파리에 체류할 당시, 개와 기니피그의 고환 추출물을 '회춘약(rejuvenating elixir)'이라는 이름으로 자신의 피하에 스스로 투여하는 실험을 함으로써, 테스토스테론 활동에 관한 연구는 진전을 보였다. 그는 『란셋(The Lancet)』에 이를 보고, 자신의 행복감과 활력이 현저하게 회복하였지만 효과는 일시적이라고 하였다.[78] 또한 그는 이 물질을 합성하려 하였디만 실패하였다. 동료 연구자들의 조롱으로 그는 인간의 안드로겐 기제 및 효과에 관한 연구를 포기했다.
1927년, 시카고대학교(University of Chicago) 생물화학과 교수 프레드 코치(Fred C. Koch)는 시카고 가축수용소(the Chicago stockyards)에 있는 소들의 고환을 이용하고, 학생들을 고용하여 분리물을 추출하는 장황한 작업을 수행하였다. 그해, 코치와 그의 학생 레뮤엘 맥기(Lemuel McGee)는 40파운드(약 18kg)의 소 고환에서 20mg의 물질을 추출, 거세된 수탉과 돼지와 쥐에게 투여하여 다시 남성화되는 현상을 포착하였다.[79] 1934년, 암스테르담대학교(University of Amsterdam) 에른스트 라케(Ernst Laqueur) 집단은 비슷한 방식으로 소 고환에서 테스토스테론을 추출했다. 그러나 동물 조직으로부터 호르몬을 대량으로 분리하여 인간을 대상으로 연구하는 것은, 1930년대 유럽 3대 거대 제약 회사인 셰링(Schering)(독일 베를린 소재), 오르가논(Organon)(네덜란드 오스 소재), 시바(Ciba)(스위스 바젤 소재)가 대규모의 스테로이드 연구 및 개발 프로그램을 시작하면서 부터였다.
네덜란드 오르가논 그룹은 최초로 테스토스테론 호르몬을 분리하였다. 이는 1935년 5월, "On Crystalline Male Hormone from Testicles (Testosterone)"이라는 논문을 통해 공표되었다.[80] 이들은 고환을 뜻하는 '테스티클(testicle)'과 '스테롤(sterol)'의 어간과 '케톤(ketone)'의 접미사를 합성하여, '테스토스테론(testosterone)'이라 명명하였다. 셰링의 아돌프 부테난트(Adolf Butenandt)는 그단스크기술대학교(Gdańsk University of Technology)의 화학연구소(Chemisches Institut)에서 분자구조를 규명하였다.[81][82]
1935년 8월, 부테난트와 하니쉬(G. Hanisch)는 콜레스테롤로부터 테스토스테론을 화학합성하였다.[83] 그로부터 1주일만에, 스위스 취리히(Zurich) 소재 시바 그룹 소속 레오폴트 루지치카(Leopold Ruzicka, 1887–1976)와 베트슈타인(A. Wettstein)은 테스토스테론 합성을 공표하였다.[84] 1939년, 부테난트와 루지치카는 각자 별도로 개발한 테스토스테론 화학합성법으로 노벨화학상(Nobel Prize in Chemistry)을 공동수상하였다.[82][85] 테스토스테론의 화학식은 17β-hydroxyandrost-4-en-3-one (C19H28O2)으로, 17번째 탄소 원자에 하이드록시기(hydroxyl group)가 하나 있는 고체형 다환식 알코올(solid polycyclic alcohol)이다. 합성 테스토스테론을 에스테르화(esterification)와 알킬화(alkylation)하여 개조할 수 있다는 것을 의미한다.
1930년대 풍부한 잠재적 테스토스테론 에스테르(testosterone ester)의 부분합성(partial synthesis)으로, 테스토스테론 효과의 특성을 설명할 수 있게 되었다. 그리하여 1936년, 코차키안(Kochakian)과 무를린(Murlin)은 연구를 통해 테스토스테론이 동화작용(anabolism)의 핵심 기제인 질소보존(nitrogen retention)을 일으킨다는 것을 개를 통해 보일 수 있었다. 이후, 엘런 케년(Allan Kenyon) 집단[86]은 유사환관증(eunuchoid) 환자 남성 및 소년, 여성에게서 테스토스테론 프로피온산염(testosterone propionate)의 동화 효과 및 안드로겐 효과를 모두 보일 수 있었다. 1930년대 초에서 1950년대에 이르는 시기를 '스테로이드 화학의 황금시기(The Golden Age of Steroid Chemistry)'라고 부른다.[87] 이 시기의 연구들은 급격히 발전하였다.[88]
기타 동물종
테스토스테론은 대부분의 척추동물(vertebrate)에게 있다. 테스토스테론과 고전적 핵 안드로겐 수용체(classical nuclear androgen receptor)은 그나토스톰 척추동물(gnathostome vertebrate) 즉 유악류척추동물(有顎類脊椎動物, jawed vertebrate)에게서 처음 나타났다.[89] 칠성장어(lamprey) 등의 아그나탄 척추동물(agnathan vertebrate) 혹은 무악류척추동물(無顎類脊椎動物, jawless vertebrates)은 테스토스테론 대신 안드로스테네디온(androstenedione)을 남성 성호르몬으로 사용한다.[90] 어류는 11-케토테스토스테론(11-ketotestosterone)이라는 것을 분비한다.[91] 곤충류에는 해당 호르몬으로 엑디손(ecdysone)이 있다.[92] 동물 전반에 걸쳐 보이는 스테로이드의 존재는 성호르몬(sex hormone)이 하나의 유구한 진화 역사를 가지고 있다는 것을 의미한다.[93]
에스트로겐과의 관계
아로마테이스 효소를 통해 에스트로겐으로 바뀐다. 아로마테이스 억제제를 통해 이러한 변환을 피할 수 있다.
공격성
한편 테스토스테론(testosterone)은 공격성(Aggression)의 발현에 주요한 역할을 하는 호르몬으로 보고된바있다. 이 호르몬이 공격성의 결과에서 유의미한 의미를 가지기도 하지만 또한 편도체의 활성화와 관련있는 정서 자극 그리고 전전두엽에 의한 억제 저항력은 충동의 필요성과 충동 정도의 조절에 테스토스테론이 주요하게 관여하는 그 역할 자체로도 매우 중요한 바를 시사한다.[94]
같이보기
참조
- ↑ “Understanding the risks of performance-enhancing drugs”. 《Mayo Clinic》 (영어). 2019년 12월 30일에 확인함.
- ↑ Mooradian AD, Morley JE, Korenman SG (Feb 1987). “Biological actions of androgens”. 《Endocrine Reviews》 8 (1): 1–28. doi:10.1210/edrv-8-1-1. PMID 3549275.
- ↑ Gaviglio CM, Crewther BT, Kilduff LP, Stokes KA, Cook CJ. Relationship between pregame concentrations of free testosterone and outcome in rugby union. Int J Sports Physiol Perform. 2014;9(2):324–31.
- ↑ Crewther BT, Thomas AG, Stewart-Williams S, Kilduff LP, Cook CJ. Is salivary cortisol moderating the relationship between salivary testosterone and hand-grip strength in healthy men? Eur J Sport Sci. 2017;17(2):188–94.
- ↑ Crewther BT, Sanctuary CE, Kilduff LP, Carruthers JS, Gaviglio CM, Cook CJ. The workout responses of salivary-free testosterone and cortisol concentrations and their association with the subsequent competition outcomes in professional rugby league. J Strength Cond Res. 2013;27(2):471–6
- ↑ Bassil N, Alkaade S, Morley JE (Jun 2009). “The benefits and risks of testosterone replacement therapy: a review”. 《Therapeutics and Clinical Risk Management》 5 (3): 427–48. doi:10.2147/tcrm.s3025. PMC 2701485. PMID 19707253.
- ↑ Tuck SP, Francis RM (2009). 〈Testosterone, bone and osteoporosis〉. 《Advances in the Management of Testosterone Deficiency》. Frontiers of Hormone Research 37. 123–32쪽. doi:10.1159/000176049. ISBN 978-3-8055-8622-1. PMID 19011293.
- ↑ Serpell B.G., Waddington G., McGrath B., Cook C.J. Is There a Link between Stress and Cognition, and Capacity to Execute Motor Skill?. Med. Sci. Sports Exerc.. 2020;52(11):2365-2372. doi:10.1249/MSS.0000000000002397
- ↑ 가 나 Luetjens, C. Marc; Weinbauer, Gerhard F. (2012). 〈Chapter 2: Testosterone: Biosynthesis, transport, metabolism and (non-genomic) actions〉. Nieschlag, Eberhard; Behre, Hermann M.; Nieschlag, Susan. 《Testosterone: Action, Deficiency, Substitution》 4판. Cambridge: Cambridge University Press. 15–32쪽. ISBN 978-1-107-01290-5.
- ↑ Torjesen PA, Sandnes L (Mar 2004). “Serum testosterone in women as measured by an automated immunoassay and a RIA”. 《Clinical Chemistry》 50 (3): 678; author reply 678–9. doi:10.1373/clinchem.2003.027565. PMID 14981046.
- ↑ Southren AL, Gordon GG, Tochimoto S, Pinzon G, Lane DR, Stypulkowski W (May 1967). “Mean plasma concentration, metabolic clearance and basal plasma production rates of testosterone in normal young men and women using a constant infusion procedure: effect of time of day and plasma concentration on the metabolic clearance rate of testosterone”. 《The Journal of Clinical Endocrinology & Metabolism》 27 (5): 686–94. doi:10.1210/jcem-27-5-686. PMID 6025472.
- ↑ Southren AL, Tochimoto S, Carmody NC, Isurugi K (Nov 1965). “Plasma production rates of testosterone in normal adult men and women and in patients with the syndrome of feminizing testes”. 《The Journal of Clinical Endocrinology & Metabolism》 25 (11): 1441–50. doi:10.1210/jcem-25-11-1441. PMID 5843701.
- ↑ Dabbs M, Dabbs JM (2000). 《Heroes, rogues, and lovers: testosterone and behavior》. New York: McGraw-Hill. ISBN 978-0-07-135739-5.
- ↑ 가 나 다 라 마 바 사 아 자 “Testosterone”. 《Drugs.com》. American Society of Health-System Pharmacists. December 4, 2015. August 20, 2016에 원본 문서에서 보존된 문서. September 3, 2016에 확인함.
- ↑ Institute of Medicine (US) Committee on Assessing the Need for Clinical Trials of Testosterone Replacement Therapy; Liverman, Catharyn T.; Blazer, Dan G. (2004). 〈Introduction〉. Testosterone and Aging: Clinical Research Directions (보고서) (영어). National Academies Press (US).
- ↑ “What is Prohibited”. 《World Anti-Doping Agency》 (영어). 2021년 7월 18일에 확인함.
- ↑ Sheffield-Moore M (2000). “Androgens and the control of skeletal muscle protein synthesis”. 《Annals of Medicine》 32 (3): 181–6. doi:10.3109/07853890008998825. PMID 10821325. S2CID 32366484.
- ↑ Handelsman, David J (January 2013). 〈Androgen Physiology, Pharmacology and Abuse〉. 《Endotext [Internet]》. 《WWW.ENDOTEXT.ORG》 (MDText.com, Inc).
- ↑ Swaab DF, Garcia-Falgueras A (2009). “Sexual differentiation of the human brain in relation to gender identity and sexual orientation”. 《Functional Neurology》 24 (1): 17–28. PMID 19403051.
- ↑ Xu HY, Zhang HX, Xiao Z, Qiao J, Li R (2019). “Regulation of anti-Müllerian hormone (AMH) in males and the associations of serum AMH with the disorders of male fertility”. 《Asian Journal of Andrology》 21 (2): 109–114. doi:10.4103/aja.aja_83_18. PMC 6413543. PMID 30381580.
- ↑ Berenbaum SA (March 2018). “Beyond Pink and Blue: The Complexity of Early Androgen Effects on Gender Development”. 《Child Development Perspectives》 12 (1): 58–64. doi:10.1111/cdep.12261. PMC 5935256. PMID 29736184.
- ↑ Hines M, Brook C, Conway GS (February 2004). “Androgen and psychosexual development: core gender identity, sexual orientation and recalled childhood gender role behavior in women and men with congenital adrenal hyperplasia (CAH)”. 《Journal of Sex Research》 41 (1): 75–81. doi:10.1080/00224490409552215. PMID 15216426. S2CID 33519930.
- ↑ Forest MG, Cathiard AM, Bertrand JA (Jul 1973). “Evidence of testicular activity in early infancy”. 《The Journal of Clinical Endocrinology & Metabolism》 37 (1): 148–51. doi:10.1210/jcem-37-1-148. PMID 4715291.
- ↑ Corbier P, Edwards DA, Roffi J (1992). “The neonatal testosterone surge: a comparative study”. 《Archives Internationales de Physiologie, de Biochimie et de Biophysique》 100 (2): 127–31. doi:10.3109/13813459209035274. PMID 1379488.
- ↑ Dakin CL, Wilson CA, Kalló I, Coen CW, Davies DC (May 2008). “Neonatal stimulation of 5-HT(2) receptors reduces androgen receptor expression in the rat anteroventral periventricular nucleus and sexually dimorphic preoptic area”. 《The European Journal of Neuroscience》 27 (9): 2473–80. doi:10.1111/j.1460-9568.2008.06216.x. PMID 18445234. S2CID 23978105.
- ↑ Kalat JW (2009). 〈Reproductive behaviors〉. 《Biological psychology》. Belmont, Calif: Wadsworth, Cengage Learning. 321쪽. ISBN 978-0-495-60300-9.
- ↑ 가 나 Pinyerd B, Zipf WB (2005). “Puberty-timing is everything!”. 《Journal of Pediatric Nursing》 20 (2): 75–82. doi:10.1016/j.pedn.2004.12.011. PMID 15815567.
- ↑ Ganong (2012). 《Ganong's Review of Medical Physiology》 24판. TATA McGRAW Hill. 423–25쪽. ISBN 978-1-25-902753-6.
- ↑ Raggatt LJ, Partridge NC (2010). “Cellular and molecular mechanisms of bone remodeling”. 《The Journal of Biological Chemistry》 285 (33): 25103–8. doi:10.1074/jbc.R109.041087. PMC 2919071. PMID 20501658.
- ↑ Mehta PH, Jones AC, Josephs RA (Jun 2008). “The social endocrinology of dominance: basal testosterone predicts cortisol changes and behavior following victory and defeat” (PDF). 《Journal of Personality and Social Psychology》 94 (6): 1078–93. CiteSeerX 10.1.1.336.2502. doi:10.1037/0022-3514.94.6.1078. PMID 18505319. April 19, 2009에 원본 문서 (PDF)에서 보존된 문서.
- ↑ Ajayi AA, Halushka PV (May 2005). “Castration reduces platelet thromboxane A2 receptor density and aggregability”. 《QJM》 98 (5): 349–56. doi:10.1093/qjmed/hci054. PMID 15820970.
- ↑ Ajayi AA, Mathur R, Halushka PV (Jun 1995). “Testosterone increases human platelet thromboxane A2 receptor density and aggregation responses”. 《Circulation》 91 (11): 2742–7. doi:10.1161/01.CIR.91.11.2742. PMID 7758179.
- ↑ Kelsey TW, Li LQ, Mitchell RT, Whelan A, Anderson RA, Wallace WH (2014년 10월 8일). “A validated age-related normative model for male total testosterone shows increasing variance but no decline after age 40 years”. 《PLOS ONE》 9 (10): e109346. Bibcode:2014PLoSO...9j9346K. doi:10.1371/journal.pone.0109346. PMC 4190174. PMID 25295520.
- ↑ Morgentaler A, Schulman C (2009). 〈Testosterone and prostate safety〉. 《Advances in the Management of Testosterone Deficiency》. Frontiers of Hormone Research 37. 197–203쪽. doi:10.1159/000176054. ISBN 978-3-8055-8622-1. PMID 19011298.
- ↑ Rhoden EL, Averbeck MA, Teloken PE (Sep 2008). “Androgen replacement in men undergoing treatment for prostate cancer”. 《The Journal of Sexual Medicine》 5 (9): 2202–08. doi:10.1111/j.1743-6109.2008.00925.x. PMID 18638000.
- ↑ Morgentaler A, Traish AM (Feb 2009). “Shifting the paradigm of testosterone and prostate cancer: the saturation model and the limits of androgen-dependent growth”. 《European Urology》 55 (2): 310–20. doi:10.1016/j.eururo.2008.09.024. PMID 18838208.
- ↑ Haddad RM, Kennedy CC, Caples SM, Tracz MJ, Boloña ER, Sideras K, Uraga MV, Erwin PJ, Montori VM (Jan 2007). “Testosterone and cardiovascular risk in men: a systematic review and meta-analysis of randomized placebo-controlled trials”. 《Mayo Clinic Proceedings》 82 (1): 29–39. doi:10.4065/82.1.29. PMID 17285783.
- ↑ Jones TH, Saad F (Dec 2009). “The effects of testosterone on risk factors for, and the mediators of, the atherosclerotic process”. 《Atherosclerosis》 207 (2): 318–27. doi:10.1016/j.atherosclerosis.2009.04.016. PMID 19464009.
- ↑ Stanworth RD, Jones TH (2008). “Testosterone for the aging male; current evidence and recommended practice”. 《Clinical Interventions in Aging》 3 (1): 25–44. doi:10.2147/CIA.S190. PMC 2544367. PMID 18488876.
- ↑ Van Anders SM, Watson NV (2006). “Menstrual cycle irregularities are associated with testosterone levels in healthy premenopausal women” (PDF). 《American Journal of Human Biology》 18 (6): 841–44. doi:10.1002/ajhb.20555. hdl:2027.42/83925. PMID 17039468. S2CID 32023452.
- ↑ Fox CA, Ismail AA, Love DN, Kirkham KE, Loraine JA (Jan 1972). “Studies on the relationship between plasma testosterone levels and human sexual activity”. 《The Journal of Endocrinology》 52 (1): 51–8. doi:10.1677/joe.0.0520051. PMID 5061159.
- ↑ van Anders SM, Dunn EJ (Aug 2009). “Are gonadal steroids linked with orgasm perceptions and sexual assertiveness in women and men?”. 《Hormones and Behavior》 56 (2): 206–13. doi:10.1016/j.yhbeh.2009.04.007. hdl:2027.42/83876. PMID 19409392. S2CID 14588630.
- ↑ Exton MS, Bindert A, Krüger T, Scheller F, Hartmann U, Schedlowski M (1999). “Cardiovascular and endocrine alterations after masturbation-induced orgasm in women”. 《Psychosomatic Medicine》 61 (3): 280–89. doi:10.1097/00006842-199905000-00005. PMID 10367606.
- ↑ Purvis K, Landgren BM, Cekan Z, Diczfalusy E (Sep 1976). “Endocrine effects of masturbation in men”. 《The Journal of Endocrinology》 70 (3): 439–44. doi:10.1677/joe.0.0700439. PMID 135817.
- ↑ Harding SM, Velotta JP (May 2011). “Comparing the relative amount of testosterone required to restore sexual arousal, motivation, and performance in male rats”. 《Hormones and Behavior》 59 (5): 666–73. doi:10.1016/j.yhbeh.2010.09.009. PMID 20920505. S2CID 1577450.
- ↑ James PJ, Nyby JG, Saviolakis GA (Sep 2006). “Sexually stimulated testosterone release in male mice (Mus musculus): roles of genotype and sexual arousal”. 《Hormones and Behavior》 50 (3): 424–31. doi:10.1016/j.yhbeh.2006.05.004. PMID 16828762. S2CID 36436418.
- ↑ 가 나 Wallen K (Sep 2001). “Sex and context: hormones and primate sexual motivation”. 《Hormones and Behavior》 40 (2): 339–57. CiteSeerX 10.1.1.22.5968. doi:10.1006/hbeh.2001.1696. PMID 11534996. S2CID 2214664.
- ↑ Hart BL (Dec 1983). “Role of testosterone secretion and penile reflexes in sexual behavior and sperm competition in male rats: a theoretical contribution”. 《Physiology & Behavior》 31 (6): 823–27. doi:10.1016/0031-9384(83)90279-2. PMID 6665072. S2CID 42155431.
- ↑ Kraemer HC, Becker HB, Brodie HK, Doering CH, Moos RH, Hamburg DA (Mar 1976). “Orgasmic frequency and plasma testosterone levels in normal human males”. 《Archives of Sexual Behavior》 5 (2): 125–32. doi:10.1007/BF01541869. PMID 1275688. S2CID 38283107.
- ↑ Roney JR, Mahler SV, Maestripieri D (2003). “Behavioral and hormonal responses of men to brief interactions with women”. 《Evolution and Human Behavior》 24 (6): 365–75. doi:10.1016/S1090-5138(03)00053-9.
- ↑ Pirke KM, Kockott G, Dittmar F (Nov 1974). “Psychosexual stimulation and plasma testosterone in man”. 《Archives of Sexual Behavior》 3 (6): 577–84. doi:10.1007/BF01541140. PMID 4429441. S2CID 43495791.
- ↑ Hellhammer DH, Hubert W, Schürmeyer T (1985). “Changes in saliva testosterone after psychological stimulation in men”. 《Psychoneuroendocrinology》 10 (1): 77–81. doi:10.1016/0306-4530(85)90041-1. PMID 4001279. S2CID 41819670.
- ↑ Rowland DL, Heiman JR, Gladue BA, Hatch JP, Doering CH, Weiler SJ (1987). “Endocrine, psychological and genital response to sexual arousal in men”. 《Psychoneuroendocrinology》 12 (2): 149–58. doi:10.1016/0306-4530(87)90045-X. PMID 3602262. S2CID 35309934.
- ↑ Miller SL, Maner JK (Feb 2010). “Scent of a woman: men's testosterone responses to olfactory ovulation cues”. 《Psychological Science》 21 (2): 276–83. doi:10.1177/0956797609357733. PMID 20424057. S2CID 18170407.
- ↑ Gangestead SW, Thornhill R, Garver-Apgar CE (2005). “Adaptations to Ovulation: Implications for Sexual and Social Behavior”. 《Current Directions in Psychological Science》 14 (6): 312–16. doi:10.1111/j.0963-7214.2005.00388.x. S2CID 53074076.
- ↑ Traish AM, Kim N, Min K, Munarriz R, Goldstein I (Apr 2002). “Role of androgens in female genital sexual arousal: receptor expression, structure, and function”. 《Fertility and Sterility》. 77 Suppl 4: S11–8. doi:10.1016/s0015-0282(02)02978-3. PMID 12007897.
- ↑ van Anders SM, Hamilton LD, Schmidt N, Watson NV (Apr 2007). “Associations between testosterone secretion and sexual activity in women”. 《Hormones and Behavior》 51 (4): 477–82. doi:10.1016/j.yhbeh.2007.01.003. hdl:2027.42/83880. PMID 17320881. S2CID 5718960.
- ↑ Tuiten A, Van Honk J, Koppeschaar H, Bernaards C, Thijssen J, Verbaten R (Feb 2000). “Time course of effects of testosterone administration on sexual arousal in women”. 《Archives of General Psychiatry》 57 (2): 149–53; discussion 155–6. doi:10.1001/archpsyc.57.2.149. PMID 10665617.
- ↑ Goldey KL, van Anders SM (May 2011). “Sexy thoughts: effects of sexual cognitions on testosterone, cortisol, and arousal in women” (PDF). 《Hormones and Behavior》 59 (5): 754–64. doi:10.1016/j.yhbeh.2010.12.005. hdl:2027.42/83874. PMID 21185838. S2CID 18691358.
- ↑ 가 나 Bolour S, Braunstein G (2005). “Testosterone therapy in women: a review”. 《International Journal of Impotence Research》 17 (5): 399–408. doi:10.1038/sj.ijir.3901334. PMID 15889125.
- ↑ 가 나 Marazziti D, Canale D (Aug 2004). “Hormonal changes when falling in love”. 《Psychoneuroendocrinology》 29 (7): 931–36. doi:10.1016/j.psyneuen.2003.08.006. PMID 15177709. S2CID 24651931.
- ↑ 가 나 van Anders SM, Watson NV (Jul 2006). “Relationship status and testosterone in North American heterosexual and non-heterosexual men and women: cross-sectional and longitudinal data”. 《Psychoneuroendocrinology》 31 (6): 715–23. doi:10.1016/j.psyneuen.2006.01.008. hdl:2027.42/83924. PMID 16621328. S2CID 22477678.
- ↑ 가 나 다 Booth A, Dabbs JM (1993). “Testosterone and Men's Marriages”. 《Social Forces》 72 (2): 463–77. doi:10.1093/sf/72.2.463.
- ↑ Mazur A, Michalek J (1998). “Marriage, Divorce, and Male Testosterone”. 《Social Forces》 77 (1): 315–30. doi:10.1093/sf/77.1.315.
- ↑ Gray PB, Chapman JF, Burnham TC, McIntyre MH, Lipson SF, Ellison PT (Jun 2004). “Human male pair bonding and testosterone”. 《Human Nature》 15 (2): 119–31. doi:10.1007/s12110-004-1016-6. PMID 26190409. S2CID 33812118.
- ↑ Gray PB, Campbell BC, Marlowe FW, Lipson SF, Ellison PT (Oct 2004). “Social variables predict between-subject but not day-to-day variation in the testosterone of US men”. 《Psychoneuroendocrinology》 29 (9): 1153–62. doi:10.1016/j.psyneuen.2004.01.008. PMID 15219639. S2CID 18107730.
- ↑ van Anders SM, Watson NV (Feb 2007). “Testosterone levels in women and men who are single, in long-distance relationships, or same-city relationships”. 《Hormones and Behavior》 51 (2): 286–91. doi:10.1016/j.yhbeh.2006.11.005. hdl:2027.42/83915. PMID 17196592. S2CID 30710035.
- ↑ “List of Gender Dysphoria Medications (6 Compared)”. 《Drugs.com》 (영어). 2020년 5월 6일에 확인함.
- ↑ Myers JB, Meacham RB (2003). “Androgen replacement therapy in the aging male”. 《Reviews in Urology》 5 (4): 216–26. PMC 1508369. PMID 16985841.
- ↑ Staff (2015년 3월 3일). “Testosterone Products: Drug Safety Communication – FDA Cautions About Using Testosterone Products for Low Testosterone Due to Aging; Requires Labeling Change to Inform of Possible Increased Risk of Heart Attack And Stroke”. 《FDA》. 2015년 3월 5일에 확인함.
- ↑ “19th WHO Model List of Essential Medicines (April 2015)” (PDF). WHO. April 2015. 2015년 5월 10일에 확인함.
- ↑ Qaseem A, Horwitch CA, Vijan S, Etxeandia-Ikobaltzeta I, Kansagara D (January 2020). “Testosterone Treatment in Adult Men With Age-Related Low Testosterone: A Clinical Guideline From the American College of Physicians”. 《Annals of Internal Medicine》 172 (2): 126–133. doi:10.7326/M19-0882. PMID 31905405.
- ↑ Parry, Nicola M. (2020년 1월 7일). “New Guideline for Testosterone Treatment in Men With 'Low T'”. 《Medscape.com》. 2020년 1월 7일에 확인함.
- ↑ de Ronde W, van der Schouw YT, Pols HA, Gooren LJ, Muller M, Grobbee DE, de Jong FH (September 2006). “Calculation of bioavailable and free testosterone in men: a comparison of 5 published algorithms”. 《Clinical Chemistry》 52 (9): 1777–84. doi:10.1373/clinchem.2005.063354. PMID 16793931.
- ↑ Hasler J, Herklotz R, Luppa PB, Diver MJ, Thevis M, Metzger J, Savoca R, Jermini F, Huber AR (2006년 1월 1일). “Impact of recent biochemical findings on the determination of free and bioavailable testosterone: evaluation and proposal for clinical use”. 《LaboratoriumsMedizin》 30 (6): 492–505. doi:10.1515/JLM.2006.050.
- ↑ “RCSB PDB - 1D2S”. 《Crystal Structure of the N-Terminal Laminin G-Like Domain of SHBG in Complex with Dihydrotestosterone》.
- ↑ Berthold AA (1849). “Transplantation der Hoden” [Transplantation of testis]. 《Arch. Anat. Physiol. Wiss.》 (독일어) 16: 42–6.
- ↑ Brown-Sequard CE (1889). “The effects produced on man by subcutaneous injections of liquid obtained from the testicles of animals”. 《Lancet》 2 (3438): 105–07. doi:10.1016/S0140-6736(00)64118-1.
- ↑ Gallagher TF, Koch FC (November 1929). “The testicular hormone”. 《J. Biol. Chem.》 84 (2): 495–500. doi:10.1016/S0021-9258(18)77008-7.
- ↑ David KG, Dingemanse E, Freud JL (May 1935). “Über krystallinisches mannliches Hormon aus Hoden (Testosteron) wirksamer als aus harn oder aus Cholesterin bereitetes Androsteron” [On crystalline male hormone from testicles (testosterone) effective as from urine or from cholesterol]. 《Hoppe-Seyler's Z Physiol Chem》 (독일어) 233 (5–6): 281–83. doi:10.1515/bchm2.1935.233.5-6.281.
- ↑ Butenandt A, Hanisch G (1935). “Umwandlung des Dehydroandrosterons in Androstendiol und Testosterone; ein Weg zur Darstellung des Testosterons aus Cholestrin” [About Testosterone. Conversion of Dehydro-androsterons into androstendiol and testosterone; a way for the structure assignment of testosterone from cholesterol]. 《Hoppe-Seyler's Z Physiol Chem》 (독일어) 237 (2): 89–97. doi:10.1515/bchm2.1935.237.1-3.89.
- ↑ 가 나 Freeman ER, Bloom DA, McGuire EJ (Feb 2001). “A brief history of testosterone”. 《The Journal of Urology》 165 (2): 371–73. doi:10.1097/00005392-200102000-00004. PMID 11176375.
- ↑ Butenandt A, Hanisch G (1935). “Uber die Umwandlung des Dehydroandrosterons in Androstenol-(17)-one-(3) (Testosterone); um Weg zur Darstellung des Testosterons auf Cholesterin (Vorlauf Mitteilung). [The conversion of dehydroandrosterone into androstenol-(17)-one-3 (testosterone); a method for the production of testosterone from cholesterol (preliminary communication)]”. 《Chemische Berichte》 (독일어) 68 (9): 1859–62. doi:10.1002/cber.19350680937.
- ↑ Ruzicka L, Wettstein A (1935). “Uber die kristallinische Herstellung des Testikelhormons, Testosteron (Androsten-3-ol-17-ol) [The crystalline production of the testicle hormone, testosterone (Androsten-3-ol-17-ol)]”. 《Helvetica Chimica Acta》 (독일어) 18: 1264–75. doi:10.1002/hlca.193501801176.
- ↑ Hoberman JM, Yesalis CE (Feb 1995). “The history of synthetic testosterone”. 《Scientific American》 272 (2): 76–81. Bibcode:1995SciAm.272b..76H. doi:10.1038/scientificamerican0295-76. PMID 7817189.
- ↑ Kenyon AT, Knowlton K, Sandiford I, Koch FC, Lotwin, G (February 1940). “A comparative study of the metabolic effects of testosterone propionate in normal men and women and in eunuchoidism”. 《Endocrinology》 26 (1): 26–45. doi:10.1210/Endo-26-1-26.
- ↑ Schwarz S, Onken D, Schubert A (Jul 1999). “The steroid story of Jenapharm: from the late 1940s to the early 1970s”. 《Steroids》 64 (7): 439–45. doi:10.1016/S0039-128X(99)00003-3. PMID 10443899. S2CID 40156824.
- ↑ de Kruif P (1945). 《The Male Hormone》. New York: Harcourt, Brace.
- ↑ Guerriero G (2009). “Vertebrate sex steroid receptors: evolution, ligands, and neurodistribution”. 《Annals of the New York Academy of Sciences》 1163 (1): 154–68. Bibcode:2009NYASA1163..154G. doi:10.1111/j.1749-6632.2009.04460.x. PMID 19456336. S2CID 5790990.
- ↑ Bryan MB, Scott AP, Li W (2008). “Sex steroids and their receptors in lampreys”. 《Steroids》 73 (1): 1–12. doi:10.1016/j.steroids.2007.08.011. PMID 17931674. S2CID 33753909.
- ↑ Nelson RF (2005). 《An introduction to behavioral endocrinology》. Sunderland, Mass: Sinauer Associates. 143쪽. ISBN 978-0-87893-617-5.
- ↑ De Loof A (October 2006). “Ecdysteroids: the overlooked sex steroids of insects? Males: the black box”. 《Insect Science》 13 (5): 325–338. doi:10.1111/j.1744-7917.2006.00101.x.
- ↑ Mechoulam R, Brueggemeier RW, Denlinger DL (September 1984). “Estrogens in insects”. 《Journal Cellular and Molecular Life Sciences》 40 (9): 942–44. doi:10.1007/BF01946450. S2CID 31950471.
- ↑ [참고](Testosterone and Aggressive Behavior in Man,Menelaos L. Batrinos,Int J Endocrinol Metab. 2012 Summer; 10(3): 563–568. Published online 2012 Jun 30. doi: 10.5812/ijem.3661) https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3693622/


