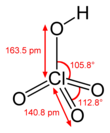
과염소산
| |||

| |||
| 이름 | |||
|---|---|---|---|
| 체계명
chloric(VII) acid | |||
| 별칭
Hyperchloric acid[1]
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.648 | ||
| EC 번호 |
| ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1873 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| HClO4 | |||
| 몰 질량 | 100.46 g/mol | ||
| 겉보기 | colorless liquid | ||
| 냄새 | odorless | ||
| 밀도 | 1.768 g/cm3 | ||
| 녹는점 | −17 °C (1 °F; 256 K) (azeotrope)[4] −112 °C (anhydrous) | ||
| 끓는점 | 203 °C (397 °F; 476 K) (azeotrope)[2] | ||
| miscible | |||
| 산성도 (pKa) | −15.2 (±2.0);[3] ≈ −10 | ||
| 짝염기 | Perchlorate | ||
| 위험 | |||
| 물질 안전 보건 자료 | ICSC 1006 | ||
| GHS 그림문자 |    
| ||
| 신호어 | 위험 | ||
| H271, H290, H302, H314, H373 | |||
| P210, P280, P303+361+353, P304+340, P310, P305+351+338, P371, P380, P375 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | Non-flammable | ||
| 관련 화합물 | |||
관련 화합물
|
Hydrochloric acid Hypochlorous acid Chlorous acid Chloric acid | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
과염소산(HClO4)은 염소의 산소산으로 무색이고 물에 녹는 액체이다. 황산이나 질산 정도의 강산이다. 초강산이지만 가장 강한 브뢴스테드-로우리 산은 아니다. pKa는 -10 정도이다.
실험식[편집]
과염소산 소듐 용액을 고농도의 황산과 반응시켜 얻는다.
- NaClO4 + H2SO4 → NaHSO4 + HClO4
안전성[편집]
과염소산은 폭발성이 있으며 상온에서 서서히 분해된다. 또 과염소산은 매우 유독한 물질로 분류된다. 피부와 눈에 손상을 줄 수 있으며 유기물이 있으면 불붙거나 폭발할 수 있다. 과염소산의 염은 폭발성 반응에서 강한 산화제이다. 물과는 심하게 발열 반응을 한다.
각주[편집]
- ↑ Samuel Fomon. 《Medicine and the Allied Sciences》 1. 148쪽.
- ↑ Handling of Perchloric acid[깨진 링크] ameslab.gov
- ↑ Trummal, A.; Lipping, L.; Kaljurand, I.; Koppel, I. A.; Leito, I. "Acidity of Strong Acids in Water and Dimethyl Sulfoxide" J. Phys. Chem. A. 2016, 120, 3663-3669. doi 10.1021/acs.jpca.6b02253.
- ↑ Safety data for concentrated perchloric acid, ca. 70% msds.chem.ox.ac.uk
외부 링크[편집]
 위키미디어 공용에 과염소산 관련 미디어 분류가 있습니다.
위키미디어 공용에 과염소산 관련 미디어 분류가 있습니다.
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |