편모
| 편모 | |
|---|---|
 세균 편모의 구조 | |
 | |
| 발음 | /fləˈdʒɛləm/ |
| 식별자 | |
| MeSH | D005407 |
| TH | H1.00.01.1.01032 |
| FMA | 67472 |
편모(flagellum, flagella)는 운동성을 제공하기 위해 특정 식물과 동물의 정자 세포와 다양한 미생물이 가진 돌출된 털이 있는 부속 기관이다.[1][2][3][4] 편모가 있는 많은 원생생물을 편모충류라고 한다.
미생물은 하나에서 많은 편모를 가질 수 있다. 예를 들어 그람 음성균인 헬리코박터 파일로리(Helicobacter pylori)는 다중 편모를 이용하여 점액 내벽에 닿아 위 상피에 도달하여 위궤양을 유발할 수 있다.[5] 일부 박테리아에서 편모는 세포 외부의 습기에 민감한 감각 소기관으로도 기능할 수 있다.[6]
세균, 고균, 진핵생물의 세 역에 걸쳐 편모는 구조, 단백질 구성 및 추진 메커니즘이 다르지만 운동성 제공이라는 동일한 기능을 공유한다. 라틴어 flagellum(flagellum)는 채찍을 의미하여 채찍 같이 헤엄치는 동작을 의미한다. 고균의 편모는 세균 편모와의 차이점을 기록하기 위해 archaellum이라고 한다.[7][8]
진핵생물의 편모와 섬모는 구조가 동일하지만 길이와 기능이 다르다.[9] 원핵생물의 선모는 더 작고 얇은 부속기관으로 기능이 다르다.
유형[편집]

편모의 세 가지 유형은 세균, 고균, 진핵생물이다.
진핵생물의 편모에는 굽힘 메커니즘으로 움직이는 디네인과 미세소관이 있다. 박테리아와 고세균은 편모에 디네인이나 미세소관이 없으며 회전 메커니즘을 사용하여 움직인다.[11]
이 세 가지 유형의 다른 차이점은 다음과 같다.
- 세균의 편모는 나선형 필라멘트이며, 각각은 시계 방향 또는 반시계 방향으로 회전할 수 있는 회전 모터가 바닥에 있다.[12][13][14] 회전 모터를 통해 여러 종류의 박테리아 운동성 중 두 가지가 나타난다.[15][16]
- 고균의 편모(archaella)는 회전 모터를 가지고 있다는 점에서 표면적으로 세균 편모와 유사하지만 많은 세부적인 특징은 다르며 비 동종으로 간주된다.[17][18][19]
- 진핵생물 편모(동물, 식물, 원생생물 세포의 편모)는 앞뒤로 휘몰아치는 복잡한 세포 돌출부이다. 진핵생물의 편모와 운동성 섬모는 구조가 동일하지만 길이, 파형, 기능이 다르다.
- 1차 섬모는 운동성이 없으며 편모와 운동성 섬모 모두에서 발견되는 9+2 축삭과는 달리 구조적으로 다른 9+0 축삭을 가지고 있다.
세균[편집]
구조 및 구성[편집]
세균성 편모는 편모의 단백질 소단위로 구성된다.[11] 그 모양은 20나노미터 두께의 속이 빈 튜브이다. 나선형이며 외막 바로 바깥쪽에 날카로운 굴곡이 있다. 이 "후크"를 사용하면 나선의 축이 세포에서 직접 멀어지도록 할 수 있다. 샤프트는 후크와 기저체 사이를 달리며 베어링 역할을 하는 세포막의 단백질 고리를 통과한다. 그람 양성 유기체는 펩티도글리칸 층에 하나, 원형질막에 하나, 이러한 기초 몸체 고리 중 2개를 가지고 있다. 그람 음성 유기체는 4개의 이러한 고리를 가지고 있다. L 고리는 리포폴리사카라이드와 결합하고, P 고리는 펩티도글리칸 층과 결합하고, M 고리는 원형질막에 내장되고, S 고리는 원형질막에 직접 부착된다. 필라멘트는 캡핑 단백질로 끝난다.[20][21]
편모 필라멘트는 모터에 의해 회전될 때 후크를 통해 박테리아를 추진하는 긴 나선형 나사이다. 그람 음성 Escherichia coli, Salmonella typhimurium, Caulobacter crescentus, Vibrio alginolyticus를 포함하여 연구된 대부분의 박테리아에서 필라멘트는 필라멘트 축에 대략 평행한 11개의 원형 필라멘트로 구성된다. 각 원형 필라멘트는 일련의 2인용 자전거(탠덤, tandem) 단백질 사슬이다. 그러나 Campylobacter jejuni에는 7개의 원형섬유가 있다.[22]
기저체는 원형질막을 통해 뻗어 있는 중앙에 있는 속이 빈 막대 모양의 "플러그"와 같은 일부 유형의 분비 구멍과 공통되는 몇 가지 특성을 가지고 있다. 세균 편모와 세균 분비 시스템 구조 및 단백질 간의 유사성은 세균 편모가 3형 분비 시스템에서 진화했다는 이론을 뒷받침하는과학적 증거를 제공한다.
모터[편집]
박테리아 편모는 내부 세포막의 편모 고정점에 위치한 단백질로 구성된 회전 엔진(Mot complex)에 의해 구동된다. 엔진은 양성자 구동력, 즉 세포의 신진 대사에 의해 설정된 농도 구배로 인해 박테리아 세포막을 가로 지르는 양성자(수소 이온)의 흐름에 의해 구동된다(Vibrio 종에는 측면 및 극성의 두 종류의 편모가 있다. 그리고 일부는 양성자 펌프가 아닌 나트륨 이온 펌프에 의해 구동된다[23]). 로터는 막을 가로질러 양성자를 운반하고 그과정에서 회전한다.
로터 단독으로 6,000-17,000rpm으로 작동할 수 있지만 편모 필라멘트가 부착된 경우 일반적으로 200-1000rpm에 도달한다. 회전 방향은 로터에서 단백질 FliG의 위치가 약간 변경되어 거의 순간적으로 편모 모터 스위치에 의해 변경될 수 있다.[24] 편모는 에너지 효율이 높고 에너지를 거의 사용하지 않는다.[25] 토크 생성에 대한 정확한 메커니즘은 아직 제대로 이해되지 않았다.[26] 편모 모터에는 온-오프 스위치가 없기 때문에 단백질 epsE는 모터를 로터에서 분리하는 기계적 클러치로 사용되어 편모를 멈추고 박테리아가 한 곳에 남아 있게 한다.[27]
편모의 원통형 모양은 미세한 유기체의 이동에 적합하다. 이 유기체는 주변 물의 점도가 질량이나 관성보다 훨씬 더 중요한 낮은 레이놀즈 수에서 작동한다.[28]
편모의 회전 속도는 양성자 동력의 강도에 따라 달라지므로 특정 형태의 속도 제어가 가능하고 일부 유형의 박테리아는 크기에 비례하여 놀라운 속도를 얻을 수 있다. 일부는 초당 대략 60개의 셀 길이를 달성한다. 이러한 속도로 박테리아가 1km를 덮는 데 약 245일이 걸린다. 느린 것처럼 보일 수 있지만 규모의 개념이 도입되면 관점이 바뀐다. 거시적인 생명체와 비교할 때 초당 몸 길이의 수로 표현하면 실제로 매우 빠르다. 예를 들어, 치타는 초당 약 25개의 몸 길이 정도만을 달릴 수 있다.[29]
편모의 사용을 통해 박테리아는 편향된 무작위 보행을 통해 유인물 쪽으로 빠르게 이동하고 기피제에서 멀리 이동할 수 있으며 편모를 시계 반대 방향 및 시계 방향으로 각각 회전하여 '달리기' 및 '뒤집기'를 수행한다. 두 회전 방향은 동일하지 않으며(편모 운동과 관련하여) 분자 스위치에 의해 선택된다.[30]]
조립[편집]
편모 조립 중에 편모의 구성 요소는 기저체의 중공 코어와 초기 필라멘트를 통과한다. 조립하는 동안 단백질 성분은 기저부보다는 편모 말단에 추가된다.[31] 시험관 내에서 편모 필라멘트는 정제된 편모를 유일한 단백질로 포함하는 용액에서 자발적으로 조립된다.[32]
진화[편집]
박테리아 편모의 적어도 10개 단백질 성분은 많은 그람 음성 박테리아에서 발견되는 3형 분비 시스템(T3SS)과 상동 단백질을 공유하므로[33] 하나가 다른 것으로 진화했을 가능성이 있다. T3SS는 편모 장치와 유사한 수의 구성 요소(약 25개의 단백질)를 가지고 있기 때문에 어떤 것이 먼저 진화했는지 결정하기 어렵다. 그러나 편모 시스템은 다양한 조절자와 샤페론을 포함하여 전반적으로 더 많은 단백질을 포함하는 것으로 보이므로 편모가 T3SS에서 진화했다고 주장되어 왔다. 그러나 편모가 먼저 진화했거나 두 구조가 병렬로 진화했을 수도 있다고 제안되었다.[34] 초기 단세포 유기체의 운동성(이동성)에 대한 요구는 진화에 의해 더 이동성이 높은 편모가 먼저 선택될 것임을 지지하지만,[34] 편모에서 진화하는 T3SS는 '환원적 진화'로 볼 수 있으며, 계통 발생 나무.[35] 두 구조가 공통 조상과 별도로 진화했다는 가설은 두 구조 사이의 단백질 유사성과 기능적 다양성을 설명한다.[36]
편모와 지적 설계 논쟁[편집]
일부 저자들은 편모가 모든 단백질이 제자리에 있을 때만 제대로 기능할 수 있다고 가정하고 진화할 수 없다고 주장했다. 즉, 편모 장치는 "환원 불가능하게 복잡"하다.[37] 그러나 많은 단백질이 삭제되거나 돌연변이될 수 있으며 편모는 때때로 효율성이 떨어지더라도 여전히 작동한다.[38] 또한, 종에 걸쳐 몇 가지 고유한 단백질이 많기 때문에 박테리아 편모 조성의 다양성은 예상보다 높았다.[39] 따라서 편모 장치는 진화론적 측면에서 분명히 매우 유연하며 단백질 성분을 완벽하게 잃거나 얻을 수 있다. 예를 들어, 대장균의 운동성을 증가시키는 다수의 돌연변이가 발견되었다.[40] 박테리아 편모의 진화에 대한 추가 증거에는 흔적 편모의 존재, 편모의 중간 형태 및 편모 단백질 서열 간의 유사성 패턴이 포함되며, 여기에는 거의 모든 핵심 편모 단백질이 비편모 단백질과의 상동성이 알려져 있다는 관찰이 포함된다.[33] 또한, 단순 반복 서브유닛의 자가 조립, 후속 분기를 통한 유전자 복제, 다른 시스템의 요소 모집('분자 브리콜라주') 및 재조합을 포함하여 편모 진화에서 중요한 역할을 하는 여러 프로세스가 확인되었다.[41]
편모 배열[편집]
박테리아의 종에 따라 편모의 수와 배열이 다르다.[42][43] 그리스어로 머리카락을 의미하는 trichos에서 따온 tricho라는 용어를 사용하여 명명되었다.[44]
- 콜레라균과 같은 Monotrichous bacteria는 단일 극성 편모를 가지고 있다.[45]
- Amphitrichous bacteria는 양쪽 끝에 각각 하나의 편모를 가지고 있다(예: Alcaligenes faecalis). 한 번에 하나의 편모만 작동하므로 어느 편모가 활성화되어 있는지 전환하여 박테리아가 빠르게 진로를 바꿀 수 있다.
- Lophotrichous bacteria는[46] 위나선균와 같이 박테리아 표면의 동일한 지점에 여러 개의 편모가 있으며 박테리아를 한 방향으로 몰아가기 위해 협력한다. 많은 경우에, 여러 편모의 기저부는 극성 소기관이라고 하는 세포막의 특수 영역으로 둘러싸여 있다.
- Peritrichous bacteria는 모든 방향으로 돌출된 편모를 가지고 있다(예: E. coli).
Monotrichous bacteria의 편모가 반시계 방향으로 회전하면 코르크 내부에서 움직이는 코르크 마개처럼 편모가 뒤에 오는 상태로 세포가 앞으로 밀려난다. 미시적 규모의 물은 일반 물과 달리 점성이 매우 높다.
이에 반해 스피로헤타는 세포의 반대 극에서 발생하는 편모 내막(endoflagella)이라고 하는 편모를 가지고 있으며, 외막을 파괴하고 electron cryotomography microscope에 의해 보여지는 바와 같이 주변 세포질 공간 내에 위치한다.[47][48][49] 세포체에 대한 필라멘트의 회전은 일반적으로 편모가 있는 박테리아의 통과를 방지할 수 있을 만큼 충분히 점성이 있는 물질을 통해서도 전체 박테리아가 코르크 마개 같은 움직임으로 앞으로 이동하도록 한다.
셀레노모나스의 특정 대형 형태에서는 30개 이상의 개별 편모가 세포체 외부에 조직되어 있으며 서로에 대해 나선형으로 꼬여 "다낭"이라고 하는 두꺼운 구조(광현미경으로 쉽게 볼 수 있음)를 형성한다.
일부 Vibrio spp. (특히 장염비브리오균[50]), 에로모나스와 같은 관련 박테리아, 두 개의 편모 시스템이 공존하며 서로 다른 유전자 세트와에너지에 대한 서로 다른 이온 구배를 사용한다. 극성 편모는 체액에서 구성적으로 발현되고 운동성을 제공하는 반면, 측면 편모는 극 편모가 회전에 너무 많은 저항을 만날 때 발현된다.[51][52][53][54][55][56] 이들은 표면이나 점성 유체에서 무리지어 움직이는 운동성을 제공한다.
번들링[편집]
번들링(Bundling)은 편모가 여러 개 있는 세포에서 발생할 수 있는 이벤트로, 편모를 함께 묶어 조정된 방식으로 회전하게 한다.
편모는 왼손 나선이며 로터에 의해 반시계 방향으로 회전하면 함께 묶이고 회전할 수 있다. 로터가 방향을 바꾸어 시계 방향으로 회전하면 편모가 번들에서 풀린다. 이로 인해 세포가 전진 동작을 멈추고 대신 제자리에서 경련을 시작할 수 있다. 이를 "텀블링(tumbling)"이라고 한다. 텀블링은 세포의 확률적 재배향을 초래하여 앞으로 헤엄치는 방향을 변경하게 한다.
어떤 자극이 번들링과 텀블링 사이의 스위치를 구동하는지 알 수 없지만 모터는 다양한 신호에 매우 잘 적응한다. 주화성("고의적인 움직임"을 설명하는 모델에서 편모의 시계 방향 회전은 세포에 유리한 화합물(예: 음식)에 의해 억제된다. 유리한 방향으로 움직일 때, 그러한 화학 유인 물질의 농도가 증가하고 따라서 텀블이 지속적으로 억제되어 앞으로 움직일 수 있다. 마찬가지로, 세포의 운동 방향이 바람직하지 않을 때(예를 들어, 화학적 유인 물질로부터 멀리 떨어져 있는 경우), 텀블은 더 이상 억제되지 않고 훨씬 더 자주 발생하여 세포가 올바른 방향으로 재배향될 가능성이 있다.
그러나 모든 편모가 시계 방향으로 회전하더라도 기하학적 및 유체 역학적 이유로 인해 번들을 형성하지 못하는 경우가 많다.[57][58]
진핵생물[편집]


이름[편집]
세균성 편모와 진핵생물의 섬모 및 편모의 구별을 강조하기 위해 일부 저자들은 이 두 개의 진핵생물 구조의 이름을 "undulipodia"(예: 1970년대 이후 마굴리스의 모든 논문)[59] 또는 "섬모"로 대체하려고 시도했다. 둘 다에 대해(예: Hülsmann, 1992;[60] Adl et al., 2012;[61] 캐빌리어스미스의 대부분의 논문), 박테리아 구조에 대해 "편모"를 보존한다. 그러나 이 기사에서 채택된 진핵생물에 대해 "섬모"와 "편모"라는 용어의 차별적인 사용은 여전히 일반적이다(예: Andersen et al., 1991;[62] Leadbeater et al., 2000).[63]
내부 구조[편집]
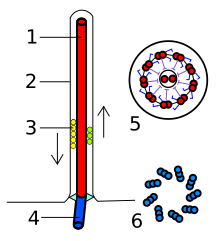
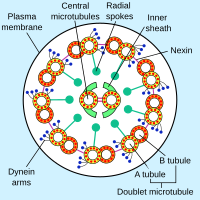
axoneme으로 알려진 진핵생물 편모의 핵심은 2개의 중앙 단일 미세소관(단 중선)을 둘러싸고 있는 이중선으로 알려진 9개의 융합된 미세소관 다발이다. 이 9+2 축삭은 진핵생물 편모의 특징이다. 진핵생물 편모의 기저에는 기저체(basal body), "안검체(blepharoplast)" 또는 키네토솜이 있으며, 이는 편모 미세소관의 미세소관 조직화 중심이며 길이가 약 500나노미터이다. 기초체는 중심소체와 구조적으로 동일하다. 편모는 세포의 원형질막으로 둘러싸여 있어 편모의 내부는 세포의 세포질에 접근할 수 있다.
축삭과 기저체 외에 형태가 비교적 일정하며 편모 장치의 다른 내부 구조는 전이대(축색체와 기저체가 만나는 곳)와 뿌리계(기저체에서 세포질로 확장되는 미세관 또는 원섬유 구조)이다), 진핵생물의 계통발생적 관계의 지표로서 더 다양하고 유용하다. 더 흔하지 않은 다른 구조로는 편모주위(또는 근축, paraxonemal) 간상체, R 섬유 및 S 섬유가 있다.[64] :63–84더 자세한 표면 구조는 아래를 참조하라.
기구[편집]
외부 9개의 이중선 미세소관 각각은 한 쌍의 디네인인 팔("내부" 및 "외부" 팔)을 인접한 미세소관으로 확장한다. 이들은 ATP 가수분해를 통해 힘을 생성한다. 편모 축삭은 또한 방사상 스포크, 외부 9개의 미세소관 이중선 각각에서 중앙 쌍을 향해 확장되는 폴리펩타이드 복합체를 포함하며, 스포크의 "머리"는 안쪽을 향한다. 방사형 스포크는 편모 운동의 조절에 관여하는 것으로 생각되지만 정확한 기능과 작용 방법은 아직 알려져 있지 않다.[65]
편모와 섬모[편집]

진핵생물의 섬모와 편모의 규칙적인 박동 패턴은 세포 수준에서 움직임을 생성한다. 예를 들면 정자의 유영과 같은 단일 세포의 추진에서부터 호흡기와 같은 세포의 고정된 층을 따라 유체의 이동에 이르기까지 다양하다.[66]
진핵 생물의 섬모와 편모는 궁극적으로 동일하지만 때때로 구조가 알려지기 이전의 전통인 운동 패턴에 따라 분류된다. 편모의 경우 움직임이 평면적이고 물결 모양인 경우가 많지만 운동성 섬모는 힘과 회복 스트로크로보다 복잡한 3차원 움직임을 수행하는 경우가 많다.[66] 또 다른 전통적인 구별 형태는 세포에 있는 9+2 소기관의 수이다.[65]
편모 내 수송[편집]
축색 소단위, 막횡단 수용체 및 기타 단백질이 편모의 길이를 따라 위아래로 이동하는 과정인 편모 내 수송은 운동성과 신호 전달 모두에서 편모의 적절한 기능에 필수적이다.[67]
진화와 발생[편집]
진핵생물의 편모 또는 섬모(아마도 조상의 특성)는[68] 비교적 다년생 상태로, 또는 편모가 있는 생활 주기 단계(예: 조이드, 배우자, 유성 포자, 지속적으로 생성되거나 아니다).[69][70][61]
첫 번째 상황은 "편모 상태"(또는 "모나도이드 조직 수준")를 가진 섬모 및 많은 진핵생물에서와 같이 다세포 유기체의 특수화된 세포(예: 해면의 choanocytes 또는 후생동물의 섬모 상피)에서 발견된다. 편모충류, 인공 그룹).
편모된 수명 주기 단계는 많은 녹조류(동물 포자 및 수컷 배우자), 선태식물 (수컷 배우자), 익룡식물(수컷 배우자), 일부 겉씨식물(소철 및은행, 수컷 배우자), 중심 규조류(수컷 배우자)와 같은 많은 그룹에서 발견된다.), 갈조류(동물 포자 및 배우자), 난균류(무성 유성 포자 및 배우자), 역모균류(동물 포자), 망형충류(동물 포자), 일부 정단복합체충류(배우자), 일부 방산충(아마 배우자),[71] 유공충(배우자) (동물 포자 및 배우자), 변형균강(동물 포자), 동물(남성 생식 세포) 및 호상균류(동물 포자와 배우자).
편모 또는 섬모는 원시 상태가 아니라 손실로 인해 일부 그룹에서 완전히 부재한다. 섬모의 소실은 홍조류, 일부 녹조류(접합조강), 소철류와 은행나무를 제외한 겉씨식물, 속씨식물, 5개형 돌말류, 일부 정단복합체충류, 일부 아메바류, 일부 후생동물의 정자,[72] 및 진균류 (제외).
유형학[편집]
편모 또는 섬모와 관련된 많은 용어가 진핵생물을 특징짓는 데 사용된다.[70][73][64] :60–63[74][75] 존재하는 표면 구조에 따라 편모는 다음과 같을 수 있다.
- 편모 편모(= 매끄럽고 말단 편모): 털이 없음, 예를 들어 후편모생물에서
- 털이 많은 편모(= tinsel, flimmer, pleuronematic 편모): 털이 있는(= mastigonemes sensu lato), 다음으로 나뉜다.
- 가는 털 (= 비관 또는 단순 털): Euglenophyceae, Dinoflagellata, 일부 Haptophyceae (Pavlovales)에서 발생
- 뻣뻣한 털 (= 관 모양의 털, retronemes, mastigonemes sensu stricto), 다음으로 나뉜다.
- bipartite hairs: 두 개의 영역이 있다. Cryptophyceae, Prasinophyceae 및 일부 Heterokonta에서 발생
- tripartite (= straminipilous) 털: 3개의 영역(기저부, 관형 샤프트 및 하나 이상의 말단 털)이 있다. 대부분의 부등편모조류에서 발생
- 스티코네마틱 편모: 한 줄의 털이 있는 편모
- 판토네틱 편모: 두 줄의 털이 있음
- acronematic: 단일 말단 유선모 또는 편모를 가진 편모(예: bodonids);[76]
- 비늘 포함: 예: Prasinophyceae
- 가시가 있는 경우: 예: 일부 갈조류
- 물결 모양의 막이 있는 경우: 예를 들어 일부 키네토플라스티드, 일부 부기체류, 운동핵편모충류 등이다.
- 코와 함께(세포의 줄기와 같은 돌출부): 예: 아푸소조아, 일부 bodonids[77]
편모의 수에 따라 세포는 다음과 같을 수 있다. (일부 저자는 "flagellated" 대신 "ciliated"를 사용함을 기억하라)[61][78]
- unflagellated: 예, 대부분의 Opisthokonta
- biflagellated: 예, 모든 Dinoflagellata, Charophyceae의 배우자, 대부분의 선태 동물 및 일부 후생 동물[72]
- 삼편모: 예, 일부 유공충의 배우자
- 사면상: 예, 일부 Prasinophyceae, Collodictyonidae
- octoflagellated: 예, 일부 Diplomonada, 일부 Prasinophyceae
- 다중 편모: 예: Opalinata, Ciliophora, Stephanopogon, Parabasalida, Hemimastigophora, Caryoblastea, Multicilia, Oedogoniales (Chlorophyta)의 배우자 (또는 조이드), 일부 다핵아베마속과 겉씨식물과 양치식물.
편모의 삽입 위치에 따라:[79]
- opisthokont: Opisthokonta에서와 같이 뒤쪽에 편모가 삽입된 세포(Vischer, 1945). Haptophyceae에서 편모는 측면에서 말단으로 삽입되지만 빠른 수영 중에는 뒤쪽으로 향한다.[80]
- akrokont: 편모가 정점에 삽입된 세포
- 아크로콘트(subakrokont): 편모가 아첨에 삽입된 세포
- pleurokont: 편모가 옆으로 삽입된 세포
박동 패턴에 따르면:
편모 유형과 관련된 기타 용어:
- isokont: 같은 길이의 편모를 가진 세포. 그것은 또한 이전에 Chlorophyta를 지칭하는 데 사용되었다.
- anisokont: 길이가 다른 편모가 있는 세포, 예를 들어 일부 Euglenophyceae 및 Prasinophyceae
- heterokont: 길이가 다른 한 쌍의 편모로 인해 Xanthophyceae를 지칭하기 위해 Luther(1899)가 도입한 용어이다. 이것은 앞쪽에 편모편모가 있고(1~2열에 세 부분으로 된 유방편모가 있음) 뒤쪽에 일반적으로 매끄러운 편모가 있는 세포를 지칭하는 데 특별한 의미를 갖다. Heterokonta 분류군을 지칭하는 데에도 사용된다.
- 스테파노콘트(stephanokont): 앞쪽 끝에 편모의 왕관이 있는 세포, 예를 들어 Oedogoniales의 배우자 및 포자, 일부 Bryopsidales의 포자 . Blackman & Tansley(1902)가 Oedogoniales를 지칭하기 위해 도입한 용어
- akont: 편모가 없는 세포. Aconta 또는 Akonta: Zygnematophyceae 및 Bacillariophyceae (Oltmanns, 1904) 또는 Rhodophyceae (Christensen, 1962)와 같은 분류학적 그룹을 지칭하는 데에도 사용되었다.
고균[편집]
일부 고균 종의 편모는 세균의 편모와 표면적으로 유사하다. 1980년대에는 전체적인 형태와 행동에 기초하여 둘의 편모가 상동인 것으로 생각되었다. 편모와 고균은 모두 세포 외부로 뻗어 있는 필라멘트로 구성되어 있으며 회전하여 세포를 추진한다. Archaeal 편모는 중앙 채널이 없는 독특한 구조를 가지고 있다. 박테리아 유형 IV 필린과 유사하게, 고균 단백질(아르케엘린)은 클래스 3 신호 펩티드로 만들어지며 유형 IV 프리필린 펩티다제 유사 효소에 의해 처리된다. 아르케엘린은 일반적으로 적절한 조립 또는 기능에 필요한 N-연결 글리칸의 추가에 의해 변형된다.[3]
1990년대의 발견은 고균과 세균 편모 사이의 수많은 세부적인 차이점을 밝혀냈다. 여기에는 다음이 포함된다.
- 세균의 편모 회전은 H+이온의 흐름인 양성자 구동력 또는 때로는 Na+ 이온의 흐름인 나트륨 원동력에 의해 구동된다. 고세균 편모 회전은 ATP에 의해 구동된다.[82]
- 박테리아 세포에는 각각 독립적으로 회전하는 많은 편모 필라멘트가 있는 경우가 많지만, 고세균 편모는 단일 어셈블리로 회전하는 많은 필라멘트 다발로 구성된다.
- 세균 편모는 끝에 편모 소단위가 추가되어 자란다. 고균 편모는 기저부에 소단위체를 추가함으로써 자란다.
- 세균성 편모는 고균보다 두껍고 세균성 필라멘트 내부에는 편모 소단위체가 필라멘트의 내부로 흘러들어올 수 있고 끝에 추가될 수 있는 충분히 큰 속이 빈 "관"이 내부에 있다.[83]
- 세균성 편모의 많은 구성 요소는 III형 분비 시스템의 구성 요소와 서열 유사성을 공유하지만 세균성 편모와 고세균의 구성 요소는 서열 유사성을 공유하지 않는다. 대신, 고세균의 일부 구성 요소는 II형 분비 시스템의 작용을 통해 조립되는 유형 IV 필리의 구성 요소와 서열 및 형태학적 유사성을 공유한다(단백질 분비 시스템의 명명법은 일관되지 않음).[83]
이러한 차이점은 세균의 편모와 고세균이 상동성이라기보다는 생물학적 유추 또는 수렴 진화의 고전적 사례가 될 수 있음을 의미한다.[84][85] 그러나 수십 년 동안 잘 알려진 박테리아 편모 연구(예:Howard Berg)와 비교할 때,[86] 고세균은 최근에야 과학적 관심을 받기 시작했다.
추가 이미지[편집]
-
[en→ko]Multiple flagella in lophotrichous arrrangement on surface of Helicobacter pylori
-
[en→ko]Physical model of a bacterial flagellum
각주[편집]
- ↑ “Prokaryotic motility structures”. 《Microbiology》 149 (Pt 2): 295–304. February 2003. doi:10.1099/mic.0.25948-0. PMID 12624192.
- ↑ “Assembly and motility of eukaryotic cilia and flagella. Lessons from Chlamydomonas reinhardtii”. 《Plant Physiology》 127 (4): 1500–7. December 2001. doi:10.1104/pp.010807. PMC 1540183. PMID 11743094.
- ↑ 가 나 《Pili and Flagella: Current Research and Future Trends》. Caister Academic Press. 2009. ISBN 978-1-904455-48-6.
- ↑ “Sperm design and sperm function”. 《Biology Letters》 2 (2): 246–9. June 2006. doi:10.1098/rsbl.2006.0449. PMC 1618917. PMID 17148374.
- ↑ “Helicobacter pylori: ulcers and more: the beginning of an era”. 《The Journal of Nutrition》 131 (10): 2789S–2793S. October 2001. doi:10.1093/jn/131.10.2789S. PMID 11584108. 2009년 2월 7일에 원본 문서 (abstract page)에서 보존된 문서. 2008년 6월 2일에 확인함.
- ↑ “Sensing wetness: a new role for the bacterial flagellum”. 《The EMBO Journal》 24 (11): 2034–42. June 2005. doi:10.1038/sj.emboj.7600668. PMC 1142604. PMID 15889148.
- ↑ “The archaellum: how Archaea swim”. 《Frontiers in Microbiology》 6: 23. 2015년 1월 27일. doi:10.3389/fmicb.2015.00023. PMC 4307647. PMID 25699024.
- ↑ Quax, TEF; Albers, SV; Pfeiffer, F (2018년 12월 14일). “Taxis in archaea.”. 《Emerging Topics in Life Sciences》 2 (4): 535–546. doi:10.1042/ETLS20180089. PMC 7289035. PMID 33525831.
- ↑ “Cilia, flagella, and microtubules”. 《The Journal of Cell Biology》 91 (3 Pt 2): 125s–130s. December 1981. doi:10.1083/jcb.91.3.125s. PMC 2112827. PMID 6459327.
- ↑ “Flagellar rotation in the archaeon Halobacterium salinarum depends on ATP”. 《Journal of Molecular Biology》 384 (1): 1–8. 2008. doi:10.1016/j.jmb.2008.08.057. PMID 18786541.
- ↑ 가 나 Alberts, Bruce (2015). 《Molecular biology of the cell》 Six판. New York, NY. 942쪽. ISBN 9780815344643.
- ↑ “Flagellar rotation and the mechanism of bacterial motility”. 《Nature》 249 (452): 73–4. May 1974. Bibcode:1974Natur.249...73S. doi:10.1038/249073a0. PMID 4598030.
- ↑ “Rapid rotation of flagellar bundles in swimming bacteria”. 《Nature》 325 (6105): 637–640. 1987. Bibcode:1987Natur.325..637L. doi:10.1038/325637a0.
- ↑ “Bacteria swim by rotating their flagellar filaments”. 《Nature》 245 (5425): 380–2. October 1973. Bibcode:1973Natur.245..380B. doi:10.1038/245380a0. PMID 4593496.
- ↑ “Movement and locomotion of microorganisms”. 《Annual Review of Microbiology》 19: 21–58. 1965. doi:10.1146/annurev.mi.19.100165.000321. PMID 5318439.
- ↑ “Bacterial motility on a surface: many ways to a common goal”. 《Annual Review of Microbiology》 57: 249–73. 2003. doi:10.1146/annurev.micro.57.030502.091014. PMID 14527279.
- ↑ “Archaeal flagella, bacterial flagella and type IV pili: a comparison of genes and posttranslational modifications”. 《Journal of Molecular Microbiology and Biotechnology》 11 (3–5): 167–91. 2006. doi:10.1159/000094053. PMID 16983194.
- ↑ “Bacterial and archaeal flagella as prokaryotic motility organelles”. 《Biochemistry. Biokhimiia》 69 (11): 1203–12. November 2004. doi:10.1007/s10541-005-0065-8. PMID 15627373.
- ↑ 〈Archaeal Flagella and Pili〉. 《Pili and Flagella: Current Research and Future Trends》. Caister Academic Press. 2009. ISBN 978-1-904455-48-6.
- ↑ “How bacteria assemble flagella”. 《Annual Review of Microbiology》 57: 77–100. 2003. doi:10.1146/annurev.micro.57.030502.090832. PMID 12730325.
- ↑ “Stabilization of flagellar filaments by HAP2 capping”. 《FEBS Letters》 568 (1–3): 105–9. June 2004. doi:10.1016/j.febslet.2004.05.029. PMID 15196929.
- ↑ “Divergence of quaternary structures among bacterial flagellar filaments”. 《Science》 320 (5874): 382–5. April 2008. Bibcode:2008Sci...320..382G. doi:10.1126/science.1155307. PMID 18420936.
- ↑ “Polar and lateral flagellar motors of marine Vibrio are driven by different ion-motive forces”. 《Nature》 355 (6356): 182–4. January 1992. Bibcode:1992Natur.355..182A. doi:10.1038/355182a0. PMID 1309599.
- ↑ Dean, Tim (2010년 8월 2일). “Inside nature's most efficient motor: the flagellar”. 《Australian Life Scientist》.
- ↑ Nagata, Yoshio (June 2014). “Unlocking the secrets of nature's nanomotor”. 《Nikkei Asian Review》.
- ↑ “Steps in the bacterial flagellar motor”. 《PLOS Computational Biology》 5 (10): e1000540. October 2009. arXiv:0904.0438. Bibcode:2009PLSCB...5E0540M. doi:10.1371/journal.pcbi.1000540. PMC 2759076. PMID 19851449.
- ↑ Whitfield, John (2008년 6월 19일). “Bacterial engines have their own clutch”. 《Nature News》 (영어): news.2008.903. doi:10.1038/news.2008.903. 2017년 5월 17일에 확인함.
- ↑ 〈Chapter 13〉. 《Living at Micro Scale: The Unexpected Physics of Being Small》. Cambridge: Harvard University Press. 2009. ISBN 978-0-674-03116-6.
- ↑ Hildebrand, Milton (November 1959). “Motions of the running Cheetah and Horse”. 《Journal of Mammalogy》 44 (4): 481–495. doi:10.2307/1376265. JSTOR 1376265. Although according to Hunter, Luke; Hamman, Dave (2003). 《Cheetah》. Struik Publishers. 37–38쪽.
the cheetah's fastest recorded speed was 110 km/h (68 mph)
- ↑ “How bacteria shift gears”. 《PLOS Biology》 9 (5): e1001061. May 2011. doi:10.1371/journal.pbio.1001061. PMC 3091840. PMID 21572986.
- ↑ “Mechanisms of type III protein export for bacterial flagellar assembly”. 《Molecular BioSystems》 4 (11): 1105–15. November 2008. doi:10.1039/b808065h. PMID 18931786.
- ↑ “Reconstitution of Bacterial Flagella In Vitro”. 《Journal of Molecular Biology》 10: 42–56. October 1964. doi:10.1016/S0022-2836(64)80026-7. PMID 14222895.
- ↑ 가 나 “From The Origin of Species to the origin of bacterial flagella”. 《Nature Reviews. Microbiology》 4 (10): 784–90. October 2006. doi:10.1038/nrmicro1493. PMID 16953248.
- ↑ 가 나 “Evolution of bacterial type III protein secretion systems”. 《Trends in Microbiology》 12 (3): 113–5. March 2004. doi:10.1016/j.tim.2004.01.003. PMID 15001186.
- ↑ “Bacterial type III secretion systems are ancient and evolved by multiple horizontal-transfer events”. 《Gene》 312: 151–63. July 2003. doi:10.1016/S0378-1119(03)00612-7. PMID 12909351.
- ↑ “Evolution of the type III secretion system and its effectors in plant-microbe interactions”. 《The New Phytologist》 177 (1): 33–47. 2008. doi:10.1111/J.1469-8137.2007.02293.X. PMID 18078471.
- ↑ Behe, M. (2007) The Edge of Evolution. Free Press, New York
- ↑ “The protein network of bacterial motility”. 《Molecular Systems Biology》 3: 128. 2007. doi:10.1038/msb4100166. PMC 1943423. PMID 17667950.
- ↑ “Novel conserved assembly factor of the bacterial flagellum”. 《Journal of Bacteriology》 188 (21): 7700–6. November 2006. doi:10.1128/JB.00820-06. PMC 1636259. PMID 16936039.
- ↑ “Novel genes associated with enhanced motility of Escherichia coli ST131”. 《PLOS ONE》 12 (5): e0176290. 2017년 5월 10일. Bibcode:2017PLoSO..1276290K. doi:10.1371/journal.pone.0176290. PMC 5425062. PMID 28489862.
- ↑ “Bacterial flagella and Type III secretion: case studies in the evolution of complexity”. 《Genome Dynamics》 3: 30–47. 2005. doi:10.1159/000107602. ISBN 978-3-8055-8340-4. PMID 18753783.
- ↑ “Bacterial flagella” (PDF). 2021년 12월 29일에 확인함.
- ↑ “Architecture of a flagellar apparatus in the fast-swimming magnetotactic bacterium MO-1”. 《Proc Natl Acad Sci U S A》 109 (50): 20643–8. December 2012. Bibcode:2012PNAS..10920643R. doi:10.1073/pnas.1215274109. PMC 3528567. PMID 23184985.
- ↑ “tricho- prefix”. 2022년 3월 26일에 확인함.
- ↑ Echazarreta, MA; Klose, KE (2019). “Vibrio Flagellar Synthesis.”. 《Frontiers in Cellular and Infection Microbiology》 9: 131. doi:10.3389/fcimb.2019.00131. PMC 6504787. PMID 31119103.
- ↑ “Lopho”. 2022년 3월 26일에 확인함.
- ↑ “Cryo-electron tomography elucidates the molecular architecture of Treponema pallidum, the syphilis spirochete”. 《Journal of Bacteriology》 191 (24): 7566–80. December 2009. doi:10.1128/JB.01031-09. PMC 2786590. PMID 19820083.
- ↑ “Native cellular architecture of Treponema denticola revealed by cryo-electron tomography”. 《Journal of Structural Biology》 163 (1): 10–7. July 2008. doi:10.1016/j.jsb.2008.03.009. PMC 2519799. PMID 18468917.
- ↑ “Comparative cryo-electron tomography of pathogenic Lyme disease spirochetes”. 《Molecular Microbiology》 71 (6): 1415–34. March 2009. doi:10.1111/j.1365-2958.2009.06613.x. PMID 19210619.
- ↑ “Analysis of the polar flagellar gene system of Vibrio parahaemolyticus”. 《Journal of Bacteriology》 182 (13): 3693–704. July 2000. doi:10.1128/JB.182.13.3693-3704.2000. PMC 94540. PMID 10850984.
- ↑ “Effect of viscosity on swimming by the lateral and polar flagella of Vibrio alginolyticus”. 《Journal of Bacteriology》 178 (16): 5024–6. August 1996. doi:10.1128/jb.178.16.5024-5026.1996. PMC 178290. PMID 8759871.
- ↑ “Dual flagellar systems enable motility under different circumstances”. 《Journal of Molecular Microbiology and Biotechnology》 7 (1–2): 18–29. 2004. doi:10.1159/000077866. PMID 15170400.
- ↑ “Bacterial lateral flagella: an inducible flagella system”. 《FEMS Microbiology Letters》 263 (2): 127–35. October 2006. doi:10.1111/j.1574-6968.2006.00403.x. PMID 16978346.
- ↑ “Regulation of lateral flagella gene transcription in Vibrio parahaemolyticus”. 《Journal of Bacteriology》 167 (1): 210–8. July 1986. doi:10.1128/jb.167.1.210-218.1986. PMC 212863. PMID 3013835.
- ↑ “Analysis of the lateral flagellar gene system of Aeromonas hydrophila AH-3”. 《Journal of Bacteriology》 188 (3): 852–62. February 2006. doi:10.1128/JB.188.3.852-862.2006. PMC 1347325. PMID 16428388.
- ↑ “Polar flagellum biogenesis in Aeromonas hydrophila”. 《Journal of Bacteriology》 188 (2): 542–55. January 2006. doi:10.1128/JB.188.2.542-555.2006. PMC 1347287. PMID 16385045.
- ↑ “A macroscopic scale model of bacterial flagellar bundling”. 《Proceedings of the National Academy of Sciences of the United States of America》 100 (26): 15481–5. December 2003. arXiv:cond-mat/0312562. Bibcode:2003PNAS..10015481K. doi:10.1073/pnas.2633596100. PMC 307593. PMID 14671319.
- ↑ “Bacterial flagella rotating in bundles: a study in helical geometry”. 《Proceedings of the National Academy of Sciences of the United States of America》 74 (1): 221–5. January 1977. Bibcode:1977PNAS...74..221M. doi:10.1073/pnas.74.1.221. PMC 393230. PMID 264676.
- ↑ “The collapse of the two-kingdom system, the rise of protistology and the founding of the International Society for Evolutionary Protistology (ISEP)”. 《International Journal of Systematic and Evolutionary Microbiology》 53 (Pt 6): 1707–14. November 2003. doi:10.1099/ijs.0.02587-0. PMID 14657097.
- ↑ “Undulipodium: End of a useless discussion”. 《European Journal of Protistology》 28 (3): 253–7. August 1992. doi:10.1016/s0932-4739(11)80231-2. PMID 23195228.
- ↑ 가 나 다 “The revised classification of eukaryotes”. 《The Journal of Eukaryotic Microbiology》 59 (5): 429–93. September 2012. doi:10.1111/j.1550-7408.2012.00644.x. PMC 3483872. PMID 23020233.
- ↑ “Terminology and nomenclature of the cytoskeletal elements associated with the flagellar/ciliary apparatus in protists”. 《Protoplasma》 164 (1–3): 1–8. 1991. doi:10.1007/bf01320809.
- ↑ Leadbeater, Barry S. C.; Green, John C., 편집. (2000). 《Flagellates: Unity, Diversity and Evolution》. The Systematics Association Special Volume 59. Taylor and Francis. ISBN 978-1-4822-6822-5.
- ↑ 가 나 Barsanti, Laura; Gualtieri, Paolo (2006). 《Algae: Anatomy, Biochemistry, and Biotechnology》. Florida, USA: CRC Press. ISBN 9780203492598.
- ↑ 가 나 Lindemann, CB; Lesich, KA (2010년 2월 15일). “Flagellar and ciliary beating: the proven and the possible.”. 《Journal of Cell Science》 123 (Pt 4): 519–28. doi:10.1242/jcs.051326. PMID 20145000.
- ↑ 가 나 Lodish, Harvey; Berk, Arnold; Zipursky, S. Lawrence; Matsudaira, Paul; Baltimore, David; Darnell, James (2000). 〈Section 19.4Cilia and Flagella: Structure and Movement〉. 《Cilia and Flagella: Structure and Movement》. ISBN 0-7167-3136-3.
- ↑ “Intraflagellar transport and cilia-dependent renal disease: the ciliary hypothesis of polycystic kidney disease”. 《Journal of the American Society of Nephrology》 15 (10): 2528–36. October 2004. doi:10.1097/01.ASN.0000141055.57643.E0. PMID 15466257.
- ↑ “Evolution of microtubule organizing centers across the tree of eukaryotes”. 《The Plant Journal》 75 (2): 230–44. July 2013. doi:10.1111/tpj.12145. PMID 23398214.
- ↑ Raven, J.A. (2000). 〈The flagellate condition〉. 《Leadbeater & Green 2000, 27–48쪽》. ISBN 9781482268225.
- ↑ 가 나 〈Spores of Fungi〉. 《2007》 3판. Cambridge: Cambridge University Press. 2007년 1월 25일. 23–24쪽. ISBN 9781139461504.
- ↑ “The chastity of amoebae: re-evaluating evidence for sex in amoeboid organisms”. 《Proceedings. Biological Sciences》 278 (1715): 2081–90. July 2011. doi:10.1098/rspb.2011.0289. PMC 3107637. PMID 21429931.
- ↑ 가 나 〈Evolution of human gametes: spermatozoa.〉. 《Gametes: the spermatozoon》. Cambridge University Press. 1995. ISBN 9780521479967.
- ↑ 《Introduction to Phycology》. Oxford: Blackwell Scientific Publications. 1987. 65쪽. ISBN 9781444314205.
- ↑ 《The Fine Structure of Algal Cells》. London: Academic Press. 1973. 57–79쪽. ISBN 9780323158237.
- ↑ 《Phycology》 4판. Cambridge University Press. 2008. 7쪽. ISBN 9781139469876.
lee tubular hairs.
- ↑ Corliss, J.O.; Lom, J (2000). 〈An annotated glossary of protozoological terms〉. Lee, J.J.; Leedale, G.F.; Bradbury, P. 《An illustrated guide to the protozoa》 2 2판. Society of Protozoologists. 1346–85쪽. ISBN 1891276239.
- ↑ 가 나 “A short guide to common heterotrophic flagellates of freshwater habitats based on the morphology of living organisms”. 《Protist》 164 (6): 842–60. November 2013. doi:10.1016/j.protis.2013.08.003. PMID 24239731.
- ↑ 《Protozoa and other Protists》. London: Edward Arnold. 1989. 98–99쪽. ISBN 9780521428057.
- ↑ 《Aquatic phycomycetes》 2판. Ann Arbor: Michigan: University of Michigan Press. 1960. 15쪽.
- ↑ “The ultrastructure and taxonomy of the Chrysophyceae and Prymnesiophyceae (Haptophyceae): a survey with some new observations on the ultrastructure of the Chrysophyceae”. 《Journal of the Linnean Society of London, Botany》 72 (2): 55–80. 1976. doi:10.1111/j.1095-8339.1976.tb01352.x.
- ↑ “Origin and evolution of flagellar movement”. 《Cell Motil》 5: 137–138. 1985.
- ↑ Madigan, Michael T. (2019). 《Brock biology of microorganisms》 Fifteen, Global판. NY, NY. 70–71쪽. ISBN 9781292235103.
- ↑ 가 나 “Assembly and function of the archaeal flagellum”. 《Biochemical Society Transactions》 39 (1): 64–9. January 2011. doi:10.1042/BST0390064. PMID 21265748.
- ↑ “The archaeal flagellum: a different kind of prokaryotic motility structure”. 《FEMS Microbiology Reviews》 25 (2): 147–74. April 2001. doi:10.1111/j.1574-6976.2001.tb00575.x. PMID 11250034.
- ↑ “Archaeal flagellum”. 《www.uniprot.org》. 2019년 6월 24일에 확인함.
- ↑ Berg, Howard C. (2003). 《E. coli in motion》 1. Aufl.판. New York: Springer. ISBN 9780387008882.

![[en→ko]Multiple flagella in lophotrichous arrrangement on surface of Helicobacter pylori](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d6/EMpylori.jpg/120px-EMpylori.jpg)
![[en→ko]Physical model of a bacterial flagellum](http://upload.wikimedia.org/wikipedia/commons/thumb/3/3c/Physical_model_of_a_bacterial_flagellum.jpg/90px-Physical_model_of_a_bacterial_flagellum.jpg)