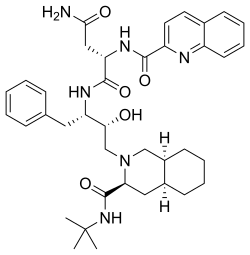
사퀴나비르
| |
| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
| (2S)-N-[(2S,3R)-4-[(3S)-3-(tert-butylcarbamoyl)-decahydroisoquinolin-2-yl]-3-hydroxy-1-phenylbutan-2-yl]-2-(quinolin-2-ylformamido)butanediamide | |
| 식별 정보 | |
| CAS 등록번호 | 127779-20-8 |
| ATC 코드 | J05AE01 |
| PubChem | 441243 |
| 드러그뱅크 | DB01232 |
| ChemSpider | 390016 |
| 화학적 성질 | |
| 화학식 | C38H50N6O5 |
| 분자량 | 670.841 g/mol |
| SMILES | eMolecules & PubChem |
| 약동학 정보 | |
| 생체적합성 | ~4% (without ritonavir boosting)[1] |
| 단백질 결합 | 98% |
| 동등생물의약품 | ? |
| 약물 대사 | Hepatic, mainly by en:CYP3A4 |
| 생물학적 반감기 | 9–15 시간 |
| 배출 | feces (81%) and urine (3%) |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B1 (오스트레일리아) |
| 법적 상태 | |
| 투여 방법 | ? |
사퀴나비르(Saquinavir, 상품명: Invirase, Fortovase)는 후천면역결핍증후군 치료 또는 예방을 위해 다른 약물과 함께 사용되는 항레트로바이러스제이다.[2] 일반적으로 효력을 증대시키기 위해 리토나비르 또는 로피나비르/리토나비르와 함께 사용된다.[2] 구강으로 투여된다.[2]
일반적인 부작용으로는 메스꺼움, 구토, 설사, 피로가 포함된다.[2] 더 심각한 부작용으로는 QT 간격 연장, 심장 블록, 고지혈증, 간질환 등의 문제가 포함된다.[2] 임신 중 복용은 안전한 것으로 보인다.[2] 프로테아제 억제제 계열에 속하며 HIV 프로테아제를 차단함으로써 동작한다.[2]
사퀴나비르는 1988년 특허를 받았으며 1995년 처음 판매되었다.[3][4] 2015년 기준으로, 미국에서 제네릭 의약품으로 판매되지는 않으며 값이 비싼 편이다.[5] 개발도상국의 도매가는 일일 대략 4.50 USD이다.[6]
의학적 사용[편집]
사키나비르는 HIV/AIDS를 치료하거나 예방하기 위해 다른 약들과 함께 병용 투여된다.[7] 일반적으로 효과를 높이기 위해 리토나비르 또는 로피나비르/리토나비르와 함께 사용된다.[7]
부작용[편집]
어느 제형에서든 사퀴나비르에 대한 가장 빈번한 부작용은 설사, 복통, 메스꺼움, 구토, 변비를 포함한 가벼운 위장 증상이다. 그 외 부작용으로는 피로, 요통, 건조한 입술과 피부, 발열이 있다.[8]
생체이용률 및 약물 상호작용[편집]
상품명 Invirase 제제로서 사퀴나비르(Saquinavir)는 단독복용시, 경구 생체이용률이 낮고 일관성이 없다. 상품명 Fortovase의 표준 투여 제형은 상품명 Invirase보다 약 8배 더 높은 활성을 나타낸다.[9]
임상에서 두 형태의 사퀴나비르(Saquinavir)의 경구 생체이용률은 PI 리토나비르(ritonavir)도 같이 투여했을 때 유의하게 증가한 것으로 나타났다. 이것은 환자의 입장에서, HIV의 복제를 효과적으로 억제할 수 있는 충분한 혈장 농도를 유지하면서 적은 양의 사퀴나비르(Saquinavir)를 복용할 수 있다는 장점이 된다.
이러한 반가운 결과의 메커니즘은 직접적으로 알려지지 않았지만 나중에 리토나비르가 사이토크롬 P450 3A4를 억제한다는 것이 밝혀졌다. 일반적으로 이 효소는 사퀴나비르(Saquinavir)를 대사시켜 비활성 형태로 만들지만 리토나비르(ritonavir)가 이 효소를 억제하기 때문에 사퀴나비르(Saquinavir)의 혈장 농도가 크게 증가하게 된다. 또한 리토나비르(ritonavir)는 적은 양으로여러 약물 운반체를 억제한다.
다른 프로테아제 억제제와 달리 사퀴나비르(Saquinavir)의 흡수는 오메프라졸(Omeprazole)에 의해 개선되는 것으로 나타났다.[10]
작용 기전[편집]
사퀴나비르(Saquinavir)는 프로테아제 억제제이다. 프로테아제는 단백질 분자를 더 작은 조각으로 분해하는 효소다. HIV 프로테아제는 세포내에서 바이러스 복제와 감염된 세포로부터 성숙 바이러스 입자의 방출 모두에 필수적인 효소이다. 사퀴나비르(Saquinavir)는 바이러스 프로테아제의 활성 부위에 결합하여 바이러스 다단백질(polyprotein)의 분해를 방지하여 바이러스의 성숙을 억제한다. 사퀴나비르(Saquinavir)는 HIV-1 및 HIV-2 프로테아제를 모두 억제한다.[11]
역사[편집]

사퀴나비르(Saquinavir)는 제약 회사 로슈(Roche)에서 개발되었다.[13] 사퀴나비르(Saquinavir)는 리토나비르(ritonavir)와 인디나비르(indinavir)보다 몇 개월 앞서 미국 식품의약국(FDA) 승인을 받은 6번째 항레트로바이러스제이자 최초의 프로테아제 억제제였다.[14] 새로운 종류의 항레트로바이러스 약물인 사퀴나비르(Saquinavir)는 AIDS관련으로 인한 사망 위험을 크게 줄이는 데 도움이 된, 고활성 항레트로바이러스 요법(HAART) 개발에 중추적인 역할을 했다. 미국에서 2년동안 사망자가 50,000에서 18,000으로 감소하였다.[12][15] 로슈(Roche)는 Invirase에 대해 "FDA 가속 승인"을 요청하였고 받아들여졌다. 이 승인은 심각한 질병 치료를 위한 약물의 출시 시간을 단축하기 위해 고안된 과정이다. 하지만 이러한 결정은 AIDS 활동가들이 엄격한 검사와 조기 접근의 이점에 대해 동의하지 않았기 때문에 논란의 여지가 있는 결정이었다.[16]
1997년 11월 7일, 생체 이용률 향상을 목적으로 재설계된 연질 젤 캡슐인 Fortovase[17]로 다시 승인되었다. 2005년 5월 로슈(Roche)는 수요 감소를 감안하였을 때, fortovase의 판매를 2006년 초에 중단할 것이라고 발표했다. 이는, AIDS 약물을 대사하는 효소를 억제하는 리토나비르(ritonavir)[18]와 함께 제제화된 인비라아제(invirase) 때문이다.[출처 필요]
사회와 문화[편집]
경제[편집]
2015년 기준[update], 제네릭 의약품으로 제공되지 않았다.[19]
제형[편집]
두가지 제형이 시장에 판매되었다:
- 사퀴나비르(saquinavir)의 생체이용률을 증가시키기 위해 리토나비르(ritonavir)와의 조합이 필요한 상품명 인비라제(Invirase)가 들어있는 경질 젤라틴 캡슐의 메실레이트 제형;
- 2006년에 전 세계적으로 중단된 상표명 Fortovase의 연질 젤라틴 캡슐(마이크로에멀젼[20], 경구 제형) 형태의 사퀴나비르(saquinavir) 제형.[21]
각주[편집]
- ↑ “Invirase (saquinavir mesylate) Capsules and Tablets, for Oral Use. Full Prescribing Information” (PDF). Genentech, Inc. 2015년 11월 24일에 원본 문서 (PDF)에서 보존된 문서. 2015년 11월 23일에 확인함.
- ↑ 가 나 다 라 마 바 사 “Saquinavir”. The American Society of Health-System Pharmacists. 2015년 9월 8일에 원본 문서에서 보존된 문서. 2015년 9월 5일에 확인함.
- ↑ Minor, Lisa K. (2006). 《Handbook of Assay Development in Drug Discovery.》. Hoboken: CRC Press. 117쪽. ISBN 9781420015706. 2016년 3월 31일에 원본 문서에서 보존된 문서.
- ↑ Fischer, Jnos; Ganellin, C. Robin (2006). 《Analogue-based Drug Discovery》 (영어). John Wiley & Sons. 509쪽. ISBN 9783527607495.
- ↑ Hamilton, Richart (2015). 《Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition》. Jones & Bartlett Learning. 72쪽. ISBN 9781284057560.
- ↑ “Saquinavir”. 《International Drug Price Indicator Guide》. 2019년 3월 1일에 원본 문서에서 보존된 문서. 2015년 9월 6일에 확인함.
- ↑ 가 나 “Saquinavir”. The American Society of Health-System Pharmacists. 2015년 9월 8일에 원본 문서에서 보존된 문서. 2015년 9월 5일에 확인함.
- ↑ “Saquinavir: MedlinePlus Drug Information” (영어). 2021년 6월 29일에 확인함.
- ↑ “Fortovase”. 《Drugs.com》. 2019년 3월 22일. 2020년 4월 28일에 원본 문서에서 보존된 문서. 2020년 1월 28일에 확인함.
- ↑ Winston A; Back D; Fletcher C; 외. (2006). “Effect of omeprazole on the pharmacokinetics of saquinavir-500 mg formulation with ritonavir in healthy male and female volunteers”. 《AIDS》 20 (10): 1401–6. doi:10.1097/01.aids.0000233573.41597.8a. PMID 16791014. S2CID 44506039.
- ↑ Raphael Dolin, Henry Masur, Michael S. Saag. "AIDS Therapy", Churchill Livingstone, (1999), p. 129.
- ↑ 가 나 다 “HIV Surveillance—United States, 1981-2008”. 2013년 11월 9일에 원본 문서에서 보존된 문서. 2013년 11월 8일에 확인함.
- ↑ J. Hilts, Philip (1995년 12월 8일). “MF.D.A. Backs A New Drug To Fight AIDS”. 《New York Times》. 2020년 10월 28일에 확인함.
- ↑ “Antiretroviral Drug Discovery and Development”. 《NIH》. 2018년 11월 26일. 2020년 10월 29일에 확인함.
- ↑ The CDC, in its Morbidity and Mortality Weekly Report, ascribes this to "highly active antiretroviral therapy", without mention of either of these drugs, see the preceding citation. A further citation is needed to make this accurate connection between this drop and the introduction of the protease inhibitors.
- ↑ “Drugs! Drugs! Drugs! An Overview of the Approved Anti-HIV Medications”. The Body. 2013년 11월 9일에 원본 문서에서 보존된 문서. 2013년 2월 20일에 확인함.
- ↑ “Drug Approval Package: Fortovase/Saquinavir NDA 20828”. 《U.S. Food and Drug Administration (FDA)》. 1999년 12월 24일. 2020년 1월 28일에 확인함.
- ↑ Withdrawal of Fortovase (PDF) 보관됨 2006-05-14 - 웨이백 머신
- ↑ “Generic Invirase Availability”. 《Drugs.com》. 2020년 7월 9일에 확인함.
- ↑ Gibaud S, Attivi D (August 2012). “Microemulsions for oral administration and their therapeutic applications” (PDF). 《Expert Opinion on Drug Delivery》 9 (8): 937–51. doi:10.1517/17425247.2012.694865. PMID 22663249. S2CID 28468973.
- ↑ News-Medical.Net. May 18, 2005 Roche to discontinue the sale and distribution of Fortovase (saquinavir) 보관됨 2015-02-22 - 웨이백 머신
외부 링크[편집]
- Saquinavir bound to proteins in the PDB
