글리옥실산: 두 판 사이의 차이
영어판 위키(2021년 4월 2일 버전)를 참고하여 한국어판 문서로 번역함. |
(차이 없음)
|
2021년 4월 7일 (수) 12:16 판

| |

| |
| 이름 | |
|---|---|
| 우선명 (PIN)
oxoacetic acid[1] | |
| 체계명
Oxoethanoic acid | |
| 별칭 | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.005.508 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C2H2O3 | |
| 몰 질량 | 74.035 g·mol−1 |
| 밀도 | 1.384 g/mL |
| 녹는점 | 80 °C (176 °F; 353 K)[4] |
| 끓는점 | 111 °C (232 °F; 384 K) |
| 산성도 (pKa) | 3.18,[2] 3.32 [3] |
| 관련 화합물 | |
다른 음이온
|
글리옥실레이트 |
관련 카복실산
|
폼산 아세트산 글리콜산 옥살산 프로피온산 피루브산 |
관련 화합물
|
아세트알데하이드 글리옥살 글리콜알데하이드 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
글리옥실산(영어: glyoxylic acid) 또는 옥소아세트산(영어: oxoacetic acid)은 유기 화합물이다. 아세트산, 글리콜산, 옥살산과 함께 글리옥실산은 C2 카복실산의 한 종류이다. 이라고도 한다. 글리옥실산은 자연에서 생성되는 무색 고체로 산업적으로 유용하다.
구조 및 명명법
글리옥실산의 구조는 카보닐기(알데하이드 작용기)를 가지고 있는 것으로 설명되지만, 알데하이드는 일부 상황에서 널리 퍼진 형태의 일부 성분일 뿐이다. 대신 글리옥실산은 종종 수화물 또는 고리형 이량체로 존재한다. 예를 들어 물이 있을 때 카보닐기는 제미날 다이올("일수화물"로 설명됨)로 빠르게 전환된다. 평형 상수(K)는 실온에서 다이하이드록시 아세트산의 형성에 대해서는 300이다.[5]
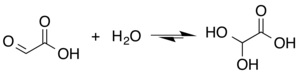 |
용액에서 일수화물은 헤미아세탈 이량체 형태와 평형 상태로 존재한다.[6]
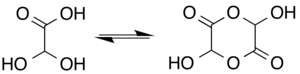 |
분리되었을 때 알데하이드 구조는 카복실 수소에 매우 근접한 알데하이드 카보닐과 함께 고리형 수소 결합 구조를 주요 형태이성질체로 가지고 있다.[7]
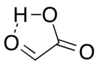 |
글리옥실산의 헨리의 법칙 상수는 KH = 1.09 × 104 × exp[(40.0 × 103/R) × (1/T − 1/298)]이다.[8]
제조
글리옥실산의 짝염기는 글리옥실레이트(영어: glyoxylate)로 알려져 있으며, 화합물이 중성 pH에서 용액에 존재하는 형태이다. 글리옥실레이트는 여러 아마이드화된 펩타이드의 생합성에서 아마이드화 과정의 부산물이다.
과거에 글리옥실산은 옥살산으로부터 전기합성적으로 제조되었다.[9][10] 유기 합성에서 황산 전해질에서 옥살산으로부터 글리옥실산을 제조하기 위해 이산화 납 음극을 사용하였다.[11]
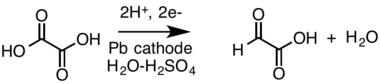 |
뜨거운 질산은 글리옥살을 글리옥실로 산화시킬 수 있다. 그러나 이 반응은 발열성이 크고 열 폭주가 일어나기 쉬우며 옥살산은 주요 부산물이다.
생물학적 역할
글리옥실산은 글리옥실산 회로의 대사 중간생성물로 글리옥실산 회로는 세균,[12]균류, 식물[13]과 같은 생물이 지방산을 탄수화물로 전환할 수 있도록 한다. 글리옥실산 회로는 균류에 대한 식물의 방어 기작의 유도에도 중요하다.[14] 글리옥실산 회로는 아이소시트르산을 글리옥실산과 석신산으로 전환시키는 아이소시트르산 분해효소의 활성을 통해 시작된다. 석신산 생합성과 같은 다양한 용도로 경로를 선택하기 위한 연구가 진행되고 있다.[15]
사람에서
글리옥실산은 크게 두 가지 경로를 통해 생성되는 데, 하나는 퍼옥시좀에서 글리콜산의 산화를 통해 생성되고 다른 하나는 미토콘드리아에서 하이드록시프롤린의 이화대사를 통해 생성된다.[16] 퍼옥시좀에서 글리옥실산은 AGT1에 의해 글리신으로 전환되거나 글리콜산 산화효소에 의해 옥살산으로 전환된다. 소량의 글리옥실산은 세포질의 젖산 탈수소효소에 의해 옥살산으로 전환된다.[17]
 |
식물에서
글리옥실산은 글리옥실산 회로의 대사 중간생성물일 뿐만 아니라 광호흡 경로의 중요한 대사 중간생성물이기도 하다. 광호흡은 루비스코가 CO2 대신 O2와 반응할 때 일어난다. 광호흡은 처음에는 에너지와 자원의 낭비인 것으로 간주되었지만, 이후의 연구에 따르면 광호흡은 탄소와 CO2를 재생성하고, 독성을 가지는 포스포글리콜산을 제거하여 방어 메커니즘을 작동시키는 중요한 역할을 하는 것으로 밝혀졌다.[18][19] 광호흡에서 글리옥실산은 퍼옥시좀에서 글리콜산 산화효소의 활성을 통해 글리콜산으로부터 생성된다. 그런 다음 SGAT와 GGAT의 작용을 통해 글리신으로 전환된 다음 미토콘드리아로 운반된다.[20][19] 또한 피루브산 탈수소효소 복합체가 글리콜산 및 글리옥실산 대사에 역할을 할 수 있다고 보고되었다.[21]
질병과의 관련성
당뇨병
글리옥실산은 제2형 당뇨병에 대한 잠재적인 초기 마커로 생각된다.[22] 당뇨병 병리의 주요 조건들 중 하나는 고혈당증으로 인한 최종 당화 산물의 생성이다.[23] 최종 당화 산물은 조직 손상 및 심혈관계 질환과 같은 당뇨병의 추가적인 합병증을 유발시킬 수 있다.[24] 이들은 일반적으로 환원당 및 알파-옥소알데하이드에 존재하는 것과 같은 반응성 알데하이드로부터 형성된다. 한 연구에서 글리옥실산의 수치는 나중에 제2형 당뇨병 진단을 받은 환자에서 유의미하게 증가하는 것으로 나타났다.[22] 상승된 수치는 진단전 최대 3년 전에 발견되어 글리옥실산이 조기 예측 마커가 될 수 있는 잠재성을 보여준다.
신장결석증
글리옥실산은 신장결석증(일반적으로 신장결석으로 알려져 있음)의 주요 원인인 고옥살산뇨의 발생에 관여한다. 글리옥실산은 옥살산 수송을 담당하는 유전자인 설페이트 음이온 수송체-1(sulfate anion transporter-1, sat-1)의 기질이자 유도 물질이며, 이를 통해 sat-1 mRNA 발현을 증가시키고 결과적으로 세포로부터 옥살산의 유출을 증가시킬 수 있다. 증가된 옥살산의 방출은 소변에 칼슘 옥살레이트를 축적시켜서 결국에 신장결석을 생성시킨다.[17]
글리옥실산의 대사 교란은 고옥살산뇨증 발병의 추가적인 메커니즘을 제공한다. HOGA1 유전자의 돌연변이는 하이드록시프롤린에서 글리옥실산 경로로의 효소인 4-하이드록시-2-옥소글루타르산 알돌레이스의 손실로 이어진다. 이 경로에서 생성된 글리옥실산은 일반적으로 세포질에서 옥살산으로의 산화를 방지하기 위해 다른 먼 곳에 저장된다. 그러나 교란된 경로는 4-하이드록시-2-옥소글루타르산의 축적을 유발하며, 이는 또한 세포질로 수송될 수 있고 다른 알돌레이스를 통해 글리옥실산으로 전환될 수 있다. 이러한 글리옥실산 분자는 옥살산으로 산화되어 옥살산의 농도를 증가시키고 고옥살산뇨증을 유발할 수 있다.[16]
반응 및 용도
글리옥실산은 아세트산보다 약 10배 정도 더 강한 산이며, 산 해리상수는 4.7 × 10−4 (pKa = 3.32)이다.
- OCHCO2H ⇄ OCHCO−
2 + H+
염기와 있으면 글리옥실산은 불균등화되어 하이드록시아세트산과 옥살산을 형성한다.
- 2 OCHCO2H + H2O → HOCH2CO2H + HO2CCO2H
글리옥실산은 요소 및 1,2-다이아미노벤젠과의 축합으로 헤테로고리를 생성한다.
페놀 유도체
일반적으로 글리옥실산은 페놀과 친전자성 방향족 치환 반응을 하며, 이 반응은 여러 다른 화합물의 합성에서 다양하게 사용된다.
페놀 자체가 있는 중간생성물은 4-하이드록시만델산이다. 4-하이드록시만델산은 암모니아와 반응하여 아목시실린의 전구체인 하이드록시페닐글리신을 생성한다. 4-하이드록시만델산의 환원은 아테놀올의 전구체인 4-하이드록시페닐아세트산을 생성한다.
글리옥실산이 페놀 성분인 구아야콜과 반응한 후 산화 및 탈카복실화되는 일련의 반응은 순 폼일화 과정으로 바닐린에 대한 경로를 제공한다.[6][25][26]
홉킨스-콜 반응
글리옥실산은 단백질에서 트립토판의 존재를 확인하는 데 사용되는 홉킨스-콜 반응의 구성 요소이다.[27]
환경화학
글리옥실산은 2차 유기 에어로졸과 함께 풍부한 케톤 및 알데하이드 함유 카복실산들 중 하나이다. 물과 햇빛이 있는 곳에서 글리옥실산은 광화학 산화를 겪을 수 있다. 여러 가지 다른 반응들이 이어질 수 있으며 다양한 다른 카복실산 및 알데하이드 생성물이 만들어진다.[28]
안전
글리옥실산은 쥐에서 2500 mg/kg의 반수 치사량으로 독성이 거의 없다.
각주
- ↑ 가 나 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 748쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ Dissociation Constants Of Organic Acids and Bases (600 compounds), http://zirchrom.com/organic.htm.
- ↑ pKa Data Compiled by R. Williams, “Archived copy” (PDF). 2010년 6월 2일에 원본 문서 (PDF)에서 보존된 문서. 2010년 6월 2일에 확인함..
- ↑ Merck Index, 11th Edition, 4394
- ↑ Sørensen, P. E.; Bruhn, K.; Lindeløv, F. (1974). “Kinetics and equilibria for the reversible hydration of the aldehyde group in glyoxylic acid.”. 《Acta Chem. Scand.》 28: 162–168. doi:10.3891/acta.chem.scand.28a-0162.
- ↑ 가 나 다 Georges Mattioda and Yani Christidis “Glyoxylic Acid” Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. doi 10.1002/14356007.a12_495
- ↑ Redington, Richard L.; Liang, Chin-Kang Jim (1984). “Vibrational spectra of glyoxylic acid monomers”. 《Journal of Molecular Spectroscopy》 104 (1): 25–39. Bibcode:1984JMoSp.104...25R. doi:10.1016/0022-2852(84)90242-X.
- ↑ Ip, H. S. Simon; Huang, X. H. Hilda; Yu, Jian Zhen (2009). “Effective Henry's law constants of glyoxal, glyoxylic acid, and glycolic acid” (PDF). 《Geophysical Research Letters》 36 (1): L01802. Bibcode:2009GeoRL..36.1802I. doi:10.1029/2008GL036212.
- ↑ Tafel, Julius; Friedrichs, Gustav (1904). “Elektrolytische Reduction von Carbonsäuren und Carbonsäureestern in schwefelsaurer Lösung”. 《Berichte der Deutschen Chemischen Gesellschaft》 37 (3): 3187–3191. doi:10.1002/cber.190403703116.
- ↑ Cohen, Julius (1920). 《Practical Organic Chemistry 2nd Ed.》 (PDF). London: Macmillan and Co. Limited. 102–104쪽.
- ↑ François Cardarelli (2008). 《Materials Handbook: A Concise Desktop Reference》. Springer. 574쪽. ISBN 978-1-84628-668-1.
- ↑ Holms WH (1987). “Control of flux through the citric acid cycle and the glyoxylate bypass in Escherichia coli”. 《Biochem Soc Symp.》 54: 17–31. PMID 3332993.
- ↑ Escher CL, Widmer F (1997). “Lipid mobilization and gluconeogenesis in plants: do glyoxylate cycle enzyme activities constitute a real cycle? A hypothesis”. 《Biol. Chem.》 378 (8): 803–813. PMID 9377475.
- ↑ Dubey, Mukesh K.; Broberg, Anders; Sooriyaarachchi, Sanjeewani; Ubhayasekera, Wimal; Jensen, Dan Funck; Karlsson, Magnus (September 2013). “The glyoxylate cycle is involved in pleotropic phenotypes, antagonism and induction of plant defence responses in the fungal biocontrol agent Trichoderma atroviride”. 《Fungal Genetics and Biology》. 58–59: 33–41. doi:10.1016/j.fgb.2013.06.008. ISSN 1087-1845. PMID 23850601.
- ↑ Zhu, Li-Wen; Li, Xiao-Hong; Zhang, Lei; Li, Hong-Mei; Liu, Jian-Hua; Yuan, Zhan-Peng; Chen, Tao; Tang, Ya-Jie (November 2013). “Activation of glyoxylate pathway without the activation of its related gene in succinate-producing engineered Escherichia coli”. 《Metabolic Engineering》 20: 9–19. doi:10.1016/j.ymben.2013.07.004. ISSN 1096-7176. PMID 23876414.
- ↑ 가 나 Belostotsky, Ruth; Pitt, James Jonathon; Frishberg, Yaacov (2012년 12월 1일). “Primary hyperoxaluria type III—a model for studying perturbations in glyoxylate metabolism”. 《Journal of Molecular Medicine》 90 (12): 1497–1504. doi:10.1007/s00109-012-0930-z. hdl:11343/220107. ISSN 0946-2716. PMID 22729392. S2CID 11549218.
- ↑ 가 나 Schnedler, Nina; Burckhardt, Gerhard; Burckhardt, Birgitta C. (March 2011). “Glyoxylate is a substrate of the sulfate-oxalate exchanger, sat-1, and increases its expression in HepG2 cells”. 《Journal of Hepatology》 54 (3): 513–520. doi:10.1016/j.jhep.2010.07.036. ISSN 0168-8278. PMID 21093948.
- ↑ “photorespiration”. 2017년 3월 9일에 확인함.
- ↑ 가 나 Peterhansel, Christoph; Horst, Ina; Niessen, Markus; Blume, Christian; Kebeish, Rashad; Kürkcüoglu, Sophia; Kreuzaler, Fritz (2010년 3월 23일). “Photorespiration”. 《The Arabidopsis Book / American Society of Plant Biologists》 8: e0130. doi:10.1199/tab.0130. ISSN 1543-8120. PMC 3244903. PMID 22303256.
- ↑ Zhang, Zhisheng; Mao, Xingxue; Ou, Juanying; Ye, Nenghui; Zhang, Jianhua; Peng, Xinxiang (January 2015). “Distinct photorespiratory reactions are preferentially catalyzed by glutamate:glyoxylate and serine:glyoxylate aminotransferases in rice”. 《Journal of Photochemistry and Photobiology B: Biology》 142: 110–117. doi:10.1016/j.jphotobiol.2014.11.009. ISSN 1011-1344. PMID 25528301.
- ↑ Blume, Christian; Behrens, Christof; Eubel, Holger; Braun, Hans-Peter; Peterhansel, Christoph (November 2013). “A possible role for the chloroplast pyruvate dehydrogenase complex in plant glycolate and glyoxylate metabolism”. 《Phytochemistry》 95: 168–176. doi:10.1016/j.phytochem.2013.07.009. ISSN 0031-9422. PMID 23916564.
- ↑ 가 나 Nikiforova, Victoria J.; Giesbertz, Pieter; Wiemer, Jan; Bethan, Bianca; Looser, Ralf; Liebenberg, Volker; Ruiz Noppinger, Patricia; Daniel, Hannelore; Rein, Dietrich (2014). “Glyoxylate, a New Marker Metabolite of Type 2 Diabetes”. 《Journal of Diabetes Research》 2014: 685204. doi:10.1155/2014/685204. ISSN 2314-6745. PMC 4265698. PMID 25525609.
- ↑ Nguyen, Dung V.; Shaw, Lynn C.; Grant, Maria B. (2012년 12월 21일). “Inflammation in the pathogenesis of microvascular complications in diabetes”. 《Frontiers in Endocrinology》 3: 170. doi:10.3389/fendo.2012.00170. ISSN 1664-2392. PMC 3527746. PMID 23267348.
- ↑ Piarulli, Francesco; Sartore, Giovanni; Lapolla, Annunziata (April 2013). “Glyco-oxidation and cardiovascular complications in type 2 diabetes: a clinical update”. 《Acta Diabetologica》 50 (2): 101–110. doi:10.1007/s00592-012-0412-3. ISSN 0940-5429. PMC 3634985. PMID 22763581.
- ↑ Fatiadi, Alexander; Schaffer, Robert (1974). “An Improved Procedure for Synthesis of DL-4-Hydroxy-3-methoxymandelic Acid (DL-"Vanillyl"-mandelic Acid, VMA)”. 《Journal of Research of the National Bureau of Standards Section A》 78A (3): 411–412. doi:10.6028/jres.078A.024. PMID 32189791.
- ↑ Kamlet, Jonas; Mathieson, Olin (1953). 《Manufacture of vanillin and its homologues U.S. Patent 2,640,083》 (PDF). U.S. Patent Office.
- ↑ R.A. Joshi (2006). 《Question Bank of Biochemistry》. New Age International. 64쪽. ISBN 978-81-224-1736-4.
- ↑ Eugene, Alexis J.; Xia, Sha-Sha; Guzman, Marcelo I. (2016). “Aqueous Photochemistry of Glyoxylic Acid”. 《J. Phys. Chem. A》 120 (21): 3817–3826. Bibcode:2016JPCA..120.3817E. doi:10.1021/acs.jpca.6b00225. PMID 27192089.

