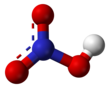
질산

| |||
| |||
| |||
| 이름 | |||
|---|---|---|---|
| IUPAC 이름
Nitric acid
| |||
| 별칭
Aqua fortis, Spirit of niter, Eau forte, Hydrogen nitrate, Acidum nitricum
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3DMet | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.832 | ||
| EC 번호 |
| ||
| 1576 | |||
| KEGG | |||
| MeSH | Nitric+acid | ||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 2031 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| HNO3 | |||
| 몰 질량 | 63.012 g·mol−1 | ||
| 겉보기 | Colorless, yellow or red fuming liquid[1] | ||
| 냄새 | acrid, suffocating[1] | ||
| 밀도 | 1.51 g cm−3, 1.41 g cm−3 [68% w/w] | ||
| 녹는점 | −42 °C (−44 °F; 231 K) | ||
| 끓는점 | 83 °C (181 °F; 356 K) 68% solution boils at 121 °C (250 °F; 394 K) | ||
| Completely miscible | |||
| log P | −0.13[2] | ||
| 증기 압력 | 48 mmHg (20 °C)[1] | ||
| 산성도 (pKa) | −1.4[3] | ||
| 짝염기 | Nitrate | ||
자화율 (χ)
|
−1.99×10−5 cm3/mol | ||
굴절률 (nD)
|
1.397 (16.5 °C) | ||
| 2.17 ± 0.02 D | |||
| 열화학 | |||
표준 몰 엔트로피 (S
|
146 J·mol−1·K−1[4] | ||
표준 생성 엔탈피 (ΔfH⦵298)
|
−207 kJ·mol−1[4] | ||
| 위험 | |||
| 물질 안전 보건 자료 | ICSC 0183 | ||
| GHS 그림문자 |  
| ||
| 신호어 | 위험 | ||
| H272, H300, H310, H330, H373, H411 | |||
| P210, P220, P260, P305+351+338, P310, P370+378 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | Non-flammable | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LC50 (median concentration)
|
138 ppm (rat, 30 min)[1] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용)
|
TWA 2 ppm (5 mg/m3)[1] | ||
REL (권장)
|
TWA 2 ppm (5 mg/m3) ST 4 ppm (10 mg/m3)[1] | ||
IDLH (직접적 위험)
|
25 ppm[1] | ||
| 관련 화합물 | |||
다른 음이온
|
Nitrous acid | ||
다른 양이온
|
Sodium nitrate Potassium nitrate Ammonium nitrate | ||
관련 화합물
|
Dinitrogen pentoxide | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
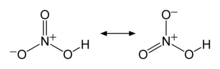
질산(窒酸, HNO3)은 무색의 액체로, 부식성과 발연성이 있는 대표적인 강산이다. 유기 화합물의 나이트로화에 쓰인다. 수용액 상에서 질산의 비율이 86%를 넘을 경우 발연질산(發煙窒酸)이라고 부른다.
화학적 특성[편집]
순수한 질산은 무색을 띠나 자외선을 쪼이면 서서히 분해되어 황갈색의 이산화질소(NO2)가 되므로, 햇빛이 잘 스며들지 않는 갈색 용기에 넣어 보관한다.
- 4 HNO3 + hv(자외선) → 4 NO2 (g) + 2 H2O + O2
금속과의 반응[편집]
금속과 반응하면 수소 기체(H2)와 질산염(NO3-)을 형성한다.
마그네슘과의 반응[편집]
- Mg + 2 HNO3 → 2 Mg(NO3)2 + H2 (g)
망가니즈와의 반응[편집]
- Mn + 2 HNO3 → 2 Mn(NO3)2 + H2 (g)
구리와의 반응[편집]
- 3 Cu + 8 HNO3 → 3 Cu2+ + 2 NO + 4 H2O + 6 NO3-
제법[편집]
실험실에서는 질산 나트륨이나 초석(질산 칼륨)에 진한 황산을 가한 뒤 가열하여 얻는다.
- 2 NaNO3 + H2SO4 → 2HNO3 + Na2SO4
- 2 KNO3 + H2SO4 → 2HNO3 + K2SO4
공업적으로는 암모니아를 백금 촉매와 함께 산화시킨 후 물과 반응시켜 얻는다(오스트발트법 또는 암모니아 산화법).
- 4NH3 + 5O2 → 4NO + 6H2O
- 2NO + O2 → 2NO2
- 3NO2 + H2O → 2HNO3 + NO
역사[편집]
질산은 익명의 유럽 연금술사의 De Inventione Veritatis에서 처음 언급되었다. 여기서 초석, 백반, 청색 비트리올(황산 구리(II))의 혼합물을 하소하여 얻는다고 되어 있다. 다시 13세기에는 알베르투스 마그누스가 초석과 흙을 가열함으로써 이를 마련한 뒤, 이것을 강수라고 부른 라몬 유이(Ramon Lull)가 이를 다시 언급하였다.[5]
글로버(Glauber)는 진한 황산을 초석과 함께 가열함으로써 오늘날에 쓰이는 질산을 얻는 과정을 고안하였다. 여기에 산소가 포함되어 있음을 증명한 앙투안 라부아지에가 1776년에 결정한 것이 실체였고 1785년 헨리 캐번디시가 이에 대한 구성을 결정하여 습기찬 공기를 통해 전기 불꽃을 내보내며 합성하는 것을 입증하였다.[5]
또한 질산은 구리나 은과도 반응할 정도로 산화력이 강하다는 점을 유용하게 써서 에칭과 같은 기법을 만들었지만, 이것이 악용되어 김영삼 질산테러 사건과 같은 테러에 쓰이기도 했다. 질산은 햇빛에 의해 분해 되므로 갈색병에 보관한다.
각주[편집]
- ↑ 가 나 다 라 마 바 사 NIOSH Pocket Guide to Chemical Hazards. “#0447”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ “nitric acid_msds”.
- ↑ Bell, R. P. (1973), 《The Proton in Chemistry》 2판, Ithaca, NY: Cornell University Press
- ↑ 가 나 Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A22쪽. ISBN 978-0-618-94690-7.
- ↑ 가 나 “Encyclopedia Britannica 1911 edition, Nitric Acid”. 2010년 12월 3일에 원본 문서에서 보존된 문서. 2010년 7월 24일에 확인함.
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |