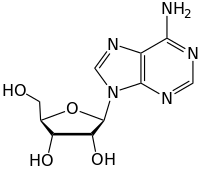
뉴클레오사이드
뉴클레오사이드(영어: nucleoside)는 뉴클레오타이드에서 인산기를 제외한 부분으로 간주되는 글리코실아민이다. 뉴클레오사이드는 핵염기(질소 염기로도 지칭됨)와 5탄당(리보스 또는 디옥시리보스)으로 구성되는 반면, 뉴클레오타이드는 핵염기, 5탄당, 한 개 이상의 인산기로 구성된다. 뉴클레오사이드에서 5탄당의 아노머 탄소는 글리코사이드 결합을 통해 퓨린 염기의 9번 질소 또는 피리미딘 염기의 1번 질소와 결합되어 있다. 뉴클레오사이드의 예로는 아데노신, 구아노신, 사이티딘, 유리딘, 디옥시티미딘, 이노신 등이 있다.[1]
뉴클레오사이드는 핵염기와 5탄당이 연결되어 있고, 뉴클레오타이드는 뉴클레오사이드와 한 개 이상의 인산기로 구성되어 있다. 따라서 뉴클레오사이드에서 5탄당의 5' 탄소의 하이드록실기는 세포의 특정 키네이스에 의해 인산화되어 뉴클레오타이드를 생성할 수 있다. 뉴클레오타이드는 DNA와 RNA를 구성하는 단위체이다.
뉴클레오사이드 및 해당하는 핵염기의 목록[편집]
다음의 표는 뉴클레오사이드(리보뉴클레오사이드 및 디옥시리보뉴클레오사이드)와 이에 해당하는 핵염기들이다.
핵염기 리보뉴클레오사이드 디옥시리보뉴클레오사이드 
아데닌

아데노신
A
디옥시아데노신
dA
구아닌

구아노신
G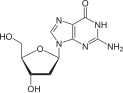
디옥시구아노신
dG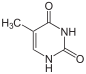
티민
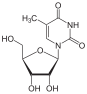
5-메틸유리딘
m5U
디옥시티미딘
dT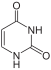
유라실

유리딘
U
디옥시유리딘
dU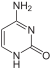
사이토신
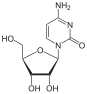
사이티딘
C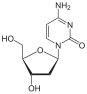
디옥시사이티딘
dC
공급원[편집]
뉴클레오사이드는 특히 간에서 신생합성 경로에 의해 생성될 수 있지만, 뉴클레오사이드는 식이에서 핵산의 섭취 및 소화를 통해 흡수된 다음 뉴클레오타이데이스에 의해 뉴클레오타이드를(디옥시티미딘 일인산과 같은)를 뉴클레오사이드(디옥시티미딘과 같은)와 인산으로 분해되어 더욱 풍부하게 공급될 수 있다. 이어서 뉴클레오사이드는 소화계의 내강에서 뉴클레오사이데이스에 의해 핵염기와 5탄당(리보스 또는 디옥시리보스)로 분해된다. 또한, 뉴클레오타이드는 세포에서 핵염기 및 리보스 1-인산 또는 디옥시리보스 1-인산으로 분해될 수 있다.
의학 및 기술에서의 이용[편집]
의학에서 몇 가지 뉴클레오사이드 유사체는 항바이러스제 또는 항암제로 사용된다.[2][3] 바이러스의 중합효소는 이들 화합물을 비주요 염기와 통합시킨다. 이들 화합물은 뉴클레오타이드로 전환됨으로써 세포에서 활성화된다. 하전된 뉴클레오타이드는 세포막을 쉽게 통과할 수 없기 때문에 뉴클레오사이드의 형태로 투여된다.
분자생물학에서 당 골격의 여러 유사체들이 존재한다. 가수분해되기 쉬운 RNA의 낮은 안정성으로 인해, RNA에 올바르게 결합하는 보다 안정된 몇 가지 대체 뉴클레오사이드/뉴클레오타이드 유사체들이 사용된다. 이것은 다른 당 골격을 사용하여 달성된다. 이들 유사체는 LNA, 모르폴리노, PNA를 포함한다.
DNA 염기서열 분석에서 다이디옥시뉴클레오타이드가 사용된다. 다이디옥시뉴클레오타이드는 3' 하이드록실기(인산기와 결합함)이 결여된 비주요 당인 다이디옥시리보스를 가지고 있다. 따라서 DNA 중합효소가 정상적인 디옥시리보뉴클레오타이드와 다이디옥시리보뉴클레오타이드를 구별할 수 없기 때문에 합성 중인 DNA 가닥에 다이디옥시리보뉴클레오타이드가 삽입될 경우 DNA 가닥의 합성이 중단된다.
핵염기와 리보스의 생물 발생 이전의 축합[편집]
생명이 어떻게 생겨났는지를 이해하려면 그럴듯한 생물 발생 이전 조건에서 생명의 핵심 구성 요소들을 형성할 수 있는 화학적 경로에 대한 지식이 필요하다. RNA 세계 가설에 따르면 자유 부동(浮動) 리보뉴클레오타이드는 원시 수프에 존재했었다. 이들은 직렬로 결합해서 RNA를 형성하는 기본 분자였다. RNA처럼 복잡한 분자는 반응성이 물리화학적 과정에 의해 지배되는 작은 분자로부터 생성되었음이 틀림없다. RNA는 퓨린 뉴클레오타이드와 피리미딘 뉴클레오타이드로 구성되며, 둘 다 신뢰할 수 있는 정보 전달, 따라서 다윈의 자연선택과 진화에 필요하다. 남(Nam) 등[4]은 RNA 형성으로 이어지는 핵심 단계인 미세 물방울에서 핵염기와 리보스의 직접적인 축합에 의해 리보뉴클레오사이드가 생성되는 것을 입증했다. 벡커(Becker) 등은 습식-건식 사이클을 사용하여 유사한 결과를 얻어냈다.[5]
같이 보기[편집]
각주[편집]
- ↑ Nelson, David L.; Cox, Michael M. (2005), Principles of Biochemistry (4th ed.), New York: W. H. Freeman, ISBN 0-7167-4339-6
- ↑ Galmarini, Carlos M.; MacKey, John R.; Dumontet, Charles (2002). “Nucleoside analogues and nucleobases in cancer treatment”. 《The Lancet Oncology》 3 (7): 415–424. doi:10.1016/S1470-2045(02)00788-X. PMID 12142171.
- ↑ Jordheim, Lars Petter; Durantel, David; Zoulim, Fabien; Dumontet, Charles (2013). “Advances in the development of nucleoside and nucleotide analogues for cancer and viral diseases”. 《Nature Reviews Drug Discovery》 12 (6): 447–464. doi:10.1038/nrd4010. PMID 23722347. S2CID 39842610.
- ↑ Nam I, Nam HG, Zare RN. Abiotic synthesis of purine and pyrimidine ribonucleosides in aqueous microdroplets. Proc Natl Acad Sci U S A. 2018 Jan 2;115(1):36-40. doi: 10.1073/pnas.1718559115. Epub 2017 Dec 18. PMID: 29255025; PMCID: PMC5776833
- ↑ Becker S, Feldmann J, Wiedemann S, Okamura H, Schneider C, Iwan K, Crisp A, Rossa M, Amatov T, Carell T. Unified prebiotically plausible synthesis of pyrimidine and purine RNA ribonucleotides. Science. 2019 Oct 4;366(6461):76-82. doi: 10.1126/science.aax2747. PMID: 31604305.