보어 모형

보어 모형(Bohr model)은 원자의 구조를 마치 태양계처럼 양전하를 띤 조그만 원자핵 주위를 전자들이 원형 궤도를 따라 돌고 있는 것으로 묘사하는 원자 모형이다. 태양계에서 태양이 중력으로 행성들을 끌어당기듯이, 보어 모형의 원자핵은 전자기력으로 전자들을 끌어당긴다. 이는 과거의 건포도 푸딩 모형(1904년)이나 토성 모형(1904년) 및 러더퍼드 모형(1911년)보다 발전한 것이었다. 보어 모형은 러더퍼드 모형을 양자역학에 근거하여 수정한 것이므로, 많은 책에서 이 둘을 합쳐서 러더퍼드-보어 모형이라고 부르기도 한다.
닐스 보어가 1913년에 도입한 보어 모형은 수소 원자의 방출선에 대한 뤼드베리 공식을 설명하는 데 성공하면서 과학계에서 지지를 얻었다. 그때까지 뤼드베리 공식은 실험적으로는 성립한다는 것이 알려져 있었지만 그 이유에 대해서는 설명할 방법이 없었기 때문이다. 보어 모형은 나중에 양자역학이 발전하면서 보다 정확한 모형(원자가 껍질)으로 대체되었으나, 간단하며 특수한 경우에 대해서는 정확한 결과를 준다는 장점으로 인해 양자역학을 처음 배우는 학생들에게 널리 가르쳐지고 있다. 아더 에리히 하스는 1910년에 보어 모형과 유사한 모형을 제시했으나 그다지 알려지지 않았다.
기원 및 역사[편집]
20세기 초에, 어니스트 러더퍼드에 의한 실험은 조그마하고 빽빽하며, 양전하를 띈 핵 주위를 감싸는 음전하의 전자 구름으로 이루어진 원자의 개념을 정립하였다.[1] 이 실험 데이터를 바탕으로, 러더퍼드는 태양계-모델의 원자 모형을 1911년에 생각해 내었지만, 그 태양계 모델에는 기술적인 문제가 존재하였다. 고전 물리학의 법칙들은 전자가 핵 주위를 공전하면서 전자기 복사를 방출할 것이라고 예측하였다. 위 과정에 따르면 전자는 에너지를 잃고 급속히 안쪽으로 말려들어올 것이고 대략 16피코초 전후로 핵에 충돌하게 되고[2] 모든 원자들이 매우 불안정한 상태가 된다는 오류가 발생한다.[3] 또한, 전자 궤도가 말려들어옴에 따라 궤도가 더 작아지고 공전주기가 빨라져 연속적으로 증가하는 진동수의 전자기 복사를 생성할 것으로 예측되었다. 그러나, 19세기 말에 이루어졌던 전기 방전 실험은 원자가 이산적으로 오직 특정한 주파수에서만 전자기파 복사를 방출한다는 것을 보였다.
이러한 한계를 극복하기 위해서, 닐스 보어는 1913년에 전자가 고전적으로 오직 특정한 움직임만 가질 수 있다고 가정했고 현재 보어의 원자모형으로 불리는 모형을 제시했다.
- 원자의 전자는 핵을 중심으로 공전한다. 전자와 원자핵과의 전기적인 인력이 구심력 역할을 하여 전자는 원자핵 주위를 원운동한다.
- 전자는 핵으로부터 이산적으로 떨어진, 오직 특정한 궤도(정상상태-전자가 특정한 에너지와 반지름을 갖는 궤도에서 등속원운동하는 상태)들에서는 전자기 복사를 방출하지 않으며 안정적으로 공전한다. 이 궤도들은 무한한 에너지 값과 관련이 있으며 에너지 껍질 혹은 에너지 준위라고 불리기도 한다. 이 궤도들에서, 전자의 가속은 고전 전자기학에 따라 복사나 에너지 손실을 야기하지 않는다. 보어 모델은 플랑크의 양자론에 기초한다.
- 전자는 오직 한 궤도에서 다른 궤도로 전이하면서만 에너지를 흡수하거나 방출할 수 있다. ν의 주파수를 가진 흡수, 방출 진동수는 의 플랑크-아인슈타인 관계식으로 기술된다.여기서 h는 플랑크 상수이다. 주기 T를 가진 궤도에서 방출하는 복사의 주파수는 로 고전 역학 주기운동에서의 주파수와 같다.
보어 모델의 중요성은 전자의 움직임을 설명하는데 고전역학의 양자조건을 도입했다는 것이다. 복사 과정은 서로 다른 주기를 가진 두 궤도를 포함하기에 작은 궤도에 대해 3번 규칙이 잘 정의되지 않았지만 보어는 3번 규칙과 양자 규칙 : 각 운동량 L은 일정한 단위의 정수배를 가질 수 밖에 없다.를 이용하여 준위간의 에너지 간격을 계산해냈다.:
N = 1, 2, 3, … 은 주 양자수라고 불리며, h bar는 h/2pi이다. N의 최솟값은 1이다. 이는 존재할 수 있는 가장 작은 궤도 반지름, 0.0529 nm를 나타내며, 보어 반지름이라고도 한다. 전자가 가장 낮은 궤도에 존재한다면, 더 이상 양성자를 향해 다가갈 수는 없다. 보어는 각 운동량 양자 규칙으로부터 수소 원자, 수소-유사 원자, 이온들의 가능한 에너지 준위들을 계산하였다.
다른 점들은:
- 아인슈타인의 광전효과처럼, 보어의 공식 또한 양자 전이시 에너지가 이산적으로 방출된다고 가정한다. 그러나, 아인슈타인과는 달리 보어는 고전적인 맥스웰 전자기 이론을 고수하였다. 보어는 광자의 존재를 믿지 않았고 전자기장의 양자화는 원자 에너지 준위의 불연속성으로 설명되었다.[4][5]
- 맥스웰 이론에 따르면, 고전적 복사의 진동수는 궤도에서 정상파를 이루는 전자의 공전 진동수와 같다. 이 결과는 보어 모델에서, n보다 k가 매우 작을 때 En과 En-k 준위 사이의 전이에서 얻어졌다. 이 전이는 n오비탈의 k번 조화 모드를 생성한다. 충분히 큰 n의 값에 대해(뤼드베리 상태라고 불린다.) 전이 과정에서 관련된 두 궤도는 거의 비슷한 공전 진동수를 가져, 고전적인 궤도 진동수가 결정된다. 그러나 작은 n(혹은 큰 K)에 대해서는, 복사 현상을 고전적인 설명으로는 해석할 수 없다. 이것은 양자 이론의 탄생을 알리며, 오직 거시적인 세계에서만 고전 이론이 양자 이론과 비슷하다는 것을 알린다.
- 보어-크래머-슬래이터 이론은 보어 모델을 확장시키는데 실패하였는데, 이는 양자 전이시 에너지 보존과 운동량 보존법칙이 위배되기 때문이다.
각운동량이 h bar의 정수배여야 한다는 보어의 조건은 1924년에 드 브로이에 의해 정립파 조건으로 다시 재해석된다 : 전자는 파동으로 묘사되고, 전자 궤도의 둘레는 파장 길이에 의해 나누어떨어진다.:
λ = h/p라는 드 브로이의 물질파로부터 보어의 규칙을 도출해 낼 수 있다. 그러나, 1913년에 보어는 그의 모델을 파동적 해석을 통해 밝히지 않고 정당화시켰다. 1913년 당시에는, 전자와 같은 입자가 파동과 같이 행동할 수 있다는 가능성이 제기되지 않았다. 1925년에, 새로운 종류의 역학인 양자역학이 제시되었다. 양자화된 전자가 움직이는 보어의 모델이 양자 역학을 통해 조금 더 정확한 모델로 확장될 수 있었다. 이 새 이론은 하이젠버그에 의해 제시되었고, 똑같은 이론의 다른 형태인 파동 역학이 오스트리아 출신의 물리학자 슈뢰딩거의 독립적인 연구 과정을 통해 확립되었다. 슈뢰딩거는 드 브로이의 물질파 이론을 도입하였으나, 양전하의 핵 전하 때문에 전자의 움직임을 묘사하는 3차원의 파동 방정식은 수소-유사 원자들에 대해서만 한정되었다.
전자의 에너지 준위[편집]
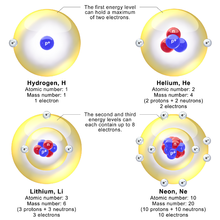
보어의 원자 모형은 두 개의 전하된 지점들이 빛 보다 훨씬 느린 속도로 궤도를 도는 시스템에서만 정확한 결과를 줄 수 있다. 이는 수소 원자모델, 헬륨이온, 리튬 이온과같이 하나의 전자 시스템을 포함할 뿐만 아니라 포지트로늄(양전자와 전자가 정전기력인력으로 인해 결합된 준안정화된 상태)과 어떤 원자의 뤼드베리 상태(하나의 전자가 다른 모든 전자들로부터 멀리 떨어진 상태)를 포함한다.
궤도를 계산하기 위해서는 두 가지 가정을 필요로 한다.
- 고전 역학
- 전자는 정전기력 인력에 의해 원 궤도에 붙잡혀있다. 여기서 전자에 가해지는 구심력은 쿨롱힘과 같다.
- 위 식에서 me는 전자의 질량, e는 전자의 전하량, ke는 쿨롱상수 그리고 Z는 원자의 원자번호이다. 위 식에서 핵의 질량은 전자의 질량보다 훨씬 크다고 가정되었다. 이 방정식은 모든 반지름에서의 전자의 속도를 결정한다.:
- 또한 이 식은 모든 반지름에서 전자의 총 에너지(역학적 에너지)를 결정한다.
- 위 식에서 역학적 에너지는 음의 부호이고 반지름 r에 반비례한다. 이는 궤도를 도는 전자를 양성자로부터 떨어뜨리는데 에너지가 필요함을 의미한다. 무한한 r값에 대하여 에너지는 0인데, 이는 양성자로부터 무한히 먼 정지한 전자의 에너지와 대응된다. 실제로 어떤 하나의 원자 시스템에서 전자는 원자핵으로 멀리 떨어질수록 원자핵에 의한 영향력이 감소하여 운동에너지가 감소하게 된다.
- 역학적 에너지는 위치 에너지의 절반인데, 이는 비리얼 정리에 의해 원이 아닌 궤도에서도 역시 적용된다.
(이때 비리얼 정리는 운동에너지(KE)와 위치에너지(PE)를 관련시켜주는 이론이다. 천체가 수축 또는 팽창하지 않는 안정한 상태에 있다고 가정할 때, KE와 PE의 관계식은 2<KE>=-<PE>로 나타내 지고 이에 따라 은하계 전체에너지(TE)=KE+PE를 달리 표현하면 TE=-KE=1/2PE 로 나타낼 수 있다.)
- 양자 역학
- 각운동량 L = mevr 은 ħ 의 정수 곱이다.:
- 속도의 대체하는 표현은 n에 관한 r의 방정식을 제공한다.:
- 그래서 어떠한 n에 대한 허용된 궤도 반지름은 다음과 같다.:
- 가장 작은 가능한 수소 원자에서의 r의 값은 보어 반지름이라고 불리며 이는 다음과 동일한 값을 가진다.:
- 어떤 원자에서의 n-th 상태에서의 에너지는 반지름과 양자 수에 의해 결정된다.:
그러므로 수소의 가장 작은 에너지 수준에서 전자는 약 -13.6eV를 가진다. 이는 원자핵으로부터 무한히 떨어진 움직이지 않는 전자보다 덜한 에너지이다. 그 다음의 에너지는 -3.4eV이다. 세 번째는 -1.51eV이다. 등등… 더 큰 n의 값이 대해서, 이것은 그 원자의 나머지 부분 주변의 큰 원 궤도에서 하나의 전자를 가진 매우 흥분된 원자의 구속된 에너지이다.
에너지 공식에서 자연 상수의 조합은 뤼드베리 energy라고 불린다.(RE):
이러한 표현은 더 자연적인 단위를 형성하는 조합에서 그것을 해석함으로써 명확해진다.
- 은 전자의 rest mass energy이다. (511 keV)
- 은 미세구조상수이다.
이러한 어원은 하나의 전자에 의해 원자핵이 궤도화되는 가정을 가지고 있기 때문에, 우리는 원자핵이 전하량 q = Z e를 가지게 함으로써 이러한 결론을 일반화 시킬 수 있다. 이 때, Z는 원자번호이다. 이것은 우리에게 수소 원자에서의 에너지 수준을 제공해줄 것인데, 실제 에너지 수준의 대략적인 크기의 정도 근사치로서 작용할 수 있다. 그래서 Z전하의 양성자를 가진 원자핵에 대하여, 그 에너지 수준은 다음과 같다.:
실제 에너지 수준은 하나의 전자보다 더 많은 전자를 가진 시스템에서는 분석적으로 풀리지 않는다. 왜냐하면 그 전자는 원자핵에 의해 영향을 받을 뿐만 아니라 쿨롱힘을 통해 다른 전자들과도 상호작용하기 때문이다. 만약 그것들이 안정했다면, 충분히 큰 원자핵은 무한대에서 양전자(모든 입자들은 자신의 반입자를 가지고 있는데, 이 때 양전자는 전자의 반입자이다. 이 반입자들은 자신의 입자를 만나면 에너지를 방출하면서 쌍소멸하게 되고, 이들은 질량은 같지만 서로 다른 전하를 띠게 된다.)를 빼내면서, 빈공간으로부터 구속 전자를 형성함으로써 그들의 전하를 감소시켰을 것이다.
이러한 사실은 보어의 모델의 중요성에 대해 러더퍼드를 확신시킴에 따라 역사적으로 중요하다. 왜냐하면 그것은 단일 이온 헬륨에 대한 스펙트럼들에서 선들의 진동수가 정확히 4의 비율(양)에 의해 수소와 다른 것이 아니라 오히려 수소 대 헬륨 시스템에 대한 감소된 질량의 4배의 비율에 의해 수소의 그것들과 다르다는 사실을 설명했기 때문이다. 포지트로늄(Positronium)에 있어서, 방정식은 감소된 질량을 역시 사용하지만, 이러한 경우에, 이것은 정확히 그 전자의 질량이 절반이 된다. 어떠한 반지름 값에 있어서, 전자와 양전자는 각각 그들의 공통 질량 중심 주위를 절반 속도로 운동하고 있고, 각각은 오직 1/4의 운동에너지를 가진다. 역학적 에너지는 무거운 원자핵 주위를 운동하는 단일 전자들에 대한 것의 절반이다.
- (positronium)
| ※ 보어의 가설을 이용해 수소원자 모델에서의 에너지(E), 반지름(r), 속도(v) 구하기 |
|---|
|
먼저, 보어의 수소원자모델에서의 세가지 전제에 대해서 살펴보자.
위 세가지 전제를 이용하여 에너지(E), 반지름(r), 속도(v)를 각각 구하는 과정은 다음과 같다. 1번의 식을 속도 v에 관하여 정리하면, - ㉠ 이 된다. 또한 2번의 식을 r에 관하여 정리하면, - ㉡ 이 된다. 위 과정을 통해서 구한 ㉠과 ㉡에 대하여, ㉠을 ㉡에 대입하면 다음과 같이 반지름 r을 얻을 수 있다. ∴ ⇔ 0.53 Å (단, 0.53 Å은 보어 반지름이다.) 그리고 나서, 앞에서 구한 반지름 r을 ㉠에 대입하면 다음과 같이 속도 v를 얻을 수 있다. ∴ (단, c는 광속) 최종적으로, 앞에서 구한 반지름 r과 속도 v를 3번의 식에 대입하면 에너지 E를 얻을 수 있다. ∴ |
뤼드베리 공식[편집]
뤼드베리 공식은 보어 공식 이전에 경험적으로 잘 알려진 공식으로, 보어의 이론을 통해 오비탈 간 에너지 수준 사이에 일어나는 양자 도약 또는 에너지의 전이를 설명할 수 있다. 보어의 공식은 플랑크 상수와 전자의 전하를 포함하여 이미 잘 알려지고 측정된 자연상수들로 리드베리 상수를 표현할 수 있기 때문에 수적 수치를 제공해 준다. 전자가 그것의 원래 에너지 상태에서 더 높은 에너지 상태로 이동하고 다시 원래 상태로 돌아올 때까지 각 상태로 도약을 하는데, 이 때 양자가 방출된다. 수소의 다른 에너지 상태에 대해 이끌어진 공식을 사용하면서 수소 원자가 방출할 수 있는 빛의 파장이 결정된다. 수소 원자에 의해 방출된 양자의 에너지는 두 수소 원자의 에너지 상태의 차이에 의해 주어진다.
여기서 nf는 나중 에너지 준위, ni는 처음 에너지 준위이다.
양자의 에너지 상태는 다음과 같다.
위에 따라 발해지는 양자의 파장은 다음과 같이 주어진다.
이것은 리드베리 공식으로 알려져있고, 리드베리 상수 R은 자연 상태에서 R is 또는 이다. 이러한 공식은 19세기 분광학 연구 과학자에게 잘 알려져 있었다. 그러나 이러한 형태에 대해 이론적이지 않은 설명 또는 보어까지 R의 수치에 대한 이론적이지 않은 예측이 있었다. 사실, 라이먼, 발머, 파셴 계열의 실험적으로 관찰된 스펙트럼의 선과 함께 보어 공식의 수반되는 동의 그리고 아직 관측되지 않은 다른 선들의 성공적인 이론적 예측 뿐만 아니라, 보어의 리드베리 상수의 어원은 그의 모델이 즉시 받아들여지는 하나의 이유였다. 한 전자보다 더 많은 전자를 가진 원자에 적용하기 위해, 리드베리 공식은 Z를 Z-b로 혹은 n을 n-b로 대체함으로써 수정될 수 있는데, 여기서 b는 다른 전자들과 내부 전자에 의한 screening 효과를 표현한 것이다. 이것은 보어가 그의 모델을 제시하기 전에 경험적으로 확립되었다.
| ※ 뤼드베리공식과 리드베리 상수 |
|---|
| 뤼드베리 공식과 리드베리 상수를 구하기 위해 전자가 임의의 양자수 nf에서 ni 로 전이 된다고 가정하자.
(단, 에너지 준위는 nf > ni) nf에서 ni 로 전자가 전이될 때, hν(단, ν는 진동수)만큼의 에너지가 방출된다. 즉, 에너지 보존 법칙에 의해 Ef = Ei + hν이다. (단, Ef는 nf에서의 에너지, Ei는 ni에서의 에너지이다.) 따라서 앞서 보어의 가설을 통해 수소원자모델에서의 E에 관한 식을 유도한 것을 바탕으로 위 식을 다음과 같이 나타낼 수 있다.
위 뤼드베리 공식에서 이 리드베리 상수(R)가 된다. ※ 뤼드베리 상수(R) vs 뤼드베리 유닛(Ry 또는 1뤼드베리) 두 가지는 서로 다른 의미를 가지고 있음에 유의하자. 리드베리 상수는 위의 뤼드베리 공식인 에 들어있는 R값(= )으로 단위는 이다. 이 값은 리드베리가 실험과정을 통해 얻은 계산치였는데 보어는 자신의 가설을 통해 이를 이미 알려진 상수들을 통해 표현하였다. 반면, 리드베리 유닛(Ry 또는 1뤼드베리)은 보어의 가설을 통해 계산한 수소 원자에서 전자가 지닌 에너지값 즉, 에서 n=1인 경우 즉, 가장 안정한 상태 의 에너지 값을 의미한다. 따라서 단위는 J(joule)이 된다.(단, eV 역시 에너지 단위 J 과 같다.) |
무거운 원자의 껍질 모델[편집]
보어는 무거운 원자들에 대한 대략적인 모델을 제공하기 위해 수소의 원자 모델을 확장시켰다. 이것은 많은 잘 알려진 원자의 특성(성질)을 재현하는 물리학의 상황을 제공했다. 무거운 원자들은 원자핵 안에 많은 양성자를 가지고, 그 전하를 상쇄시키기 위한 더 많은 전자들을 가진다.
보어의 생각은 각 별개의 궤도가 오직 특정한 전자의 수만을 붙잡을 수 있다는 것이다. 그 궤도가 다 채워지고 난 후, 그 다음 궤도가 사용된다. 이것은 그 원자가 껍질 구조를 가진다는 것인데, 각 껍질은 보어의 궤도에 상응한다. 이러한 모델은 심지어 수소의 모델보다 훨씬 더 대략적이다. 왜냐하면 그것은 상호 연관성이 없는 것으로 각 껍질 내 전자들을 취급하기 때문이다. 그러나 전자들 간의 반발은 가리움 효과에 의해 어떻게든 설명된다.
바깥 궤도에 있는 전자들은 원자핵 궤도를 돌 뿐만 아니라, 그것들은 내부 전자 주변을 운동한다, 그래서 그들이 느끼는 실질적인 전하 Z는 내부 궤도의 전자들의 수에 의해 감소된다. 예를 들어, 리튬 원자는 가장 낮은 1s 오비탈에 2개의 전자를 가지고, Z=2에서 이러한 오비탈을 가진다. 각각 하나는 Z=3의 핵 전하가 다른 전자들의 가리움 효과를 상쇄시키는 것을 보여주는데, 이는 노골적으로 말하면 약 1단위의 핵 전하를 감소시킨다. 이것은 가장 안쪽의 전자들이 대략 보어 반지름의 1/4만큼의 궤도를 돌고 있는 것을 의미한다. 리튬에서 가장 바깥쪽 전자는 대략 Z=1에서 궤도운동을 하는데, 이는 두 내부 전자들이 약 2정도의 핵 전하를 감소시키기 때문이다. 이러한 바깥 전자는 원자핵으로부터 거의 1보어 반지름 거리에 존재해야만 한다. 왜냐하면 그 전자들은 강하게 서로 격퇴하고, 실질적인 전하 기술은 매우 대략적이기 때문이다; 실질적인 전하Z는 대개 하나의 정수로 표현되지 않는다.
그러나 모즐리의 법칙은 실험적으로 가장 안쪽 전자쌍들을 조사하고, 그들이 대략적으로 Z-1의 핵 전하를 보일 수 있음을 보였다. 반면에, 가장 바깥 껍질에 오직 하나의 전자를 가진 원자나 이온에서 가장 바깥쪽 전자는 Z-k라는 실질적인 전하를 가지는 속 궤도를 회전하는데, 이 때 k는 내부 껍질에 있는 전자들의 전체 수이다.
껍질 모델은 19세기 후반까지 원소 주기율표 상에서 암호화되어 있던 많은 미궁 속에 있는 원자의 특성들을 질적으로 설명해줄 수 있다. 원자의 크기라는 하나의 특성은 대략적으로 순수한 결정형 고체의 밀도와 기체의 속도를 측정함으로써 결정될 수 있다. 원자들은 주기율표 상에서 오른쪽으로 갈수록 더 작아지려는 경향이 있고, 다음 주기로 갈수록 더 커지려는 경향이 있다. 주기율표의 오른쪽에 있는 원자들은 전자를 얻으려는 경향이 있는 반면, 왼쪽에 있는 원자들은 그것들을 잃어버리려는 경향이 있다. 주기율표의 마지막 족의 원소들은 화학적으로 불활성기체들이다.
껍질 모델에서, 이러한 현상은 껍질 채움에 의해 설명된다. 왜냐하면 그들은 그 궤도가 다 찰 때까지 같은 크기의 궤도를 채우고 있기 때문인데, 이는 주기율표 상에서 그 다음 원자가 전자 간의 반발력에 의해 그것이 팽창됨을 야기함에 따라 바깥 전자를 느슨히 구속하고 있음을 의미한다. 첫 번째 보어 궤도는 그것이 두 개의 전자를 가질 때 가득 채워 지는데, 이는 왜 헬륨이 비활성인지를 설명한다. 두 번째 궤도는 8개의 전자를 수용하고, 그것이 꽉 채웠을 때 원자가 네온인데, 이 역시 비활성이다. 세 번째 궤도는 더 올바른 좀머펠트의 이론에서 여분의 d오비탈 전자가 있다는 것을 제외하고, 다시 8개를 포함한다. 세 번째 궤도는 아마 여분으로 10d 전자를 붙잡을지도 모르지만, 이러한 위치는 그 다음 궤도로부터 몇몇 더 많은 오비탈들이 채워질 때까지 전자들이 채워지지 못한다. 그 불규칙적인 채움 패턴은 전자들의 상호작용의 효과인데, 이것은 보어 또는 좀머펠트 원자모형으로는 설명되지 않고, 심지어 현재 다룸에 있어서도 계산하기 어렵다.
모즐리의 법칙과 K-alpha X-ray 방출선의 계산[편집]
닐스 보어는 1962에 “당신은 실제로 러더퍼드의 업적(원자핵)이 진지하게 받아들여지지 않았다고 본다. 우리는 오늘날 이해할 수는 없지만, 그것은 진지하게 전혀 받아들여지지 않는다. 그것이 어떤 위치에 있는지에 대한 언급이 없다. 그 큰 변화는 모즐리에서 왔다”고 말했다.[6] 1913년에 헨리 모즐리는 전자충돌에 영향을 받아 원자들에 의해 방출된 가장 강한 X-ray 선과 그들의 원자번호(양성자수) Z사이에 경험에 의한 관계를 발견하였다.
헨리 모즐리의 경험론적 공식은 요한네스 뤼드베리와 닐스 보어의 공식으로부터 유래됨에 따라 발견되었다. 여기에 두 가지의 가정이 추가되는데, 그것은 첫째, X-ray선이 양자수 1과 2의 에너지 준위 사이에서의 전이로부터 온다는 것과, 둘째, 수소보다 무거운 원자에 대한 방정식에서는 양성자수 Z가 고려되어야한다는 것이다. 이에 의해 뤼드베리와 보어의 공식에서 수소원자로 가정했을 때의 원자번호(양성자수)(Z)=1이 로 바뀌어야 한다는 것이다.
모즐리는 그의 결론에 대해 골치아파하며 보어에게 편지를 보냈다. 그러나 보어는 도와줄 수 없었다. 그 시대에, 그는 상정된 가장 안쪽의 전자의 K 껍질이 최소한 4개의 전자를 가져야 하며, 깔끔히 결론을 설명해왔던 2개의 전자를 가져서는 안된다 라는 것을 생각하였다. 그래서 모즐리는 이론적인 설명없이 그의 결론을 공표했다. 나중에, 그 효과가 사람들은 오직 2개 전자들을 포함하는 안쪽 궤도를 가진, 전하 가리움에 의해 야기됨을 알게 되었다. 실험에서, 원자에서 가장 안쪽 전자들 중 하나는 하나의 남아있는 전자를 포함하여, 가장 낮은 보어 궤도에서 빈공간을 남기면서, 힘이 약해진다. 그 때, 이러한 빈공간은 다음 궤도로부터의 전자들에 의해 가득 채워지는데, 이 때 그 다음궤도는 n=2이다. 그러나 n=2의 전자들은 Z-1의 실질적인 전하를 보이는데, 하나의 전자가 핵의 전하 +Z를 가리고 그것을 -1에 의해 낮추는 가장 낮은 보어 궤도에 남아있을 때, 이는 원자핵의 전하에 대한 적절한 값이다.
두 번째 껍질에서 첫 번째 껍질로 떨어짐에 따라 전자에 의해 얻어진 에너지는 K-alpha 선들에 대한 모즐리의 법칙을 제공한다.
또는
여기서, Rv = RE/h는 3.28 x 1015 Hz과 동일한 진동수의 관점에서 뤼드베리 상수이다. 11과 31사이에 Z값에 대하여, 이러한 후자의 관계()는 원자번호에 비교하여 X-ray진동수의 제곱근의 단순한(선형의) 구성에서 경험적으로 모즐리에 의해 이끌어졌다. 그것의 제한된 타당성에도 불구하고,[7] 모즐리의 법칙은 객관적인 원자번호의 의미를 성립시켰을뿐만 아니라, 보어가 말한 것처럼, 그것은 또한 원자핵 전하의 전체적인 단위에 대해 나타내는 원자번호를 가지고, 러더퍼드/반 덴 브루크/보어의 원자의 원자핵 모형의 타당성을 성립시킨 뤼드베리 어원보다도 더 타당하다.
같이 보기[편집]
- 프랑크-헤르츠 실험, 모즐리의 법칙 - 초기에 보어 모형에 대한 근거가 되었다.
- 비활성 쌍 효과 - 보어 모형을 이용하면 잘 설명된다.
- 라이먼 계열
- 발머 계열
- 슈뢰딩거 방정식
- 양자역학
각주[편집]
- ↑ Niels Bohr (1913). “On the Constitution of Atoms and Molecules, Part I” (PDF). 《Philosophical Magazine》 26 (151): 1–24. Bibcode:1913PMag...26....1B. doi:10.1080/14786441308634955.
- ↑ “Olsen and McDonald 2005” (PDF). 2019년 9월 9일에 원본 문서 (PDF)에서 보존된 문서. 2020년 11월 11일에 확인함.
- ↑ “CK12 – Chemistry Flexbook Second Edition – The Bohr Model of the Atom”. 2014년 9월 30일에 확인함.
- ↑ Stachel, John (2009). 〈Bohr and the Photon〉. 《Quantum Reality, Relativistic Causality, and Closing the Epistemic Circle》. Dordrecht: Springer. 79쪽.
- ↑ Louisa Gilder, "The Age of Entanglement" The Arguments 1922 p. 55, "Well, yes," says Bohr. "But I can hardly imagine it will involve light quanta. Look, even if Einstein had found an unassailable proof of their existence and would want to inform me by telegram, this telegram would only reach me because of the existence and reality of radio waves." 2009
- ↑ “Interview of Niels Bohr by Thomas S. Kuhn, Leon Rosenfeld, Erik Rudinger, and Aage Petersen”. Niels Bohr Library & Archives, American Institute of Physics. 1962년 10월 31일. 2019년 3월 27일에 확인함.
- ↑ M.A.B. Whitaker (1999). “The Bohr–Moseley synthesis and a simple model for atomic x-ray energies”. 《European Journal of Physics》 20 (3): 213–220. Bibcode:1999EJPh...20..213W. doi:10.1088/0143-0807/20/3/312.
참고 문헌[편집]
- Niels Bohr (1913). “On the Constitution of Atoms and Molecules, Part I” (PDF). 《Philosophical Magazine》 26 (151): 1–24. doi:10.1080/14786441308634955.
- Niels Bohr (1913). “On the Constitution of Atoms and Molecules, Part II Systems Containing Only a Single Nucleus” (PDF). 《Philosophical Magazine》 26 (153): 476–502. doi:10.1080/14786441308634993.
- Niels Bohr (1913). “On the Constitution of Atoms and Molecules, Part III Systems containing several nuclei”. 《Philosophical Magazine》 26: 857–875. doi:10.1080/14786441308635031.
- Niels Bohr (1914). “The spectra of helium and hydrogen”. 《Nature》 92 (2295): 231–232. Bibcode:1913Natur..92..231B. doi:10.1038/092231d0.
- Niels Bohr (1921). “Atomic Structure”. 《Nature》 107 (2682): 104–107. Bibcode:1921Natur.107..104B. doi:10.1038/107104a0.
- A. Einstein (1917). “Zum Quantensatz von Sommerfeld und Epstein”. 《Verhandlungen der Deutschen Physikalischen Gesellschaft》 19: 82–92. Reprinted in The Collected Papers of Albert Einstein, A. Engel translator, (1997) Princeton University Press, Princeton. 6 p. 434. (provides an elegant reformulation of the 보어–Sommerfeld quantization conditions, as well as an important insight into the quantization of non-integrable (chaotic) dynamical systems.)
더 읽어보기[편집]
- Linus Carl Pauling (1970). 〈Chapter 5-1〉. 《General Chemistry》 3판. San Francisco: W.H. Freeman & Co.
- Reprint: Linus Pauling (1988). 《General Chemistry》. New York: Dover Publications. ISBN 0-486-65622-5.
- George Gamow (1985). 〈Chapter 2〉. 《Thirty Years That Shook Physics》. Dover Publications.
- Walter J. Lehmann (1972). 〈Chapter 18〉. 《Atomic and Molecular Structure: the development of our concepts》. John Wiley and Sons.
- Paul Tipler and Ralph Llewellyn (2002). 《Modern Physics》 4판. W. H. Freeman. ISBN 0-7167-4345-0.
- Klaus Hentschel: Elektronenbahnen, Quantensprünge und Spektren, in: Charlotte Bigg & Jochen Hennig (eds.) Atombilder. Ikonografien des Atoms in Wissenschaft und Öffentlichkeit des 20. Jahrhunderts, Göttingen: Wallstein-Verlag 2009, pp. 51–61
- Steven and Susan Zumdahl (2010). 〈Chapter 7.4〉. 《Chemistry》 8판. Brooks/Cole. ISBN 978-0-495-82992-8.
- Helge Kragh (2011). “Conceptual objections to the Bohr atomic theory — do electrons have a "free will" ?”. 《European Physical Journal H》 36 (3): 327. Bibcode:2011EPJH...36..327K. doi:10.1140/epjh/e2011-20031-x.






































![{\displaystyle \nu ={Z^{2}e^{4}m_{\mathrm {e} } \over 8\varepsilon _{0}^{2}h^{3}}{[{1 \over n_{\mathrm {i} }^{2}}-{1 \over n_{\mathrm {f} }^{2}}]}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4222928d49804142f0347c421dc777b1a68e02b2)





