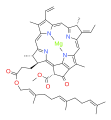
세균엽록소
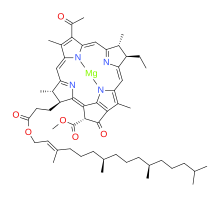
| |
| 이름 | |
|---|---|
| IUPAC 이름
[methyl (3S,4S,13R,14R,21R)-9-acetyl-14-ethyl-4,8,13,18-tetramethyl-20-oxo-3-(3-oxo-3-([(2E,7R,11R)-3,7,11,15-tetramethylhexadec-2-en-1-yl]oxy)propyl)-13,14-dihydrophorbine-21-carboxylatato(2−)-kappa4N23,N24,N25,N26]magnesium
| |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| KEGG | |
PubChem CID
|
|
| |
| |
| 성질 | |
| MgC 55H 74N 4O 6 | |
| 몰 질량 | 911.524 g·mol−1 |
| 겉보기 | 청록색 분말 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
세균엽록소(細菌葉綠素, 영어: bacteriochlorophyll, BChl)는 다양한 광영양 세균에서 생성되는 광합성 색소이다. 박테리오클로로필이라고도 한다. 세균엽록소는 1932년에 코르넬리스 베르나르두스 반 니엘에 의해 발견되었다. 세균엽록소는 식물, 조류, 남세균의 주요 색소인 엽록소와 관련이 있다.[1] 세균 엽록소를 함유한 생물체는 에너지 요구량을 유지하기 위해 광합성을 수행하지만, 그 과정은 산소 비발생성이며 부산물로 산소를 생성하지 않는다. 이들은 식물이나 남세균에 의해 흡수되지 않는 파장의 빛을 사용한다. Mg2+를 양성자(H+)로 대체하면 페오피틴 형태인 세균페오피틴(영어: bacteriochlorophyll, BPh)이 생성된다.
종류[편집]
세균엽록소의 주요 종류는 다음의 표와 같다.
| 색소 | 분류군 | 생체 내 적외선 흡수 최대값 (nm) |
|---|---|---|
| 세균엽록소 a | 홍색세균, 헬리오박테리아과, 녹색황세균, 녹만균류, 클로라시도박테리움속[2] | 805, 830–890 |
| 세균엽록소 b | 홍색세균 | 835–850, 1020–1040 |
| 세균엽록소 c | 녹색황세균, 녹만균류, 클로라시도박테리움속,[2] 클로로바쿨룸 테피둠 | 745–755 |
| 세균엽록소 d | 녹색황세균 | 705–740 |
| 세균엽록소 e | 녹색황세균 | 719–726 |
| 세균엽록소 f | 세균엽록소 c/d와 유사하게 세균엽록소 e합성의 돌연변이로 발견되었다. 진화적으로 유리하지 않다.[3] | 700–710 |
| 세균엽록소 g | 헬리오박테리아과 | 670, 788 |
구조[편집]
세균엽록소 a, 세균엽록소 b, 세균엽록소 g는 세균클로린이다. 즉 해당 분자에는 두 개의 환원된 피롤 고리(B와 D)가 있는 세균클로린 거대 고리가 있다. 세균엽록소 c, 세균엽록소 d, 세균엽록소 e, 세균엽록소 f는 클로린이다. 즉 해당 분자에는 한 개의 환원된 피롤 고리(D)가 있는 클로린 거대 고리가 있다.[4]
 |
엽록소 c~f는 피롤 고리 B와 C에 서로 다른 알킬기가 부착된 밀접하게 관련된 동족체 형태로 생성되며 아래에서는 세스퀴테르펜 알코올 파르네솔로 에스터화된 가장 간단한 버전으로 그려져 있다.[5] 대부분의 변이는 8번과 12번 위치에서 일어나며 메틸기전이효소의 변이에 기인할 수 있다.[6] 세균엽록소 cS는 세균엽록소 c의 8-에틸,12-메틸 동족체에 대한 용어이다.[7]
세균엽록소 g는 고리(A)의 8번 위치에 비닐기를 가지고 있다.[8]
- 주요 세균엽록소의 구조
-
세균엽록소 a
-
세균엽록소 b
-
세균엽록소 c
-
세균엽록소 d
-
세균엽록소 e
-
세균엽록소 f
-
세균엽록소 g
생합성[편집]
많은 종류의 세균엽록소가 알려져 있지만[4][9] 생합성 경로에 클로로필라이드 a가 중간생성물로 포함된다는 공통점을 가지고 있다.[10]
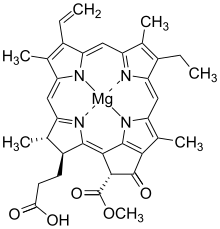 |
클로린 코어 세균엽록소 c~f는 엽록소 b, 엽록소 d, 엽록소 e가 만들어지는 방식과 유사하게 클로로필라이드 a의 곁사슬의 일련의 효소 변형에 의해 생성된다. 세균클로린 코어 세균엽록소 a, 세균엽록소 b, 세균엽록소 g는 C7과 C8 사이의 이중 결합을 환원시키기 위해 클로로필라이드 a 환원효소(COR)에 의해 수행되는 독특한 단계를 필요로 한다.[9]
대조적으로 아이소세균클로린은 별도의 경로를 통해 유로포르피리노젠 III로부터 생합성되며 이는 시로헴, 보조 인자 F430, 코발라민의 생성으로 이어진다. 일반적인 중간생성물은 시로하이드로클로린이다.[11]
같이 보기[편집]
각주[편집]
- ↑ Niel, C. B. (1932). “On the morphology and physiology of the purple and green sulphur bacteria”. 《Archiv für Mikrobiologie》 3: 1–112. doi:10.1007/BF00454965. S2CID 19597530.
- ↑ 가 나 Bryant, Donald A.; 외. (2007년 7월 27일), “Candidatus Chloracidobacterium thermophilum: An Aerobic Phototrophic Acidobacterium” (PDF), 《Science》 317 (5837): 523–526, Bibcode:2007Sci...317..523B, doi:10.1126/science.1143236, PMID 17656724, S2CID 20419870
- ↑ Vogl, Kajetan; 외. (2012년 8월 10일). “Bacteriochlorophyll f: properties of chlorosomes containing the "forbidden chlorophyll"”. 《Front. Microbiol.》 3: article 298, pages 1–12. doi:10.3389/fmicb.2012.00298. PMC 3415949. PMID 22908012.
- ↑ 가 나 Senge, Mathias O.; Smith, Kevin M. (2004). 〈Biosynthesis and Structures of the Bacteriochlorophylls〉. 《Anoxygenic Photosynthetic Bacteria》. Advances in Photosynthesis and Respiration 2. 137–151쪽. doi:10.1007/0-306-47954-0_8. ISBN 0-7923-3681-X.
- ↑ Harada, Jiro; Shibata, Yutaka; Teramura, Misato; Mizoguchi, Tadashi; Kinoshita, Yusuke; Yamamoto, Ken; Tamiaki, Hitoshi (2018). “In Vivo Energy Transfer from Bacteriochlorophyll c , d , e , or f to Bacteriochlorophyll a in Wild-Type and Mutant Cells of the Green Sulfur Bacterium Chlorobaculum limnaeum”. 《ChemPhotoChem》 2 (3): 190–195. doi:10.1002/cptc.201700164.
- ↑ Gomez Maqueo Chew, A; Frigaard, NU; Bryant, DA (September 2007). “Bacteriochlorophyllide c C-8(2) and C-12(1) methyltransferases are essential for adaptation to low light in Chlorobaculum tepidum.”. 《Journal of Bacteriology》 189 (17): 6176–84. doi:10.1128/JB.00519-07. PMC 1951906. PMID 17586634.
- ↑ Gloe, A; Risch, N (1978년 8월 1일). “Bacteriochlorophyll cs, a new bacteriochlorophyll from Chloroflexus aurantiacus.”. 《Archives of Microbiology》 118 (2): 153–6. doi:10.1007/BF00415723. PMID 697505. S2CID 20011765.
- ↑ Tsukatani, Yusuke; Yamamoto, Haruki; Mizoguchi, Tadashi; Fujita, Yuichi; Tamiaki, Hitoshi (2013). “Completion of biosynthetic pathways for bacteriochlorophyll g in Heliobacterium modesticaldum: The C8-ethylidene group formation”. 《Biochimica et Biophysica Acta (BBA) - Bioenergetics》 1827 (10): 1200–1204. doi:10.1016/j.bbabio.2013.06.007. PMID 23820336.
- ↑ 가 나 Chew, Aline Gomez Maqueo; Bryant, Donald A. (2007). “Chlorophyll Biosynthesis in Bacteria: The Origins of Structural and Functional Diversity”. 《Annual Review of Microbiology》 61: 113–129. doi:10.1146/annurev.micro.61.080706.093242. PMID 17506685.
- ↑ Willows, Robert D. (2003). “Biosynthesis of chlorophylls from protoporphyrin IX”. 《Natural Product Reports》 20 (6): 327–341. doi:10.1039/B110549N. PMID 12828371.
- ↑ Battersby, Alan R. (2000). “Tetrapyrroles: The pigments of life: A Millennium review”. 《Natural Product Reports》 17 (6): 507–526. doi:10.1039/B002635M. PMID 11152419.