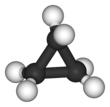
사이클로프로페인

| |||
| |||
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Cyclopropane[2] | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.000.771 | ||
| KEGG | |||
PubChem CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C3H6 | |||
| 몰 질량 | 42.08 g/mol | ||
| 겉보기 | Colorless gas | ||
| 냄새 | Sweet smelling | ||
| 밀도 | 1.879 g/L (1 atm, 0 °C) | ||
| 녹는점 | −128 °C (−198 °F; 145 K) | ||
| 끓는점 | −33 °C (−27 °F; 240 K) | ||
| 산성도 (pKa) | ~46 | ||
자화율 (χ)
|
-39.9·10−6 cm3/mol | ||
| 위험 | |||
| 주요 위험 | Highly flammable Asphyxiant | ||
| 물질 안전 보건 자료 | External MSDS | ||
| NFPA 704 (파이어 다이아몬드) | |||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
사이클로프로페인(cyclopropane) 또는 시클로프로판은 C3H6의 화학식을 가져 분자에 탄소원자가 세개인 사이클로알케인이다. 결합각이 60도여서 불안정하므로 첨가반응을 잘하지만 브로민수 탈색반응은 잘 하지 못한다. 탄소원자 3개가 한 평면상에 배열되는 구조를 가진다.
역사[편집]
사이클로프로페인은 1881년 어거스트 프로인트에 의해 발견되었으며, 그는 또한 그의 논문에게 신물질에 대한 올바른 구조식까지 제시했다.[3]프로인트는 1,3-다이브로모프로페인을 나트륨을 반응시켜, 분자내 부르츠 반응을 통해 이를 합성했다.[4]1887년 나트륨 대신 아연을 이용한 구스타프슨에 의해 그 수율이 향상되었다.[5] 사이클로프로페인은 상업적으로 이용되지 않다가 1929년 헨더슨과 루카스에 의해 마취제로서의 성질이 발견되고,[6] 1936년 산업적으로 생산되기 시작했다.[7] 현재는 비슷한 역할을 하는 다른 물질로 대체되어 쓰이지 않는다.
마취제[편집]
사이클로프로페인은 Ralph M. Waters에 의해 의학적인 용도로 도입되었다. 사이클로프로페인은 상대적으로 강한, 자극적이지 않고 달콤한 향을 가졌으며, 최소 폐포 농도(minimum alveolar concentration)는 17.5%,[8] 혈액/기체 분배 계수(blood/gas partition coefficient)는 0.55로 나타났다. 이는 사이클로 프로페인과 산소의 혼합물 흡입으로 인한 마취 유도가 빠르고 불쾌하지 않다는 뜻이다. 그러나 장기간 사용시 급격한 혈압감소로 부정맥을 일으킬 수 있는 잠재성이 있었다. 이는 '사이클로프로페인 쇼크'로 알려져있다.[9] 이러한 이유에서, 그리고 높은 가격과 폭발성때문에 이후 마취의 유도에만 사용되다가 1980년대 중반부터 의학적인 용도로 사용하지 못하게 되었다.[10]
약리학[편집]
사이클로프로페인은 GABAA와 글리세린 수용체에 대해 비활성을 나타내며, NMDA 수용체 대항체로서 작용한다.[11][12] 또한 AMPA 수용체와 니코틴 아세틸콜린 수용체를 억제하는 효과를 나타내고, 특정 K2P 통로를 활성화시킨다.[11][12][13]
구조와 결합[편집]

삼각형 형태의 사이클로프로페인의 구조는 60°의 결합각을 나타나게 하는데, 이는 열역학적으로 안정한 109.5°보다 작은 값(sp3 혼성 오비탈을 형성)으로서 고리 변형이 크게 나타난다. 또한 수소 원자들의 가려진 입체 배열로 인해 비틀림 변형 또한 나타난다. 따라서 일반적인 알케인보다 불안정한 결합을 가지게 되고, 높은 반응성을 가지게 된다.
탄소간의 결합은 굽은 결합으로 기술되는데,[14]이 모형에서 탄소 원자간의 결합은 바깥족으로 굽어있고, 내부 오비탈의 각도가 104°로 나타나게 된다. 이것은 결합 변형의 수준을 감소시키며, sp3 혼성 오비탈을 변형시켜 sp5 혼성을 나타내게 된다.[15],[16] (1⁄6만큼의 s 오비탈의 성질을 가짐.) 따라서 탄소간 결합은 일반적인 결합에 피해 π 성질을 가지게 된다.(동시에 탄소-수소 결합의 경우 s 성질을 더 많이 가진다.)[17] 또한 탄소간의 결합은 일반적인 탄소간 결합보다 약하고, 그 결합길이가 151pm로 153pm의 일반적인 알케인 결합 길이보다 짧게 나타난다.(알켄의 경우 146pm를 나타낸다.)[18]
사이클로프로페인의 세 개의 시그마 결합을 형성하는 여섯 개의 전자에 의한 고리형 비편재화에 의한 안정성을 통해 Michael J. S. Dewar는 사이클로프로페인의 변형 에너지(27.6 kcal/mol, 사이클로헥세인을 0 kcal/mol으로 할 때)가 사이클로 뷰테인(26.2 kcal/mol)에 비해 큰 차이를 나타내지 않음을 설명하였다.[19] 이러한 안정화는 벤젠과 같은 분자에서 나타나는 π-방향족성과 달리 σ-방향족성을 나타내게 한다.[20][21] 다른 연구에서는 σ-방향족성의 역할과 ring current의 존재를 지지하지 않으며, 에너지 측면의 안정화와 사이클로 프로페인의 비정상적인 자기적 특성을 설명하는 대안을 제시한다.[22]
합성[편집]
사이클로프로페인은 처음에는 부르츠 반응에 의해 제조되었으나,[23] 나트륨을 아연으로 대체함으로서 그 수율이 향상되었다.[5]
- BrCH2CH2CH2Br + 2 Na → (CH2)3 + 2 NaBr
사이클로프로페인화[편집]
사이클로프로페인 고리는 피레트린과 같은 다양한 생체 분자에서 발견된다. 이러한 고리를 형성하는 반응을 사이클로프로페인화라고 부른다.
각주[편집]
- ↑ Merck Index, 11th Edition, 2755.
- ↑ 〈Front Matter〉. 《Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 137쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
- ↑ August Freund (1881). “Über Trimethylen” [On trimethylene]. 《Journal für Praktische Chemie》 26 (1): 367–377. doi:10.1002/prac.18820260125.
- ↑ August Freund (1882). “Über Trimethylen” [On trimethylene]. 《Monatshefte für Chemie …》 3 (1): 625–635. doi:10.1007/BF01516828.
- ↑ 가 나 G. Gustavson (1887). “Ueber eine neue Darstellungsmethode des Trimethylens” [On a new method of preparing trimethylene]. 《Journal für Praktische Chemie》 36: 300–305. doi:10.1002/prac.18870360127.
- ↑ G. H. W. Lucas; V. E. Henderson (1929년 8월 1일). “A New Anesthetic: Cyclopropane : A Preliminary Report”. 《Can Med Assoc J》 21 (2): 173–5. PMC 1710967. PMID 20317448.
- ↑ H. B. Hass; E. T. McBee; G. E. Hinds (1936). “Synthesis of Cyclopropane”. 《Industrial & Engineering Chemistry》 28 (10): 1178–81. doi:10.1021/ie50322a013.
- ↑ Eger, Edmond I.; Brandstater, Bernard; Saidman, Lawrence J.; Regan, Michael J.; Severinghaus, John W.; Munson, Edwin S. (1965). “Equipotent Alveolar Concentrations of Methoxyflurane, Halothane, Diethyl Ether, Fluroxene, Cyclopropane, Xenon and Nitrous Oxide in the Dog”. 《Anesthesiology》 26 (6): 771–777. doi:10.1097/00000542-196511000-00012.
- ↑ JOHNSTONE, M; Alberts, JR (July 1950). “Cyclopropane anesthesia and ventricular arrhythmias.”. 《British heart journal》 12 (3): 239–44. doi:10.1136/hrt.12.3.239. PMC 479392. PMID 15426685.
- ↑ MacDonald, AG (June 1994). “A short history of fires and explosions caused by anaesthetic agents.”. 《British journal of anaesthesia》 72 (6): 710–22. doi:10.1093/bja/72.6.710. PMID 8024925.
- ↑ 가 나 Hugh C. Hemmings; Philip M. Hopkins (2006). 《Foundations of Anesthesia: Basic Sciences for Clinical Practice》. Elsevier Health Sciences. 292–쪽. ISBN 0-323-03707-0.
- ↑ 가 나 Hemmings, Hugh C. (2009). “Molecular Targets of General Anesthetics in the Nervous System”. 《Suppressing the Mind》: 11–31. doi:10.1007/978-1-60761-462-3_2.
- ↑ Hara K, Eger EI, Laster MJ, Harris RA (December 2002). “Nonhalogenated alkanes cyclopropane and butane affect neurotransmitter-gated ion channel and G-protein-coupled receptors: differential actions on GABAA and glycine receptors”. 《Anesthesiology》 97 (6): 1512–20. doi:10.1097/00000542-200212000-00025. PMID 12459679.[깨진 링크(과거 내용 찾기)]
- ↑ Eric V. Anslyn and Dennis A. Dougherty. Modern Physical Organic Chemistry. 2006. pages 850-852
- ↑ http://isites.harvard.edu/fs/docs/icb.topic93502.files/Lectures_and_Handouts/06-Handouts/deMeijere.pdf
- ↑ http://isites.harvard.edu/fs/docs/icb.topic1032290.files/lecture%203.pdf
- ↑ Knipe, edited by A.C. (2007). 《March's advanced organic chemistry reactions, mechanisms, and structure.》 6판. Hoboken, N.J.: Wiley-Interscience. 219쪽. ISBN 0470084944.
- ↑ Allen, Frank H.; Kennard, Olga; Watson, David G.; Brammer, Lee; Orpen, A. Guy; Taylor, Robin (1987). “Tables of bond lengths determined by X-ray and neutron diffraction. Part 1. Bond lengths in organic compounds”. 《Journal of the Chemical Society, Perkin Transactions 2》 (12): S1–S19. doi:10.1039/P298700000S1.
- ↑ S. W. Benson, Thermochemical Kinetics, S. 273, J. Wiley & Sons, New York, London, Sydney, Toronto 1976
- ↑ Dewar, M. J. (1984). “Chemical Implications of σ Conjugation”. 《J. Am. Chem. Soc.》 106: 669–682. doi:10.1021/ja00315a036.
- ↑ Cremer, D. (1988). “Pros and Cons of σ-Aromaticity”. 《Tetrahedron》 44 (2): 7427–7454. doi:10.1016/s0040-4020(01)86238-4.
- ↑ Wu, Wei; Ma, Ben; Wu, Judy I-Chia; von Ragué, Schleyer; Mo, Yirong (2009). “Is Cyclopropane Really the σ-Aromatic Paradigm?”. 《Chemistry: A European Journal》 15 (38): 9730–9736. doi:10.1002/chem.200900586.
- ↑ August Freund (1881). “Über Trimethylen” [On trimethylene]. 《Journal für Praktische Chemie》 26 (1): 367–377. doi:10.1002/prac.18820260125.