아닐린
| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Aniline[1] | |||
| 체계명
Benzenamine | |||
| 별칭
Phenylamine
Aminobenzene Benzamine | |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| 3DMet | |||
| 605631 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.000.491 | ||
| EC 번호 |
| ||
| 2796 | |||
| KEGG | |||
PubChem CID
|
|||
| RTECS 번호 |
| ||
| UNII | |||
| UN 번호 | 1547 | ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C6H7N | |||
| 몰 질량 | 93.129 g·mol−1 | ||
| 겉보기 | Colorless to yellow liquid | ||
| 밀도 | 1.0297 g/mL | ||
| 녹는점 | −6.3 °C (20.7 °F; 266.8 K) | ||
| 끓는점 | 184.13 °C (363.43 °F; 457.28 K) | ||
| 3.6 g/100 mL at 20 °C | |||
| 증기 압력 | 0.6 mmHg (20° C)[2] | ||
| 산성도 (pKa) |
| ||
자화율 (χ)
|
−62.95·10−6 cm3/mol | ||
| 점도 | 3.71 cP (3.71 mPa·s at 25 °C) | ||
| 열화학 | |||
표준 연소 엔탈피 (ΔcH⦵298)
|
−3394 kJ/mol | ||
| 위험 | |||
| 주요 위험 | potential occupational carcinogen | ||
| GHS 그림문자 |    
| ||
| 신호어 | 위험 | ||
| H301, H311, H317, H318, H331, H341, H351, H372, H400 | |||
| P201, P202, P260, P261, P264, P270, P271, P272, P273, P280, P281, P301+310, P302+352, P304+340, P305+351+338, P308+313, P310, P311, P312, P314, P321, P322, P330, P333+313, P361 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | 70 °C (158 °F; 343 K) | ||
| 770 °C (1,420 °F; 1,040 K) | |||
| 폭발 한계 | 1.3–11%[2] | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LDLo (lowest published)
|
195 mg/kg (dog, oral) 250 mg/kg (rat, oral) 464 mg/kg (mouse, oral) 440 mg/kg (rat, oral) 400 mg/kg (guinea pig, oral)[4] | ||
LC50 (median concentration)
|
175 ppm (mouse, 7 h)[4] | ||
LCLo (lowest published)
|
250 ppm (rat, 4 h) 180 ppm (cat, 8 h)[4] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용)
|
TWA 5 ppm (19 mg/m3) [skin][2] | ||
REL (권장)
|
Ca [potential occupational carcinogen][2] | ||
IDLH (직접적 위험)
|
100 ppm[2] | ||
| 관련 화합물 | |||
| 1-Naphthylamine 2-Naphthylamine | |||
관련 화합물
|
Phenylhydrazine Nitrosobenzene Nitrobenzene | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
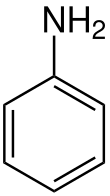
아닐린(영어: aniline, 독일어: anilin)은 벤젠의 수소 하나가 아민기로 치환된 화합물을 말한다. 화학식은 C6H5NH2이다.
성질[편집]
순수한 아닐린은 상온에서 특유의 냄새가 나고 무색투명한 액체 상태로 존재한다. 그러나 공기 중에서는 서서히 붉게 변하고 마지막에는 불투명한 흑색으로 변하게 된다. 끓는점은 184°C, 녹는점은 -6°C이다. 밀도는 1.0215g/ml이다. 인화점은 76°C이다. 물에는 약간 녹고 에탄올, 에테르, 벤젠 등의 유기 용매에는 잘 녹는다. 알칼리 금속이나 알칼리 토금속을 아닐린에 녹이면 수소가 발생하면서 C6H5HNNa 등의 금속 화합물이 생성된다.[6]
제법[편집]
니트로벤젠을 주석 또는 철과 염산으로 환원시켜 얻거나 니켈, 구리 등을 촉매로 하여 환원시킨다.[6]
용도[편집]
아닐린은 다음과 같은 용도로 사용된다.[6]
안전성[편집]
아닐린은 강력한 독성이 있기 때문에 취급에 주의해야 한다. 아닐린은 헤모글로빈과 결합하여 산소의 운반을 방해한다. 지속적인, 또는 반복적인 노출은 식욕감소, 빈혈, 체중감소, 신경계 이상, 신장 이상, 간이나 연골의 손상을 야기할 수 있다.[7] 흡입하거나 피부를 통해서 흡수될 경우 중독을 일으킬 수 있다. 아닐린을 보관할 때는 마개를 단단히 막아 어두운 곳에 두어야 한다.[6]
섭취[편집]
독성이 높다. 1g만 먹어도 위험하다. 증상은 흡입 시와 유사하다.[7]
흡입[편집]
독성이 높다. 혈액의 산소운반능력을 감소시킨다. 입술이나 혀가 파랗게 변할 수 있으며 두통, 구역질, 어지러움, 충격, 호흡기 마비, 그리고 사망에 이를 수 있다.[7]
피부[편집]
피부를 통해서 흡수될 수 있다. 피부를 통해 흡수될 경우 흡입 시와 증상이 유사하다. 피부를 자극하고 피부염을 일으킬 수 있다.[7]
눈[편집]
증기는 눈을 자극한다. 눈물, 흐린 시야를 야기할 수 있다. 튈 경우 각막에 손상을 입을 수 있다.[7]
각주[편집]
- ↑ 《Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book)》. Cambridge: The Royal Society of Chemistry. 2014. 416, 668쪽. doi:10.1039/9781849733069-FP001. ISBN 978-0-85404-182-4.
Aniline, for C6H5-NH2, is the only name for a primary amine retained as a preferred IUPAC name for which full substitution is permitted on the ring and the nitrogen atom. It is a Type 2a retained name; for the rules of substitution see P-15.1.8.2. Substitution is limited to substituent groups cited as prefixes in accordance with the seniority of functional groups explicitly expressed or implied in the functional parent compound name. The name benzenamine may be used in general nomenclature.
- ↑ 가 나 다 라 마 NIOSH Pocket Guide to Chemical Hazards. “#0033”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ Vollhardt, P.; Schore, Neil (2018). 《Organic Chemistry》 8판. W. H. Freeman. 1031쪽. ISBN 9781319079451.
- ↑ 가 나 다 “Aniline”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
- ↑ GOV, NOAA Office of Response and Restoration, US. “ANILINE | CAMEO Chemicals | NOAA”. 《cameochemicals.noaa.gov》. 2016년 6월 16일에 확인함.
- ↑ 가 나 다 라 化學大辭典編集委員會 편, 성용길, 김창홍 역, 〈아닐린〉, 《화학대사전》(Vol. 5), 서울: 世和, 2001, 533~534쪽.
- ↑ 가 나 다 라 마 “MSDS”. 2016년 3월 5일에 원본 문서에서 보존된 문서. 2018년 10월 31일에 확인함.
참고 문헌[편집]
- 化學大辭典編集委員會 편, 성용길, 김창홍 역, 《화학대사전》, 서울: 世和, 2001.
- https://web.archive.org/web/20080615034446/http://www.jtbaker.com/msds/englishhtml/a6660.htm