세레콕시브
| |

| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
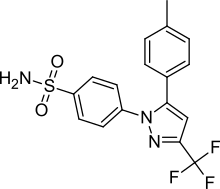
| 4-[5-(4-Methylphenyl)-3-(trifluoromethyl)pyrazol-1-yl]benzenesulfonamide | |
| 식별 정보 | |
| CAS 등록번호 | 169590-42-5 |
| ATC 코드 | L01XX33 M01AH01 |
| PubChem | 2662 |
| 드러그뱅크 | DB00482 |
| ChemSpider | 2562 |
| 화학적 성질 | |
| 화학식 | C17H14F3N3O2S |
| 분자량 | 381.373 |
| 약동학 정보 | |
| 생체적합성 | Unknown[1] |
| 단백질 결합 | 97% (mainly to serum albumin)[1] |
| 동등생물의약품 | ? |
| 약물 대사 | Liver (mainly CYP2C9)[1] |
| 생물학적 반감기 | 7.8 hours; 11 hours (mild hepatic impairment); 13 hours (moderate-severe hepatic impairment)[1] |
| 배출 | Faeces (57%), urine (27%)[1] |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B3(오스트레일리아) ?(미국) |
| 법적 상태 | |
| 투여 방법 | By mouth |
세레콕시브(Celecoxib)는 COX-2 선택적 비스테로이드 항염증제(NSAID)이다. 상품명 쎄레브렉스(Celebrex)로 알려져 있기도 하다. 세레콕시브는 골관절염, 류마티스 관절염, 강직성 척주염, 성인의 급성 통증, 월경통, 2세 이상의 소아기특발성관절염 환자의 통증 및 염증 조절을 위하여 사용된다.
대한민국 식품의약품안전처에서는 골관절염(퇴행관절염)의 증상이나 징후의 완화, 류마티스관절염의 증상이나 징후의 완화, 강직척추염의 증상 및 징후의 완화,성인의 급성 통증 완화(수술후, 발치후 진통), 원발월경통의 증상 조절을 위한 사용이 허가되어 있다.
세레콕시브 투약 이후 주된 부작용으로는 심혈관계질환, 상부 위장관 출혈 등이 있다. 2013년 발표된 세레콕시브와 기타 비스테로이드 항염증제간의 메타분석 논문에 따르면 세레콕시브의 심혈관계질환 유발의 위험비는 나프록센의 1.49배, 디클로페낙의 0.97배, 이부프로펜의 0.92배로 나타났으며, 상부위장관출혈의 위험비는 나프록센의 0.37배, 디클로페낙의 0.94배, 이부프로펜의 0.40배로 조사되었다.[4]
각주[편집]
- ↑ 가 나 다 라 마 McCormack PL (December 2011). “Celecoxib: a review of its use for symptomatic relief in the treatment of osteoarthritis, rheumatoid arthritis and ankylosing spondylitis”. 《Drugs》 71 (18): 2457–89. doi:10.2165/11208240-000000000-00000. PMID 22141388.
- ↑ “Celebrex 100mg capsule - Summary of Product Characteristics (SmPC)”. 《(emc)》. 2020년 1월 13일. 2020년 5월 5일에 확인함.
- ↑ “Celebrex- celecoxib capsule”. 《DailyMed》. 2019년 5월 31일. 2021년 2월 24일에 원본 문서에서 보존된 문서. 2020년 5월 5일에 확인함.
- ↑ “Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs: meta-analyses of individual participant data from randomised trials”. 《The Lancet》 382 (9894): 769–779. 2013년 8월. doi:10.1016/s0140-6736(13)60900-9. ISSN 0140-6736. PMC 3778977. PMID 23726390.
