면역글로불린 A

1 H-사슬
2 L-사슬
3 J-사슬
4 분비형 요소
면역글로불린 A(영어: immunoglobulin A, IgA)는 점막 면역에 주요 역할을 하는 항체이다. 점막에서 생산되는 IgA는 다른 종류의 항체를 모두 합친 것보다 많다.[1] 장의 내강으로 분비되는 IgA는 하루에 3-5 g이고,[2] 몸 전체에서 생산되는 면역글로불린의 15%를 차지한다.[3]
IgA는 두 종류(IgA1과 IgA2)가 있고 분비형 IgA(sIgA)라고 불리는 이합체형으로 존재할 수 있다. 분비형 IgA은 눈물, 침, 땀, 초유 등 점막 분비물과 비뇨생식관, 위장관, 전립선과 호흡 상피의 분비물에 있는 주요 면역글로불린이다. 혈액에도 소량 존재한다. IgA의 분비형 요소는 IgA를 단백질 가수분해효소로부터 보호하여 위장관 환경에서 분해되지 않게 하고, 신체 분비물에서 증식하는 미생물로부터 보호한다.[4] sIgA는 또한 다른 면역글로불린의 염증 효과를 억제할 수 있다.[5] IgA의 옵소닌화는 매우 약하고 보체를 활성화시키는 능력도 떨어진다. IgA의 중쇄는 α형이다.
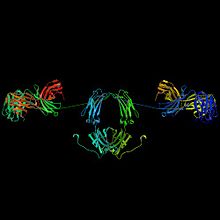
형태[편집]
IgA1과 IgA2[편집]
IgA에는 두 동형(isotype) IgA1과 IgA2가 있다. IgA1과 IgA2를 분비하는 세포의 비율은 인체의 림프조직마다 다양하다.[6] IgA1는 혈청에 많고, IgA2는 혈청보다는 점막 분비물에 더 많다.[7] 혈액 내 IgA는 단량체이고 IgA1:IgA2 = 10:1이다. 장관내 형질세포가 생산하는 IgA는 이합체이고 IgA1:IgA2 = 2:3이다.[8]
IgA2는 중쇄와 경쇄가 이황결합이 아닌 비공유결합으로 연결되어 있다. 장에서 특이적으로 발달한 장연관 림프조직(GALT)에서는 비장, 말초림프절 등 림프조직보다 IgA2 생산량 비율이 더 크다. IgA1과 IgA2는 외분비물, 즉 초유, 모유, 눈물, 침에 들어있다.[7] 단백질 항원보다 다당류 항원이 IgA2를 유도하는 경향이 크다.[6]
혈청형과 분비형[편집]
IgA는 혈청에 있는지, 혹은 분비된 것인지에 따라 형태가 다르다. 분비형 IgA(secretory IgA, sIgA)는 IgA 단량체가 추가적인 사슬로 2-4개 결합한 중합체로, 총 분자량은 385 kDa이다. IgA 단량체를 결합시키는 것은 J 사슬(joining chain)이다. J 사슬은 분자량이 15 kDa인 폴리펩타이드로, 시스테인이 많고 다른 면역글로불린과 구조적으로 완전히 다르다. J 사슬은 IgA를 분비하는 세포에서 생산된다. 점막으로 외분비되는 올리고형 IgA에는 상피세포에서 생산된 분비성분(secretory component, 70 kDa)도 포함된다. 분비성분은 폴리-Ig 수용체(130 kDa)가 상피세포를 가로질러 눈물, 침, 땀, 장액으로 올리고형 IgA를 수송하고 분해되면서 올리고형 IgA에 남은 부분이다.
활성[편집]
점막에 IgA가 많은 것은 중합체형 IgA(polymeric IgA, pIgA)를 생산하는 형질세포와 중합체형 면역글로불린 수용체(pIgR)라는 면역글로불린 수용체를 발현하는 점막 상피세포가 협력하기 때문이다. 중합체형 IgA는 활성화된 형질세포에서 방출되어 근처의 중합체형 면역글로불린 수용체에 결합한다. 수용체에 결합한 IgA는 점막 상피세포를 가로질러 수송되고, 중합체형 면역글로불린 수용체를 자르면서 외분비된다.[9]
혈액에서 IgA는 면역 효과기세포에 발현되는 FcαRI(혹은 CD89)라는 Fc 수용체와 상호작용하여 염증 반응을 개시한다.[9] IgA가 FcαRI에 결합하면 항체의존 세포매개 세포독성(ADCC), 호산구와 호염기구의 탈과립, 단핵구, 대식세포, 호중구에 의한 식세포작용, 그리고 다형핵 백혈구에 의한 호흡폭발을 일으킨다.[9]
분비형 IgA는 일차적으로 병원균에 있는 리간드에 결합하여 상피세포 수용체에 결합하지 못하도록 한다.[10] 분비형 IgA는 전형적 보체경로를 활성화하는 능력과 옵소닌화 능력이 낮다.[11] 병원체 하나에 IgA가 결합하는 것으로는 대개 부족하고, 여러 특이적인 항원결정인자에 결합해야 상피에 대한 접근을 입체적으로 저해할 수 있다.[10] IgA는 염증을 일으키지 않으면서도 병원체가 장 내강에 접근하지 못하게 한다. IgA 레퍼토리에는 장 내의 미생물(공생)이 발현하는 항원에 대한 특이적인 항체가 포함되며, 이 항체는 장 내의 미생물에 감염되는 경우를 제외하고는 혈액에서 발견되지 않는다.[11]
면역적 차단은 다가항원이나 병원체에 항체가 교차결합하여 점막층에 항원을 붙잡거나, 연동으로 제거하는 과정이다. 분비형 IgA의 분비성분을 구성하는 다당류 사슬은 장 상피 꼭대기층에 있는 점막층에 결합할 수 있다.[10]
특이적인 항원에 대한 분비형 IgA는 M 세포와 그 아래의 면역 세포들이 담당한다. M 세포는 항원을 수집하고 그 아래의 수지상세포와 T 세포가 활성화되며, 장연관 림프조직(GALT)과 장간막 림프절, 소장에 있는 독립적인 림프소포에서 B 세포 개별형 전환(class switching)이 일어난다.[10]
장 내강으로 이동[편집]
중합체 IgA는 대개 분비형인 이합체로, 점막 표면 가까이에 있는 고유판 내의 형질세포가 생산한다. 이합체 IgA는 상피세포의 바닥가쪽 표면에 있는 중합체 면역글로불린 수용체에 결합하여 세포내이입되어 들어간다. 수용체-IgA 복합체는 세포 구획을 가로질러 상피세포의 내강쪽 경계까지 이동한다. 내강쪽 표면에 다다르면 수용체를 분해하고 일부(이를 분비성분이라는 함)만 이합체 IgA 분자에 남기고 내강으로 방출 및 확산된다.[12] 장에서 분비성분이 있는 IgA 복합체는 상피세포를 덮고 있는 점액층에 결합하여 잠재적인 항원이 세포에 다다르기 전에 중화하는 장벽을 형성한다.
병리학[편집]
IgA가 감소하거나 없는 상태를 선택적 IgA 결핍이라고 한다. 이는 임상적으로 심각한 면역결핍상태이다.
임질을 일으키는 Neisseria gonorrhœae,[13] 폐렴 연쇄상구균(Streptococcus pneumoniae),[14] 기회감염균인 Haemophilus influenzae B형은[15] IgA를 분해하는 단백질분해효소를 방출한다.
IgA 신증은 신장에 IgA가 침착되어 생긴다. 만성 질병으로, IgA가 축적되는 이유는 아직 밝혀지지 않았고, 신장에 축적된 IgA 복합체가 보체 연쇄반응을 활성화한다는 가설이 있다.[16]
셀리악병은 IgA 항근내막 항원(antiendomysial antibody)의 존재로 진단하므로, IgA와 관련이 있다.[17][18]
헤노흐-쇤라인(독일어: Henoch–Schönlein) 자반증은 IgA과 보체성분 3(C3)이 작은 혈관에 축적되는 전신질환이다. 대개 어린이에게서 나타나고 피부와 결합조직, 음낭, 관절, 위장관과 신장에 나타난다. 상기도 감염이 잇따르며 간이 증집된 IgA를 제거하면서 몇 주 후에 회복된다.[19]
각주 및 참고 문헌[편집]
- ↑ S Fagarasan and T Honjo (2003). “Intestinal IgA Synthesis: Regulation of Front-line Body Defenses”. 《Nature Reviews Immunology》 3 (1): 63–72. doi:10.1038/nri982. PMID 12511876.
- ↑ P. Brandtzaeg, R. Pabst (2004). “Let's go mucosal: communication on slippery ground”. 《Trends Immunology》 25 (11): 570–577. doi:10.1016/j.it.2004.09.005. PMID 15489184.
- ↑ AJ Macpherson, E Slack (2007). “The functional interactions of commensal bacteria with intestinal secretory IgA”. 《Current Opinion in Gastroenterology》 23 (6): 673–678. doi:10.1038/nrmicro2114. PMID 17906446.
- ↑ Junqueira, Luiz C.; Jose Carneiro (2003). 《Basic Histology》. McGraw-Hill. ISBN 0-8385-0590-2.
- ↑ Holmgren, J; Czerkinsky, C (April 2005). “Mucosal immunity and vaccines”. 《Nature Medicine》 11 (4s): S45–S53. doi:10.1038/nm1213. PMID 15812489.
- ↑ 가 나 Simell B, Kilpi T, Käyhty H (Mar 2006). “Subclass distribution of natural salivary IgA antibodies against pneumococcal capsular polysaccharide of type 14 and pneumococcal surface adhesin A (PsaA) in children”. 《Clinical and experimental immunology》 143 (3): 543–9. doi:10.1111/j.1365-2249.2006.03009.x. PMC 1809616. PMID 16487254.
- ↑ 가 나 Delacroix DL, Dive C, Rambaud JC, Yaerman JP (1982년 10월). “IgA subclasses in various secretions and in serum”. 《Immunology》 47 (2): 383–5. PMC 1555453. PMID 7118169.
- ↑ Kenneth Murphy, Paul Travers, Mark Walport (2008년 8월 25일). 〈9장 체액 면역반응〉. 김희제 외 9인 역. 《면역생물학》 7판. E PUBLIC. 388쪽. ISBN 978-89-6224-204-1.
- ↑ 가 나 다 Snoeck V, Peters I, Cox E (2006). “The IgA system: a comparison of structure and function in different species”. 《Vet. Res.》 37 (3): 455–67. doi:10.1051/vetres:2006010. PMID 16611558.
- ↑ 가 나 다 라 Mantis, Nicholas, Rol, Nicolas, Corthésy, Blaise (Nov 2011). 《Mucosal Immunology》 4 (6): 603–11. doi:10.1038/mi.2011.41. PMC 3774538. PMID 21975936 //www.ncbi.nlm.nih.gov/pmc/articles/PMC3774538.
|제목=이(가) 없거나 비었음 (도움말) - ↑ 가 나 Kenneth Murphy, Paul Travers, Mark Walport (2008년 8월 25일). 〈11장 점막면역계〉. 김희제 외 9인 역. 《면역생물학》 7판. E PUBLIC. 454-456쪽. ISBN 978-89-6224-204-1.
- ↑ CS Kaetzel, JK Robinson, KR Chintalacharuvu, JP Vaerman, and ME Lamm (1991). “The polymeric immunoglobulin receptor (secretory component) mediates transport of immune complexes across epithelial cells: a local defense function for IgA”. 《Proc Natl Acad Sci USA》 88 (19): 8796–8800. doi:10.1073/pnas.88.19.8796. PMC 52597. PMID 1924341.
- ↑ Halter R, Pohlner J, Meyer TF (1984년 7월). “IgA protease of Neisseria gonorrhoeae: isolation and characterization of the gene and its extracellular product”. 《The EMBO Journal》 3 (7): 1595–601. PMC 557564. PMID 6430698.
- ↑ Proctor M, Manning PJ (1990년 9월). “Production of immunoglobulin A protease by Streptococcus pneumoniae from animals”. 《Infection and immunity》 58 (9): 2733–7. PMC 313560. PMID 2117567.
- ↑ St Geme JW 3rd, de la Morena ML, Falkow S (1994년 10월). “A Haemophilus influenzae IgA protease-like protein promotes intimate interaction with human epithelial cells”. 《Molecular microbiology》 14 (2): 217–33. doi:10.1111/j.1365-2958.1994.tb01283.x. PMID 7830568.
- ↑ Brake M, Somers D, Sondheimer JH (2014년 9월 16일). “IgA Nephropathy : Pathophysiology”. 《Medscape》. 2014년 12월 1일에 확인함.
- ↑ Prince HE, Norman GL, Binder WL (2000년 3월). “Immunoglobulin A (IgA) deficiency and alternative celiac disease-associated antibodies in sera submitted to a reference laboratory for endomysial IgA testing”. 《Clinical and diagnostic laboratory immunology》 7 (2): 192–6. doi:10.1128/cdli.7.2.192-196.2000. PMC 95847. PMID 10702491.
- ↑ Cunningham-Rundles C (2001년 9월). “Physiology of IgA and IgA deficiency”. 《J. Clin. Immunol.》 21 (5): 303–9. doi:10.1023/A:1012241117984. PMID 11720003.
- ↑ Rai A, Nast C, Adler S (1999년 12월). “Henoch-Schönlein purpura nephritis”. 《J Am Soc Nephrol.》 10 (12): 2637–44. PMID 10589705.
