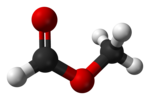
폼산 메틸
| |||

| |||
| 이름 | |||
|---|---|---|---|
| 우선명 (PIN)
Methyl formate | |||
| 체계명
Methyl methanoate | |||
| 별칭
R-611
| |||
| 식별자 | |||
3D 모델 (JSmol)
|
|||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.003.166 | ||
| EC 번호 |
| ||
PubChem CID
|
|||
| UNII | |||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| 성질 | |||
| C2H4O2 | |||
| 몰 질량 | 60.052 g·mol−1 | ||
| 겉보기 | Colorless liquid | ||
| 냄새 | pleasant[1] | ||
| 밀도 | 0.98 g/cm3 | ||
| 녹는점 | −100 °C (−148 °F; 173 K) | ||
| 끓는점 | 32 °C (90 °F; 305 K) | ||
| 30% (20°C)[1] | |||
| 증기 압력 | 634 hPa (476 mmHg) (20°C)[1] | ||
자화율 (χ)
|
-32.0·10−6 cm3/mol | ||
| 위험 | |||
| 물질 안전 보건 자료 | Oxford MSDS | ||
| GHS 그림문자 |  
| ||
| 신호어 | 위험 | ||
| H224, H302, H319, H332, H335 | |||
| P210, P233, P240, P241, P242, P243, P261, P264, P270, P271, P280, P301+312, P303+361+353, P304+312, P304+340, P305+351+338, P312, P330, P337+313, P370+378, P403+233, P403+235, P405, P501 | |||
| NFPA 704 (파이어 다이아몬드) | |||
| 인화점 | −19 °C; −2 °F; 254 K[1] | ||
| 폭발 한계 | 4.5%-23%[1] | ||
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |||
LD50 (median dose)
|
1622 mg/kg (oral, rabbit)[2] | ||
LCLo (lowest published)
|
50,000 ppm (guinea pig, 20 min)[2] | ||
| NIOSH (미국 건강 노출 한계): | |||
PEL (허용)
|
TWA 100 ppm (250 mg/m3)[1] | ||
REL (권장)
|
TWA 100 ppm (250 mg/m3) ST 150 ppm (375 mg/m3)[1] | ||
IDLH (직접적 위험)
|
4500 ppm[1] | ||
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |||
폼산 메틸(영어: methyl formate)은 폼산의 메틸 에스터이다. IUPAC 이름은 메탄산 메틸(영어: methyl methanoate)이다. 폼산 메틸은 카복실산 에스터의 가장 간단한 예로서 에터 냄새가 나고 증기압이 높으며 표면 장력이 낮은 무색 액체이다. 이는 상업적으로 관심이 있는 다른 많은 화합물의 전구체이다.[4]
생산[편집]
실험실에서는 메탄올과 폼산의 축합 반응을 통해 다음과 같이 생성할 수 있다.
- HCOOH + CH3OH → HCOOCH3 + H2O
그러나 산업용 폼산 메틸은 일반적으로 나트륨 메톡사이드와 같은 강염기가 있는 상태에서 메탄올과 일산화 탄소(카보닐화)를 결합하여 생산한다.[4]

이 공정은 상업적으로 BASF사 등에 의하여 실시하고 있는데 폼산 메틸에 대하여 96%의 선택성이 있다. 이 공정에서의 촉매는 일반적으로 합성 가스에서 파생되는 일산화 탄소의 공급원에 존재할 수 있는 수분에 민감하므로, 매우 건조한 일산화 탄소가 필수적이다.[5]
용도[편집]
폼산 메틸은 주로 포름아미드, 다이메틸폼아마이드, 폼산 제조에 사용된다. 이들 화합물은 다수의 유용한 유도체를 위한 전구체 또는 빌딩 블록이다.
증기압이 높기 때문에 속건성 마감재로 사용되며 일부 폴리우레탄 폼 용도(예: Foam Supplies Inc.에서 제조한 Ecomate ® )의 발포제로 사용되며 CFC, HCFC 및 HFC를 대체한다. 포름산 메틸은 오존층 파괴 가능성과 지구 온난화 가능성이 전혀 없다. 포름산 메틸은 살충제로도 사용된다.
때때로 주목을 끄는 포름산 메틸의 역사적 사용은 냉장 분야였다. 독성이 낮은 냉매가 도입되기 전에는 유명한 GE Monitor Top의 일부 모델과 같은 가정용 냉장고에서 이산화황 대신에 포름산 메틸이 사용되었다.
참고 자료[편집]
- ↑ 가 나 다 라 마 바 사 아 NIOSH Pocket Guide to Chemical Hazards. “#0417”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ 가 나 “Methyl formate”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
- ↑ “Methyl formate”. 《pubchem.ncbi.nlm.nih.gov》 (영어). 2021년 12월 19일에 확인함.
- ↑ 가 나 Werner Reutemann and Heinz Kieczka "Formic Acid" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi 10.1002/14356007.a12_013
- ↑ W. Couteau, J. Ramioulle, US Patent US4216339