사이클린 의존성 인산화효소 1
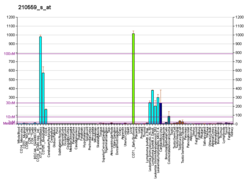
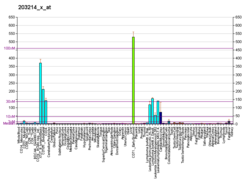
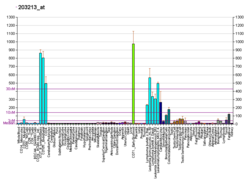
사이클린 의존성 인산화효소 1(영어: Cyclin-dependent kinase 1, Cdk1)은 고도로 보존된 세린/트레오닌 단백질 인산화효소로 기능하고 세포 주기 조절에 있어 주요 인자이다.[5] 세포 분열 주기 단백질 2 동족체 (영어: cell division cycle protein 2 homolog, Cdc 2 homolog)라고도 불린다. 출아효모균 Saccharomyces cerevisiae, 분열효모균 Schizosaccharomyces pombe에서 주로 연구되었으며, 각각 cdc28과 cdc2로 유전자에 암호화되어있다.[6] 인간에서 Cdk1은 CDC2 유전자에 암호화되어있다.[7] Cdk1은 사이클린과 복합체를 형성해 저마다 표적 기질을 인산화해, 세포주기를 진행시킨다.[8]
구조
[편집]
Cdk1은 약 34 kDa의 작은 단백질로, 고도로 보존되어있다. 사람에서 Cdk1의 동족체와 효모에서의 동족체는 약 63% 아미노산 배열이 동일하다. 게다가, cdc2유전자에 돌연변이가 발생한 효모는 인간 동족체로 돌연변이 표현형으로부터 회복 할 수 있다.[7] Cdk1은 다른 단백질 인산화효소에도 공통적으로 존재하고 단백질 인산화효소 모티프로 대부분 이루어져있다. 다른 인산화효소와 유사하게 Cdk1에는 ATP가 결합할 수 있는 갈라진 홈이 존재한다. 기질은 홈의 입구 부근에서 결합하고 Cdk1은 ATP의 γ-인산과 기질 세린/트레오닌 잔기의 하이드록시기 사이에 공유결합 형성을 촉매한다.
촉매 코어에 더해 Cdk1은 다른 사이클린 의존성 인산화효소와 유사한 활성화 루프 (T 루프)를 가진다. 사이클린과 상호작용하지 않았을 때, T 루프는 Cdk1 활성부위에 기질이 결합는 것을 억제한다. 또한 Cdk1은 PSTAIRE 헬릭스 (C 헬릭스)를 억제한다. 이 헬릭스는 사이클린의 결합에 함께 움직여 활성부위의 재배치하고, Cdk1의 인산화효소 활성을 촉진한다. 이런 기본적 기작은 Cdk2 같은 다른 Cdk와 같지만 구체적인 상호작용양식은 Cdk마다 다르다.[9][10]
기능
[편집]사이클린과 결합한 Cdk1에 있어 인산화는 세포주기 진행을 야기한다. Cdk1의 활성은 출아효모균 S. cerevisiae에서 가장 잘 이해가 가기 때문에 여기서는 S. cerevisiae의 Cdk1 (Cdc28)의 활성에 대해 기술한다.[5]
출아효모균에 있어 세포주기 진행의 시작은 SBF (SCB-binding factor)와 MBF (MCB-binding factor), 두 가지 조절복합체에 의해 제어된다. 이 같은 2 가지 복합체는 G1/S 기 유전자 전사를 개시하지만, 통상적으론 비활성상태로 있다. SBF는 Whi5에 의해 저해되고있지만, Cln3-Cdk1 (척추동물에선 사이클린 D)에 의해 인산화하여 Whi5는 핵으로부터 반출되고 G1/S 레귤론의 전사가 진행된다. 이 레귤론에 G1/S기의 사이클린 Cln1, 2 (척추동물에선 사이클린 E)가 포함된다.[11] G1/S 기 사이클린-Cdk1 복합체에 의해 S기로 진행하기 위해 준비 (중십체의 복제 등)가 행해지며, S기 사이클린 (Clb5, 6, 척추동물에선 사이클린 A)의 수준이 증가한다. S기 사이클린-Cdk1 복합체는 직접적인 복제원점의 초기화가 행해지지만,[12] 이른 S기의 개시는 Sic1에 의해 억제된다.
또한 G1/S기 사이클린 혹은 S기 사이클린-Cdk1 복합체의 활성화에 의해 Sic1의 수준은 급격하게 줄어들고, S기로의 진행을 행한다. 그 후 M기 사이클린 (Clb1, 2, 3, 4 등, 척추동물에선 사이클린 B)과 Cdk1의 복합체에 의해 인산화가 방추체 조립이나 자매염색분체 분리가 일어난다. 또한, Cdk1에 있어 인산화는 유비퀴틴 합성 효소로 인해 APCCdc20도 활성화해, 염색분체의 분리나 더 나아가 M기 사이클린 분해를 활성화시킨다. 이 M기 사이클린 파괴로 인해 유사분열 최종단계 (방추체의 해체 등)가 일어난다.
조절
[편집]Cdk1은 사이클린 결합으로 인해 조절된다. 사이클린 결합으로 인해 Cdk1 활성부위로의 접근이 변화하고 Cdk1 인산화효소 활성이 가능해진다. 또한 사이클린은 Cdk1 활성에 특이성을 부여한다. 적어도 일부의 사이클린에는 기질과 직접상호작용할 수 있는 소수성 패치가 존재해 그로인해 표적특이성을 띄게 된다.[13] 사이클린은 특정한 세포 내 부위에 있는 Cdk1의 표적화를 진행시킨다.
Cdk1은 사이클린으로 인한 조절에 더불어 인산화에 의해서도 조절된다. 보존된 티로신 잔기 (인간에선 Try15)의 인산화는 Cdk1을 저해한다. 이 인산화로 인해 ATP의 결합 배열이 변화해 효율적인 인산화효소 활성이 저해되는 것으로 생각된다. 분열효모균 S. pombe에선, DNA 합성이 완료되지 않았을 때, 이 인산화가 안정화시켜 유사분열의 진행을 막는다.[14] 모든 진핵생물에서 보존된 Wee1이 Tyr15의 인화를 일으키고 Cdc25 패밀리 구성요소의 단백질 인산가수분해효소가 이 활성에 길항한다. 이러한 인자 간의 균형으로 세포주기의 진행이 제어되는 것으로 예상된다. 거기에 더해 Wee1은 Cdr1, Cdr2, Pom1 같은 인자에 의해 제어된다.
Cdk-사이클린 복합체는 Cdk 저해 인자의 직접적인 결합에 의해 제어된다. 이런 단백질 중 하나가 위에서 말한 Sic1이다. Sci은 S기 사이클린 Clb5,6-Cdk1 결합체에 직접결합해 저해하는 인자이다. G1/S기 사이클린 Cln1,2-Cdk1에 의해 Sic1 복수 개소의 인산화는 Sic1의 유비퀴틴화와 분해 시기, 즉 S기로의 진행 시기를 결정한다고 생각된다. Sic1에 의한 저해가 극복되어야지만 Clb5,6이 활성화하고 S기가 개시된다.
상호작용
[편집]Cdk1은 이하의 인자들과 상호작용하는 것으로 나타난다.
같이 보기
[편집]각주
[편집]- ↑ 가 나 다 GRCh38: Ensembl release 89: ENSG00000170312 - 앙상블, May 2017
- ↑ 가 나 다 GRCm38: Ensembl release 89: ENSMUSG00000019942 - 앙상블, May 2017
- ↑ “Human PubMed Reference:”. 《National Center for Biotechnology Information, U.S. National Library of Medicine》.
- ↑ “Mouse PubMed Reference:”. 《National Center for Biotechnology Information, U.S. National Library of Medicine》.
- ↑ 가 나 Morgan, David L. (2007). 《The cell cycle: principles of control》. London: New Science Press. 30–31쪽. ISBN 978-0-19-920610-0.
- ↑ Nasmyth K (April 1993). “Control of the yeast cell cycle by the Cdc28 protein kinase”. 《Curr. Opin. Cell Biol.》 5 (2): 166–179. doi:10.1016/0955-0674(93)90099-C. PMID 8507488.
- ↑ 가 나 Lee, Melanie; Nurse, Paul (Jun 1987). “Complementation used to clone a human homologue of the fission yeast cell cycle control gene cdc2”. 《Nature》 327 (6117): 31–35. doi:10.1038/327031a0. PMID 3553962.
- ↑ Enserink JM, Kolodner RD (May 2010). “An overview of Cdk1-controlled targets and processes”. 《Cell Division》 5 (11): 11. doi:10.1186/1747-1028-5-11. PMC 2876151. PMID 20465793.
- ↑ Jeffrey PD, Russo AA, Polyak K, Gibbs E, Hurwitz J, Massagué J, Pavletich NP (July 1995). “Mechanism of CDK activation revealed by the structure of a cyclinA-CDK2 complex”. 《Nature》 376 (6538): 313–320. doi:10.1038/376313a0. PMID 7630397.
- ↑ Brown, Nicholas R.; Korolchuk, Svitlana; Martin, Mathew P.; Stanley, Will A.; Moukhametzianov, Rouslan; Noble, Martin E. M.; Endicott, Jane A. (2015년 4월 13일). “CDK1 structures reveal conserved and unique features of the essential cell cycle CDK”. 《Nature Communications》 6: 6769. doi:10.1038/ncomms7769. ISSN 2041-1723. PMC 4413027. PMID 25864384.
- ↑ Skotheim JM, Di Talia S, Siggia ED, Cross FR (July 2008). “Positive feedback of G1 cyclins ensures coherent cell cycle entry”. 《Nature》 454 (7202): 291–296. doi:10.1038/nature07118. PMC 2606905. PMID 18633409.
- ↑ Cross FR, Yuste-Rojas M, Gray S, Jacobson MD (July 1999). “Specialization and targeting of B-type cyclins”. 《Mol Cell》 4 (1): 11–19. doi:10.1016/S1097-2765(00)80183-5. PMID 10445023.
- ↑ Brown NR, Noble ME, Endicott JA, Johnson LN (November 1999). “The structural basis for specificity of substrate and recruitment peptides for cyclin-dependent kinases”. 《Nat. Cell Biol.》 1 (7): 438–443. doi:10.1038/15674. PMID 10559988.
- ↑ Elledge SJ (December 1996). “Cell cycle checkpoints: preventing an identity crisis”. 《Science》 274 (5293): 1664–1672. doi:10.1126/science.274.5293.1664. PMID 8939848.
- ↑ Pathan N, Aime-Sempe C, Kitada S, Basu A, Haldar S, Reed JC (2001). “Microtubule-targeting drugs induce bcl-2 phosphorylation and association with Pin1”. 《Neoplasia》 3 (6): 550–9. doi:10.1038/sj.neo.7900213. PMC 1506558. PMID 11774038.
- ↑ Pathan N, Aime-Sempe C, Kitada S, Haldar S, Reed JC (2001). “Microtubule-targeting drugs induce Bcl-2 phosphorylation and association with Pin1”. 《Neoplasia》 3 (1): 70–9. doi:10.1038/sj.neo.7900131. PMC 1505024. PMID 11326318.
- ↑ 가 나 Shanahan F, Seghezzi W, Parry D, Mahony D, Lees E (February 1999). “Cyclin E associates with BAF155 and BRG1, components of the mammalian SWI-SNF complex, and alters the ability of BRG1 to induce growth arrest”. 《Mol. Cell. Biol.》 19 (2): 1460–9. doi:10.1128/mcb.19.2.1460. PMC 116074. PMID 9891079.
- ↑ Pines J, Hunter T (September 1989). “Isolation of a human cyclin cDNA: evidence for cyclin mRNA and protein regulation in the cell cycle and for interaction with p34cdc2”. 《Cell》 58 (5): 833–846. doi:10.1016/0092-8674(89)90936-7. PMID 2570636.
- ↑ Kong M, Barnes EA, Ollendorff V, Donoghue DJ (March 2000). “Cyclin F regulates the nuclear localization of cyclin B1 through a cyclin-cyclin interaction”. 《EMBO J.》 19 (6): 1378–1388. doi:10.1093/emboj/19.6.1378. PMC 305678. PMID 10716937.
- ↑ Koff A, Giordano A, Desai D, Yamashita K, Harper JW, Elledge S, Nishimoto T, Morgan DO, Franza BR, Roberts JM (September 1992). “Formation and activation of a cyclin E-cdk2 complex during the G1 phase of the human cell cycle”. 《Science》 257 (5077): 1689–1694. doi:10.1126/science.1388288. PMID 1388288.
- ↑ Hannon GJ, Casso D, Beach D (March 1994). “KAP: a dual specificity phosphatase that interacts with cyclin-dependent kinases”. 《Proc. Natl. Acad. Sci. U.S.A.》 91 (5): 1731–1735. doi:10.1073/pnas.91.5.1731. PMC 43237. PMID 8127873.
- ↑ Gyuris J, Golemis E, Chertkov H, Brent R (November 1993). “Cdi1, a human G1 and S phase protein phosphatase that associates with Cdk2”. 《Cell》 75 (4): 791–803. doi:10.1016/0092-8674(93)90498-F. PMID 8242750.
- ↑ He J, Xu J, Xu XX, Hall RA (July 2003). “Cell cycle-dependent phosphorylation of Disabled-2 by cdc2”. 《Oncogene》 22 (29): 4524–4530. doi:10.1038/sj.onc.1206767. PMID 12881709.
- ↑ Reuter TY, Medhurst AL, Waisfisz Q, Zhi Y, Herterich S, Hoehn H, Gross HJ, Joenje H, Hoatlin ME, Mathew CG, Huber PA (October 2003). “Yeast two-hybrid screens imply involvement of Fanconi anemia proteins in transcription regulation, cell signaling, oxidative metabolism, and cellular transport”. 《Exp. Cell Res.》 289 (2): 211–221. doi:10.1016/S0014-4827(03)00261-1. PMID 14499622.
- ↑ Kupfer GM, Yamashita T, Naf D, Suliman A, Asano S, D'Andrea AD (August 1997). “The Fanconi anemia polypeptide, FAC, binds to the cyclin-dependent kinase, cdc2”. 《Blood》 90 (3): 1047–54. PMID 9242535.
- ↑ Zhan Q, Antinore MJ, Wang XW, Carrier F, Smith ML, Harris CC, Fornace AJ (May 1999). “Association with Cdc2 and inhibition of Cdc2/Cyclin B1 kinase activity by the p53-regulated protein Gadd45”. 《Oncogene》 18 (18): 2892–2900. doi:10.1038/sj.onc.1202667. PMID 10362260.
- ↑ Jin S, Antinore MJ, Lung FD, Dong X, Zhao H, Fan F, Colchagie AB, Blanck P, Roller PP, Fornace AJ, Zhan Q (June 2000). “The GADD45 inhibition of Cdc2 kinase correlates with GADD45-mediated growth suppression”. 《J. Biol. Chem.》 275 (22): 16602–16608. doi:10.1074/jbc.M000284200. PMID 10747892.
- ↑ Yang Q, Manicone A, Coursen JD, Linke SP, Nagashima M, Forgues M, Wang XW (November 2000). “Identification of a functional domain in a GADD45-mediated G2/M checkpoint”. 《J. Biol. Chem.》 275 (47): 36892–36898. doi:10.1074/jbc.M005319200. PMID 10973963.
- ↑ Vairapandi M, Balliet AG, Hoffman B, Liebermann DA (September 2002). “GADD45b and GADD45g are cdc2/cyclinB1 kinase inhibitors with a role in S and G2/M cell cycle checkpoints induced by genotoxic stress”. 《J. Cell. Physiol.》 192 (3): 327–338. doi:10.1002/jcp.10140. PMID 12124778.
- ↑ Tao W, Zhang S, Turenchalk GS, Stewart RA, St John MA, Chen W, Xu T (February 1999). “Human homologue of the Drosophila melanogaster lats tumour suppressor modulates CDC2 activity”. 《Nat. Genet.》 21 (2): 177–181. doi:10.1038/5960. PMID 9988268.
- ↑ Kharbanda S, Yuan ZM, Rubin E, Weichselbaum R, Kufe D (August 1994). “Activation of Src-like p56/p53lyn tyrosine kinase by ionizing radiation”. 《J. Biol. Chem.》 269 (32): 20739–43. PMID 8051175.
- ↑ Pathan NI, Geahlen RL, Harrison ML (November 1996). “The protein-tyrosine kinase Lck associates with and is phosphorylated by Cdc2”. 《J. Biol. Chem.》 271 (44): 27517–27523. doi:10.1074/jbc.271.44.27517. PMID 8910336.
- ↑ Luciani MG, Hutchins JR, Zheleva D, Hupp TR (July 2000). “The C-terminal regulatory domain of p53 contains a functional docking site for cyclin A”. 《J. Mol. Biol.》 300 (3): 503–518. doi:10.1006/jmbi.2000.3830. PMID 10884347.
- ↑ Ababneh M, Götz C, Montenarh M (May 2001). “Downregulation of the cdc2/cyclin B protein kinase activity by binding of p53 to p34(cdc2)”. 《Biochem. Biophys. Res. Commun.》 283 (2): 507–512. doi:10.1006/bbrc.2001.4792. PMID 11327730.
- ↑ Tan F, Lu L, Cai Y, Wang J, Xie Y, Wang L, Gong Y, Xu BE, Wu J, Luo Y, Qiang B, Yuan J, Sun X, Peng X (July 2008). “Proteomic analysis of ubiquitinated proteins in normal hepatocyte cell line Chang liver cells”. 《Proteomics》 8 (14): 2885–2896. doi:10.1002/pmic.200700887. PMID 18655026.