아바카비르
| |
| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
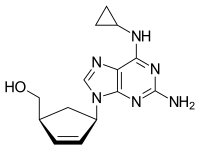
| {(1S,4R)-4-[2-amino-6-(cyclopropylamino)-9H-purin-9-yl]cyclopent-2-en-1-yl}methanol | |
| 식별 정보 | |
| CAS 등록번호 | 136470-78-5 |
| ATC 코드 | J05AF06 |
| PubChem | 441300 |
| 드러그뱅크 | DB01048 |
| ChemSpider | 390063 |
| 화학적 성질 | |
| 화학식 | C14H18N6O |
| 분자량 | 286.332 g/mol |
| SMILES | eMolecules & PubChem |
| 물리적 성질 | |
| 녹는점 | 165 °C (329 °F) |
| 약동학 정보 | |
| 생체적합성 | 83% |
| 동등생물의약품 | ? |
| 약물 대사 | Liver |
| 생물학적 반감기 | 1.54 ± 0.63 h |
| 배출 | 콩팥 (아바카비르 1.2%, 5'카르복실산 매개물 30%, 5'글루코나이드 매개물 36%, 기타 매개물 15%). 대변 (16%) |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B3(오스트레일리아) C(미국) |
| 법적 상태 | |
| 투여 방법 | 구강 투여 |
아바카비르(Abacavir)는 지아젠(Ziagen)이라는 상호명으로 판매되는 후천면역결핍증후군 예방 및 치료제다.[1][2] 뉴클레오사이드 유사물 역전사 효소 억제제(NRTIs)로,[3] 단독으로 사용되는것은 권고되지 않아 병용된다.[4] 알약이나 물약으로 경구 복용되며, 3개월 이상의 유아에게서 안전성이 검증되었다.[1][5]
심각한 부작용은 잘 나타나지 않는다.[5] 일반적인 부작용으로는 구토, 수면장애, 발열, 피로감 등이 있다. 더 심한 부작용으로는 과민증, 간 간손상, 젖산산증 등이 있다.[1] 유전자 검사를 통해 환자의 과민성을 알 수 있다. 과민증의 증상으로는 발진, 구토, 호흡곤란 등이 있다.[5]
아바카비르는 1988년 특허를 받았고, 1998년 미국에서 사용 승인을 받았다.[6][7] 현재 가장 안전하고 효과적인 의약품으로 의료제도에서 필수적인 의약품 목록인 WHO 필수 의약품 목록에 등재되어 있다.[8] 제네릭 의약품이다.[1] 2014년 기준으로 개발도상국에서 도매가는 0.36~0.83달러이다.[9] 2016년 기준으로 미국에서 한달치 의약품을 구매하기 위해서는 70.50달러가 필요하다.[10] 라미부딘, 지도부딘, 돌루테그라비르 등과 다른 HIV 약물과 함께 판매된다.[5][3] 아바카비르/라미부딘의 경우 주요 약물로 분류된다.[8]
부작용
일반적인 부작용으로는 메스꺼움, 두통, 피로, 구토, 설사, 식욕 감퇴, 수면장애 등이 있다. 드물지만 심각한 부작용으로는 발진, AST 및 ALT랑 상승, 우울증, 불안, 발열 및 오한, URI, 젖산산증, 이상지지혈증, 고지혈증, 지질영양이상증 등이 있다.[11][12]
간 질환이 있는 사람들은 아바카비르를 사용할 경우 병을 악화시킬 수 있기 때문에 주의해야 한다. 간 질환의 징후로는 메스꺼움과 구토, 복통, 검은 소변, 누런 피부색과 흰자위 등이 있다. 다른 뉴클레오사이드 약물과 마찬가지로 드물게 젖산산증이 나타나기도 한다. 젖산산증의 증상으로는 빠르고 불규칙한 심박, 특이한 근육통, 피로, 호흡곤란, 메스꺼움과 구토와 함께 복통이 있다.[13] 아바카비르는 또한 면역 재조직 염증 증후군(immune reconstitution inflammatory syndrome, IRIS)을 유발할 수 있으며, 체지방의 변화뿐만 아니라 심장마비의 위험도 증가시킬 수 있다.
실험실에서 아바카비르 저항 HIV주(strain)가 개발되었는데, 라미부딘, 디다노신, 잘시타빈 등에도 저항성을 띈다. 단백질 가수 분해 효소억제제 내성이 있는 HIV 균주는 아바카비르에 내성이 없을 가능성이 높다. 생후 3개월 미만의 유아에게 사용이 금지되며, 과다복용의 영향에 대해서는 알려진 바가 거의 없다. 약물 과다복용 환자들은 병원 응급실로 옮겨져 치료를 받아야 한다.
과민성증후군
과민반응은 HLA-B57이라는 사람백혈구항원 B 좌위의 대립유전자와 관련이 있다.[14][15][16]
기작
아바카비르는 뉴클레오사이드 역전사 효소 억제제로 바이러스 복제에 관여하여 항바이러스기능을 한다. 구아노신 유사물로 인산화되어 카르보비르 3인산염(CBV-TP)이 되는데, CBV-TP는 다른 구아노신들과 바이러스 DNA에 끼워넣어진다. 일단 CBV-TP가 바이러스 DNA에 들어가게 되면 이후 전사 및 역전사효소의 활성이 억제된다.[17]
합성

각주
- ↑ 가 나 다 라 “Abacavir Sulfate”. The American Society of Health-System Pharmacists. 8 September 2017에 원본 문서에서 보존된 문서. 31 July 2015에 확인함.
- ↑ “Drug Name Abbreviations Adult and Adolescent ARV Guidelines”. 《AIDSinfo》. 9 November 2016에 원본 문서에서 보존된 문서. 8 November 2016에 확인함.
- ↑ 가 나 “Nucleoside reverse transcriptase inhibitors (NRTIs or 'nukes') - HIV/AIDS”. 《www.hiv.va.gov》. 9 November 2016에 원본 문서에서 보존된 문서. 8 November 2016에 확인함.
- ↑ “What Not to Use Adult and Adolescent ARV Guidelines”. 《AIDSinfo》. 9 November 2016에 원본 문서에서 보존된 문서. 8 November 2016에 확인함.
- ↑ 가 나 다 라 Yuen GJ, Weller S, Pakes GE (2008). “A review of the pharmacokinetics of abacavir.”. 《Clinical Pharmacokinetics》 47 (6): 351–71. doi:10.2165/00003088-200847060-00001. PMID 18479171.
- ↑ Fischer, Janos; Ganellin, C. Robin (2006). 《Analogue-based Drug Discovery》. John Wiley & Sons. 505쪽. ISBN 9783527607495. 8 September 2017에 원본 문서에서 보존된 문서.
- ↑ Kane, Brigid M. (2008). 《HIV/AIDS Treatment Drugs》. Infobase Publishing. 56쪽. ISBN 9781438102078. 8 September 2017에 원본 문서에서 보존된 문서.
- ↑ 가 나 World Health Organization (2019). 《World Health Organization model list of essential medicines: 21st list 2019》. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ “International Drug Price Indicator Guide”. 《ERC》. 2016년 11월 20일에 확인함.
- ↑ “NADAC as of 2016-12-07 | Data.Medicaid.gov”. 《Centers for Medicare and Medicaid Services》. 21 December 2016에 원본 문서에서 보존된 문서. 12 December 2016에 확인함.
- ↑ “Abacavir Adverse Reactions”. 《Epocrates Online》.
- ↑ Professional Drug Facts
- ↑ “Abacavir”. 《AIDSinfo》. 6 March 2017에 원본 문서에서 보존된 문서. 8 November 2016에 확인함.
- ↑ Mallal S, Phillips E, Carosi G, 외. (2008). “HLA-B*5701 screening for hypersensitivity to abacavir”. 《New England Journal of Medicine》 358 (6): 568–579. doi:10.1056/nejmoa0706135. PMID 18256392.
- ↑ Rauch A, Nolan D, Martin A, 외. (2006). “Prospective genetic screening decreases the incidence of abacavir hypersensitivity reactions in the Western Australian HIV cohort study”. 《Clinical Infectious Diseases》 43 (1): 99–102. doi:10.1086/504874. PMID 16758424.
- ↑ Dean L (2015). 〈Abacavir Therapy and HLA-B*57:01 Genotype〉. Pratt VM, McLeod HL, Rubinstein WS, 외. 《Medical Genetics Summaries》. National Center for Biotechnology Information (NCBI). PMID 28520363. Bookshelf ID: NBK315783. 2019년 1월 14일에 확인함.
- ↑ Product Information: ZIAGEN(R) oral tablets, oral solution, abacavir sulfate oral tablets, oral solution. ViiV Healthcare (per Manufacturer), Research Triangle Park, NC, 2015.
- ↑ Crimmins MT, King BW (1996). “An Efficient Asymmetric Approach to Carbocyclic Nucleosides: Asymmetric Synthesis of 1592U89, a Potent Inhibitor of HIV Reverse Transcriptase”. 《The Journal of Organic Chemistry》 61 (13): 4192–4193. doi:10.1021/jo960708p. PMID 11667311.
Further reading
- Dean L (April 2018). 〈Abacavir Therapy and HLA-B*57:01 Genotype〉. Pratt VM, McLeod HL, Rubinstein WS, 외. 《Medical Genetics Summaries》. National Center for Biotechnology Information (NCBI). PMID 28520363.
External links
- “Abacavir”. 《Drug Information Portal》. U.S. National Library of Medicine.
- Abacavir pathway on PharmGKB
- Abacavir dosing guidelines from the Clinical Pharmacogenetics Implementation Consortium (CPIC)
- Abacavir dosing guidelines from the Dutch Pharmacogenetics Working Group (DPWG)
