심장박출량
심장박출량[1](心臟搏出量, 영어: cardiac output) 또는 심박출량(心搏出量)은 심장의 심실이 시간 당 뿜어내는 혈액의 양을 가리키는 심장학 용어이다. 그만큼의 혈액이 온몸순환과 허파순환을 흐르게 되므로 순환계의 기능을 따질 때 반드시 고려하여야 할 중요한 변수가 된다.[2] 수식적으로 심장박출량()은 심박수()와 일회박출량()의 곱과 같다.
건강한 성인이 가만히 있을 때 박출량은 약 70-80 mL, 심박수는 분당 약 60-75회이므로, 심장박출량은 분당 5 L 정도로 추산된다.[3] 그러나 심장박출량의 값은 나이·체격·운동·기초대사율 등 다양한 요인으로 말미암아 크게 달라진다.[2] 예컨대 마라톤 선수가 달리기를 할 때는 심장박출량이 7배까지도 상승할 수 있다.[4]
심장박출량과 밀접하게 연관된 개념은 정맥에서 심장으로 들어가는 혈액의 흐름을 가리키는 복귀 정맥혈(영어: venous return)이다. 순환계통이 정상 상태(steady state)를 이루어 어디에서도 혈액이 쌓이거나 빠져나오는 일이 없다면 심장박출량과 복귀 정맥혈은 반드시 서로 같다.[2] 하지만 정상 상태가 아니면 두 변수의 값은 서로 달라질 수 있다. 두 변수의 결정 요인 역시 다르다. 심장박출량을 직접 결정하는 것은 심장 기능인 반면 복귀 정맥혈은 주로 말초혈관계의 상태에 의존한다.[5][6] 20세기 중반 미국의 생리학자 아서 가이튼은 심장과 말초혈관계가 서로 영향을 주고받는 과정에서 심장박출량 및 복귀 정맥혈이 결정되는 방식을 일련의 실험과 수학적 모형으로 해명하였다.[7] 가이튼의 모형은 오늘날 심장생리학의 표준적인 설명으로 자리 잡았다.[8][9]
심장박출량 및 복귀 정맥혈은 심장 기능과 말초혈관계 기능에 모두 영향을 받는다. 가이튼을 비롯한 일부 생리학자는 이 가운데 혈관 기능의 중요성을 특히 강조하였다. 이들의 견해에 따르면, 정상적인 상황에서 심장은 유입되는 혈액을 그대로 내뿜는 역할을 한다. 따라서 심장박출량을 결정하는 데에 핵심적인 역할을 하는 것은 심장 기능보다도 오히려 말초순환계와 관련된 요인들이다. 대체로 조직은 저마다 필요에 알맞게 관류를 조절한다. 예컨대 조직의 산소 소모량이 증가하면 주변 혈관이 확장되어 혈류량이 늘어나는 식이다. 복귀 정맥혈은 이처럼 몸 곳곳에서 요구하는 혈류량의 총합이며, 심장 기능이 정상이라면 이것이 곧 심장박출량이 된다. 따라서 심장박출량을 결정하는 것은 조직·기관의 관류 요구량이다.[2][10] 가이튼의 모형이 널리 받아들여진 것과 달리, 말초혈관계와 복귀 정맥혈의 역할을 중시한 가이튼의 해석은 지금까지도 논쟁의 대상이 되고 있다.[7][11][12][13][14][15]
가이튼 모형
[편집]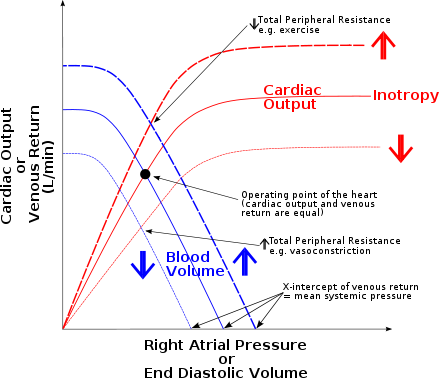
가이튼 모형(Guyton model)에서는 한편으로 심장과 허파가 어떻게 심장박출량을 결정하는지 따지고, 다른 한편으로는 온몸순환을 이루는 말초혈관계가 복귀 정맥혈을 조절하는 과정을 따진다.[5] 이때 두 가지 혈류가 어떻게 균형을 이루는지 해명하는 것이 문제로 된다. 심장박출량과 복귀 정맥혈은 일시적으로 서로 달라질 수 있다. 그 격차를 제때 조정하지 않아 불균형 상태가 지속된다면, 혈액이 계속 쌓이거나 부족해져 혈액 순환이 지장을 받을 것이다. 따라서 순환계통이 원활하게 작동하는 원리를 이해하려면 심장박출량과 복귀 정맥혈의 격차를 조정하여 정상 상태를 유지하는 기제가 무엇인지 밝혀야 한다. 이 기제를 매개하는 핵심 변수는 바로 오른심방압력 또는 중심정맥압이다.[16]
심장박출량과 복귀 정맥혈이 다르면 중심정맥계(central venous compartment), 즉 우심방 및 가슴안의 대혈관으로 둘러싸인 공간의 부피가 변한다. 심장박출량이 더 크면 혈액이 빠져나가 부피가 작아지고, 복귀 정맥혈이 더 크면 혈액이 쌓여 부피가 커진다. 이 공간은 탄성이 있는 조직으로 둘러싸여 있기 때문에 부피가 변하면 압력 즉 중심정맥압도 함께 변하게 된다. 실험을 통해 중심정맥압이 높을수록 심장박출량은 크고 복귀 정맥혈은 작은 경향이 있음이 밝혀졌다. 즉 심장박출량과 복귀 정맥혈의 격차에 반응하여 중심정맥압이 변화하며, 이에 따라 격차가 줄어드는 쪽으로 두 혈류량이 조정됨으로써 정상 상태가 유지되는 것이다. 이런 의미에서 중심정맥압은 일종의 '오류 신호(error signal)' 역할을 한다고 볼 수 있다.[6][8][16]
가이튼은 중심정맥압을 매개로 심장박출량과 복귀 정맥혈이 조절되는 기제를 시각적으로 나타내는 방법을 고안하였다.[17] 가로축이 오른심방압력 또는 중심정맥압에 해당하고 세로축이 혈류량에 해당하는 평면을 그리면, 심장박출량과 중심정맥압의 관계를 나타낸 심장기능곡선 또는 심박출량곡선은 우상향하고, 복귀 정맥혈과 중심정맥압의 관계를 나타낸 혈관기능곡선 또는 정맥 복귀 곡선은 우하향한다.[7][9][18] 정상 상태에서 심장박출량과 복귀 정맥혈은 서로 같아야 하며, 오른심방압력은 두 변수에 공통으로 관여하는 하나의 값이다. 따라서 두 곡선이 만나는 점의 세로 좌표가 정상 상태의 심장박출량이자 복귀 정맥혈이 되고, 가로 좌표가 정상 상태의 오른심방압력이 될 수밖에 없다.[5] 일시적인 변동으로 오른심방압력이 이 값에서 벗어나더라도, 변동을 되돌리려는 방향으로 심장박출량과 복귀 정맥혈이 변화하므로 곧 정상 상태가 회복된다.[19] 이처럼 두 곡선을 같은 평면에 나타낸 것을 가이튼 그림(영어: Guyton diagram, Guyton's cross plot)이라 부른다.[8][20]
심박출량곡선
[편집]심박출량곡선이 우상향하는 한 가지 이유는 프랑크-스탈링 법칙이다. 중심정맥압이 높을수록 이완기말압력이 높고, 따라서 심근이 많이 늘어나 있게 되므로 더 강하게 수축하여 박출량이 커진다. 또다른 이유는 심방이 확장될수록 심박수도 빨라지기 때문이다. 우심방이 확장되면 굴심방결절이 직접 영향을 받아 심박수가 높게는 10-15%까지 상승한다. 우심방 확장은 또한 교감신경을 매개로도 심박수를 상승시키는데 이를 베인브리지 반사라고 부른다.[2] 물론 심장이 혈액을 무한정 많이 뿜어낼 수는 없으므로, 오른심방압력이 일정 정도 이상 높아지는 영역에 이르면 심박출량곡선은 차츰 완만해지다가 평평해진다. 심박출량곡선의 최댓값은 보통 분당 13 L 정도이다.[21]

심박출량곡선의 기울기 및 최댓값은 심장 기능을 반영한다. 심장 기능이란 매우 다양한 요인을 포괄하지만, 결과적으로 심박출량곡선의 기울기가 가팔라서 같은 오른심방압력에서도 심장박출량이 더 크다면 심장 기능이 더 좋은 것이라고 말할 수 있다.[22] 심장 기능을 강화하는 대표적인 요인 한 가지는 자율신경계의 작용이고, 또 다른 한 가지는 심근의 적절한 비대이다. 교감신경이 작용하면 심장이 더 효율적으로 수축하여, 심박출량곡선의 최댓값이 크게는 2배까지 상승한다. 또한 적절한 운동은 심근 비대를 유발한다. 마라톤 선수는 심장이 일반인보다 50-75%가량 무거워서 심박출량곡선의 최댓값이 일반인의 1.6-2배에 이른다. 마라톤 선수가 달리기를 할 때에는 두 요인이 함께 작용하여, 심박출량곡선의 최댓값을 일반인의 2.5배 수준인 분당 30-40 L까지 끌어올린다. 한편 심근·심장판막·심장 전기 전도계에 영향을 미치는 다양한 질병으로 말미암아 심장 기능이 악화할 수 있다.[21]
심박출량곡선이 가로축과 만나는 점은 곧 심방이 전혀 확장되어 있지 않아 심장박출량이 0인 상태를 나타낸다. 이 점의 가로 좌표는 곧 심방 주변 조직의 압력 즉 가슴막안압(영어: intrapleural pressure)에 해당하며, 보통 -4 mmHg 정도이다. 가슴막안압은 다양한 요인에 의해 변화한다. 보통 호흡에 의해 2 mmHg 정도씩 증감하며, 거칠게 숨을 쉬는 경우 50 mmHg까지도 변동할 수 있다. 가슴막안압이 변하면 심박출량곡선도 좌우로 이동하는데, 예컨대 날숨을 쉬어 가슴막안압이 2 mmHg 증가하면 심박출량곡선 전체가 그만큼 오른쪽으로 평행이동하게 된다.[5][20]
정맥 복귀 곡선
[편집]가이튼은 개의 오른심장을 들어내어 기계식 펌프로 대체하는 실험을 통해 정상 상태에서 복귀 정맥혈과 오른심방압력 사이의 관계를 알아보았다. 오른심방압력을 가로축, 정상 상태 복귀 정맥혈을 세로축에 나타내었을 때, 두 변수의 관계는 우하향하는 직선의 모양새를 띠는 것으로 드러났다.[23] 이러한 관계가 성립하는 까닭은 오른심방압력이 복귀 정맥혈을 거스르는 일종의 배압(back pressure)으로 작용하기 때문이라고도 생각할 수 있고[5], 복귀 정맥혈이 곧 심장박출량인 정상 상태에서 심장이 효과적으로 혈액을 정맥계에서 동맥계로 옮길수록 오른심방압력이 감소하기 마련인 이치라고도 이해할 수 있다.[11][13][19][24]
심장박출량이 무한정 커질 수 없듯이, 복귀 정맥혈이 증가하는 데에도 한계가 있다. 오른심방압력이 약 -2 mmHg 미만으로 매우 낮아지면 가슴안으로 들어가는 큰 정맥들의 혈관벽이 음압 때문에 서로 달라붙어 버리는 허탈(collapse)이 일어난다. 이를 고려하면 정맥 복귀 곡선은 전체적으로 오른심방압력이 양의 값인 영역에서는 우하향하는 직선이다가, 오른심방압력이 낮은 쪽 영역으로 넘어가면 완만해져서 결국 수평한 직선으로 이어지는 모양새이다.[5]
정맥 복귀 곡선의 가로 절편은 복귀 정맥혈이 0일 때, 즉 온몸순환이 정지했을 때의 오른심방압력에 해당한다. 그런데 혈액의 흐름이 없으면 압력차가 없어서 온몸순환을 이루는 말초혈관계 전체의 혈압이 이 값으로 똑같을 것이다. 그러므로 이 압력 값은 온몸의 혈관에 혈액이 들어차 있는 정도를 반영하리라고 생각할 수 있으며, 따라서 평균 전신 충만압이라고 부른다. 실험적으로 측정된 평균 전신 충만압은 7 mmHg 정도이다. 한편 가로 절편이 같을 때, 직선이 가파를수록 일정한 가로 좌표에 대한 세로 좌표 값이 크다. 즉 동일한 평균 전신 충만압 및 오른심방압력 값이 주어졌을 때 복귀 정맥혈이 더 크다는 뜻이다. 압력 조건과 혈류량의 관계를 매개한다는 점에서 직선의 기울기가 일종의 저항을 반영한다고 생각할 수 있다. 따라서 직선의 기울기의 역수를 정맥 복귀 저항(영어: resistance to venous return)이라고 부른다.[5][25]
이상의 정의를 종합하면 복귀 정맥혈의 수식을 얻는다.
여기서 와 은 각각 정상 상태의 오른심방압력과 복귀 정맥혈을 가리키며, 는 평균 전신 충만압을, 는 정맥 복귀 저항을 가리킨다.[5]
심장박출량과 심장 기능
[편집]
심장박출량은 박출량과 심박수의 곱으로 주어지며, 박출량은 다시 전부하·후부하·수축력에 의해 결정된다. 따라서 전부하·후부하·수축력·심박수에 영향을 미치는 요인이라면 무엇이든 심장 기능을 변화시킬 수 있다.[26]
전부하
[편집]전부하란 심근이 수축을 시작하기 직전에 늘어나 있는 정도를 뜻하며, 프랑크-스탈링 법칙에 의해 전부하가 클수록 박출량도 대체로 크다. 이때 오른심방압력을 전부하의 척도로 보면, 전부하의 영향은 심박출량곡선에 이미 반영되어 있다고 생각할 수 있다.[15] 하지만 심근이 늘어난 정도와 가장 직접 관련이 있는 변수는 압력이 아니라 부피이다. 이완기말 압력-용적 관계(영어: end-diastolic pressure-volume relation, EDPVR)는 전부하에 영향을 미치는 여러 다른 요인에 영향을 받기 때문에 사람에 따라, 같은 사람이라도 상황에 따라 달라질 수 있다. 그러면 같은 값일 때 심실이 채워지는 정도가 달라지므로 심박출량곡선의 모양이 변하게 된다.[22][27]
이완기말 압력-용적 관계는 이완 상태의 심실이 늘어나기 쉬운 정도, 즉 심실의 수동적 유순도(영어: passive compliance)를 나타낸다. 심근이 심근 경색 등으로 손상을 받거나 비대증으로 두꺼워지면, 같은 부피만큼 늘어나기 위해 심실벽에 가해져야 하는 압력이 커진다. 심장을 둘러싸는 심막에 질병이 생겨 뻣뻣해져도 마찬가지이다.[22][27] 고려하여야 할 또다른 요인은 심실 상호의존성(영어: ventricular interdependence)이다. 우심실과 좌심실은 근섬유를 공유하며, 심실중격 및 심막을 통해 한쪽의 압력이 다른 쪽으로 전파된다. 따라서 한쪽 심실에 혈액이 많이 들어차면 나머지 한쪽 심실의 유순도가 저하된다. 심막이 뻣뻣할 때 심실 상호의존성은 더욱 두드러진다.[22]
후부하
[편집]후부하는 심실이 수축을 시작한 후 대동맥판이 열리고 나서부터 심실이 대동맥으로 혈액을 뿜어내기 위해 심실벽에서 유지되어야 하는 응력을 가리킨다. 동맥계에서 심실의 수축을 거세게 저항할수록 대동맥판이 더 일찍 닫힐 것이므로, 같은 양의 혈액을 뿜어내기 위해서는 심실이 더 강하게 수축해야 할 것이다. 즉 후부하에 영향을 미치는 요인은 주로 동맥계의 혈역학적 특성이며, 다른 조건이 일정할 때 후부하가 클수록 심장박출량은 감소한다.[27][28] 보통 대동맥의 혈압이 높을수록 심실이 더 강하게 수축해야 대동맥판이 열릴 것이므로 후부하가 크다고 본다. 다만 대동맥의 혈압은 심실이 수축하는 동안에도 이완기혈압과 수축기혈압 사이에서 크게 변동하므로, 평균동맥압을 후부하의 근사적인 척도라고 간주하곤 한다.[26] 물론 실제로 동맥으로 혈액이 방출되는 과정은 매우 복잡하기 때문에 후부하는 단순히 평균동맥압에 비례하지 않는다.[22][28]
후부하에 영향을 미치는 또다른 중요한 요인은 심실의 크기이다. 심근이 수축하면서 발생하는 힘의 방향은 심실벽 표면에 수직인 방향이 아니라 표면과 나란한 방향이다. 이 힘이 벽에 수직인 방향의 압력(벽면횡단압력, 영어: transmural pressure)으로 전환될 수 있는 까닭은 심실이 둥그렇기 때문이다. 심실벽이 안쪽으로 굽어 있기에, 표면과 나란한 방향의 힘을 모두 합치면 알짜힘은 심실 안쪽을 향하게 되는 것이다. 따라서 심실의 부피가 커서 심실벽이 상대적으로 평평하면 심근이 똑같이 수축하더라도 작은 압력만이 발생한다. 이러한 관계를 수학적으로 표현한 것이 라플라스 법칙이다. 심실의 모양을 구로 어림하였을 때, 심실벽의 응력 와 벽면횡단압력 사이에는 다음과 같은 관계식이 성립한다.
여기서 는 심실의 반지름, 는 심실벽의 두께를 가리킨다. 이처럼 심실 반지름이 클수록 같은 압력을 생성하기 위해 심근이 더 강하게 수축해야 하므로 후부하도 크다.[28][29]
심박수
[편집]심박수와 심장박출량 사이의 관계는 단순하지 않다. 일반적으로 심박수가 박출량과 더불어 심장박출량을 결정하는 독립적인 요인인 것처럼 기술되곤 하지만, 실제로는 전부하·후부하·수축력을 매개로 박출량에 영향을 미치기 때문이다. 예컨대 심박수가 증가하면 심실에 혈액이 찰 시간이 줄어들기 때문에 전부하는 감소한다. 한편 심근 수축을 유발하는 칼슘 이온이 미처 다 제거되기 전에 다음 수축이 시작되므로 수축력은 증가하는 경향이 있다. 이러한 기제가 종합적으로 작용하여, 심박수가 증가할수록 박출량은 줄어든다. 그런데 심박수가 100회 미만일 때에는 박출량이 줄어드는 정도가 완만한 반면, 심박수가 200회 이상으로 몹시 빨라지면 박출량이 심박수 증가를 상쇄하기에 충분할 만큼 많이 감소한다. 결과적으로 심박수와 심장박출량 사이 관계는 대략 뒤집어진 U자 모양 곡선으로 그려진다.[30]
복귀 정맥혈과 혈관 기능
[편집]혈관의 확장성
[편집]
혈관계의 중요한 특징은 혈관벽이 탄성이 있어 늘어날 수 있다는 것이다. 동맥의 탄성 덕분에 심장이 주기적으로 수축하는 압력 변동이 완화되므로, 모세혈관에 전달되는 혈압은 일정하고 안정적이다. 한편 정맥은 압력이 거의 변하지 않은 채로 크게 늘어날 수 있으므로 혈액을 저장하는 역할을 담당한다.[31] 이 같은 특성 때문에, 혈관계를 단단한 파이프로 이루어진 배관계와 같이 생각할 수 없다.[10]

혈관벽이 늘어나기 쉬운 정도를 정량적으로 나타내는 한 가지 척도는 용량(영어: capacitance) 또는 유순도(영어: compliance)이다. 혈관에 부피 만큼 혈액이 더 들어찼을 때 혈관벽에 가해지는 압력이 만큼 변한다면, 혈관의 유순도 는
로 정의된다. 유순도는 부피 탄성 계수의 역수와 비슷하게 계산되지만, 부피 탄성 계수를 셈할 때 중요한 값은 현재 부피에 대한 상대적인 변화율()인 반면 유순도를 셈할 때에는 절대적인 부피 변화량()이 사용된다는 차이가 있다. 따라서 부피 탄성 계수가 똑같아도 전체 부피가 크면 유순도의 값도 크다. 동맥에 비해 정맥은 부피가 약 3배 크고 부피 탄성 계수가 약 8배 작으므로 유순도는 약 24배 높다.[31]
혈관의 부피 변화를 따질 때 고려하여야 할 또다른 사항은, 혈관벽이 축 늘어져 있기 때문에 혈액을 조금만 채우면 혈관벽에 압력을 가하지 않을 수도 있다는 점이다. 풍선에 숨을 불어넣을 때 얼마간 부풀기 전까지는 풍선이 탱탱해지지 않고 늘어진 채로 있는 이치와 같다. 이처럼 혈관벽에 조금이라도 압력을 가하려면 먼저 일정량의 혈액을 채워야 하며, 부피를 그보다 더 늘릴 때에야 비로소 유순도에 의해 정의되는 만큼 압력이 증가하기 시작한다. 압력 변화의 기준이 되는 이 부피 값을 비부하용적(영어: unstressed volume)이라고 하며, 혈관에 들어 있는 혈액 가운데 비부하용적만큼을 제외하고 남은 부피를 부하용적(영어: stressed volume)이라고 부른다.[25] (물론 이는 추상적인 구분으로, 실제로 부하용적만큼의 혈액만이 혈관벽에 압력을 가하고 있는 것은 아니다. 혈관 안의 혈액은 어디에서나 똑같이 압력을 받고 있다. 이처럼 혼동을 야기하기 쉽다는 이유로, '비부하용적'과 '부하용적' 대신 '안정부피(영어: rest volume)'와 '동적 부피(영어: dynamic volume)'라는 용어를 사용하자는 주장이 제기되기도 했다.[13][14])
혈관의 압력-부피 관계는 다양한 요인으로 변화한다. 대표적인 예는 교감신경의 작용으로 혈관 주변 민무늬근이 수축하는 경우이다. 이처럼 혈관긴장도(영어: vascular tone)가 증가하면 부피가 똑같아도 혈관벽에 가해지는 압력이 강해진다. 이때 혈관의 압력-부피 곡선을 살펴보면, 기울기가 일정한 채로 평행이동하는 경향이 있다. 즉 혈관의 유순도는 크게 변하지 않으며, 주로 변하는 것은 부하용적-비부하용적의 분배이다.[32]
수학적 모형
[편집]온몸순환만을 고려할 때, 정맥 복귀 곡선의 수식을 다음처럼 도출할 수 있다. 동맥계가 시작하는 지점부터 정맥계가 끝나는 지점까지 말초혈관계통이 한 줄로 이어져 있다고 가정하고, 원점 즉 대동맥에서의 혈압을 , 온몸순환의 끝 즉 우심방에서의 혈압을 라고 하자. 정상 상태에서는 순환계통의 어느 지점에서든 통과하는 혈류량이 같아야 하며, 이 값이 곧 심장박출량이자 복귀 정맥혈 가 될 것이다. 그러면 온몸순환의 총 저항 는 다음처럼 정의된다.
이제 동맥계가 시작하는 지점을 원점으로 생각하고, 그로부터 만큼 나아간 특정 지점의 혈압을 라고 하며, 원점부터 그 지점까지의 말초혈관계통을 한 덩어리로 간주하였을 때의 총 부하용적, 총 저항, 총 유순도를 각각 , , 라고 하자. 그리고 지점 에서 출발하여 짧은 거리 만큼 나아갔을 때, 두 지점 와 사이의 분절이 갖는 부하용적, 저항, 유순도를 각각 , , 라고 하자. 이를 원점에서 정맥계의 끝까지 적분한 값은 온몸순환의 총 부하용적, 저항, 유순도와 같다.
- , ,
이때 유순도의 정의에 따라
이고, 저항의 정의에 따라
이므로, 대입하여 정리하면 다음을 얻는다.
즉 복귀 정맥혈과 오른심방압력 사이에는 선형 관계가 성립하며 그 기울기는 음수이다. 이 식을 복귀 정맥혈에 대한 가이튼의 수식
과 견주어 보면, 평균 전신 충만압 와 정맥 복귀 저항 가 다음처럼 주어짐을 알 수 있다.[7]
평균 전신 충만압
[편집]평균 전신 충만압 는 순환계의 총 부하용적 와 총 유순도 의 비로 주어진다. 혈관계의 유순도는 대체로 일정하기 때문에[32], 평균 전신 충만압이 변하는 경우는 대개 혈액의 전체 부피가 변하거나 혹은 전체 혈액 중 비부하용적과 부하용적의 비중이 변하는 경우이다.[5] 전자의 대표적인 예는 출혈과 수혈이다. 후자의 대표적인 예는 자율신경계의 작용이다. 교감신경이 비부하용적을 부하용적으로 모집(recruit)하는 작용은 매우 효율적이어서, 전체 혈액의 25%가량을 출혈로 잃어버리더라도 혈액순환이 거의 정상에 가깝게 이루어질 수 있다.[25][31]
정맥 복귀 저항
[편집]정맥 복귀 저항 공식
의 의미를 따져 보면, 순환계통의 모든 지점마다 그곳에서부터 정맥계 끝까지의 누적된 저항 을 구한 다음, 그 부위의 유순도의 상대적 크기 만큼 가중치를 주어 가중평균을 셈한 값이다.[7] 부분적분을 적용하여 수식을 변형하면 그 함의를 한결 분명히 알아볼 수 있다.
이 수식에 따르면 정맥 복귀 저항이란 순환계통 곳곳의 저항 에 라는 가중치를 주어 가중평균을 셈한 것이다. 이때 는 동맥계의 시작에서부터 특정 지점까지의 누적된 유순도를 가리키므로, 같은 저항이라도 동맥계 쪽에 위치한 것보다 정맥계 쪽에 위치한 것이 정맥 복귀 저항에 크게 기여한다. 더군다나 정맥계의 유순도는 동맥계의 약 30배에 이른다. 따라서 정맥 복귀 저항은 주로 정맥계 저항에 좌우된다. 전체 정맥 복귀 저항에서 차지하는 비중은 동맥계 저항이 1/3, 정맥계 저항이 2/3 정도라고 추산된다.[5][7]
정맥 복귀 저항의 정의가 이처럼 미묘한 것은 혈관계의 확장성 때문이라고 이해할 수 있다. 어떤 이유로 정맥계 특정 부분의 저항이 증가하면 그보다 상류의 혈압이 상승한다. 정맥계는 매우 유순하므로, 압력이 조금만 커지더라도 부피가 크게 늘어난다. 정맥계에 혈액이 고여서 심장으로 유입되지 못하므로 정맥 복귀가 지장을 받는다. 반면 동맥계 특정 부분의 저항이 증가하면, 그보다 상류에 있는 동맥들의 유순도가 매우 낮기 때문에 혈압이 크게 상승한다. 이 때문에 심장에 가해지는 후부하가 커질 수는 있겠으나, 심장 기능이 이를 감당하기에 충분하기만 하다면 압력차 상승이 저항 증가를 상쇄하여 복귀 정맥혈은 크게 달라지지 않는다.[5][33]
심장의 허용적 역할
[편집]심장박출량 및 복귀 정맥혈의 결정 과정에서 심장 기능보다 말초혈관계 기능이 중요한 까닭으로 순환계통의 다음과 같은 특성이 거론되었다.[10]
- 심장은 수동적으로 채워질 뿐, 음압을 형성하여 능동적으로 혈액을 빨아들이지 않는다. 심근이 수축할 때에는 에너지가 사용되지만 이완할 때에는 사용되지 않는다.
- 혈관 벽은 강직되어 있는 것이 아니라 탄성이 있다. 특히 정맥은 매우 유순하여, 혈액이 들어오면 곧바로 흘러나가는 것이 아니라 혈관 벽을 늘리면서 그 자리에 고일 수 있다.
심장이 혈액순환에서 담당하는 허용적 역할(permissive role)은 다음처럼 비유된 바 있다.
| “ | 이 유형 펌프의 예로는 방광이 있다. 방광은 축 늘어져 있고 그 속은 비어 있으며, 음압을 형성하거나 수뇨관·콩팥으로부터 빨아들이지 않는다. 비워질 때에만 에너지를 사용한다. 방광에서 소변을 배출하는 빈도와 1회 소변량을 곱함으로써 주어진 시간 동안 소변의 흐름을 계산할 수는 있겠다. 그러나 (···) 이러한 유형의 펌프는 일을 함으로써 흐름을 만들어내기는 하지만, 그 출력은 오로지 외부 요인(예컨대 콩팥 기능)에 의해서만 결정된다. 소변 생산량이 일정할 때, 소변 배출 빈도와 1회 소변량은 서로의 역수이다. 방광을 두 배 자주 비우면 한 번에 배출되는 소변량은 절반이 된다. | ” |
— 로버트 앤더슨, 《심혈관계통의 거시 생리학》[10]
|
가이튼 모형에 대한 비판
[편집]중심정맥압의 역할
[편집]
가이튼은 개에서 오른심방압력과 복귀 정맥혈의 관계를 측정한 실험을 보고하면서 오른심방압력이 통제변인, 복귀 정맥혈이 종속변인인 것처럼 기술하였고, 두 변수의 관계를 그래프로 그릴 때에도 오른심방압력을 가로축에, 복귀 정맥혈을 세로축에 나타내었다.[23] 그러나 가이튼의 실험 조건을 비판적으로 분석한 일부 학자들은 오히려 복귀 정맥혈이 통제변인 역할을 했는데 가이튼이 인과관계를 혼동했던 것이라고 지적했다. 따라서 그래프를 그릴 때에는 복귀 정맥혈을 가로축에 나타내는 것이 더 적절하며, 가이튼이 제안한 '정맥 환류 곡선'(venous return curve)이라는 이름 역시 복귀 정맥혈이 종속변수인 듯한 인상을 주므로 '혈관 기능 곡선'(vascular function curve)이라는 이름으로 대체하자고도 주장하였다.[11][18] 오늘날 일부 심장생리학 교과서는 이러한 비판을 받아들여 혈관기능곡선을 소개할 때에는 복귀 정맥혈을 가로축에 나타내되, 정상 상태를 분석할 목적으로 혈관기능곡선을 심박출량곡선과 겹쳐 놓아야 할 때에만 가로·세로축을 통일하기 위해 불가피하게 그래프를 뒤집는다고 설명하기도 한다.[9]
한편 가이튼은 통제된 실험 환경에서와 달리 생체 내에서는 오른심방압력이 심장박출량·복귀 정맥혈을 결정하는 독립변수가 아니라고 보았다. 오른심방압력과 관련해서 심장이 정맥계에서 동맥계로 혈액을 옮기는 한 가지 기제와 정맥계로부터 우심방으로 혈액이 흘러 들어오는 또다른 기제가 동시에 작용하고 있기 때문이다.[34] 심장 기능과 혈관 기능의 균형에 따라 정상 상태의 오른심방압력 및 심장박출량·복귀 정맥혈이 동시에 결정되므로[17], 무엇이 독립변수이고 종속변수인지 따지는 것은 무의미하다고 보았다.[6]
| “ | 오른심방압력이 심장박출량의 주된 결정 요인 중 하나인 것이 아니라, 오히려 오른심방압력이 심장박출량과 더불어 동시에 결정되는 것이다.
[R]ight atrial pressure is not one of the primary determinants of cardiac output but, instead, is itself determined simultaneously along with cardiac output. |
” |
— 아서 가이튼[17]
|
오늘날 가이튼 모형의 지지자들도 대체로 이와 같은 입장이지만[7][19][35], 일부 학자들은 중심정맥압이 심장박출량·복귀 정맥혈을 결정하는 데에 중요한 독립변수라고 그 역할을 강조하였다.[8] 특히 중심정맥압이 심박출량곡선의 가로축에 놓여 전부하를 나타낸다는 점에 주목하여, 수혈·출혈 등으로 전체 혈액량이 변하면 중심정맥압도 변화하며 프랑크-스탈링 법칙에 따라 심장박출량 역시 변화한다는 식으로 설명하곤 하였다.[36] 가이튼 모형을 비판하는 학자들은 의사가 이와 같은 설명을 곧이곧대로 받아들인다면, 오른심방압력이 체액량의 지표이니 오른심방압력이 낮으면 무조건 수액 투여가 필요한 것으로 오해할지도 모른다고 지적하였다.[12] 가이튼 모형의 통상적 해석에 따른다면 체액량과 가장 밀접하게 연관된 변수는 오른심방압력이 아니라 평균 전신 충만압이며, 수액 투여 시 심장박출량이 개선될지 여부(영어: volume responsiveness)는 심박출량곡선까지 함께 고려하여야 하므로 단순하게 판단하기 어렵다.[37]
같이 보기
[편집]- 일회박출량(stroke volume)
- 박출작업량(stroke work)
- 확장기말 용적(end-diastolic volume)
- 수축기말 용적(end-systolic volume)
- 심근 수축력(contractility, 심근 수축성)
- 전부하(preload)
- 후부하(afterload)
- 아서 가이튼
- 복귀 정맥혈
- 중심정맥압
- 오른심방압력
각주
[편집]- ↑ 대한의협 의학용어 사전 https://www.kmle.co.kr/search.php?Search=cardiac+output&EbookTerminology=YES&DictAll=YES&DictAbbreviationAll=YES&DictDefAll=YES&DictNownuri=YES&DictWordNet=YES
- ↑ 가 나 다 라 마 Hall, Hall, & Guyton, 2021, pp. 245-246.
- ↑ Herring, Paterson, & Levick, 2018, p. 6.
- ↑ Hall, Hall, & Guyton, 2021, p. 261.
- ↑ 가 나 다 라 마 바 사 아 자 차 카 Hall, Hall, & Guyton, 2021, pp. 250-254.
- ↑ 가 나 다 Kenny, 2020, pp. 336-338.
- ↑ 가 나 다 라 마 바 사 Sunagawa, Kenji (2017년 7월). “Guyton’s venous return curves should be taught at medical schools (complete English translation of Japanese version)”. 《The Journal of Physiological Sciences》 (영어) 67 (4): 447–458. doi:10.1007/s12576-017-0533-0. ISSN 1880-6546.
- ↑ 가 나 다 라 Herring, Paterson, & Levick, 2018, pp. 97-98.
- ↑ 가 나 다 Pappano, & Wier, 2019, pp. 187-188.
- ↑ 가 나 다 라 Anderson, 2012, pp. 3-5.
- ↑ 가 나 다 Beard, Daniel A.; Feigl, Eric O. (2011년 9월). “Understanding Guyton's venous return curves”. 《American Journal of Physiology-Heart and Circulatory Physiology》 (영어) 301 (3): H629–H633. doi:10.1152/ajpheart.00228.2011. ISSN 0363-6135. PMC 3191500. PMID 21666119.
- ↑ 가 나 Beard, Daniel A.; Feigl, Eric O. (2013년 12월). “CrossTalk opposing view: Guyton's venous return curves should not be taught”. 《The Journal of Physiology》 (영어) 591 (23): 5795–5797. doi:10.1113/jphysiol.2013.260034. ISSN 0022-3751.
- ↑ 가 나 다 Brengelmann, George L. (2019년 11월 1일). “Venous return and the physical connection between distribution of segmental pressures and volumes”. 《American Journal of Physiology-Heart and Circulatory Physiology》 (영어) 317 (5): H939–H953. doi:10.1152/ajpheart.00381.2019. ISSN 0363-6135.
- ↑ 가 나 Dalmau, Rafael (2019년 11월 1일). “Venous return: a fresh start”. 《American Journal of Physiology-Heart and Circulatory Physiology》 (영어) 317 (5): H1102–H1104. doi:10.1152/ajpheart.00575.2019. ISSN 0363-6135.
- ↑ 가 나 Persichini, Romain; Lai, Christopher; Teboul, Jean-Louis; Adda, Imane; Guérin, Laurent; Monnet, Xavier (2022년 12월). “Venous return and mean systemic filling pressure: physiology and clinical applications”. 《Critical Care》 (영어) 26 (1). doi:10.1186/s13054-022-04024-x. ISSN 1364-8535.
- ↑ 가 나 Harris, David M., 편집. (2023). 〈Hemodynamic Interactions〉. 《Mohrman and Heller's Cardiovascular Physiology》 10판. New York: McGraw-Hill Education. ISBN 978-1-264-61761-6.
- ↑ 가 나 다 Guyton, Arthur C. (1955년 1월 1일). “Determination of Cardiac Output By Equating Venous Return Curves With Cardiac Response Curves”. 《Physiological Reviews》 (영어) 35 (1): 123–129. doi:10.1152/physrev.1955.35.1.123. ISSN 0031-9333.
- ↑ 가 나 Levy, M N (1979년 6월). “The cardiac and vascular factors that determine systemic blood flow.”. 《Circulation Research》 (영어) 44 (6): 739–747. doi:10.1161/01.RES.44.6.739. ISSN 0009-7330.
- ↑ 가 나 다 Boulpaep, Emile L. (2017). 〈Regulation of Arterial Pressure and Cardiac Output〉. Boron, Walter F.; Boulpaep, Emile L. 《Medical physiology》 3판. Philadelphia, PA: Elsevier. 549-552쪽. ISBN 978-1-4557-4377-3.
- ↑ 가 나 Kenny, 2020, pp. 64-65.
- ↑ 가 나 Hall, Hall, & Guyton, 2021, pp. 247-248.
- ↑ 가 나 다 라 마 Kenny, 2020, pp. 51-63.
- ↑ 가 나 Guyton, Arthur C.; Lindsey, Arthur W.; Abernathy, Berry; Richardson, Travis (1957년 6월 1일). “Venous Return at Various Right Atrial Pressures and the Normal Venous Return Curve”. 《American Journal of Physiology-Legacy Content》 (영어) 189 (3): 609–615. doi:10.1152/ajplegacy.1957.189.3.609. ISSN 0002-9513.
- ↑ Brengelmann, George L. (2003년 3월 1일). “A critical analysis of the view that right atrial pressure determines venous return”. 《Journal of Applied Physiology》 (영어) 94 (3): 849–859. doi:10.1152/japplphysiol.00868.2002. ISSN 8750-7587.
- ↑ 가 나 다 Kenny, 2020, pp. 44-50.
- ↑ 가 나 Harris, David M., 편집. (2023). 〈The Heart Pump〉. 《Mohrman and Heller's Cardiovascular Physiology》 10판. New York: McGraw-Hill Education. ISBN 978-1-264-61761-6.
- ↑ 가 나 다 Pappano, & Wier, 2019, pp. 179-180.
- ↑ 가 나 다 Courneya, Carol-Ann; Parker, Michael J. (2011). 〈Cardiac Output (Starling Curves): Getting It Started〉. 《Cardiovascular physiology: a clinical approach》. The integrated physiology series 1판. Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins Health. 93-111쪽. ISBN 978-0-7817-7485-7.
- ↑ Herring, Paterson, & Levick, pp. 98-101.
- ↑ Pappano, & Wier, 2019, pp. 193-194.
- ↑ 가 나 다 Hall, Hall, & Guyton, 2021, pp. 183-184.
- ↑ 가 나 Tyberg, John (2002년 10월 1일). “How changes in venous capacitance modulate cardiac output”. 《Pflügers Archiv European Journal of Physiology》 445 (1): 10–17. doi:10.1007/s00424-002-0922-x. ISSN 0031-6768.
- ↑ Anderson, 2012, pp. 10-12.
- ↑ Hall, Hall, & Guyton, 2021, p. 188.
- ↑ Kenny, Jon-Emile S. (2023년 8월 7일). “A framework for heart-lung interaction and its application to prone position in the acute respiratory distress syndrome”. 《Frontiers in Physiology》 14. doi:10.3389/fphys.2023.1230654. ISSN 1664-042X. PMID 37614757.
- ↑ Herring, Paterson, & Levick, 2018, p. 95.
- ↑ Kenny, 2020, pp. 319-327.
참고문헌
[편집]- Anderson, Robert M. (2012). 《The Gross Physiology of the Cardiovascular System》 2판. Tuscon, AZ: Racquet Press. ISBN 978-1105522239.
- Herring, Niel; Paterson, David J.; Levick, J. R. (2018). 《Levick's Introduction to Cardiovascular Physiology》 6판. Boca Raton: CRC Press. ISBN 978-0-8153-6361-3.
- Pappano, Achilles J; Wier, Withrow Gil (2019). <Control of Cardiac Output: Coupling of Heart and Blood Vessels>. 《Cardiovascular Physiology》 11판. Mosby physiology series. Philadelphia: Elsevier. 176-200쪽. ISBN 978-0-32-59484-4.
- Kenny, J. E. (2020). 《An Approach to Mechanical Heart-Lung Interaction》 1판. Toronto: Spectral Envelope Publishing House. ISBN 978-1-7773232-0-2.
- Hall, John E., Hall, Michael E., & Guyton, Arthur C. (2021). 《Guyton and Hall Textbook of Medical Physiology》 14판. Philadelphia: Elsevier. ISBN 978-0-323-59712-8.




![{\displaystyle {\rm {CO_{[L/min]}=SV_{[L/beat]}\times HR_{[beats/min]}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ea7ef88f8919ce5e8d6d086bf7291835f8adf0b7)








































