사이토시스
이 문서는 자연스럽지 않게 번역되었으며, 기계 번역을 통해 작성되었을 수도 있습니다. (2022년 4월) |

사이토시스는 많은 양의 분자가 세포 안팎으로 이동하는 수송 메커니즘이다.
사이토시스에는 세 가지 주요 유형이 있다. 세포 안쪽으로의 이동인 세포내이입, 세포 바깥으로의 이동인 세포외배출, 안팎 둘 다의 이동인 트랜스사이토시스이다.
어원과 발음
[편집]사이토시스(/saɪˈtoʊsɪs/)라는 단어는 세포라는 뜻의 cyto-와 -osis의 결합 형태이다. 이 용어는 1961년 Novikoff에 의해 만들어졌다.[1]
세포내이입
[편집]엔도사이토시스는 세포가 단백질과 같은 분자를 세포막으로 삼켜 세포 외부에서 흡수하는 경우이다. 많은 중요한 물질이 세포막을 통과할 수 없는 큰 극성 분자이기 때문에 대부분의 세포에서 사용된다. 세포내이입의 두 가지 주요 유형은 음세포작용와 식세포작용이다.
음세포작용
[편집]음세포작용은 작은 수성 입자를 인식하는 막 수용체와 함께 흡수하는 것이다. 이는 유체 상 세포내이입의 한 예이며 일반적으로 세포 내에서 연속적인 과정이다. 입자는 clathrin 코팅된 구덩이의 사용을 통해 흡수된다. 이 클라트린으로 코팅된 구덩이는 수명이 짧고 입자를 리소좀으로 전달하기 위한 소포를 형성하는 역할만 한다. 클라트린으로 코팅된 구덩이는 세포질로 침투하여 클라트린으로 코팅된 소포를 형성한다. 그러면 클라트린 단백질이 해리된다.[2] 남은 것은 초기 엔도솜으로 알려져 있다. 초기 엔도솜은 후기 엔도솜과 합쳐진다. 이것은 세포내이입된 입자가 리소좀으로 수송되도록 하는 소포이다. 여기에 후기 엔도솜의 내용물을 분해하는 가수분해 효소가 있다. 때로는 분해되지 않고 리간드와 함께 세포내이입된 수용체가 원형질막으로 되돌아가 세포내이입 과정을 계속한다.
수용체 매개 세포내이입
[편집]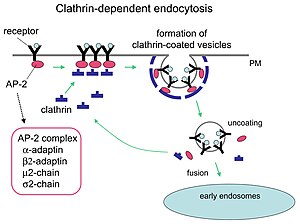
수용체 매개 세포내이입은 음세포작용 중 하나이다. 원형질막의 클라트린 코트에 있는 단백질은 거대분자나 리간드를 결합하고 포획하는 경향이 있다. 그러나 음세포작용를 일으킨 것은 수용체가 아니며, 수용체와 리간드가 존재하는지 여부에 관계없이 소포가 형성되었을 것이다.[3] 이것이 아래에서 설명하는 식균 작용과 달리 여전히 계속해서 유발되지 않는 현상인 이유이다.
식세포작용
[편집]식작용이라고도 알려진 식세포작용은 박테리아와 같은 더 큰 입자가 세포질로 흡수되는 것이다. 더 작은 단세포 유기체에서는이러한 방법으로 먹이를 먹는다. 더 큰 다세포 유기체에서는 오래되거나 손상된 세포를 파괴하거나 미생물 침입자를 섭취하는 방법이다.
박테리아를 섭취하는 경우 박테리아는 수성 환경에서 항체에 의해 결합된다. 이 항체가 세포 표면의 수용체와 만나면 원형질막이 박테리아를 둘러싸기 위해 확장되어 반응한다. 따라서 식균 작용은 무작위로 발생하는 이벤트가 아니다. 수용체에 결합하는 리간드에 의해 유발된다.
식균 작용을 위해 특별히 설계된 세포도 있는데, 이러한 세포에는 자연 살해 세포, 대식세포 및 호중구가 포함된다. 이들은 전부 면역반응에 관여하며 외부 물질이나 항원 물질을 분해하는 역할을 한다.[4]
엑소사이토시스
[편집]
세포외배출는 세포가 분비 소포의 내용물을 세포막 밖으로 보낼 때이다. 소포는 세포막과 융합하고 그 내용물(보통 단백질)은 세포 밖으로 방출된다. 엑소사이토시스에는 구성 분비와 조절 분비의 두 가지 유형이 있다. 이 두 가지 유형 모두에서 소포는 골지체에서 싹을 틔우고 원형질막으로 이동하여 세포에서 세포외로 배출된다. 리소좀의 엑소사이토시스는 일반적으로 지질 이중층을 보충함으로써 원형질막의 손상된 영역을 복구하는 역할을 한다.[5]
구성적 분비
[편집]구성적 분비(조절되지 않은 세포외유출)는 골지체에서 싹이 나는 소포가 용해성 단백질뿐만 아니라 소포 융합 후 원형질막에 남아있을 지질과 단백질을 모두 포함하는 경우이다. 이러한 유형의 분비는 조절되지 않다. 소포는 결국 원형질막으로 이동하여 융합한다. 세포의 내용물은 세포외 공간으로 방출되고 소포막의 구성요소(혈장막 지질 및 단백질)는 세포의 원형질막의 일부로 스스로를 확립한다.
조절된 분비
[편집]조절된 분비(조절된 엑소사이토시스)는 세포가 세포막에 소포의 융합과 그 내용물의 방출을 조절하는 신경 전달 물질이나 호르몬과 같은 세포 외 공간으로부터 신호를 받을 때 일어난다. 소포는 원형질막으로 운반된 뒤, 막과 융합하고, 그 내용물을 세포외 공간으로 방출하라는 신호를 받을 때까지 거기에 있는다.[6]
트랜스사이토시스
[편집]트랜스사이토시스(transcytosis)는 입자가 한 막에서 다른 막으로 셔틀되도록하는 일종의 세포 분열이다. 예시로는 수용체가 일반적으로 상피 세포의 기저 또는 측면 막에 있지만 정점 쪽으로 이동해야 하는 경우이다. 이것은 한 원형질막 도메인에서 다른 원형질막 도메인으로의 이동을 방지하는 밀착 연접으로 인한 트랜스사이토시스를 통해서만 수행할 수 있다. 이러한 유형의 세포증식증은 일반적으로 상피, 장 세포 및 모세혈관에서 발생한다. 트랜스사이토시스는 또한 병원성 분자와 유기체에 의해 이용될 수 있다.
여러 연구에 따르면 박테리아는 잔 세포의 트랜스사이토시스를 통해 장내강으로 쉽게 들어갈 수 있다.[7] 그러나 다른 연구에서는 트랜스사이토시스가 약물이 혈뇌 장벽을 통과하도록 하는 역할을 할 수 있다는 아이디어를 탐색하고 있다. 이 사실을 이용하면 특정 약물 요법이 뇌에서 더 잘 활용될 수 있다.[8]
세포증식의 방법은 물질을 세포 안팎으로, 세포를 통해 이동할 뿐만 아니라 세포의 원형질막에서 막을 추가하거나 빼기도 한다. 멤브레인의 표면적이 결정된다. 두 메커니즘의 균형에 의해 세포의 항상성 환경에 영향을 준다.[출처 필요]
같이 보기
[편집]각주
[편집]- ↑ Rieger, R.; Michaelis, A.; Green, M.M. 1991. Glossary of Genetics. Classical and Molecular (Fifth edition). Springer-Verlag, Berlin, .
- ↑ Rappoport JZ (June 2008). "Focusing on clathrin-mediated endocytosis". The Biochemical Journal412 (3): 415–23. doi 10.1042/BJ20080474. PMID 18498251
- ↑ Mukherjee S, Ghosh RN, Maxfield FR (July 1997). "Endocytosis". Physiological Reviews 77 (3): 759–803. PMID 9234965. Retrieved 2012-11-14
- ↑ Lodish, H. Berk, A., Kaiser, C., Kreiger, M., Bretscher, A., Ploegh, H., Amon, A., Scott, M. (2012) Molecular Cell Biology (7th ed.). W.H. Freeman and Co. New York: New York.
- ↑ Xu, J., Toops, K. A., Diaz, F., Carvajal-Gonzalez, J. M., Gravotta, D., Mazzoni, F., ... & Lakkaraju, A. (2012). Mechanism of polarized lysosome exocytosis in epithelial cells. Journal of Cell Science 125(24): 5937-5943
- ↑ Lodish, H. Berk, A., Kaiser, C., Kreiger, M., Bretscher, A., Ploegh, H., Amon, A., Scott, M. (2012) Molecular Cell Biology (7th ed.). W.H. Freeman and Co. New York: New York.
- ↑ Nikitas, G.; Deschamps, C.; Disson, O.; Niault, T.; Cossart, P.; Lecuit, M. (2011). "Transcytosis of Listeria monocytogenes across the intestinal barrier upon specific targeting of goblet cell accessible E-cadherin". Journal of Experimental Medicine 208 (11): 2263–2277. doi 10.1084/jem.20110560. PMC 3201198. PMID 21967767
- ↑ Y. Joy Yu, et al. (2001). “Boosting Brain Uptake of a Therapeutic Antibody by Reducing Its Affinity for a Transcytosis Target”. Science Translational Medicine 3 (84): 84ra44. doi 10.1126/scitranslmed.3002230. PMID 21613623
