이성질체
이성질체(異性質體, 영어: isomer)는 같은 원자 번호와 질량수를 가지면서 반감기(半減期), 에너지 상태, 방사능의 성질이 다른 원자핵을 가리키거나 또는 분자식은 같지만 다른 물리적ㆍ적 성질을 갖는 화합물을 가리킨다. 이 경우에서는 분자 안에서 원자의 배열 방식이 다르기 때문에 이러한 화합물이 생긴다. 이러한 분자식은 같지만 서로 다른 물리/화학적 성질을 갖는 이성질체의 분자들은 원소의 종류와 개수는 같으나 구성 원자단이나 구조가 완전히 다르거나, 구조가 같더라도 상대적인 배열이 달라서 다른 성질을 갖게 된다.[1] 이는 동일한 원자들이 이들간의 서로 다른 배열에서 분자의 구조나 형태가 원자간 또는 분자 간 상호작용 및 광학적 성질을 비롯한 다양한 특성을 변화시킴으로써 분자의 성질을 바꿀 수 있기 때문이다. 이러한 반응은 이성질체화 반응이라고 한다.
이성질체는 다양한 물질에 존재할 수 있지만, 특히 탄소는 4개의 서로 다른 원자와 공유결합이 가능하므로 다양한 이성질체를 형성할 수 있다. 이는 지구상에 풍부하게 존재하는 유기물로서 탄소가 갖는 중요한 성질이기 때문에, 유기분자를 다루는 유기화학이나 입체화학에서는 이를 중요하게 다룬다. 한편 착물에서도 착물의 중심 금속과 리간드사이의 결합에 의하여 이성질체가 발생할 수 있으므로 무기화학에서도 이성질체를 다루기도 한다.
생체 내에서 이성질체는 광학 활성에 의한 광학 이성질체에 대한 특이적 환경(카이랄성 환경)에 따라서 물리적 성질이 같음에도 한가지 광학 이성질체만 생리적 활성을 갖는 경우가 많다. 이를테면, 생체 분자를 구성하는 아미노산은 단백질을 구성할 때 광학 이성질체 중 L-form만 사용한다.[2] 이러한 특성 때문에, 이성질체는 생화학, 약학에서도 중요하게 다뤄지고 있다.
이성질체의 종류[편집]
이성질체는 화학적 결합의 순서가 바뀌는지 여부에 따라서 구조 이성질체와 입체 이성질체로 나뉜다. 구조 이성질체는 화학적 결합의 순서(결합 관계)가 다른 분자로 치환기의 명칭이 바뀌어 IUPAC 명명법(IUPAC chemical nomenclature)에따른 명칭이 바뀌는 경우가 일반적이다. 입체 이성질체는 광학 활성 유무에 따라서 광학 이성질체와 부분입체 이성질체로 크게 구분하며, 부분입체 이성질체는 입체 이성질현상의 근거에 따라서 기하 이성질체와 형태 이성질체등으로 구분한다.
구조 이성질체[편집]

|
| C3H8O의 구조 이성질체 |
구조 이성질체는 원자의 연결 순서가 다른 이성질현상이다. 같은 분자식을 갖지만, 원자의 연결 순서가 바뀌므로 치환기의 종류가 바뀌거나 치환된 위치가 바뀐다. 따라서 구조 이성질체는 같은 분자식이라고 하더라도 여러 가지 이성질체가 존재할 수 있다. 이를테면, C5H12의 분자식을 갖는 펜테인은 n-펜테인, iso-펜테인(2-메틸뷰테인), tert-펜테인(2,2-다이메틸프로페인)의 3가지 종류의 이성질체가 존재하며, 사슬이 길어짐에 따라서 C10H22의 분자식을 갖는 데케인은 모두 75개[3]의 이성질체가 존재하게 된다. 구조 이성질체들은 일반적으로 작용기의 변화나 골격의 변화로 인해 끓는점, 녹는점을 포함한 물리적 성질이 달라진다.
착화합물에서는 중심 금속에 대한 리간드의 결합 원소가 달라져서 배위 이성질체가 형성되는데, 이를 구조 이성질체의 일종으로 분류할 수 있다.
입체 이성질체[편집]
입체 이성질체는 결합의 순서와는 관계없이 결합의 기하적 위치에 의하여 차이를 보이는 이성질체이다. 광학 이성질체의 거울상처럼 물리적 성질이 동일할 수도 있지만, 부분입체 이성질체와 같이 물리적 성질이 달라질수도 있다.
광학 이성질체[편집]
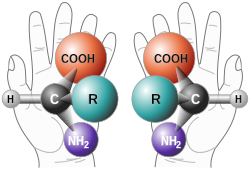
광학 이성질체는 카이랄성분자가 갖는 이성질체이다. 거울상 이성질체라고도 한다. 거울상으로 만들어지는 두 이성질체는 작용기의 배열이 달라서 서로 겹쳐지지 않는다. 광학 이성질체는 회전 편광현상을 갖고 있으며, CIP 규칙에 따라 S 배열(라틴어로 sinister, 왼쪽을 나타낸다.)과 R 배열(라틴어로 rectus, 오른쪽을 나타낸다.)로 구분되며, 이와 무관하지만 회전 편광의 방향에 따라서 좌회전성(levorotatory)과 우회전성(dextrorotatory) 분자로도 나눌 수 있다. 광학 이성질체인 두 분자는 각각의 순물질에 대하여 어는점이나 끓는점이 서로 같지만, 라세미 혼합물(S, R배열이 1:1로 존재하는 균등 혼합물로 광학 활성이 없다.)과는 차이를 보인다.[4]
부분입체 이성질체[편집]

|

|
| D-트레오스 | D-에리트로오스 |
| 부분입체 이성질체의 사례 |
부분입체 이성질체는 입체 이성질체 중에서 광학 반전이 일어나지 않는 두 분자간의 관계이다. 부분입체 이성질체에는 이중 결합 등의 회전 불가능한 결합이 생성하는 기하 이성질체, 단일 결합의 회전에 의해서 일시적인 배열이 달라져 있는 형태 이성질체, 혹은 입체 중심이 여러개 존재하지만 거울상을 이루지 못하는 일반적인 부분입체 이성질체 등이 포함된다. 입체 중심이 존재하더라도 대칭면이 존재하는 부분입체 이성질체는 특별히 메조(meso) 화합물이라 한다.
모든 부분입체 이성질체는 광학 반전이 일어나지 않으며, 물리적 성질은 분리할 수 없는 형태 이성질체를 제외하면 일반적으로 다르다. 다른 이성질체로는 에피머나 아노머 등이 있다.
같이 보기[편집]
- 카이랄성
- 유기화학
- 입체화학
- 구조 이성질체
- 입체 이성질체
- 부분입체 이성질체
- 거울상 이성질체
- 기하 이성질체
- 형태 이성질체
- 회전 이성질체
- 당뇨병
- 피트산(en:Phytic acid, IP6)
- 이노시톨
각주[편집]
- ↑ IUPAC Gold Book
- ↑ John E. McMurry 外,《기본유기화학》(Cengage Learning, 2007) 547p.
- ↑ The 75 Isomers of Decane
- ↑ 상게서, 214p.
