다루나비르: 두 판 사이의 차이
잔글 봇: 틀 이름 및 스타일 정리 |
작용기전 |
||
| 22번째 줄: | 22번째 줄: | ||
=== 약물 상호작용 === |
=== 약물 상호작용 === |
||
다루나비르는 다른 항레트로바이러스와 같은 HIV/AIDS와 양성자 펌프 억제제 및 H2 수용체 길항제 같은 항산화제를 복용중인 사람들이 일반적으로 복용하는 약물과 상호작용할 수 있습니다.<ref name=":03">{{웹 인용|url=http://www.prezista.com/patients/full-product-information|title=Drug Monograph, Prezista|archive-url=https://web.archive.org/web/20161111061346/http://www.prezista.com/patients/full-product-information|archive-date=2016-11-11|url-status=live}}</ref> [[:en:St._John's_wort|St. John's wort]](식물 이름)는 대사 효소 ''[[CYP3A4|CYP3A]]''에 의해서 다루나비르의 분해를 증가시킴으로써 다루나비르의 효과를 감소시킬 수 있습니다. |
다루나비르는 다른 항레트로바이러스와 같은 HIV/AIDS와 양성자 펌프 억제제 및 H2 수용체 길항제 같은 항산화제를 복용중인 사람들이 일반적으로 복용하는 약물과 상호작용할 수 있습니다.<ref name=":03">{{웹 인용|url=http://www.prezista.com/patients/full-product-information|title=Drug Monograph, Prezista|archive-url=https://web.archive.org/web/20161111061346/http://www.prezista.com/patients/full-product-information|archive-date=2016-11-11|url-status=live}}</ref> [[:en:St._John's_wort|St. John's wort]](식물 이름)는 대사 효소 ''[[CYP3A4|CYP3A]]''에 의해서 다루나비르의 분해를 증가시킴으로써 다루나비르의 효과를 감소시킬 수 있습니다. |
||
== '''작용기전''' == |
|||
다루나비르는 프로테아제(PR)의 비펩타이드 억제제로, 다수의 수소 결합을 통해 PR의 활성자리에 자신을 결합시킵니다. 다루나비르는 HIV-1 프로테아제와의 상호작용을 강화시키고 HIV-1 프로테아제 돌연변이에 대한 내성을 높이기 위해 개발되었습니다. <ref name="Leonis, G. 2012">{{cite journal|title=Computational Studies of Darunavir into HIV-1 Protease and DMPC Bilayer: Necessary Conditions for Effective Binding and the Role of the Flaps|journal=J. Chem. Inf. Model.|last1=Leonis|first1=G.|last2=Czyznikowska|first2=Z.|year=2012|volume=52|issue=6|pages=1542–1558|doi=10.1021/ci300014z|pmid=22587384|display-authors=et al}}</ref> 4.5 x 10<sup>−12</sup> M K<sub>d</sub>(분해 상수)를 가지고 PR과의 상호작용이 훨씬 강하며 분해 상수는 다른 프로테아제 억제제의 1/100 ~ 1/1000입니다.<ref name="King, N. M. 2004">{{cite journal|title=Structural and Thermodynamic Basis for the Binding of TMC114, a Next-Generation Human Immunodeficiency Virus Type 1 Protease Inhibitor|journal=Journal of Virology|last1=King|first1=N. M.|last2=Prabu-Jeyabalan|first2=M.|year=2004|volume=78|issue=21|pages=12012–21|doi=10.1128/JVI.78.21.12012-12021.2004|pmc=523255|pmid=15479840|display-authors=et al|s2cid=828919|doi-access=free}}</ref> 이러한 강력한 상호작용은 PR 활성자리의 구조와 다루나비르 사이의 수소 결합 때문입니다(그림 2). 다루나비르의 구조는 FDA가 개발하고 승인한 대부분의 PI보다 더 많은 수소 결합을 만들 수 있게 해줍니다.<ref name="ReferenceB">{{cite journal|title=Resilience to Resistance of HIV-1 Protease Inhibitors: Profile of Darunavir|journal=AIDS Rev.|last1=Lefebvre|first1=E.|last2=Schiffer|first2=C. A.|year=2008|volume=10|issue=3|pages=131–142|pmc=2699666|pmid=18820715}}</ref> 게다가, HIV-1 프로테아제의 골격는 돌연변이 발생 시에도 공간적 형태을 유지하고 있습니다. <ref>{{cite journal|title=Role of darunavir in the management of HIV infection|journal=HIV AIDS (Auckl)|last1=Lascar|first1=R. M.|last2=Benn|first2=P.|year=2009|volume=1|pages=31–39|doi=10.2147/hiv.s5397|pmc=3218677|pmid=22096377}}</ref>그래서 다루나비르는 프로테아제의 이 안정된 부분 과 상호작용하기에 PR-PI [[상호작용]]은 돌연변이에 의해 방해될 가능성이 낮습니다.<ref name="ReferenceB" /> |
|||
[[File:Figure_3.a.tiff|링크=https://en.wikipedia.org/wiki/File:Figure_3.a.tiff|왼쪽|섬네일|Figure 3. Ribbon structure of PR with darunavir in active site: Structures colored as in Fig. 1. with certain residues partaking in hydrogen bonding further highlighted. The catalytic aspartates, 25 and 25’, are in orange and the other interacting residues in green. Right image is a magnified view of the image on the left (PDB 4qdb).]] |
|||
=== 촉매 자리 === |
|||
HIV-1 프로테아제의 화학적 활성은 [https://terms.naver.com/entry.naver?docId=189335&cid=50331&categoryId=50331 호모다이머]의 각 사본에 하나씩 있는 활성자리의 두 가지 Asp25 and Asp25’자리에 의존합니다. <ref name="Zhang, Y. 2014">{{cite journal|title=Investigation on the mechanism for the binding and drug resistance of wild type and mutations of G86 residue in HIV-1 protease complexed with Darunavir by molecular dynamic simulation and free energy calculation|journal=J. Molecular Modeling|last1=Li|first1=D.|last2=Zhang|first2=Y.|year=2014|volume=20|issue=2|page=2122|doi=10.1007/s00894-014-2122-y|pmid=24526384|display-authors=et al|s2cid=23262721}}</ref> Darunavir는 수소 결합을 통해 아스파르트산 및 활성 부위의 뼈대와 상호작용하며, 특히 Asp25, Asp25', Asp 29, Asp 30, Asp 30' 및 Gly 27에 결합됩니다(그림 3). 이 상호작용은 바이러스성 폴리펩타이드들이 활성 자리에 접근하는 것을 경쟁적으로 억제하고 이 단백질의 효소 부분에 강하게 결합하기 때문에 바이러스 복제를 방지할 수있습니다.<ref name="Leonis, G. 2012" /> |
|||
2021년 6월 16일 (수) 15:57 판
이 문서에는 분류가 달려 있지 않습니다. 적절한 분류를 다신 후 이 틀을 제거해주세요. |
| 파일:File:Darunavir structure.svg | |
| |
| 체계적 명칭 (IUPAC 명명법) | |
|---|---|
| [(1R,5S,6R)-2,8-dioxabicyclo[3.3.0]oct-6-yl] N-[(2S,3R)-4- [(4-aminophenyl)sulfonyl- (2-methylpropyl)amino]-3-hydroxy-1-phenyl- butan-2-yl] carbamate | |
| 식별 정보 | |
| CAS 등록번호 | 206361-99-1 |
| ATC 코드 | J05AE10 |
| PubChem | 213039 |
| 드러그뱅크 | DB01264 |
| ChemSpider | 184733 |
| 화학적 성질 | |
| 화학식 | C27H37N3O7S |
| 분자량 | ? |
| 유의어 | TMC114, DRV, darunavir ethanolate |
| 약동학 정보 | |
| 생체적합성 | 37% (without ritonavir), 82% (with ritonavir) |
| 단백질 결합 | 95% |
| 동등생물의약품 | ? |
| 약물 대사 | hepatic (CYP3A4) |
| 생물학적 반감기 | 15 hours (with ritonavir) |
| 배출 | Feces (80%), urine (14%) |
| 처방 주의사항 | |
| 허가 정보 | |
| 임부투여안전성 | B2(오스트레일리아)[1]?(미국)[1] |
| 법적 상태 | |
| 투여 방법 | By mouth |
Prezista라는 상품명으로 판매되는 Darunavir(다루나비르(DRV))는 에이즈 치료 및 예방에 사용되는 항레트로바이러스제입니다. 일반적으로 다른 항레트로바이러스제와 함께 사용할 것을 권장합니다.[2][3]루나비르 역가를 밎추기 위해 위해 소량의 ritonavir나 cobicistat와 함께 종종 사용됩내다.[2]것은 바늘에 찔리는 부상이나 기타 잠재적 노출 후 예방에도 사용될 수 있습니다.[2]하루에 한 번에서 두 번 복용합니다.[2]
일반적인 부작용으로는 설사, 메스꺼움, 복통, 두통, 발진, 구토 등이 있습니다.[2][3] 심각한 부작용으로는 알레르기 반응, 간 질환, 중독성표피박리증 같은 피부 발진이 있습니다.[2] 임신 중 사용에는 연구가 잘 되어있지만, 아기에게는 안전해 보입니다.[4] 프로테아제 억제제(PI) 효과로 HIV 프로테아제를 차단해 효과가 있습니다.[2]
다루나비르는 2006년 미국에서, 2007년 2월 유럽연합에서 의료용 허가를 받았습니다.[2][5] 세계보건기구의 필수 의약품 목록에 올라 있습니다.[6] 고정된 용량의 복합약으로 약물 다루나비르/코비시스타트(Rezolsta)는 단일 알약으로 이용할 수 있습니다.[7]
의학적 사용
다루나비르는 에이즈 연구 자문위원회(DHHS)가 과거에 HIV 치료를 받았는지 여부와 관계없이 성인 및 청소년을 대상으로 하는 추천되는 치료방법입니다.[8] HIV 치료를 받은 적이 없는 환자들을 대상으로 한 연구에서 다루나비르는 하루 1회 투약으로 96주차 lopinavir/ritonavir만큼 효과가 있었습니다.[9] 그래서 이전에 HIV를 이전에 치료받지 않은 사람들에 대해 한에 2008년 10월 21일 FDA에 의해 승인되었습니다.[10]다른 항레트로바이러스제와 마찬가지로 다루나비르는 HIV/AIDS를 치료하지 못합니다.[11] 단 3세 이상 성인과 어린이의 인체면역결핍바이러스(HIV-1) 감염 치료를 위해 다른 항레트로바이러스제나 ritonavir와 공동 투여해 사용됩니다.[12][13]
부작용
Darunavir를 복용하는 일반적으로 사람들은 큰문제가 없습니다. 발진이 가장 흔한 부작용(환자의 7%)입니다. 그 밖에 일반적인 부작용으로는 설사(2.3%), 두통(3.8%), 복통(2.3%), 변비(2.3%), 구토(1.5%) 등이 있습니다.[14] 다루나비르 역시 알레르기 반응을 일으킬 수 있으며 리토나비르(ritonavir) 알레르기가 있는 사람도 다루나비르에 대한 반응을 보일 수 있습니다.[14]
다루나비르와 같은 프로테아제 억제제 약을 복용하는 환자들에게서 고혈당, 당뇨병 또는 당뇨병의 악화, 근육통, 혈우병 환자의 출혈 증가가 보고되고 있습니다.[14] 다리, 팔, 얼굴의 지방 손실, 복부 및 기타 내장기관의 지방 증가, 유방 확대, 목 뒷면의 지방 덩어리생성 등 HIV 약을 복용하는 환자들에게서 체지방의 변화가 관찰되고 있습니다. 이러한 부작용의 원인과 장기적인 건강 영향은 알려지지 않았습니다.[14]
약물 상호작용
다루나비르는 다른 항레트로바이러스와 같은 HIV/AIDS와 양성자 펌프 억제제 및 H2 수용체 길항제 같은 항산화제를 복용중인 사람들이 일반적으로 복용하는 약물과 상호작용할 수 있습니다.[15] St. John's wort(식물 이름)는 대사 효소 CYP3A에 의해서 다루나비르의 분해를 증가시킴으로써 다루나비르의 효과를 감소시킬 수 있습니다.
작용기전
다루나비르는 프로테아제(PR)의 비펩타이드 억제제로, 다수의 수소 결합을 통해 PR의 활성자리에 자신을 결합시킵니다. 다루나비르는 HIV-1 프로테아제와의 상호작용을 강화시키고 HIV-1 프로테아제 돌연변이에 대한 내성을 높이기 위해 개발되었습니다. [16] 4.5 x 10−12 M Kd(분해 상수)를 가지고 PR과의 상호작용이 훨씬 강하며 분해 상수는 다른 프로테아제 억제제의 1/100 ~ 1/1000입니다.[17] 이러한 강력한 상호작용은 PR 활성자리의 구조와 다루나비르 사이의 수소 결합 때문입니다(그림 2). 다루나비르의 구조는 FDA가 개발하고 승인한 대부분의 PI보다 더 많은 수소 결합을 만들 수 있게 해줍니다.[18] 게다가, HIV-1 프로테아제의 골격는 돌연변이 발생 시에도 공간적 형태을 유지하고 있습니다. [19]그래서 다루나비르는 프로테아제의 이 안정된 부분 과 상호작용하기에 PR-PI 상호작용은 돌연변이에 의해 방해될 가능성이 낮습니다.[18]
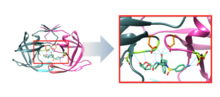
촉매 자리
HIV-1 프로테아제의 화학적 활성은 호모다이머의 각 사본에 하나씩 있는 활성자리의 두 가지 Asp25 and Asp25’자리에 의존합니다. [20] Darunavir는 수소 결합을 통해 아스파르트산 및 활성 부위의 뼈대와 상호작용하며, 특히 Asp25, Asp25', Asp 29, Asp 30, Asp 30' 및 Gly 27에 결합됩니다(그림 3). 이 상호작용은 바이러스성 폴리펩타이드들이 활성 자리에 접근하는 것을 경쟁적으로 억제하고 이 단백질의 효소 부분에 강하게 결합하기 때문에 바이러스 복제를 방지할 수있습니다.[16]
- ↑ 가 나 인용 오류:
<ref>태그가 잘못되었습니다;Drugs.com pregnancy라는 이름을 가진 주석에 텍스트가 없습니다 - ↑ 가 나 다 라 마 바 사 아 “Darunavir”. The American Society of Health-System Pharmacists. 2016년 11월 10일에 원본 문서에서 보존된 문서. 2016년 11월 28일에 확인함.
- ↑ 가 나 “Prezista- darunavir tablet, film coated Prezista- darunavir suspension”. 《DailyMed》. 2019년 6월 6일. 2020년 4월 21일에 확인함.
- ↑ “Darunavir (Prezista) Use During Pregnancy”. 《Drugs.com》. 2018년 10월 23일. 2020년 4월 21일에 확인함.
- ↑ “Prezista EPAR”. 《European Medicines Agency (EMA)》. 2020년 4월 21일에 확인함.
 이 문서는 퍼블릭 도메인 출처의 본문을 포함합니다.
이 문서는 퍼블릭 도메인 출처의 본문을 포함합니다.
- ↑ World Health Organization (2019). 《World Health Organization model list of essential medicines: 21st list 2019》. Geneva: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ “Darunavir / Cobicistat”. 《AIDSinfo》. U.S. Department of Health and Human Services.
- ↑ Panel on Antiretroviral Guidelines for Adults and Adolescents (2019년 12월 18일). “Guidelines for the Use of Antiretroviral Agents in Adults and Adolescents with HIV” (PDF). Department of Health and Human Services. 2020년 4월 21일에 확인함. 요약문.
- ↑ hivandhepatitis.com 보관됨 2007-07-13 - 웨이백 머신, Efficacy and Safety of Boosted Darunavir (Prezista) Are Superior to Lopinavir/ritonavir (Kaletra) at 96 Weeks: ARTEMIS Trial, 2008-10-28, URL 보관됨 2009-07-19 - 웨이백 머신.
- ↑ hivandhepatitis.com 보관됨 2007-07-13 - 웨이백 머신, Darunavir (Prezista) Receives Full Traditional Approval, Dose Set for Treatment-naive Patients, Caution Urged for Pregnant Women, 2008-10-24, URL 보관됨 2009-05-19 - 웨이백 머신.
- ↑ “Drug Monograph, Prezista”. 2016년 11월 11일에 원본 문서에서 보존된 문서.
- ↑ “Prezista- darunavir tablet, film coated Prezista- darunavir suspension”. 《DailyMed》. 2019년 6월 6일. 2020년 4월 21일에 확인함.
- ↑ “Prezista EPAR”. 《European Medicines Agency (EMA)》. 2020년 4월 21일에 확인함.
 이 문서는 퍼블릭 도메인 출처의 본문을 포함합니다.
이 문서는 퍼블릭 도메인 출처의 본문을 포함합니다.
- ↑ 가 나 다 라 “Drug Monograph, Prezista”. 2016년 11월 11일에 원본 문서에서 보존된 문서.
- ↑ “Drug Monograph, Prezista”. 2016년 11월 11일에 원본 문서에서 보존된 문서.
- ↑ 가 나 Leonis, G.; Czyznikowska, Z.; 외. (2012). “Computational Studies of Darunavir into HIV-1 Protease and DMPC Bilayer: Necessary Conditions for Effective Binding and the Role of the Flaps”. 《J. Chem. Inf. Model.》 52 (6): 1542–1558. doi:10.1021/ci300014z. PMID 22587384.
- ↑ King, N. M.; Prabu-Jeyabalan, M.; 외. (2004). “Structural and Thermodynamic Basis for the Binding of TMC114, a Next-Generation Human Immunodeficiency Virus Type 1 Protease Inhibitor”. 《Journal of Virology》 78 (21): 12012–21. doi:10.1128/JVI.78.21.12012-12021.2004. PMC 523255. PMID 15479840. S2CID 828919.
- ↑ 가 나 Lefebvre, E.; Schiffer, C. A. (2008). “Resilience to Resistance of HIV-1 Protease Inhibitors: Profile of Darunavir”. 《AIDS Rev.》 10 (3): 131–142. PMC 2699666. PMID 18820715.
- ↑ Lascar, R. M.; Benn, P. (2009). “Role of darunavir in the management of HIV infection”. 《HIV AIDS (Auckl)》 1: 31–39. doi:10.2147/hiv.s5397. PMC 3218677. PMID 22096377.
- ↑ Li, D.; Zhang, Y.; 외. (2014). “Investigation on the mechanism for the binding and drug resistance of wild type and mutations of G86 residue in HIV-1 protease complexed with Darunavir by molecular dynamic simulation and free energy calculation”. 《J. Molecular Modeling》 20 (2): 2122. doi:10.1007/s00894-014-2122-y. PMID 24526384. S2CID 23262721.
