수소화 리튬
| |
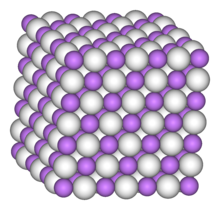
 __Li+ __H−
Structure of Lithium hydride. | |

| |
| 식별자 | |
|---|---|
3D 모델 (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.028.623 |
PubChem CID
|
|
| RTECS 번호 |
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| LiH | |
| 몰 질량 | 7.95 g/mol |
| 겉보기 | colorless to gray solid[1] |
| 밀도 | 0.78 g/cm3[1] |
| 녹는점 | 688.7 °C (1,271.7 °F; 961.9 K)[1] |
| 끓는점 | 900–1,000 °C (1,650–1,830 °F; 1,170–1,270 K) (decomposes)[2] |
| reacts | |
| 용해도 | slightly soluble in dimethylformamide reacts with ammonia, 다이에틸 에터, 에탄올 |
자화율 (χ)
|
−4.6·10−6 cm3/mol |
굴절률 (nD)
|
1.9847[3]:43 |
| 구조 | |
| fcc (NaCl-type) | |
a = 0.40834 nm[3]:56
| |
| 6.0 D[3]:35 | |
| 열화학 | |
열용량 (C)
|
3.51 J/(g·K) |
표준 몰 엔트로피 (S
|
170.8 J/(mol·K) |
표준 생성 엔탈피 (ΔfH⦵298)
|
−90.65 kJ/mol |
기브스 자유 에너지 (ΔfG˚)
|
−68.48 kJ/mol |
| 위험 | |
| 주요 위험 | extremely strong irritant, highly toxic, highly corrosive |
| 물질 안전 보건 자료 | ICSC 0813 |
| NFPA 704 (파이어 다이아몬드) | |
| 200 °C (392 °F; 473 K) | |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose)
|
77.5 mg/kg (oral, rat)[5] |
LC50 (median concentration)
|
22 mg/m3 (rat, 4 h)[6] |
| NIOSH (미국 건강 노출 한계): | |
PEL (허용)
|
TWA 0.025 mg/m3[4] |
REL (권장)
|
TWA 0.025 mg/m3[4] |
IDLH (직접적 위험)
|
0.5 mg/m3[4] |
| 관련 화합물 | |
다른 양이온
|
Sodium hydride Potassium hydride Rubidium hydride Caesium hydride |
관련 화합물
|
Lithium borohydride Lithium aluminium hydride |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
수소화 리튬은 화학식 LiH의 무기 화합물이다. 무색 고체지만 가끔 회색의 경우도 있다. 염화나트륨과 성질이 비슷하다. 녹는점이 높으며 반응을 보이지 않는 용매에는 녹지 않는다. 이온 성질을 띠는 화합물 중 가장 가볍다. 900-1000도에서 결정이 분해되어, 리튬과 수소로 분해된다. 모스 굳기는 약 3.5다.
생산[편집]
리튬 금속과 수소 가스를 반응시키면 발생한다. 이러한 방법은 섭씨 600도보다 높은 환경에서 더 쉽게 쓸 수 있다.
이외에 수소화 리튬을 만드는 방법은 수소화 알루미늄 리튬(200 °C), 수소화 붕소 리튬(300 °C), n-부틸리튬(150 °C) 등을 열분해하는 방법이 있다.
반응[편집]
수소화 리튬은 습도가 낮은 공기와 빠르게 반응하여 수산화리튬, 산화리튬 혹은 탄산리튬을 발생시킨다. 습한 공기에서는 자연 발화하여, 여러 질소 화합물을 생성한다. 순수한 산소와는 아무 반응도 일으키지 않지만, 가열할 경우 폭발적인 연소가 일어난다. 물과도 반응하여 수산화 이온, 리튬 이온, 수소를 생성한다.
각주[편집]
- ↑ 가 나 다 Lide, D. R., 편집. (2005). 《CRC Handbook of Chemistry and Physics》 86판. Boca Raton (FL): CRC Press. 4.70쪽. ISBN 0-8493-0486-5.
- ↑ David Arthur Johnson; Open University (2002년 8월 12일). 《Metals and chemical change》. Royal Society of Chemistry. 167–쪽. ISBN 978-0-85404-665-2. 2011년 11월 1일에 확인함.
- ↑ 가 나 다 Smith, R. L.; Miser, J. W. (1963). 《Compilation of the properties of lithium hydride》. NASA.
- ↑ 가 나 다 NIOSH Pocket Guide to Chemical Hazards. “#0371”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ Chambers, Michael. “ChemIDplus - 7580-67-8 - SIAPCJWMELPYOE-UHFFFAOYSA-N - Lithium hydride - Similar structures search, synonyms, formulas, resource links, and other chemical information.”. 《chem.sis.nlm.nih.gov》. 2018년 4월 10일에 확인함.
- ↑ “Lithium hydride”. 《Immediately Dangerous to Life and Health Concentrations (IDLH)》. National Institute for Occupational Safety and Health (NIOSH).
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |

