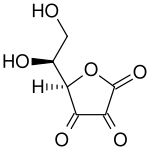
디하이드로아스코르브산
| |
| 이름 | |
|---|---|
| IUPAC 이름
L-threo-hexo-2,3-diulosono-1,4-lactone
| |
| 체계명
(5R)-5-[(1S)-1,2-dihydroxyethyl]oxolane-2,3,4-trione | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.007.019 |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| C6H6O6 | |
| 몰 질량 | 174.108 g·mol−1 |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
디하이드로아스코르브산(영어: dehydroascorbic acid, DHA)은 아스코르브산(비타민 C의 주요 형태)의 산화된 형태에서 볼 수 있다. 포도당 수송체를 통해 세포의 소포체로 활발하게 유입된다.[1] 이것은 글루타티온과 다른 싸이올에 의해 다시 아스코르브산염으로 환원되는 반응 안에서 안정적으로 순환된다.[2] (유리) 자유 라디칼 상태의 세미디하이드로아스코르브산(semidehydroascorbic acid, SDA)도 산화된 아스코르브산 그룹에 속한다고 본다.
비타민 C
[편집]비타민 C에 대한 나트륨 의존성 수송체가 존재하지만 주로 특수화된 세포에 존재하는 반면 포도당 수송체, 가장 주목할 만한 GLUT1은 대부분의 세포에서 비타민 C(산화된 형태, DHA)를 수송한다.[3] 아스코르브산염으로 돌아가면 필요한 효소 보조 인자와 세포 내 항산화제를 생성한다(미토콘드리아로의 수송 참조).
 |
디하이드로아스코르브산에 대해 여기에 표시된 구조는 일반적으로 표시되는 교과서적인 참고 구조이다. 그러나 이 1,2,3-트라이카보닐은 너무 친전자성이어서 수용액에서 몇 밀리초 이상 지속된다. 분광학적 연구에 의해 나타난 실제 구조는 6-OH와 3-카보닐기 사이의 빠른 헤미케탈 형성의 결과이다. 2-카보닐의 수화도 관찰된다.[4] 안정화된 형태의 반감기를 고려한 수명은 일반적으로 생물학적 조건에서 대략 6분 정도로 추정된다고 알려져 있다.[5] 파괴는 에스터 결합의 비가역적 가수분해로 인해 일어나며 추가적인 분해 반응이 뒤따른다. 디하이드로아스코르브산 용액의 결정화는 불완전한 안정성의 5환식 이량체 구조를 제공한다.[1] 디하이드로아스코르브산을 세포로 능동적으로 수송한 후 환원 및 재사용함으로써 아스코르브산염을 재활용하면 인간이 포도당으로부터 합성할 수 없는 능력이 완화될 수 있다.[6][3]
같이 보기
[편집]각주
[편집]- ↑ 가 나 May, J. M. (1998). “Ascorbate function and metabolism in the human erythrocyte”. 《Frontiers in Bioscience》 3 (4): d1–10. doi:10.2741/a262. PMID 9405334.
- ↑ Welch, R. W.; Wang, Y.; Crossman, A. Jr.; Park, J. B.; Kirk, K. L.; Levine, M. (1995). “Accumulation of Vitamin C (Ascorbate) and Its Oxidized Metabolite Dehydroascorbic Acid Occurs by Separate Mechanisms”. 《Journal of Biological Chemistry》 270 (21): 12584–12592. doi:10.1074/jbc.270.21.12584. PMID 7759506.
- ↑ 가 나 Lee, Y. C.; Huang, H. Y.; Chang, C. J.; Cheng, C. H.; Chen, Y. T. (2010). “Mitochondrial GLUT10 facilitates dehydroascorbic acid import and protects cells against oxidative stress: Mechanistic insight into arterial tortuosity syndrome”. 《Human Molecular Genetics》 19 (19): 3721–33. doi:10.1093/hmg/ddq286. PMID 20639396.
- ↑ Kerber, R. C. (2008). “"As Simple as Possible, but Not Simpler"—The Case of Dehydroascorbic Acid”. 《Journal of Chemical Education》 85 (9): 1237. Bibcode:2008JChEd..85.1237K. doi:10.1021/ed085p1237.
- ↑ Kimoto, E.; Tanaka, H.; Ohmoto, T.; Choami, M. (1993). “Analysis of the transformation products of dehydro-L-ascorbic acid by ion-pairing high-performance liquid chromatography”. 《Analytical Biochemistry》 214 (1): 38–44. doi:10.1006/abio.1993.1453. PMID 8250252.
- ↑ Montel-Hagen, A.; Kinet, S.; Manel, N.; Mongellaz, C.; Prohaska, R.; Battini, J. L.; Delaunay, J.; Sitbon, M.; Taylor, N. (2008). “Erythrocyte Glut1 triggers dehydroascorbic acid uptake in mammals unable to synthesize vitamin C”. 《Cell》 132 (6): 1039–48. doi:10.1016/j.cell.2008.01.042. PMID 18358815.
