탄화 칼슘

| |

| |
| |
| 이름 | |
|---|---|
| 우선명 (PIN)
Calcium acetylide | |
| 체계명
Calcium ethynediide | |
| 별칭
Calcium percarbide
Calcium carbide Calcium dicarbide | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.000.772 |
| EC 번호 |
|
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| CaC2 | |
| 몰 질량 | 64.099 g/mol |
| 겉보기 | White powder to grey/black crystals |
| 밀도 | 2.22 g/cm3 |
| 녹는점 | 2,160 °C (3,920 °F; 2,430 K) |
| 끓는점 | 2,300 °C (4,170 °F; 2,570 K) |
| Rapid hydrolysis | |
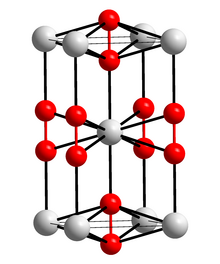
| 구조 | |
| Tetragonal[1] | |
| D174h, I4/mmm, tI6 | |
| 6 | |
| 열화학 | |
표준 몰 엔트로피 (S
|
70 J·mol−1·K−1 |
표준 생성 엔탈피 (ΔfH⦵298)
|
−63 kJ·mol−1 |
| 위험 | |
| 주요 위험 | Reacts with water to release acetylene gas[2] |
| GHS 그림문자 |  
|
| 신호어 | 위험 |
| H260 | |
| NFPA 704 (파이어 다이아몬드) | |
| 305 °C (581 °F; 578 K) (acetylene) | |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
탄화 칼슘(Calcium carbide, CaC2)은 칼슘 카바이드(calcium carbide), 줄여서 카바이드(carbide)라고도 불리며, 두 개의 탄소 원자가 삼중 공유 결합을 한 2- 음이온과, 2+ 전하를 띠는 칼슘 양이온이 이온 결합한 물질이다.
제조법[편집]
성질[편집]
참고 문헌[편집]
- 고등학교 화학1, 우규환 외 5인 공저, (주)중앙교육진흥연구소, 2002.7.30 교육인적자원부 검정, Ⅱ.화학과 인간-1.주변의 탄소화합물.
각주[편집]
- ↑ Massalimov, I. A.; Kireeva, M. S.; Sangalov, Yu. A. (2002). “Structure and Properties of Mechanically Activated Barium Peroxide”. 《Inorganic Materials》 38 (4): 363. doi:10.1023/A:1015105922260. S2CID 91881752.
- ↑ NFPA Hazard Rating Information for Common Chemicals. Northeastern University
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |

