이플루오린화 제논
보이기

| |
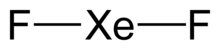
| |
| |

| |
| 이름 | |
|---|---|
| IUPAC 이름
Xenon difluoride
Xenon(II) fluoride | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.033.850 |
PubChem CID
|
|
| UNII | |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| F2Xe | |
| 몰 질량 | 169.290 g·mol−1 |
| 겉보기 | White solid |
| 밀도 | 4.32 g/cm3, solid |
| 녹는점 | 128.6 °C (263.5 °F; 401.8 K)[2] |
| 25 g/L (0 °C) | |
| 증기 압력 | 6.0×102 Pa[1] |
| 구조 | |
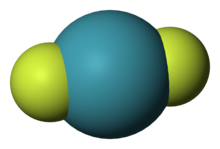
| parallel linear XeF2 units | |
| Linear | |
| 0 D | |
| 열화학 | |
표준 몰 엔트로피 (S
|
254 J·mol−1·K−1[3] |
표준 생성 엔탈피 (ΔfH⦵298)
|
−108 kJ·mol−1[3] |
| 위험 | |
| 주요 위험 | Corrosive to exposed tissues. Releases toxic compounds on contact with moisture.[5] |
| 물질 안전 보건 자료 | PELCHEM MSDS |
| GHS 그림문자 |   
|
| 신호어 | 위험 |
| H272, H301, H314, H330 | |
| P210, P220, P221, P260, P264, P270, P271, P280, P284, P301+310+330, P303+361+353, P304+340+310, P305+351+338, P331, P363, P370+378, P403+233, P405, P501[4] | |
| NFPA 704 (파이어 다이아몬드) | |
| 관련 화합물 | |
다른 음이온
|
Xenon dichloride Xenon dibromide |
다른 양이온
|
Krypton difluoride Radon difluoride |
관련 화합물
|
Xenon tetrafluoride Xenon hexafluoride |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
이플루오린화 제논(Xenon difluoride)은 화학식 XeF2를 갖는 강력한 불소화제이며 가장 안정적인 크세논 화합물 중 하나이다. 대부분의 공유 결합 무기 플루오린화물과 마찬가지로 습기에 민감하다. 수증기와 접촉하면 분해되지만 그 외에는 보관 시 안정적이다. 이플루오린화 제논은 조밀하고 무색의 결정성 고체이다.
메스꺼운 냄새가 나고 증기압이 낮다.
각주
[편집]- ↑ Melita Tramšek; Boris Žemva (2006). “Synthesis, Properties and Chemistry of Xenon(II) Fluoride” (PDF). 《Acta Chim. Slov.》 53 (2): 105–116. doi:10.1002/chin.200721209.
- ↑ Hindermann, D. K., Falconer, W. E. (1969). “Magnetic Shielding of 19F in XeF2”. 《J. Chem. Phys.》 50 (3): 1203. Bibcode:1969JChPh..50.1203H. doi:10.1063/1.1671178.
- ↑ 가 나 Zumdahl, Steven S. (2009). 《Chemical Principles 6th Ed.》. Houghton Mifflin Company. A23쪽. ISBN 978-0-618-94690-7.
- ↑ “Sigma Aldrich Xenon Difluoride SDS”. 《Sigma Aldrich》. Millpore Sigma. 2022년 11월 2일에 확인함.
- ↑ “MSDS: xenon difluoride” (PDF). BOC Gases. 2010년 6월 1일에 확인함.
외부 링크
[편집]| 이 글은 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |

