인산염: 두 판 사이의 차이
내용 삭제됨 내용 추가됨
잔글편집 요약 없음 |
잔글 위키데이터와 로컬이 같은 위키공용분류 링크 조정 |
||
| 27번째 줄: | 27번째 줄: | ||
== 외부 링크 == |
== 외부 링크 == |
||
* {{위키공용분류-줄 |
* {{위키공용분류-줄}} |
||
* {{PubChem|1061}} |
* {{PubChem|1061}} |
||
* {{언어링크|en}} [http://mazamascience.com/Minerals/USGS US Minerals Databrowser] provides data graphics covering consumption, production, imports, exports and price for phosphate and 86 other minerals |
* {{언어링크|en}} [http://mazamascience.com/Minerals/USGS US Minerals Databrowser] provides data graphics covering consumption, production, imports, exports and price for phosphate and 86 other minerals |
||
2018년 5월 23일 (수) 04:37 판
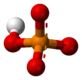
인산염(燐酸鹽, 영어: phosphate, 문화어: 린산염)은 인산의 염을 가리키는 무기 화합물이다. 하나의 인과 4개의 산소로 구성된 다원자 이온 또는 근본 물질에서 형성된 물질이다. 인산 이온(phosphate ion)은 −3 값의 전하를 가지고 PO43-로 써서 나타낸다. 다시 말해 인산에 있는 수소 이온을 금속 이온 따위의 양이온으로 치환한 염을 가리킨다. 인산염을 이용하면 농업과 공업에 쓰이는 인을 얻을 수 있고, 식품 첨가물로도 사용된다.
특성
-
H
3PO
4 -
H
2PO−
4 -
HPO2−
4 -
PO3−
4
- 세 가지 반응
- 25 °C 환경 (mol/L)
- (pKa1 2.12)
- (pKa2 7.21)
- (pKa3 12.67)
용해
- 1산성염인 이차염과 정염인 삼차염은 알칼리염만 물에 녹는다.
- 2산성염인 일차염은 모두 물에 녹는다.
같이 보기
외부 링크
 위키미디어 공용에 인산염 관련 미디어 분류가 있습니다.
위키미디어 공용에 인산염 관련 미디어 분류가 있습니다.- (영어) 인산염 - PubChem
- (영어) US Minerals Databrowser provides data graphics covering consumption, production, imports, exports and price for phosphate and 86 other minerals




![{\displaystyle K_{a1}={\frac {[{\mbox{H}}^{+}][{\mbox{H}}_{2}{\mbox{PO}}_{4}^{-}]}{[{\mbox{H}}_{3}{\mbox{PO}}_{4}]}}\simeq 7.5\times 10^{-3}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7e81fc5d22c187e5acc19c15b8422a604474b916)
![{\displaystyle K_{a2}={\frac {[{\mbox{H}}^{+}][{\mbox{HPO}}_{4}^{2-}]}{[{\mbox{H}}_{2}{\mbox{PO}}_{4}^{-}]}}\simeq 6.2\times 10^{-8}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c10e3502ce38d504ebf659f7411f2d2f24015c25)
![{\displaystyle K_{a3}={\frac {[{\mbox{H}}^{+}][{\mbox{PO}}_{4}^{3-}]}{[{\mbox{HPO}}_{4}^{2-}]}}\simeq 2.14\times 10^{-13}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/42097ca31fd0468791802af675f407bda4e4c871)