방출 스펙트럼
방출 스펙트럼(放出-, 영어: emission spectrum)은 한 원소 또는 여러 원소가 합해져 있는 분자의 전자들이 들뜨게 될 때, 방출되는 전자기파 스펙트럼이다. 각 원자의 방출 스펙트럼은 독특하며 그 원소가 알려지지 않은 분자들의 일부인지 아닌지를 결정해 주는 데 쓰일 수 있다. 비슷하게 분자의 방출 스펙트럼은 화학적인 분석을 위해 사용된다.방출스펙트럼 사이사이에는 검은 띠가 있다.
기원
[편집]원자 안에 전자들이 들뜨게 될 때(예를 들면 열을 가해줌으로써), 추가적인 에너지를 전자들에게 주어 더 높은 에너지 궤도로 올라간다. 그 전자들이 다시 제자리도 돌아오고 들뜬 상태를 떠날 때, 에너지는 광자의 형태로 재방출된다. 그 광자의 파장(또는 주파수)은 두 에너지 궤도 상태 사이의 차이에 의해 결정된다. 방출된 광자들은 그 원소의 방출 스펙트럼을 만든다.
원자의 방출 스펙트럼에서 오직 특정한 색깔이 나타난다는 그 사실은 오직 특정한 빛의 주파수가 방출된다는 의미이다. 이 주파수들 각각은 다음 공식에 의해 에너지와 관련이 있다 :
여기서 E는 광자의 에너지이고, f는 광자의 주파수, h는 플랑크 상수이다. 특정한 에너지를 가지는 광자가 원자에 의해 방출된다는 것이다. 이 방출 스펙트럼의 원리는 네온 사인의 다양한 색깔 뿐만 아니라, 화학적인 불꽃 실험에 의해 설명된다.
원자가 방출할 수 있는 빛의 주파수는 안에 있는 전자들의 상태에 의존된다. 들뜬 상태가 되었을 때, 전자들은 더 높은 에너지 준위 또는 궤도로 올라간다. 전자들이 바닥 상태로 다시 떨어질 때, 빛이 방출된다.

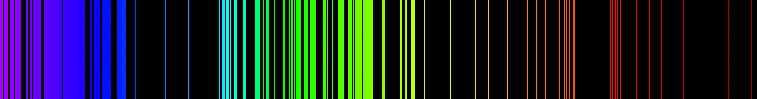
선 스펙트럼
[편집]기체를 유리관에 넣어 마개를 막고 압력을 내린 전관의 극에 고전압을 걸어서 방전하면, 네온 사인의 빨강이나 수은의 파랑 같은 기체 특유의 색으로 빛난다. 이 빛을 분광기를 사용하여 스펙트럼으로 나누면 많은 휘선이 나타난다. 또, 철이나 구리의 극 사이의 빛은 똑같이 많은 휘선이 나타나는 스펙트럼이 된다. 이것을 선 스펙트럼이라고 한다. 선 스펙트럼은 원자로부터 나오는 빛으로 원자가 고유의 스펙트럼을 가지고 있는 것에서 비롯된다. 이 원자로부터의 스펙트럼은 원자의 기체 또는 증기가 전자와 충돌해서 들뜨고, 빛을 내놓은 것으로 들뜨는 조건에 따라서 선 스펙트럼의 강도에도 변화가 있다. 그러나 원자가 자계나 전계 등 외부로부터의 영향이 없는 자연 상태로 빛을 발할 때에 그 파장은 매우 안정해서 일정한 값이 된다. 원소로부터 나오는 이와 같은 많은 선 스펙트럼을 해석하면 원소의 여러 가지 상태를 알 수가 있다. 이것은 원자 물리, 더 나아가서는 양자론의 기초가 된 중요한 실마리의 하나이다.
분자로부터의 복사
[편집]위에 거론된 전자기적 천이에서와 같이, 분자의 에너지 또한 회전성의 천이, 진동성의 천이, 그리고 전자기 천이를 통해 바꿀 수 있다. 이들의 에너지 천이는 종종 잘 알려진 스펙트럼 밴드로 많은 다른 스펙트럼 선의 가까운 그룹을 만들어 낸다. 풀리지 않은 스펙트럼 밴드는 연속 스펙트럼에서 나타난다.

