과산화 바륨: 두 판 사이의 차이
내용 삭제됨 내용 추가됨
편집 요약 없음 태그: 동음이의 링크 |
|||
| 1번째 줄: | 1번째 줄: | ||
{{chembox |
|||
| Watchedfields = changed |
|||
| verifiedrevid = 443750435 |
|||
| ImageFile = Peroxid barnatý.JPG |
|||
| ImageFile2 = BaO2structure.jpg |
|||
| IUPACName = barium peroxide |
|||
| OtherNames = Barium binoxide,<br/>Barium dioxide |
|||
|Section1={{Chembox Identifiers |
|||
| InChI = 1/Ba.O2/c;1-2/q+2;-2 |
|||
| SMILES = [Ba+2].[O-][O-] |
|||
| InChIKey = ZJRXSAYFZMGQFP-UHFFFAOYAZ |
|||
| StdInChI_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChI = 1S/Ba.O2/c;1-2/q+2;-2 |
|||
| StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} |
|||
| StdInChIKey = ZJRXSAYFZMGQFP-UHFFFAOYSA-N |
|||
| CASNo = 1304-29-6 |
|||
| CASNo_Ref = {{cascite|correct|CAS}} |
|||
| UNII_Ref = {{fdacite|correct|FDA}} |
|||
| UNII = T892KY013Y |
|||
| EINECS = 215-128-4 |
|||
| PubChem = 14773 |
|||
| ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} |
|||
| ChemSpiderID=14090 |
|||
| RTECS = CR0175000 |
|||
| UNNumber = 1449 |
|||
}} |
|||
|Section2={{Chembox Properties |
|||
| Formula = BaO<sub>2</sub> |
|||
| MolarMass = 169.33 g/mol (anhydrous) <br> 313.45 (octahydrate) |
|||
| Appearance = Grey-white crystalline (anhydrous) <br> colorless solid (octahydrate) |
|||
| Odor = odorless |
|||
| Density = 5.68 g/cm<sup>3</sup> (anhydrous) 2.292 g/cm<sup>3</sup> (octahydrate) |
|||
| MeltingPtC = 450 |
|||
| BoilingPtC = 800 |
|||
| BoilingPt_notes = (decomposes to [[barium oxide|BaO]] & [[oxygen|O<sub>2</sub>]].<ref name=Ceramic>Accommodation of Excess Oxygen in Group II Monoxides - S.C. Middleburgh, R.W. Grimes and K.P.D. Lagerlof Journal of the American Ceramic Society 2013, Volume 96, pages 308–311. {{doi|10.1111/j.1551-2916.2012.05452.x}}</ref>) |
|||
| Solubility = ''anhydrous'' <hr> 0.091 g/100 mL (20 °C) <br> ''octahydrate'' <hr> 0.168 g/cm<sup>3</sup> |
|||
| SolubleOther = dissolves with decomposition in acid |
|||
| MagSus = -40.6·10<sup>−6</sup> cm<sup>3</sup>/mol |
|||
}} |
|||
|Section3={{Chembox Structure |
|||
| CrystalStruct = Tetragonal <ref>{{cite journal |last1=Massalimov |first1=I. A. |last2=Kireeva |first2=M. S. |last3=Sangalov |first3=Yu. A. |title=Structure and Properties of Mechanically Activated Barium Peroxide |year=2002 |journal=Inorganic Materials |volume=38 |issue=4 |pages=363–366 |doi=10.1023/A:1015105922260}}</ref> |
|||
| SpaceGroup = D<sup>17</sup><sub>4h</sub>, I4/mmm, [[Pearson symbol|tI6]] |
|||
| Coordination = 6 |
|||
}} |
|||
|Section7={{Chembox Hazards |
|||
| GHSPictograms = {{GHS03}}{{GHS07}} |
|||
| GHSSignalWord = Warning |
|||
| HPhrases = {{H-phrases|272|302|332}} |
|||
| PPhrases = {{P-phrases|210|220|221|261|264|270|271|280|301+312|304+312|304+340|312|330|370+378|501}} |
|||
| NFPA-H = 2 |
|||
| NFPA-F = 0 |
|||
| NFPA-R = 2 |
|||
| NFPA-S = ox |
|||
| FlashPt = |
|||
| AutoignitionPt = |
|||
}} |
|||
}} |
|||
'''과산화바륨'''(Barium peroxide)은 [[화학식]] [[바륨|Ba]][[과산화물|O<sub>2</sub>]]의 [[무기 화합물]]이다. 이 백색 고체(불순물일 때에는 회색)는 가장 일반적인 무기 [[과산화물]] 중 하나이며 최초로 발견된 과산화물이다. 산화제이며 분화 시 밝은 녹색을 보이기 때문에 [[불꽃놀이]]에 일부 사용되며 역사적으로 [[과산화 수소]]의 선구자적 물질로 사용되었다. |
'''과산화바륨'''(Barium peroxide)은 [[화학식]] [[바륨|Ba]][[과산화물|O<sub>2</sub>]]의 [[무기 화합물]]이다. 이 백색 고체(불순물일 때에는 회색)는 가장 일반적인 무기 [[과산화물]] 중 하나이며 최초로 발견된 과산화물이다. 산화제이며 분화 시 밝은 녹색을 보이기 때문에 [[불꽃놀이]]에 일부 사용되며 역사적으로 [[과산화 수소]]의 선구자적 물질로 사용되었다. |
||
== 같이 보기 == |
== 같이 보기 == |
||
* [[산화 바륨]] |
* [[산화 바륨]] |
||
== 각주 == |
|||
{{각주}} |
|||
{{토막글|화학}} |
{{토막글|화학}} |
||
2022년 2월 27일 (일) 14:27 판

| |
| |
| 이름 | |
|---|---|
| IUPAC 이름
barium peroxide
| |
| 별칭
Barium binoxide,
Barium dioxide | |
| 식별자 | |
3D 모델 (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.013.754 |
| EC 번호 |
|
PubChem CID
|
|
| RTECS 번호 |
|
| UNII | |
| UN 번호 | 1449 |
CompTox Dashboard (EPA)
|
|
| |
| |
| 성질 | |
| BaO2 | |
| 몰 질량 | 169.33 g/mol (anhydrous) 313.45 (octahydrate) |
| 겉보기 | Grey-white crystalline (anhydrous) colorless solid (octahydrate) |
| 냄새 | odorless |
| 밀도 | 5.68 g/cm3 (anhydrous) 2.292 g/cm3 (octahydrate) |
| 녹는점 | 450 °C (842 °F; 723 K) |
| 끓는점 | 800 °C (1,470 °F; 1,070 K) (decomposes to BaO & O2.[1]) |
| anhydrous 0.091 g/100 mL (20 °C) octahydrate 0.168 g/cm3 | |
| 용해도 | dissolves with decomposition in acid |
자화율 (χ)
|
-40.6·10−6 cm3/mol |
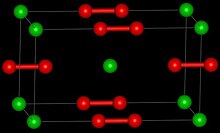
| 구조 | |
| Tetragonal [2] | |
| D174h, I4/mmm, tI6 | |
| 6 | |
| 위험 | |
| GHS 그림문자 |  
|
| 신호어 | 경고 |
| H272, H302, H332 | |
| P210, P220, P221, P261, P264, P270, P271, P280, P301+312, P304+312, P304+340, P312, P330, P370+378, P501 | |
| NFPA 704 (파이어 다이아몬드) | |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.
| |
과산화바륨(Barium peroxide)은 화학식 BaO2의 무기 화합물이다. 이 백색 고체(불순물일 때에는 회색)는 가장 일반적인 무기 과산화물 중 하나이며 최초로 발견된 과산화물이다. 산화제이며 분화 시 밝은 녹색을 보이기 때문에 불꽃놀이에 일부 사용되며 역사적으로 과산화 수소의 선구자적 물질로 사용되었다.
같이 보기
각주
- ↑ Accommodation of Excess Oxygen in Group II Monoxides - S.C. Middleburgh, R.W. Grimes and K.P.D. Lagerlof Journal of the American Ceramic Society 2013, Volume 96, pages 308–311. doi 10.1111/j.1551-2916.2012.05452.x
- ↑ Massalimov, I. A.; Kireeva, M. S.; Sangalov, Yu. A. (2002). “Structure and Properties of Mechanically Activated Barium Peroxide”. 《Inorganic Materials》 38 (4): 363–366. doi:10.1023/A:1015105922260.
| 이 글은 화학에 관한 토막글입니다. 여러분의 지식으로 알차게 문서를 완성해 갑시다. |

