결핵의 치료: 두 판 사이의 차이
잔글 →2차 약제 |
|||
| 141번째 줄: | 141번째 줄: | ||
* 간염: PZA, RMP, INH |
* 간염: PZA, RMP, INH |
||
* 발진: PZA, RMP, EMB |
* 발진: PZA, RMP, EMB |
||
;[[혈소판 감소]] |
|||
혈소판 감소는 RMP에 의한 것으로, 복용량의 테스트는 필요하지 않다. 아래에 RMP를 제외한 요법을 설명한다. (보다 상세한 내용은 [[리팜피신]]의 설명을 참조한다.) |
|||
==== 리팜피신을 제외한 요법 ==== |
|||
결핵균이 이소니아지드에 내성을 갖지 않고 리팜피신에 내성을 갖게 되는 경우는 드물다.<ref name="PLOS2008">{{저널 인용 |저자=O'Riordan P, Schwab U, Logan S ''et al.'' |제목=Rapid molecular detection of rifampicin resistance facilitates early diagnosis and treatment of multidrug-resistant tuberculosis: case control study |저널=PLoS ONE |volume=3 |issue=9 |pages=e3173 |작성년도=2008년 |doi=10.1371/journal.pone.0003173|pmid=18779863|pmc=2526158}}</ref> 하지만, 리팜피신에 대한 과민증은 드물지 않다.([[간독증]]이나 혈소판 감소는 리팜피신 복용을 중단하는 가장 흔한 원인이다.) 또한, 1차 치료 약제 중 리팜피신은 가장 비싸고, 따라서, 빈곤이 심한 나라에서는 리팜피신을 제외한 요법이 종종 사용된다. 리팜피신은 결핵 치료에서 사용할 수 있는 가장 강력한 살균 약제이며, 리팜피신을 뺀 모든 치료 요법은 표준 요법보다 월등히 길다. |
|||
영국내에서는 18HE 또는 12HEZ를 추천한다. 미국내에서는 9 ~ 12HEZ에 퀴놀론계 항균제(예를 들면, MXF)를 선택적으로 사용할 것을 추천한다. |
|||
== 주석 == |
== 주석 == |
||
2011년 2월 7일 (월) 07:32 판
틀:의학정보주의사항 본 문서에서는 결핵 감염시의 의학적 치료를 설명한다.
기본적인 '단기' 치료로는 이소니아지드, 리팜피신, 피라진아마이드, 에탐부톨을 두 달 간 복용하고, 이소니아지드와 리팜피신만 이후 4달 동안 복용한다. 환자는 6개월이면 치료가 되었다고 추정된다.(단, 2 ~ 3% 정도는 악화된다.) 잠복기의 결핵은, 6 ~ 9개월 간 이소니아지드만 복용한다.
신체 기관이 민감하다면, 치료는 이소니아지드, 리팜피신, 피라진아마이드를 두 달 간 복용하고, 이어 이소니아지드와 리팜피신을 5개월 간 복용한다. 에탐부톨은 사용할 필요가 없다.
약제
| 1차 결핵 약제 | ||
| 약 | 3자 | 1자 |
|---|---|---|
 에탐부톨 |
EMB | E |
 이소니아지드 |
INH | H |
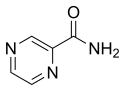 피라진아마이드 |
PZA | Z |
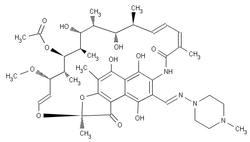 리팜피신 |
RMP | R |
 스트렙토마이신 |
STM | S |
| 2차 결핵 약제 | ||
 시프로플록사신 |
CIP | |
 목시플록사신 |
MXF | |
 P-아미노살리실산 |
PAS | P |
1차 약제
항결핵 1차 약제는 모두 3자의 고유 명칭과 1자로 줄인 명칭이 있다.
약물 요법(Drug regimens)은 표준화된 방법으로 유사하게 축약한다. 약제는 이들의 단수 약자를 사용하여 목록에 포함되었다. 접두사는 치료가 계속되어야 하는 기간의 개월수를 표시한다. 아래첨자는 간간이 복용하는 것을 의미한다.(3의 경우, 주 3회를 의미) 그리고, 아래첨자가 없으면 매일 복용하는 것을 의미한다. 대부분의 약물 요법은 초기에 고강도 단계가 있고, 합병 또는 박멸 단계가 이어진다. 두 단계는 '/'로 나누어진다. 즉,
- 2HREZ/4HR3
는 이소니아지드, 리팜피신, 에탐부톨, 피라진아마이드를 2달 간 매일 복용하고, 4달 간 이소니아지드와 리팜피신을 주 3회 복용하는 것을 의미한다.
이러한 표준 약어는 이후 문서에서 사용된다.
2차 약제
결핵의 치료에는 여섯 종류의 2차 약제(SLD)가 있다. 이들이 2차 약제로 분류된 것은 다음 중 한 가지 이유에 해당된다. 약이 1차 약제보다 효과적이지 못하거나(P-아미노살리실산), 독성 부작용이 있거나(시클로세린), 여러 개발도상국에서 사용이 불가능한 경우(플로로퀴놀론)이다.
- 아미노글리코사이드: 아미카신 (AMK), kanamycin (KM);
- 폴리펩타이드: capreomycin, 비오마이신, enviomycin;
- 플로로퀴놀론: ciprofloxacin (CIP), levofloxacin, moxifloxacin (MXF);
- thioamide: 에티오나마이드, 프로치온아마이드
- 시클로세린 (이 종류의 유일한 항생제);
- 아미노살리실산 (PAS 또는 P).
3차 약제
WHO의 2차 약제 목록에는 없지만 도움이 되는 것들도 있다.
- 리파부틴(rifabutin)
- macrolide: 즉, clarithromycin (CLR);
- 리네졸리드 (LZD);
- thioacetazone (T);
- thioridazine;
- 아르기닌
- 비타민 D
- R207910.
이들 약제는 '3차 약제'라 할 수도 있는데, 그다지 큰 효과가 없거나(clarithromycin), 효과가 입증되지 않은 경우(linezolid, R207910)이다. 리파부틴은 효과적이나 WHO 목록에는 포함되어 있지 않는데, 이는 대부분의 개발도상국에서는 가격이 터무니없이 비싸기 때문이다.
표준 요법
표준 요법의 근거
결핵은 50여 년 간 조합된 요법으로 치료해 왔다. 약제는 단독으로 사용하지 않으며(잠복기의 결핵이나 화학적 예방은 제외), 하나의 약제를 사용하는 요법은 내성이 빠르게 증가하는 결과가 되어 치료에 실패하게 된다.[1][2] 결핵을 치료하기 위해 복수의 약제를 사용하는 이유는 단순한 확률에 기초한다. 개별적인 약제에 내성을 부여하는 자연적인 돌연변이의 빈도는 잘 알려져 있다. EMB는 107에 하나, STM과 INH는 108에 하나, RMP는 1010에 하나이다.[3]
폐결핵이 심한 환자는 체내에는 약 1012의 세균이 있으며, 결과적으로 약 105개의 세균은 EMP에 내성을 갖고, 104개는 STM에, 104개는 INH에, 10²개는 RMP에 내성을 갖는다. 내성을 갖는 돌연변이는 자연적, 독립적으로 발생하므로, 해당 환자가 INH와 RMP에 모두 내성을 갖는 세균을 보유할 확률은 1 in 108 x 1 in 1010 = 1 in 1018이 되며, 네 개의 약제에 모두 내성을 갖게 될 확륙은 1 in 1033이다. 이는 지나치게 대략적인 계산이기는 하나, 여러 약제를 사용하는 치료를 설명하는 데에는 유용하다.
조합된 요법을 지지하는 다른 이론적 이유가 있는데, 이는 요법에 사용되는 서로 다른 약제들이 서로 다른 형태로 작용한다는 것이다. INH는 분열하는 세균을 죽인다(bactericidal). EMB는 결핵균을 죽이며, RMP는 균을 죽이고, 멸균(sterilizing)의 효과가 있다. PZA는 세균을 죽이는 효과는 약하지만, 산성의 환경, 대식세포 안쪽, 급성 염증 내부에 위치한 세균에 대해서 매우 효과적이다.
사용되는 모든 결핵 치료 요법은 1953년 리팜피신이 등장하기 전까지는 18개월 또는 그 이상이 걸렸다. 1953년, 영국의 표준 치료는 3SPH/15PH 또는 3SPH/15SH2였다. 1965년부터 1970년 사이, EMB가 PAS를 대체했다. 1968년부터는 RMP가 결핵의 치료에 쓰였고, 1970년대 영국흉부협회(British Thoracic Society)의 연구는 2HRE/7HR이 효과적임을 보여주었다. 1984년, 영국흉부협회는 2HRZ/4HR가 2년 간 3% 안쪽의 재발률을 보일 만큼 효과적임을 보였다.[4][5] 1995년, INH의 내성이 증가한다는 인식과 함께, 영국흉부협회는 EMB 또는 STM을 요법에 포함시킬 것을 추천하였다. 2HREZ/4HR 또는 2SHRZ/4HR 로, 현재 추천되는 요법이다. WHO 또한 2개월 간의 치료 후에도 배양균이 양성 반응을 보이거나(결핵균이 모두 듣는 환자의 15% 정도), 치료 초기에 양쪽으로 심한 공동이 있는 경우 HR의 상태를 6개월 간 유지할 것을 추천하였다.
폐 외 결핵
폐에 영향을 주지 않는 결핵을 'extra-pulmonary tuberculosis'라 한다. 단, 중추신경계의 질병은 제외한다.
영국과 WHO는 2HREZ/4HR, 미국에서는 2HREZ/7HR을 추천한다. 무작위-통제 실험(randomised-controlled trials)으로는, 임파선 결핵[6]과 척추 결핵[7][8][9]의 경우, 6개월 치료가 9개월 치료와 같았다는 증거가 있다.
중추신경계의 결핵
결핵은 중추신경계(뇌 또는 척수)에도 영향을 줄 수 있는데, 이 경우는 각각 결핵성 수막염, 결핵성 뇌염, 결핵성 척수염이라 부른다. 기본적인 치료로 12개월간의 약(2HREZ/10HR)과 스테로이드가 필수적이다. 뇌척수액 배양균의 절반 미만의 경우에 양성반응을 보여 진단이 어렵다.
불이행
환자들이 불규칙적으로, 그리고, 신뢰할 수 없는 방법으로 결핵 치료를 받으면, 치료에 실패하거나, 재발하거나, 약제에 내성을 가진 결핵으로 발전할 위험이 매우 높아진다..
환자들이 약 복용에 실패하는 이유는 여러 가지가 있다. 결핵의 증상은 보통 결핵 치료가 시작되고 수 주 내에 해결되어, 약을 계속 먹어야 할 동기를 잃는다. 규칙적인 후속 조치가 필요한데, 약 복용을 제대로 하고 있는지, 환자가 약을 먹는 데에 문제가 없는지를 확인해야 한다. 환자들에게는 알약들을 규칙적으로 복용하는 중요성, 치료를 마쳐야 하는 중요성을 설명해야 하는데, 이는 재발 또는 약제에 대한 내성의 발전 등의 위험 때문이다.
주된 불평은 알약의 양이 너무 많다는 것이다. 그 주범은 PZA인데, PZA 시럽으로 대체할 수 있다. 알약의 크기가 정말 문제이고, 액체형이 없다면, PZA는 빠질 수 있지만, 그럴 경우 치료 기간이 꽤 늘어난다는 것을 설명해야 한다.
또 다른 불평은 약의 흡수를 용이하게 하기 위해 공복인 상태에서 복용해야 한다는 것이다. 이는 환자가 그대로 따르기 어려우며(예를 들면, 식사 시간이 불규칙한 경우), 환자들이 매일 약을 먹기 위해 1시간 일찍 일어나야 함을 의미할 수도 있다.
지방과 함께 복용하면 RMP의 흡수가 줄어지만, 탄수화물과 단백질, 또는 제산제에는 영향받지 않는다.[10][11] 따라서, 환자는 식사에 지방이나 기름이 포함되어 있지 않다면 식사 때에 약을 복용해도 된다.(예를 들면, 커피 한잔이나 잼을 바른 토스트)[12] 식사와 함께 약을 먹는 것은환자가 공복에 약을 먹었을 때에 느끼는 메스꺼움을 완화하는 데 도움이 된다. INH의 흡수에 대한 음식의 영향은 확실하지 않다. 두 차례의 연구에서는 음식으로 흡수가 줄어듬을 보였다.[13][14] 하지만, 한 연구에서는 차이가 없었다.[15] PZA와 EMB에는 음식이 작은 영향을 주는데, 의학적으로 중요하지 않을 수 있다.[16][17]
부작용
개개의 항결핵제의 부작용에 대한 정보는 각 약제의 문서를 참조한다.
주요 부작용에 관련된 일은 조심스럽게 서술해 왔다.[18]
100명의 환자x달에
- INH 0.49
- RMP 0.43
- EMB 0.07
- PZA 1.48
- 모두 더하면 2.47
이는, 8.6%의 환자가 기본 요법(2HREZ/4HR)의 과정에서 치료 약을 바꾸어야 한다는 계산이 된다. 이 연구에서 주요 부작용으로 가장 위험해지는 사람들은 다음과 같다.
- 나이가 60세 이상인 경우
- 여성
- HIV 양성 환자
- 아시아인
어떤 약이 어떤 부작용의 원인인지 알아내는 것은 매우 어려울 수 있다. 하지만, 각각의 상대적인 빈도수는 알려져 있다.[19] 다음은, 빈도가 낮아지는 순서의 문제가 되는 약들이다.
- 혈소판 감소: RMP
- 신경 장애: INH
- 현기증: STM
- 간염: PZA, RMP, INH
- 발진: PZA, RMP, EMB
혈소판 감소는 RMP에 의한 것으로, 복용량의 테스트는 필요하지 않다. 아래에 RMP를 제외한 요법을 설명한다. (보다 상세한 내용은 리팜피신의 설명을 참조한다.)
리팜피신을 제외한 요법
결핵균이 이소니아지드에 내성을 갖지 않고 리팜피신에 내성을 갖게 되는 경우는 드물다.[20] 하지만, 리팜피신에 대한 과민증은 드물지 않다.(간독증이나 혈소판 감소는 리팜피신 복용을 중단하는 가장 흔한 원인이다.) 또한, 1차 치료 약제 중 리팜피신은 가장 비싸고, 따라서, 빈곤이 심한 나라에서는 리팜피신을 제외한 요법이 종종 사용된다. 리팜피신은 결핵 치료에서 사용할 수 있는 가장 강력한 살균 약제이며, 리팜피신을 뺀 모든 치료 요법은 표준 요법보다 월등히 길다.
영국내에서는 18HE 또는 12HEZ를 추천한다. 미국내에서는 9 ~ 12HEZ에 퀴놀론계 항균제(예를 들면, MXF)를 선택적으로 사용할 것을 추천한다.
주석
- ↑ “Streptomycin treatment of pulmonary tuberculosis”. 《British Medical Journal》 2 (4582): 769~82. doi:10.1136/bmj.2.4582.769. PMC 2091872. PMID 18890300.
- ↑ Empirical treatment with a fluoroquinolone delays the treatment for tuberculosis and is associated with a poor prognosis in endemic areas. 《Thorax》 61 (10): 903~8. doi:10.1136/thx.2005.056887. PMC 2104756. PMID 16809417 //www.ncbi.nlm.nih.gov/pmc/articles/PMC2104756.
|제목=이(가) 없거나 비었음 (도움말) - ↑ David HL. “Probability distribution of drug-resistant mutants in unselected populations of Mycobacterium tuberculosis”. 《Applied Microbiology》 20 (5): 810~4. PMC 377053. PMID 4991927.
- ↑ Britishthoracicsociety. “A controlled trial of 6 months' chemotherapy in pulmonary tuberculosis. Final report: results during the 36 months after the end of chemotherapy and beyond. British Thoracic Society”. 《British Journal of Diseases of the Chest》 78 (4): 330~6. doi:10.1016/0007-0971(84)90165-7. PMID 6386028.
- ↑ Ormerod LP, Horsfield N. “Short-course antituberculous chemotherapy for pulmonary and pleural disease: 5 years' experience in clinical practice”. 《British Journal of Diseases of the Chest》 81 (3): 268~71. doi:10.1016/0007-0971(87)90160-4. PMID 3663498.
- ↑ Campbell IA, Ormerod LP, Friend JA, Jenkins PA, Prescott RJ. “Six months versus nine months chemotherapy for tuberculosis of lymph nodes: final results” 87 (8): 621~3. doi:10.1016/S0954-6111(05)80265-3. PMID 8290746.
- ↑ Upadhyay SS, Saji MJ, Yau AC. “Duration of antituberculosis chemotherapy in conjunction with radical surgery in the management of spinal tuberculosis”. 《Spine》 21 (16): 1898~903. doi:10.1097/00007632-199608150-00014. PMID 8875723.
- ↑ “Five-year assessment of controlled trials of short-course chemotherapy regimens of 6, 9 or 18 months' duration for spinal tuberculosis in patients ambulatory from the start or undergoing radical surgery. Fourteenth report of the Medical Research Council Working Party on Tuberculosis of the Spine”. 《International Orthopaedics》 23 (2): 73~81. PMID 10422019.
- ↑ Parthasarathy R, Sriram K, Santha T, Prabhakar R, Somasundaram PR, Sivasubramanian S. “Short-course chemotherapy for tuberculosis of the spine. A comparison between ambulant treatment and radical surgery--ten-year report”. 《The Journal of Bone and Joint Surgery. British Volume》 81 (3): 464~71. PMID 10872368.
- ↑ Purohit SD, Sarkar SK, Gupta ML, Jain DK, Gupta PR, Mehta YR. “Dietary constituents and rifampicin absorption”. 《Tubercle》 68 (2): 151~2. doi:10.1016/0041-3879(87)90034-1. PMID 3660467.
- ↑ Peloquin CA, Namdar R, Singleton MD, Nix DE. “Pharmacokinetics of rifampin under fasting conditions, with food, and with antacids”. 《Chest》 115 (1): 12~8. doi:10.1378/chest.115.1.12. PMID 9925057.
- ↑ Siegler DI, Bryant M, Burley DM, Citron KM, Standen SM. “Effect of meals on rifampicin absorption”. 《Lancet》 2 (7874): 197~8. PMID 4135611.
- ↑ Peloquin CA, Namdar R, Dodge AA, Nix DE. “Pharmacokinetics of isoniazid under fasting conditions, with food, and with antacids”. 《The International Journal of Tuberculosis and Lung Disease》 3 (8): 703~10. PMID 10460103.
- ↑ Joshi MV, Saraf YS, Kshirsagar NA, Acharya VN. “Food reduces isoniazid bioavailability in normal volunteers”. 《The Journal of the Association of Physicians of India》 39 (6): 470~1. PMID 1938852.
- ↑ Zent C, Smith P. “Study of the effect of concomitant food on the bioavailability of rifampicin, isoniazid and pyrazinamide”. 《Tubercle and Lung Disease》 76 (2): 109~13. doi:10.1016/0962-8479(95)90551-0. PMID 7780091.
- ↑ Peloquin CA, Bulpitt AE, Jaresko GS, Jelliffe RW, James GT, Nix DE. “Pharmacokinetics of pyrazinamide under fasting conditions, with food, and with antacids”. 《Pharmacotherapy》 18 (6): 1205~11. PMID 9855317.
- ↑ Peloquin CA, Bulpitt AE, Jaresko GS, Jelliffe RW, Childs JM, Nix DE. “Pharmacokinetics of ethambutol under fasting conditions, with food, and with antacids”. 《Antimicrobial Agents and Chemotherapy》 43 (3): 568~72. PMC 89161. PMID 10049268.
- ↑ Yee D, Valiquette C, Pelletier M, Parisien I, Rocher I, Menzies D. “Incidence of serious side effects from first-line antituberculosis drugs among patients treated for active tuberculosis”. 《American Journal of Respiratory and Critical Care Medicine》 167 (11): 1472~7. doi:10.1164/rccm.200206-626OC. PMID 12569078.
- ↑ Ormerod LP, Horsfield N. “Frequency and type of reactions to antituberculosis drugs: observations in routine treatment”. 《Tubercle and Lung Disease》 77 (1): 37~42. doi:10.1016/S0962-8479(96)90073-8. PMID 8733412.
- ↑ O'Riordan P, Schwab U, Logan S; 외. “Rapid molecular detection of rifampicin resistance facilitates early diagnosis and treatment of multidrug-resistant tuberculosis: case control study”. 《PLoS ONE》 3 (9): e3173. doi:10.1371/journal.pone.0003173. PMC 2526158. PMID 18779863.
