열역학 과정에서 단열과정(斷熱過程, adiabatic process)이란 어떤 열역학계가 외부와 열 및 물질의 출입이 차단된 채로 변화하는 과정을 일컫는다. 즉,

에서  가 0이다.
단열 과정은 가역 과정일 수도, 비가역 과정일 수도 있다.
가 0이다.
단열 과정은 가역 과정일 수도, 비가역 과정일 수도 있다.
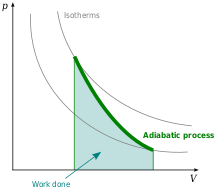
압력-부피 도표에서 단열 과정을 나타내는 곡선을 단열 곡선(斷熱曲線, adiabat)이라고 한다.
단열 과정의 예[편집]
단열 팽창[편집]
W>0 일 때 열기관이 일을 한 만큼 내부 에너지가 작아진다. 기체의 온도가 내려간다.
단열 압축[편집]
W<0 일 때 열기관이 일을 받은 만큼 내부 에너지가 증가한다. 기체의 온도가 올라간다.
이상 기체의 가역 단열 과정[편집]
 이상 기체의 단열 곡선
이상 기체의 단열 곡선
 압력-부피-온도 공간에서의 단열 곡선. 여기서 온도축을 사영하여 없애면 압력-부피 평면의 단열 곡선을 얻는다.
압력-부피-온도 공간에서의 단열 곡선. 여기서 온도축을 사영하여 없애면 압력-부피 평면의 단열 곡선을 얻는다.
입자당 자유도가  개인 이상 기체의 경우,
개인 이상 기체의 경우,

이다. 따라서 압력-부피 도표에서 단열 곡선은
 상수
상수
의 꼴이다. 보통 변수

를 단열 계수(adiabatic index)로 정의한다.
단원자 기체의 경우에는  이므로
이므로  이다. 이원자 기체의 경우에는
이다. 이원자 기체의 경우에는  이므로
이므로  이다.
이다.
같이 보기[편집]
외부 링크[편집]




























