고도산화공정
고도산화공정(Advanced Oxidation Process, AOP)은 넓은 의미로는, ·OH라디칼을 이용한 산화반응을 통해서 물이나 폐수 속의 유기용매를(또는 가끔은 무기용매를) 제거하는 화학적 처리 방법이다. 그러나 실제로 폐수처리에서는 더 구체적으로, 오존(O3)과, 과산화수소(H2O2) 또는 UV 광선을 쓰는 화학 공정 중의 일부를 나타낸다. in situ chemical oxidation도 이 중 하나이다.
고도산화공정은 매우 반응성이 높은 하이드록실 라디칼(·OH)들을 이용한다. 이러한 화학종들은 현존하는 가장 강한 산화제로서 사실상 물에 녹아있는 그 어떤 화합물도 산화시킬 수 있으며, 종종 확산 제어 반응 속도로 작용한다. 결과적으로, ·OH가 생성되는 순간 오염물질들과 무차별적으로 반응하며, 매우 빠르고 효율적으로 오염물질을 작은 무기분자들로 분해한다. 하이드록실 라디칼은 한 개 또는 여러 개의 주 산화제(예를 들어 오존, 과산화수소, 산소 등) 또는 에너지원이나 촉매(자외선, 이산화 티타늄 등)으로부터 생성된다. ·OH라디칼의 수득률을 높이기 위해서 이러한 반응물의 투여량과 순서, 조합 등을 매우 정확하고 사전에 예상한 상태에서 반응시킨다. 일반적으로, 잘 조정된 반응 조건에서는 고도산화공정으로 적어도 5ppb에서 수백 ppm까지 오염물질의 농도를 줄일 수 있으므로, 총유기탄소량과 화학적 산소 요구량을 상당히 감소시켜 "21세기의 정수처리기술"이라는 칭호를 얻게 되었다.
고도산화공정은 특히나 폐수 속에 녹아있는 방향족 화합물, 살충제, 석유 구성성분, 휘발성 유기화합물 등 생물학적으로 독성이거나 잘 분해되지 않는 물질을 대상으로 유용하다. 또한, 이차처리를 마친 폐수를 다시 소독하는 삼차처리에도 이용될 수 있다. 이를 통해 상당량의 오염물질들은 물, 이산화탄소, 염 같은 안정한 무기 화합물로 변환된다(무기화 작용). 고도산화공정을 이용한 폐수 처리의 목적은 깨끗하게 처리된 폐수의 독성과 화학 오염물질을 줄여서 폐수를 다시 시냇물이나 아니면 적어도, 재래식 하수 처리장에 보낼 수 있도록 하는 것이다.
·OH를 이용한 산화공정은 19세기부터 이용해왔지만(분석적이었지만 Fenton시약이 있었다), Glaze가 "물 정화를 하기에 충분한"양의 ·OH생산을 제안하고 "고도산화공정"이라는 용어를 처음 1987년에 정의하기 이전까지는 폐수처리에 이러한 산화제들을 활용하는 것은 주목받지 못하였다. 아직까지도 상대적으로 높은 가격때문에 상업적으로 대규모 사용되지 않고 있다(특히 개발도상국에선). 그러나, 매우 높은 산화력과 높은 효율때문에 고도산화공정은 다루기 힘든 유기물과 무기물을 제거하는 삼차 처리 과정에서 많이 쓰이게 되었다. 물 재사용에 대한 관심이 증대하고, 수질 오염에 대한 규정이 엄격해지면서, 전면적인 고도산화의 상용화가 가속되고 있다. 현재 전 세계적으로 대략 500개의 상업화된 고도산화시설이 존재하며 그 중 대부분은 유럽이나 미국에 있다. 중국과 같은 다른 나라들도 고도산화에 관심을 보이고 있다.
화학적 원리[편집]
일반적으로, 고도산화에 쓰이는 화학적 원리는 크게 세가지로 나눌 수 있다:
- · OH의 형성;
- · OH에 의한 표적 분자에 대한 초기 공격과 파편에 대한 파괴
- 최종적인 무기화 작용이 진행될때까지의 OH에 의한 후속 공격.
·OH 합성의 메커니즘(파트1)은 고도산화기술의 종류에 매우 의존한다. 예를 들어, 오존화, UV/H2O2 와 광촉매 산화작용은 각각 다른 ·OH합성 경로를 가진다:
- UV / H 2 O 2 :[1]
- H2O2 + UV → 2·OH (H2O2 의 O-O결합의 균형분해가 2·OH라디칼을 생성한다)
- 오존 기반 AOP :[2]
- O3 + HO− → HO2− + O2 (O3 와 하이드록실 이온간의 반응이 H2O2 생성(음전하의 형태로)
- O3 + HO2− → HO2· + O3−· (두번째 O3 분자가 HO2− 와 반응하여 오존 라디칼 음이온 (ozonide radical)생성)
- O3−· + H+ → HO3· (오존 라디칼 음이온에 양성자 첨가로 ·OH 생성)
- HO3· → ·OH + O2
- 여기에 제시된 반응 단계는 반응 순서의 일부일 뿐이다. 자세한 내용은 참고 문헌을 참조한다.
- TiO 2를 이용한 광촉매 산화 :[2]
- TiO2 + UV → e− + h+ ( 광촉매의 표면에 빛 조사 시 생기는 들뜬 전자 (e−) 와 띠틈(h+) )
- 생성)
- Ti(IV) + H2O
 Ti(IV)-H2O (촉매표면에서 물 흡수)
Ti(IV)-H2O (촉매표면에서 물 흡수) - Ti(IV)-H2O + h+
 Ti(IV)-·OH + H+ 반응성이 높은 띠틈이 물과 반응
Ti(IV)-·OH + H+ 반응성이 높은 띠틈이 물과 반응 - 여기에 제시된 반응 단계는 반응 순서의 일부일 뿐이다. 자세한 내용은 참고 문헌을 참조한다.
아직까지 3번 부분의 자세한 메커니즘에 대한 정설은 존재하지 않지만, 학자들은 2번 반응에서 ·OH에 의한 표적분자의 공격의 과정에 관한 실마리를 찾은 상태이다. 본질적으로, ·OH 은 라디칼분자이고, 매우 반응성 높은 친전자체로 작용해야 한다. 그러므로 초기 공격반응 중 두 종류는 수소제거반응과 첨가반응이다. 기술 지침서에서 채택된 뒤 나중에 다시 개선된 아래 계획은, ·OH를 이용한 벤젠의 산화 메커니즘에 관한 것이다.
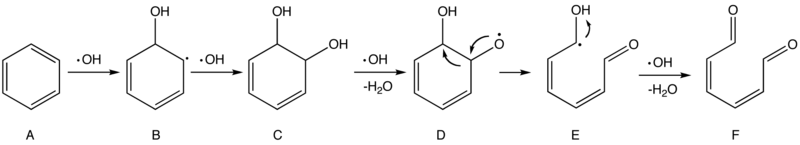
반응식 1. 하이드록실 라디칼에 의한 벤젠의 산화 메커니즘 제안
처음 두 반응은 (A)의 방향족 고리를 분해시켜 중간체 C에 있는 두 개의 하이드록실기를(–OH) 만드는 친전자성 반응이다. 나중에 한 ·OH분자가 하이드록실기중 하나에 있는 수소원자를 잡게 되고, 라디칼종(D)를 만든다. 이 화합물은 더 안정한 (E)로 쉽게 재배열된다. 그리고 나서 E는 순조롭게 ·OH의 공격을 받고 2,4-hexadiene-1,6-dione (F)를 생성하게 된다. 충분한 ·OH 라디칼이 있는 이상, F에서 그후로 계속 공격이 일어나 마지막에는 F가 H2O 나CO2 같은 작고 안정한 분자들로 분해된다. 그러나, 이러한 과정은 충분히 가능성 있지만 부분적으로 밝혀지지 않은 메커니즘들로 이루어져 있다.
장점[편집]
고도산화반응은 수처리에 있어서 많은 독보적 장점을 가지고 있다:
- 수용성 상태의 유기 화합물을 효과적으로 제거할 수 있으며, 오염물질을 다른 상으로 바꾸거나 수집하는 것보다 능률적이다.
- ·OH의 매우 큰 반응성 덕분에, 사실상 거의 모든 수용성 오염물질과 무차별적으로 반응한다. 그러므로 활용분야가 전부는 아니더라도, 다양한 유기오염물질을 제거하는 많은 방면에 걸친다.
- 몇몇 중금속들 또한 침전된 M(OH)x의 형태로 제거가능하다.
- 몇몇 고도산화과정에서는, 소독작용 또한 가능하다. 그렇기에 고도산화공정 하나만으로 수질문제를 한번에 해결할 수도 있다.
- OH가 환원되면 최종적으로 H2O가 생성되기 때문에, 이론적으로 물에 다른 해로운 물질들이 남지 않는다.
현재 결점[편집]
그러나 고도산화공정도 완벽하지 않으며, 몇몇 단점들이 존재한다.
- 가장 중요한 단점은, 고도산화는 비용이 상당히 많이 들며, 이는 반응을 지속시키기 위해 비싼 화학시약들이 계속 투입되어야 하기 때문이다. 자연스럽게도, 제거해야하는 오염물질의 양에 비례해서 하이드록실 라디칼과 다른 시약들이 요구된다.
- 몇몇 기술에서는 고도산화를 안정적으로 수행하기 위해 오염수의 사전처리가 필요하게 되는데 이는 비용적으로나 기술적으로나 부담이 클 수 있다. 예를 들어, 중탄산 이온(HCO3−)은 눈에 띄게 ·OH의 농도를 줄이는데, 이는 H2O 와 훨씬 더 반응성이 적은 화합물인 ·CO3−을 내놓는 소기 과정 때문이다. 결과적으로, 고도산화를 포기하거나 중탄산이 먼저 제거되어야 한다.
- 많은 양의 오염수를 고도산화공정만 써서 처리하는 것은 비용적으로 비효율적이다. 그대신, 고도산화공정을 마지막 단계에 배치하여 일차 그리고 이차처리가 다량의 오염물질을 제거한 뒤에 사용하는 것이 효과적이다.
미래[편집]
고도산화공정이라는 용어는 1987년에 처음 정의되었기 때문에 이에 관한 이론과 적용에 있어서 급격한 발전을 이뤄왔다. 지금까지, TiO2/UV시스템, H2O2/UV systems과, Fenton, photo-Fenton, 그리고Electro-Fenton system들에 대한 철저한 검토가 수행되어 왔다. 그러나, 아직까지도 고도산화공정들에 대한 많은 연구가 더욱 필요한 실정이다.
최근 트렌드는 효율적이고 경제적으로 새롭게 수정된 공정의 개발이다. 실제로, 건설적인 해결책을 제시하는 여러 연구가 있었다. 예를 들어, TiO2에 비금속 원소를 투여하여 광촉매성을 증진시키거나, 초음파처리를 적용하여 하이드록실 라디칼의 생성을 증가시키는 방법등이 있다.
관련 자료들[편집]
참고 문헌[편집]
- ↑ W.T.M. Audenaert; Y. Vermeersch; S.W.H. Van Hulle; P. Dejans; A. Dumouilin; I. Nopens (2011). “Application of a mechanistic UV/hydrogen peroxide model at full-scale: Sensitivity analysis, calibration and performance evaluation”. 《Chemical Engineering Journal》 171 (1): 113–126. doi:10.1016/j.cej.2011.03.071.
- ↑ 가 나 Beltrán, Fernando J. (2004). 《Ozone Reaction Kinetics for Water and Wastewater Systems》. CRC Press, Florida. ISBN 978-1-56670-629-2.
추가 자료[편집]
- Michael OD Roth: Chemical oxidation: Technology for the Nineties, volume VI: Technologies for the Nineties: 6 (Chemical oxidation) W. Wesley corner fields and John A. Roth, Technomic Publishing CO, Lancaster among other things. 1997, ISBN 1-56676-597-8. (engl.)
- Oppenländer, Thomas (2003). 《Advanced Oxidation Processes (AOPs): Principles, Reaction Mechanisms, Reactor Concepts》. Wiley VCH, Weinheim. ISBN 978-3-527-30563-6.

